沪教版化学九年级下册 第7章 第2节 常见的酸和碱(第2课时)课件(共25张PPT内嵌视频)
文档属性
| 名称 | 沪教版化学九年级下册 第7章 第2节 常见的酸和碱(第2课时)课件(共25张PPT内嵌视频) |  | |
| 格式 | pptx | ||
| 文件大小 | 58.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-08-21 10:27:13 | ||
图片预览




文档简介
(共25张PPT)
第七章 应用广泛的酸、碱、盐
第二节 常见的酸和碱
第二课时 酸的化学性质
+
=
你见过鸡蛋跳舞吗
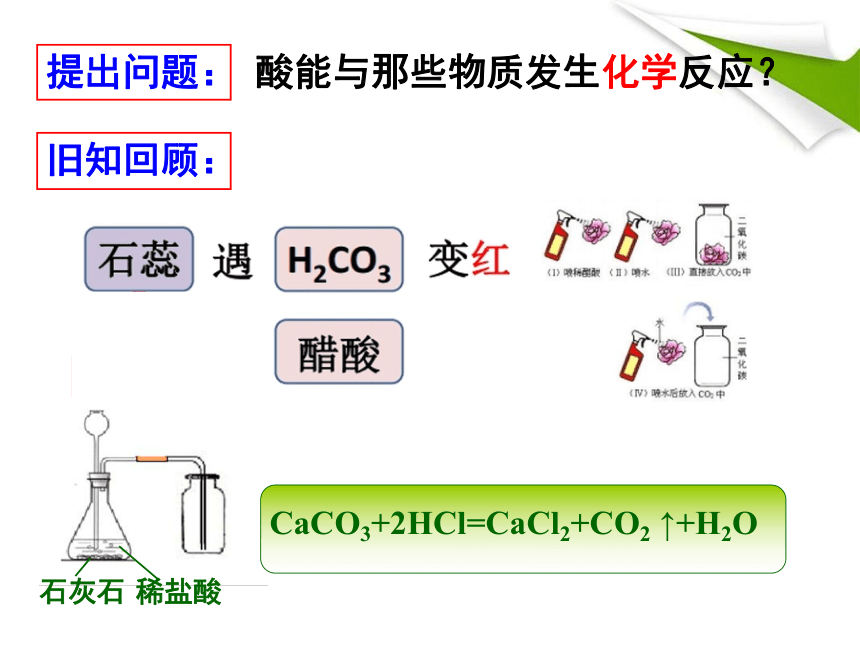
提出问题:
酸能与那些物质发生化学反应?
旧知回顾:
石灰石
稀盐酸
CaCO3+2HCl=CaCl2+CO2 ↑+H2O
提出问题:
酸能与那些物质发生化学反应?
生活情境:
小明看见爸爸常常用稀盐酸给铁制器皿除锈,他自己想亲自试一试。于是,他找出一颗生锈铁钉来,放入足量稀盐酸中,然后,美滋滋地去睡觉了……可是,当他醒来之后,发现铁钉不见了,这是为什么呢?
猜想与假设:
酸可能与---
石蕊等指示剂、
CaCO3同类的物质发生反应。
猜想与假设:
酸可能与---
石蕊等指示剂、
铁(Fe)等金属、
铁锈(Fe2O3)……发生反应。
CaCO3同类的物质、
根据下列药品,设计实验方案。
设计实验:
提出问题:
酸能与那些物质发生化学反应?
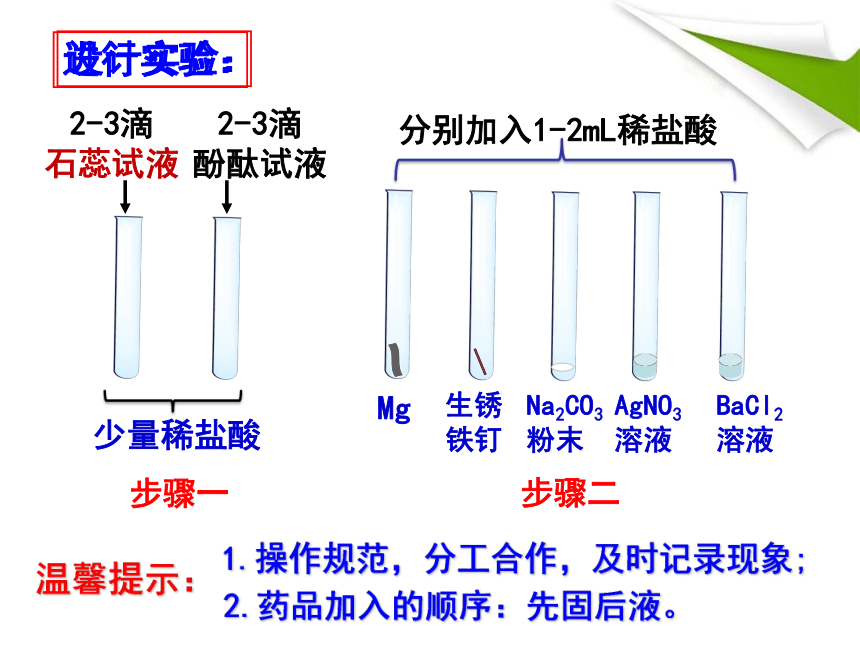
设计实验:
少量稀盐酸
2-3滴
石蕊试液
2-3滴
酚酞试液
Mg
生锈铁钉
Na2CO3
粉末
AgNO3
溶液
BaCl2
溶液
分别加入1-2mL稀盐酸
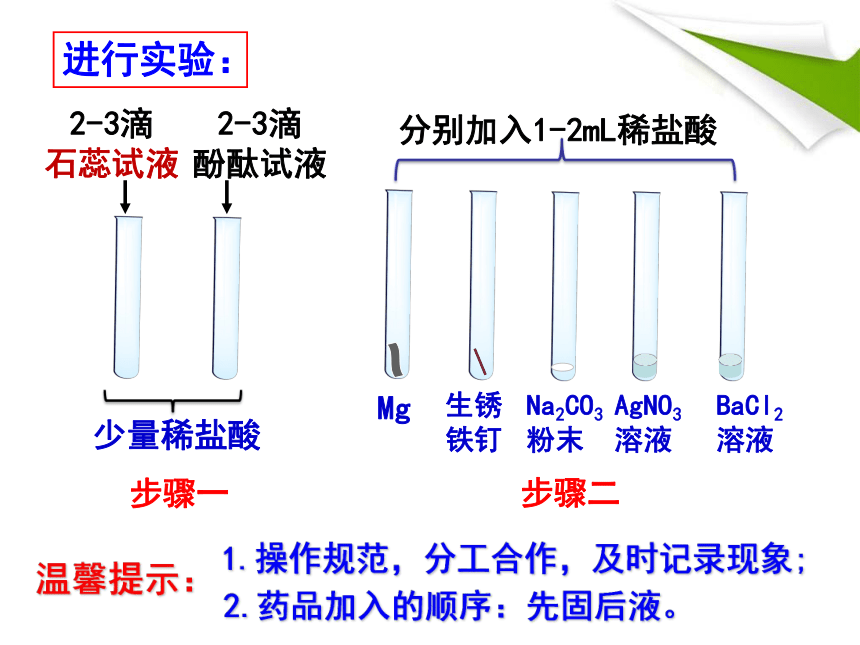
进行实验:
步骤一
步骤二
温馨提示:
1.操作规范,分工合作,及时记录现象;
2.药品加入的顺序:先固后液。
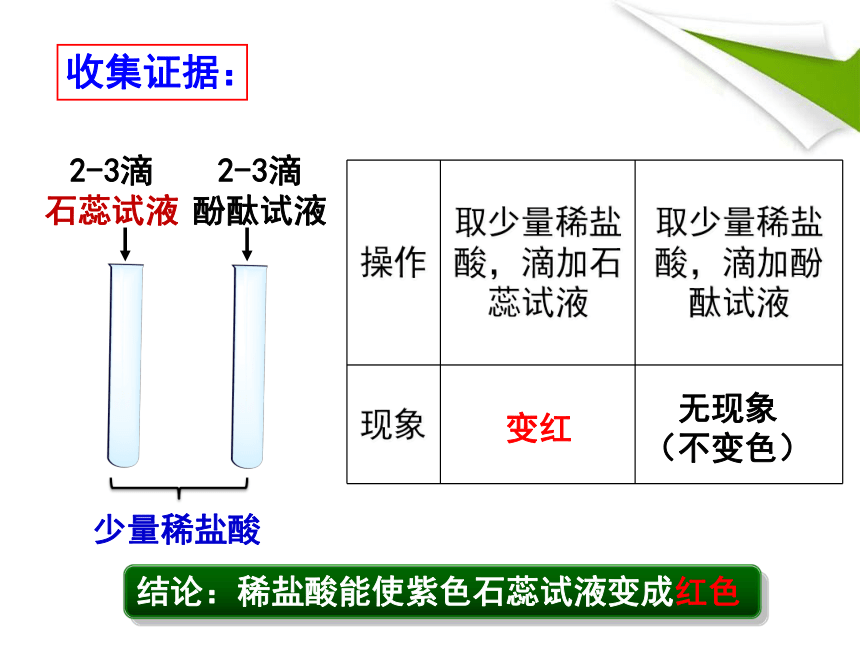
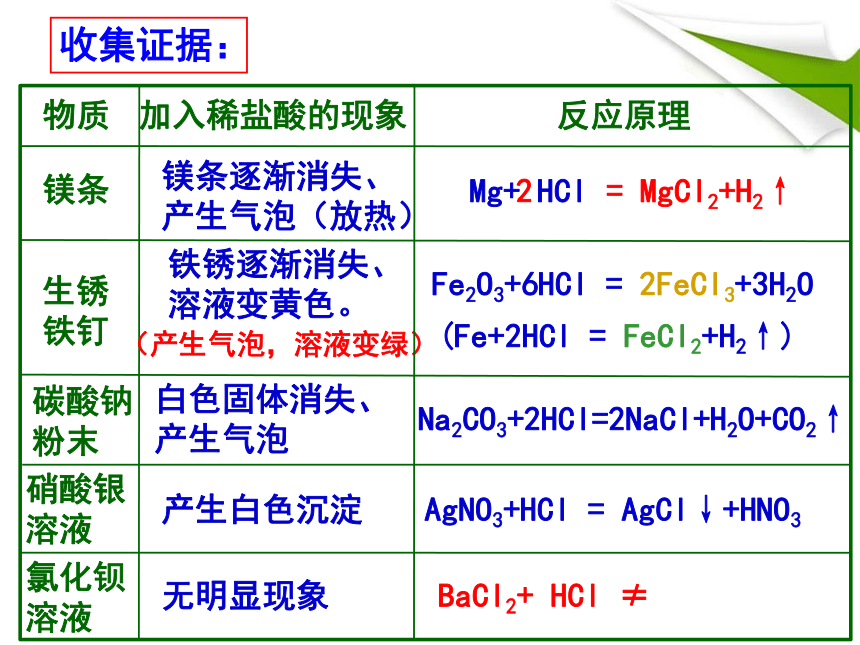
收集证据:
少量稀盐酸
2-3滴
石蕊试液
2-3滴
酚酞试液
操作 取少量稀盐酸,滴加石蕊试液 取少量稀盐酸,滴加酚酞试液
现象
变红
无现象
(不变色)
结论:稀盐酸能使紫色石蕊试液变成红色
少量稀盐酸
2-3滴
石蕊试液
2-3滴
酚酞试液
Mg
生锈铁钉
Na2CO3
粉末
AgNO3
溶液
BaCl2
溶液
分别加入1-2mL稀盐酸
进行实验:
步骤一
步骤二
温馨提示:
1.操作规范,分工合作,及时记录现象;
2.药品加入的顺序:先固后液。
镁条
生锈铁钉
碳酸钠粉末
加入稀盐酸的现象
镁条逐渐消失、产生气泡(放热)
铁锈逐渐消失、溶液变黄色。
白色固体消失、产生气泡
硝酸银溶液
氯化钡溶液
产生白色沉淀
无明显现象
物质
(产生气泡,溶液变绿)
Fe2O3+6HCl = 2FeCl3+3H2O
Na2CO3+2HCl=2NaCl+H2O+CO2↑
AgNO3+HCl = AgCl↓+HNO3
BaCl2+ HCl ≠
Mg+ HCl -
反应原理
(Fe+2HCl = FeCl2+H2↑)
收集证据:
= MgCl2+H2↑
2
镁条
生锈铁钉
碳酸钠粉末
和盐酸反应化学方程式
Fe2O3+ 6HCl = 2FeCl3 +3H2O
Na2CO3+2HCl = 2NaCl+H2O+CO2↑
硝酸银溶液
氯化钡溶液
AgNO3+HCl = AgCl↓+HNO3
BaCl2+ HCl ≠
Mg + 2HCl = MgCl2 + H2↑
物质
(Fe+ 2HCl = FeCl2 + H2↑)
交流与讨论1:
由金属阳离子和酸根阴离子构成的化合物,化学上把这类化合物称为盐。
注意:由于NH4+与金属阳离子性质相似,可以看作金属阳离子,因此NH4Cl﹑(NH4)2SO4等也属于盐。
如:Na2CO3、BaCl2、MgCl2、NaCl、FeCl3等
交流与讨论1:
镁条
生锈铁钉
碳酸钠粉末
和盐酸反应化学方程式
Fe2O3+ 6HCl = 2FeCl3 +3H2O
Na2CO3+2HCl = 2NaCl+H2O+CO2↑
硝酸银溶液
氯化钡溶液
AgNO3+HCl = AgCl↓+HNO3
BaCl2+ HCl ≠
Mg + 2HCl = MgCl2 + H2↑
物质
(Fe+ 2HCl = FeCl2 + H2↑)
归纳总结:
请同学们从反应物与生成物所属物质类别的角度归纳稀盐酸的化学性质。
镁条
锈铁钉
碳酸钠粉末
和盐酸反应化学方程式
Fe2O3+ 6HCl = 2FeCl3 +3H2O
Na2CO3+2HCl = 2NaCl+H2O+CO2↑
硝酸银溶液
氯化钡溶液
AgNO3+HCl = AgCl↓+HNO3
BaCl2+ HCl ≠
Mg + 2HCl = MgCl2 + H2↑
物质
(Fe + 2HCl = FeCl2 + H2↑)
交流与讨论2:
Fe2O3 + 6HCl = 2FeCl3 + 3H2O
AgNO3 + HCl = AgCl↓+ HNO3
化合物
化合物
化合物
化合物
Fe2O3 + 6HCl = 2FeCl3 + 3H2O
AgNO3 + HCl = AgCl↓+ HNO3
两种化合物互相交换成分生成另外两种化合物的反应称为复分解反应。
AB + CD === AD + CB
交流与讨论2:
CaCO3+2HCl = CaCl2+H2O+CO2
思维驿站
H2CO3
Na2CO3
+2HCl = 2NaCl+H2O+CO2
H2CO3
评价与反思:
Mg
Fe2O3
Na2CO3粉末
分别加入1-2mL稀硫酸
活动探究:
进行实验:
稀硫酸与盐酸的化学性质相似吗?
镁条
锈铁钉
碳酸钠粉末
实验现象
镁条消失、产生气泡(放热)
铁锈消失、溶液变为黄色。(产生气泡,溶液变为绿色)
白色固体消失、产生气泡
你能写出这些反应的化学方程式吗?
物质
Mg+H2SO4 = MgSO4+H2↑
Fe2O3+3H2SO4=Fe2(SO4)3+3H2O
(Fe+H2SO4 = FeSO4 + H2↑)
Na2CO3+H2SO4=Na2SO4+H2O+CO2↑
反应原理
探究结果:
盐 酸
HCl
硫 酸
H2SO4
H
H
H+
H+
H+
H+
H+
H+
溶于水后解离出相同的阳离子——氢离子。
稀硫酸和盐酸为什么具有相似的化学性质?
交流与讨论1:
酸
酸碱指示剂
使无色酚酞
使石蕊试液
活泼金属
盐
金属氧化物
盐 + H2↑
盐 + H2O
新盐+新酸
变红色
不变色
小结
酸的通性
酸的化学性质存在差异吗?
BaCl2+ HCl ≠
BaCl2+ H2SO4 = ?
由于不同的酸溶于水时解离出的酸根阴离子不同,其性质也存在差异。
交流与讨论2:
BaSO4↓ + 2HCl
评价与反思:
我们使用酸的时候应该注意些什么?
HCl
Cu
CO2
NaCl
Fe2O3
Fe
Cu
CO2
H2SO4
CO2
NaCl
CaCO3
H2SO4
NaCl
Cu
CO2
H2SO4
入口
出口
小羊选择哪条路才不会羊入狼口呢
找出这几条路中谁是狼
酸 + 金属 → 盐 + 氢气
酸 + 金属氧化物 →盐 + 水
酸 + 盐 → 新酸 + 新盐
学以致用
你知道用稀盐酸浸泡除去水垢[主要成分:CaCO3、Mg(OH)2]的原理吗?
更上一层楼
酸还有其它的化学性质吗?
课后探索
请同学们课后查阅资料,了解酸的这些性质在生活、生产和科学研究中有哪些应用。
谢谢!
第七章 应用广泛的酸、碱、盐
第二节 常见的酸和碱
第二课时 酸的化学性质
+
=
你见过鸡蛋跳舞吗
提出问题:
酸能与那些物质发生化学反应?
旧知回顾:
石灰石
稀盐酸
CaCO3+2HCl=CaCl2+CO2 ↑+H2O
提出问题:
酸能与那些物质发生化学反应?
生活情境:
小明看见爸爸常常用稀盐酸给铁制器皿除锈,他自己想亲自试一试。于是,他找出一颗生锈铁钉来,放入足量稀盐酸中,然后,美滋滋地去睡觉了……可是,当他醒来之后,发现铁钉不见了,这是为什么呢?
猜想与假设:
酸可能与---
石蕊等指示剂、
CaCO3同类的物质发生反应。
猜想与假设:
酸可能与---
石蕊等指示剂、
铁(Fe)等金属、
铁锈(Fe2O3)……发生反应。
CaCO3同类的物质、
根据下列药品,设计实验方案。
设计实验:
提出问题:
酸能与那些物质发生化学反应?
设计实验:
少量稀盐酸
2-3滴
石蕊试液
2-3滴
酚酞试液
Mg
生锈铁钉
Na2CO3
粉末
AgNO3
溶液
BaCl2
溶液
分别加入1-2mL稀盐酸
进行实验:
步骤一
步骤二
温馨提示:
1.操作规范,分工合作,及时记录现象;
2.药品加入的顺序:先固后液。
收集证据:
少量稀盐酸
2-3滴
石蕊试液
2-3滴
酚酞试液
操作 取少量稀盐酸,滴加石蕊试液 取少量稀盐酸,滴加酚酞试液
现象
变红
无现象
(不变色)
结论:稀盐酸能使紫色石蕊试液变成红色
少量稀盐酸
2-3滴
石蕊试液
2-3滴
酚酞试液
Mg
生锈铁钉
Na2CO3
粉末
AgNO3
溶液
BaCl2
溶液
分别加入1-2mL稀盐酸
进行实验:
步骤一
步骤二
温馨提示:
1.操作规范,分工合作,及时记录现象;
2.药品加入的顺序:先固后液。
镁条
生锈铁钉
碳酸钠粉末
加入稀盐酸的现象
镁条逐渐消失、产生气泡(放热)
铁锈逐渐消失、溶液变黄色。
白色固体消失、产生气泡
硝酸银溶液
氯化钡溶液
产生白色沉淀
无明显现象
物质
(产生气泡,溶液变绿)
Fe2O3+6HCl = 2FeCl3+3H2O
Na2CO3+2HCl=2NaCl+H2O+CO2↑
AgNO3+HCl = AgCl↓+HNO3
BaCl2+ HCl ≠
Mg+ HCl -
反应原理
(Fe+2HCl = FeCl2+H2↑)
收集证据:
= MgCl2+H2↑
2
镁条
生锈铁钉
碳酸钠粉末
和盐酸反应化学方程式
Fe2O3+ 6HCl = 2FeCl3 +3H2O
Na2CO3+2HCl = 2NaCl+H2O+CO2↑
硝酸银溶液
氯化钡溶液
AgNO3+HCl = AgCl↓+HNO3
BaCl2+ HCl ≠
Mg + 2HCl = MgCl2 + H2↑
物质
(Fe+ 2HCl = FeCl2 + H2↑)
交流与讨论1:
由金属阳离子和酸根阴离子构成的化合物,化学上把这类化合物称为盐。
注意:由于NH4+与金属阳离子性质相似,可以看作金属阳离子,因此NH4Cl﹑(NH4)2SO4等也属于盐。
如:Na2CO3、BaCl2、MgCl2、NaCl、FeCl3等
交流与讨论1:
镁条
生锈铁钉
碳酸钠粉末
和盐酸反应化学方程式
Fe2O3+ 6HCl = 2FeCl3 +3H2O
Na2CO3+2HCl = 2NaCl+H2O+CO2↑
硝酸银溶液
氯化钡溶液
AgNO3+HCl = AgCl↓+HNO3
BaCl2+ HCl ≠
Mg + 2HCl = MgCl2 + H2↑
物质
(Fe+ 2HCl = FeCl2 + H2↑)
归纳总结:
请同学们从反应物与生成物所属物质类别的角度归纳稀盐酸的化学性质。
镁条
锈铁钉
碳酸钠粉末
和盐酸反应化学方程式
Fe2O3+ 6HCl = 2FeCl3 +3H2O
Na2CO3+2HCl = 2NaCl+H2O+CO2↑
硝酸银溶液
氯化钡溶液
AgNO3+HCl = AgCl↓+HNO3
BaCl2+ HCl ≠
Mg + 2HCl = MgCl2 + H2↑
物质
(Fe + 2HCl = FeCl2 + H2↑)
交流与讨论2:
Fe2O3 + 6HCl = 2FeCl3 + 3H2O
AgNO3 + HCl = AgCl↓+ HNO3
化合物
化合物
化合物
化合物
Fe2O3 + 6HCl = 2FeCl3 + 3H2O
AgNO3 + HCl = AgCl↓+ HNO3
两种化合物互相交换成分生成另外两种化合物的反应称为复分解反应。
AB + CD === AD + CB
交流与讨论2:
CaCO3+2HCl = CaCl2+H2O+CO2
思维驿站
H2CO3
Na2CO3
+2HCl = 2NaCl+H2O+CO2
H2CO3
评价与反思:
Mg
Fe2O3
Na2CO3粉末
分别加入1-2mL稀硫酸
活动探究:
进行实验:
稀硫酸与盐酸的化学性质相似吗?
镁条
锈铁钉
碳酸钠粉末
实验现象
镁条消失、产生气泡(放热)
铁锈消失、溶液变为黄色。(产生气泡,溶液变为绿色)
白色固体消失、产生气泡
你能写出这些反应的化学方程式吗?
物质
Mg+H2SO4 = MgSO4+H2↑
Fe2O3+3H2SO4=Fe2(SO4)3+3H2O
(Fe+H2SO4 = FeSO4 + H2↑)
Na2CO3+H2SO4=Na2SO4+H2O+CO2↑
反应原理
探究结果:
盐 酸
HCl
硫 酸
H2SO4
H
H
H+
H+
H+
H+
H+
H+
溶于水后解离出相同的阳离子——氢离子。
稀硫酸和盐酸为什么具有相似的化学性质?
交流与讨论1:
酸
酸碱指示剂
使无色酚酞
使石蕊试液
活泼金属
盐
金属氧化物
盐 + H2↑
盐 + H2O
新盐+新酸
变红色
不变色
小结
酸的通性
酸的化学性质存在差异吗?
BaCl2+ HCl ≠
BaCl2+ H2SO4 = ?
由于不同的酸溶于水时解离出的酸根阴离子不同,其性质也存在差异。
交流与讨论2:
BaSO4↓ + 2HCl
评价与反思:
我们使用酸的时候应该注意些什么?
HCl
Cu
CO2
NaCl
Fe2O3
Fe
Cu
CO2
H2SO4
CO2
NaCl
CaCO3
H2SO4
NaCl
Cu
CO2
H2SO4
入口
出口
小羊选择哪条路才不会羊入狼口呢
找出这几条路中谁是狼
酸 + 金属 → 盐 + 氢气
酸 + 金属氧化物 →盐 + 水
酸 + 盐 → 新酸 + 新盐
学以致用
你知道用稀盐酸浸泡除去水垢[主要成分:CaCO3、Mg(OH)2]的原理吗?
更上一层楼
酸还有其它的化学性质吗?
课后探索
请同学们课后查阅资料,了解酸的这些性质在生活、生产和科学研究中有哪些应用。
谢谢!
