沪教版化学九年级下册第7章应用广泛的酸·碱·盐基础实验8酸与碱的化学性质 课件(共21张PPT)
文档属性
| 名称 | 沪教版化学九年级下册第7章应用广泛的酸·碱·盐基础实验8酸与碱的化学性质 课件(共21张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.8MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-08-24 00:00:00 | ||
图片预览



文档简介
(共21张PPT)
基础实验8 酸与碱的化学性质
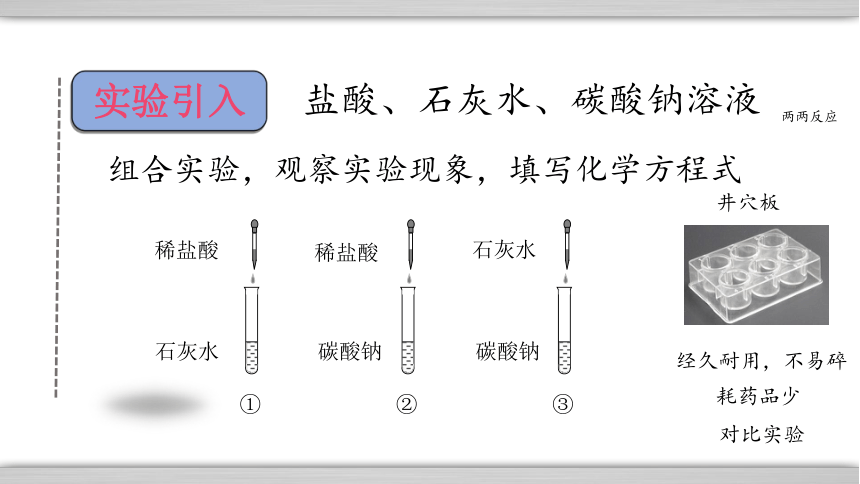
实验引入
盐酸、石灰水、碳酸钠溶液
组合实验,观察实验现象,填写化学方程式
碳酸钠
石灰水
稀盐酸
稀盐酸
石灰水
碳酸钠
②
③
①
两两反应
井穴板
经久耐用,不易碎
耗药品少
对比实验
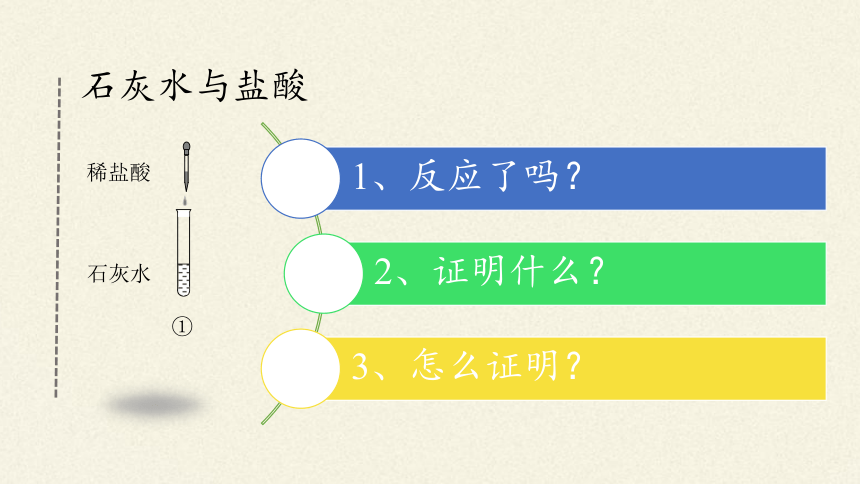
稀盐酸
石灰水
①
石灰水与盐酸
1、反应了吗?
2、证明什么?
3、怎么证明?
活动一:石灰水与盐酸反应实验设计
根据药品设计实验方案:酚酞试液、稀盐酸、稀NaOH溶液、碳酸钙、锌粒、氧化铜、氢氧化铜、氯化铜溶液、氯化铁溶液、硝酸银溶液、pH试纸等
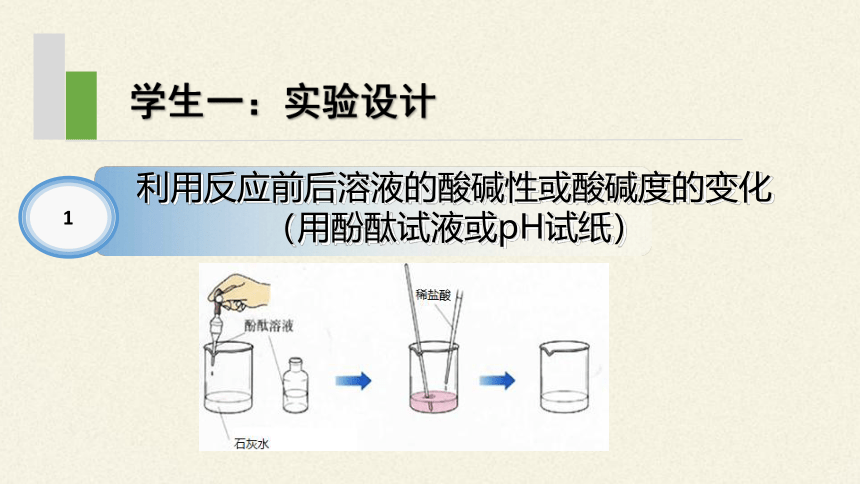
学生一:实验设计
1
利用反应前后溶液的酸碱性或酸碱度的变化
(用酚酞试液或pH试纸)
下列方法可行吗?
4
金属氧化物(CuO)
3
活泼金属(Zn)
2
碳酸盐(CaCO3)_
5
难溶性碱[Cu(OH)2]
6
盐溶液(AgNO3溶液)
我们还可以……
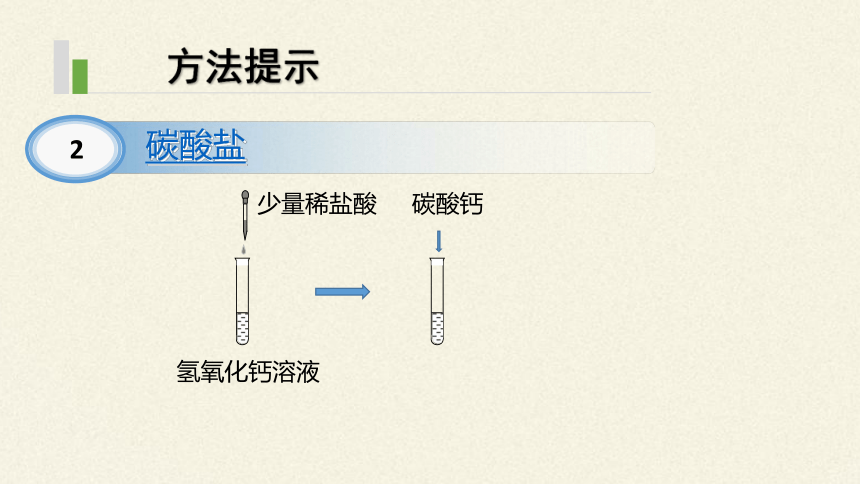
2
碳酸盐
氢氧化钙溶液
少量稀盐酸
碳酸钙
方法提示
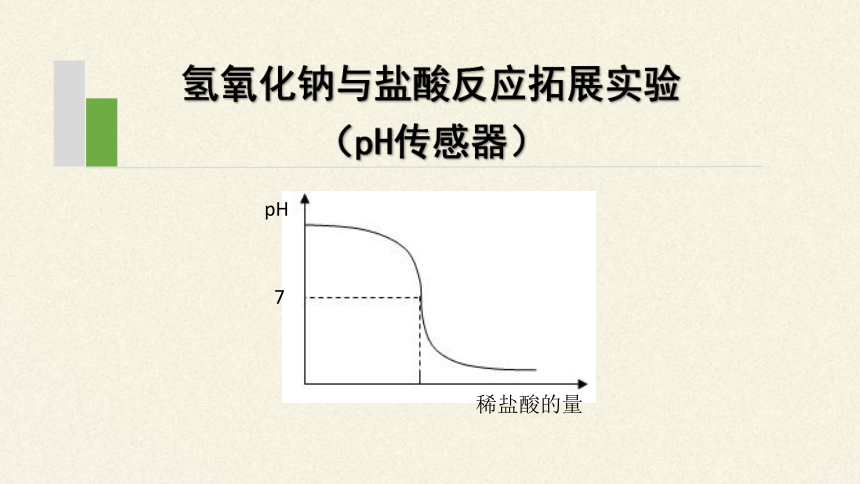
氢氧化钠与盐酸反应拓展实验
(pH传感器)
pH
稀盐酸的量
7
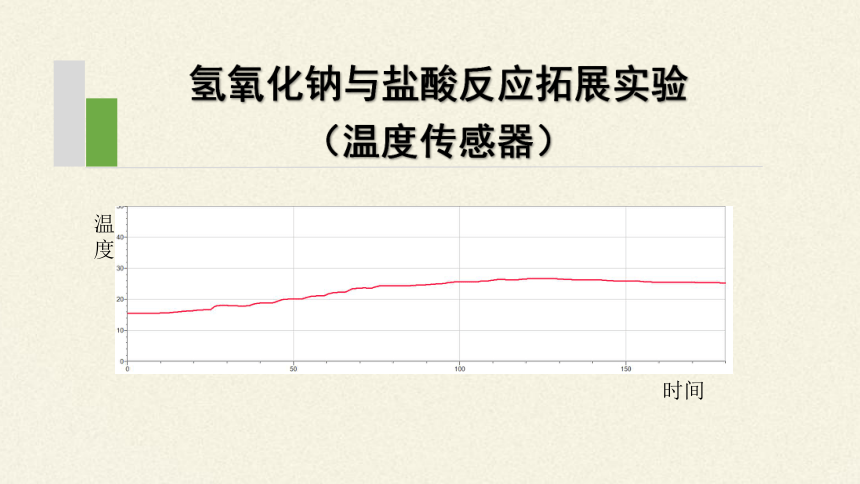
氢氧化钠与盐酸反应拓展实验
(温度传感器)
时间
温度
小结
无形
反应物减少
生成物增加
反应物性质
温度的变化
生成物性质
能量的改变
有形
2020/7/31
选项 所用试剂或用品 现象和结论
A 氯化镁溶液 出现白色沉淀,则氢氧化钠过量
B 硝酸钡溶液 出现白色沉淀,则硫酸过量
C 铁片 有气泡产生,则硫酸过量
D pH试纸 pH=7,则恰好完全反应
(2017.仪征2模) 为了探究氢氧化钠溶液与稀硫酸是否恰好完全反应,分别取少量反应后的溶液,用下表中的方法进行实验。其中,不正确的是( )
B
文字
实验装置图
数据表
坐标图
流程图
资料卡
活动二:实验探究题变化的呈现形式
2020/7/31
现有一包白色粉末,其中含有CuSO4、BaCl2、NaOH、Na2CO3、NaCl中的一种或几种。某化学小组为确定白色粉末的成分,进行了如下实验:
①取一定量粉末,加入足量水,振荡,得到无色透明溶液;
CuSO4、BaCl2、NaOH、Na2CO3、NaCl
不能共存
文字呈现
×
CuSO4、BaCl2、NaOH、Na2CO3、NaCl中的一种或几种。
①取一定量白色粉末,加入足量水,振荡,得到无色
透明溶液;
②取少量①的溶液,加入足量盐酸,有气泡产生。
CuSO4、BaCl2、NaOH、Na2CO3 、NaCl
文字呈现
不能共存
×
×
③另取少量①的溶液,加入足量氯化钙充分反应后再滴加无色酚酞,溶液呈无色。
×
某矿石由氧化镁、氧化铁、氧化铜和二氧化硅组成,用它制备氢氧化镁的流程示意图如图所示(已知:二氧化硅不溶于水也不与稀盐酸反应)
MgO
Fe2O3
CuO
SiO2
Mg(OH)2
MgCl2
FeCl3
CuCl2
HCl
氢氧化物 Fe(OH)3 Cu(OH)2 Mg(OH)2
开始沉淀的pH 1.5 4.2 8.6
完全沉淀的pH 3.2 6.7 11.1
Fe(OH)3
Cu(OH)2
流程图呈现
粗还原铁粉中含有Fe和少量Fe2O3、Fe3C杂质,用氢气在高温下还原可得到精还原铁粉。现测定粗还原铁粉中Fe2O3的质量和碳元素的质量分数,按如下装置进行实验:
Fe2O3
Fe3C
H2O
CH4
CH4
CO2
H2O
CO2
装置图呈现
Fe2O3+3H2 高温 2Fe+3H2O
已知:Fe3C+2H2 高温 3Fe+CH4 3CH4+4Fe2O3 高温 3CO2+6H2O+8Fe
2020/7/31
粗还原铁粉的质量为10.000g,装置B、D、E分别增重0.540g、0.270g、0.220g,计算样品中Fe2O3的质量和碳元素的质量分数(要求写计算过程)。
Fe2O3~ H2O
Fe3C~ CH4 ~ CO2 ~ C
3
装置图呈现
2020/7/31
粗还原铁粉的质量为10.000g,装置B、D、E分别增重0.540g、0.270g、0.220g,计算样品中Fe2O3的质量和碳元素的质量分数(要求写计算过程)。
Fe2O3~ H2O
Fe3C~ CH4 ~ CO2~C
3
160 54
X 0.54
X=1.6g
44 12
Y=0.06
0.22 Y
装置图呈现
从无形到有形
从有形到变形
学习、人生……从无到有的过程
从有界到无疆
仪征市大仪中学化学组 王光朝
谢 谢
基础实验8 酸与碱的化学性质
实验引入
盐酸、石灰水、碳酸钠溶液
组合实验,观察实验现象,填写化学方程式
碳酸钠
石灰水
稀盐酸
稀盐酸
石灰水
碳酸钠
②
③
①
两两反应
井穴板
经久耐用,不易碎
耗药品少
对比实验
稀盐酸
石灰水
①
石灰水与盐酸
1、反应了吗?
2、证明什么?
3、怎么证明?
活动一:石灰水与盐酸反应实验设计
根据药品设计实验方案:酚酞试液、稀盐酸、稀NaOH溶液、碳酸钙、锌粒、氧化铜、氢氧化铜、氯化铜溶液、氯化铁溶液、硝酸银溶液、pH试纸等
学生一:实验设计
1
利用反应前后溶液的酸碱性或酸碱度的变化
(用酚酞试液或pH试纸)
下列方法可行吗?
4
金属氧化物(CuO)
3
活泼金属(Zn)
2
碳酸盐(CaCO3)_
5
难溶性碱[Cu(OH)2]
6
盐溶液(AgNO3溶液)
我们还可以……
2
碳酸盐
氢氧化钙溶液
少量稀盐酸
碳酸钙
方法提示
氢氧化钠与盐酸反应拓展实验
(pH传感器)
pH
稀盐酸的量
7
氢氧化钠与盐酸反应拓展实验
(温度传感器)
时间
温度
小结
无形
反应物减少
生成物增加
反应物性质
温度的变化
生成物性质
能量的改变
有形
2020/7/31
选项 所用试剂或用品 现象和结论
A 氯化镁溶液 出现白色沉淀,则氢氧化钠过量
B 硝酸钡溶液 出现白色沉淀,则硫酸过量
C 铁片 有气泡产生,则硫酸过量
D pH试纸 pH=7,则恰好完全反应
(2017.仪征2模) 为了探究氢氧化钠溶液与稀硫酸是否恰好完全反应,分别取少量反应后的溶液,用下表中的方法进行实验。其中,不正确的是( )
B
文字
实验装置图
数据表
坐标图
流程图
资料卡
活动二:实验探究题变化的呈现形式
2020/7/31
现有一包白色粉末,其中含有CuSO4、BaCl2、NaOH、Na2CO3、NaCl中的一种或几种。某化学小组为确定白色粉末的成分,进行了如下实验:
①取一定量粉末,加入足量水,振荡,得到无色透明溶液;
CuSO4、BaCl2、NaOH、Na2CO3、NaCl
不能共存
文字呈现
×
CuSO4、BaCl2、NaOH、Na2CO3、NaCl中的一种或几种。
①取一定量白色粉末,加入足量水,振荡,得到无色
透明溶液;
②取少量①的溶液,加入足量盐酸,有气泡产生。
CuSO4、BaCl2、NaOH、Na2CO3 、NaCl
文字呈现
不能共存
×
×
③另取少量①的溶液,加入足量氯化钙充分反应后再滴加无色酚酞,溶液呈无色。
×
某矿石由氧化镁、氧化铁、氧化铜和二氧化硅组成,用它制备氢氧化镁的流程示意图如图所示(已知:二氧化硅不溶于水也不与稀盐酸反应)
MgO
Fe2O3
CuO
SiO2
Mg(OH)2
MgCl2
FeCl3
CuCl2
HCl
氢氧化物 Fe(OH)3 Cu(OH)2 Mg(OH)2
开始沉淀的pH 1.5 4.2 8.6
完全沉淀的pH 3.2 6.7 11.1
Fe(OH)3
Cu(OH)2
流程图呈现
粗还原铁粉中含有Fe和少量Fe2O3、Fe3C杂质,用氢气在高温下还原可得到精还原铁粉。现测定粗还原铁粉中Fe2O3的质量和碳元素的质量分数,按如下装置进行实验:
Fe2O3
Fe3C
H2O
CH4
CH4
CO2
H2O
CO2
装置图呈现
Fe2O3+3H2 高温 2Fe+3H2O
已知:Fe3C+2H2 高温 3Fe+CH4 3CH4+4Fe2O3 高温 3CO2+6H2O+8Fe
2020/7/31
粗还原铁粉的质量为10.000g,装置B、D、E分别增重0.540g、0.270g、0.220g,计算样品中Fe2O3的质量和碳元素的质量分数(要求写计算过程)。
Fe2O3~ H2O
Fe3C~ CH4 ~ CO2 ~ C
3
装置图呈现
2020/7/31
粗还原铁粉的质量为10.000g,装置B、D、E分别增重0.540g、0.270g、0.220g,计算样品中Fe2O3的质量和碳元素的质量分数(要求写计算过程)。
Fe2O3~ H2O
Fe3C~ CH4 ~ CO2~C
3
160 54
X 0.54
X=1.6g
44 12
Y=0.06
0.22 Y
装置图呈现
从无形到有形
从有形到变形
学习、人生……从无到有的过程
从有界到无疆
仪征市大仪中学化学组 王光朝
谢 谢
