沪教版化学九年级下册第7章应用广泛的酸·碱·盐 第3节几种重要的盐 课件(共17张PPT)
文档属性
| 名称 | 沪教版化学九年级下册第7章应用广泛的酸·碱·盐 第3节几种重要的盐 课件(共17张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 30.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-08-31 00:00:00 | ||
图片预览


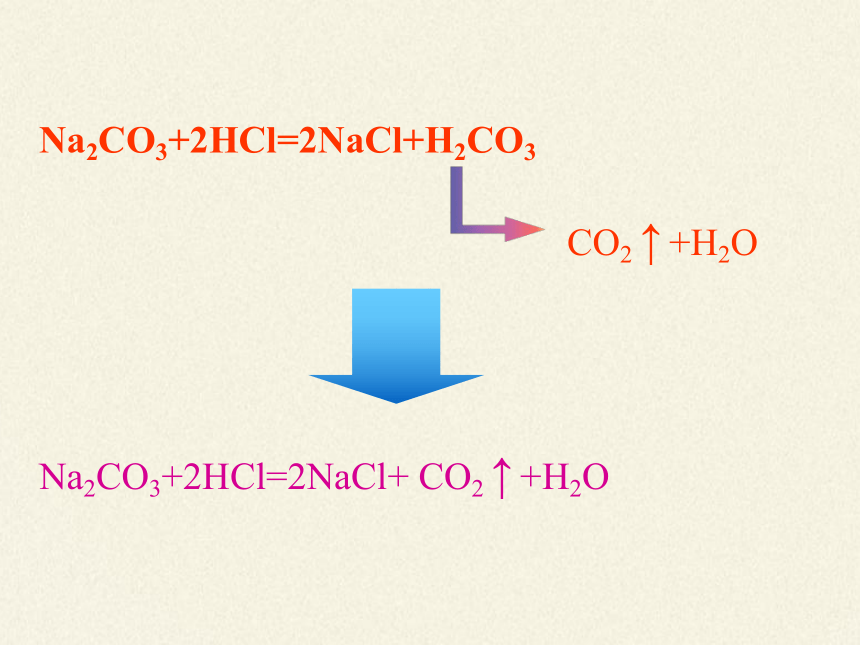
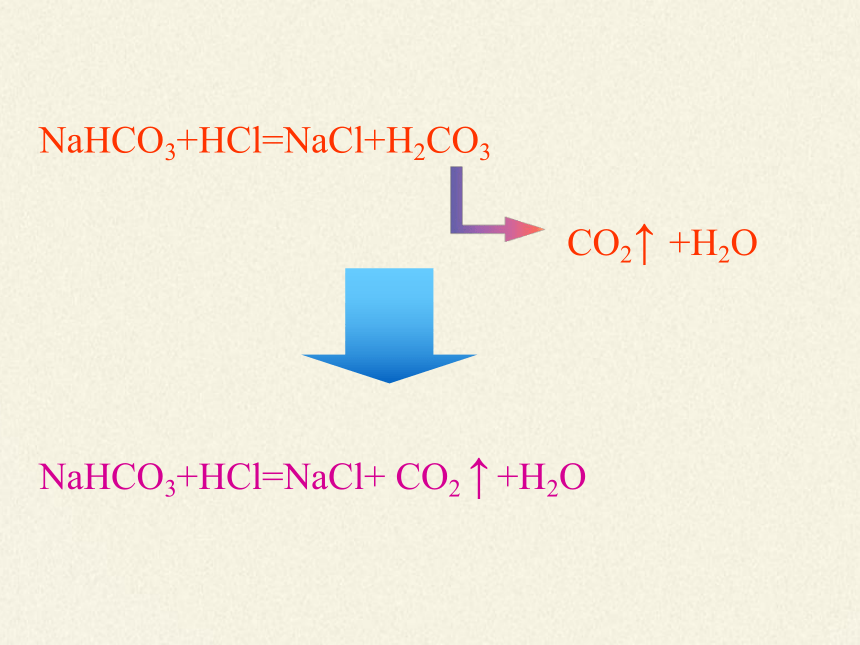
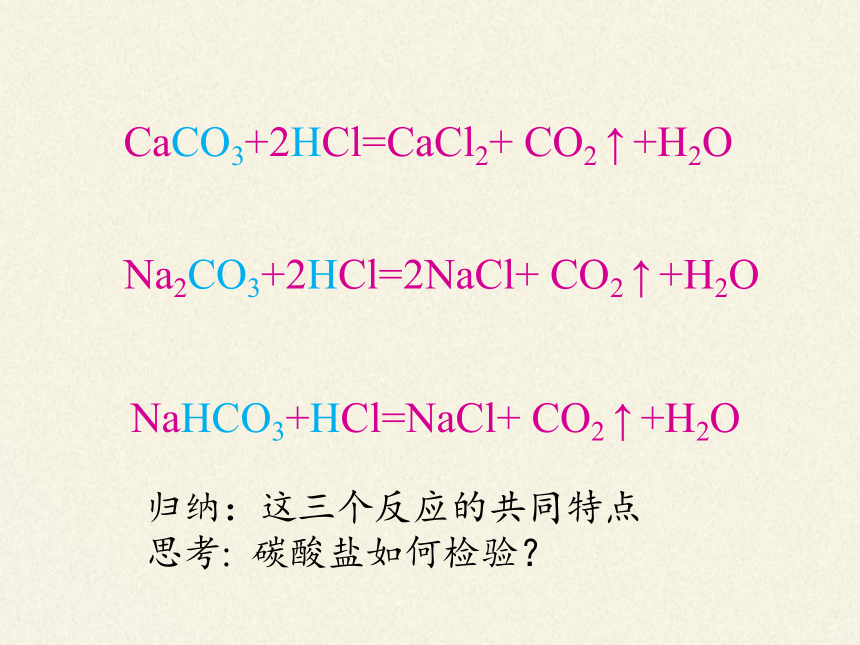

文档简介
(共17张PPT)
第3节 几种重要的盐
三、碳酸钠(Na2CO3 ) 碳酸氢钠(NaHCO3 ) 碳酸钙(CaCO3)
名 称 颜色、状态 主 要 用 途
碳酸钠 [苏打、纯碱]
碳酸氢钠 [小苏打]
碳酸钙
返回
白色、固体
白色、固体
白色、固体
发酵粉的主要成分、治疗胃酸过多的药剂
用于生产玻璃、造纸、纺织、洗涤剂
可作作补钙剂。石灰石、大理石作作建筑材料、也用于实验室制取二氧化碳
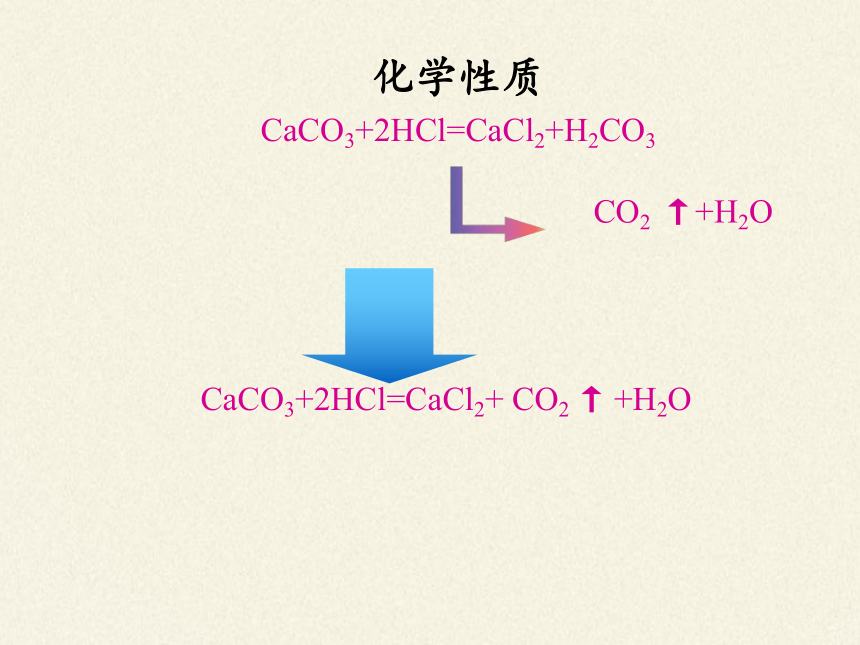
化学性质
CaCO3+2HCl=CaCl2+H2CO3
CO2 ↑+H2O
CaCO3+2HCl=CaCl2+ CO2 ↑ +H2O
Na2CO3+2HCl=2NaCl+H2CO3
CO2 ↑ +H2O
Na2CO3+2HCl=2NaCl+ CO2 ↑ +H2O
NaHCO3+HCl=NaCl+H2CO3
CO2↑ +H2O
NaHCO3+HCl=NaCl+ CO2 ↑ +H2O
归纳:这三个反应的共同特点
思考: 碳酸盐如何检验?
CaCO3+2HCl=CaCl2+ CO2 ↑ +H2O
Na2CO3+2HCl=2NaCl+ CO2 ↑ +H2O
NaHCO3+HCl=NaCl+ CO2 ↑ +H2O
碳酸盐(即CO32- 、HCO3-)的检验方法
实验操作 实验现象
实验结论
向少量样品中加入稀盐酸,将产生的气体通入澄清石灰水。 有无色气体生成,澄清石灰水变浑浊。 该样品是碳酸盐。
实验11-2 碳酸钠溶液+澄清石灰水
现象
分析
Na2CO3 + Ca(OH)2 = CaCO3 + 2NaOH
出现白色沉淀
二者发生反应,生成一种难溶物
返回
它们的性质有什么不同呢?
适宜的鉴别方法有…
1、厨房里有两瓶白色固体,一瓶是食盐,一瓶是纯碱。想想看,我们能用哪些方法鉴别它们呢?
探究思考题
探究:如何鉴别氯化钠溶液和碳酸钠溶液?
方法 实验现象、结论 原理
(用化学方程式表示)
1.
2.
3.
4.
Na2CO3+2HCl==2NaCl+H2O+CO2↑
Na2CO3+Ca(OH)2==CaCO3↓+2NaOH
酚酞试液
显红色的为碳酸钠溶液
无色的为氯化钠溶液
pH试纸
pH>7 ,碳酸钠溶液
pH=7,氯化钠溶液
稀盐酸
有大量气泡产生的是碳酸钠溶液
无明显现象的为氯化钠溶液
氢氧化钙
溶液
有白色沉淀产生的是碳酸钠溶液
无明显现象的为氯化钠溶液
它们的性质有什么不同呢?
鉴别的顺序…
2、不用其他试剂,如何区分出氯化钙溶液、氯化钠溶液、碳酸钠溶液和硫酸铜溶液?
探究思考题
1、下列物质中,全部是盐类的一组是( )
A、食盐、高锰酸钾、苏打、干冰
B、硫酸铜、纯碱、碳铵、亚硝酸钠
C、碳酸钙、烧碱、碳酸钠、食醋
D、氯化钡、硫酸、熟石灰、过氧化氢
2、为使馒头松软可口,常在揉面时加入食用碱。为了探究食用碱
的主要成分,向其中加入了稀盐酸,发现产生了一种能使澄清
的石灰水变浑浊的气体,则食用碱中可能含有 ( )
A、食盐 B、烧碱 C、纯碱 D、味精
3、食盐、食醋、纯碱均是家庭厨房中常用的物质,利用这些物
质,我能够完成的实验是 ( )
①检验自来水中是否含有氯离子;②除去热水瓶中的水垢;
③区分食盐和纯碱;④检验鸡蛋壳中是否含有碳酸钙。
A、①② B、①③ C、①④ D、②③④
学情检查:
B
C
D
4.用做鉴别碳酸根离子的试剂是 [ ]
A.稀硫酸 B.食盐水
C.石灰水 D.稀盐酸和澄清石灰水
5.在改进制碱法方面,曾做出杰出贡献的我国科学家是 [ ]
A.侯德榜 B.拉瓦锡 C.道尔顿 D.汤姆生
D
A
6、下列物质间不能发生复分解反应的是( )
A、碳酸钙和稀盐酸
B、硝酸钠溶液和氯化钾溶液
C、氯化钡溶液和硫酸钾溶液
D、氯化铁溶液和氢氧化钠溶液
8、下列化肥与碱混合后,能闻到氨气气味的是( )
A.硫酸铵 B.硫酸钾
C.氯化钠 D.硝酸钾
7、农业生产中有一种氮肥,若运输过程中受到猛烈撞击,会发生
爆炸性分解,其反应的化学方程式为:2X = 2N2↑+O2↑+4H2O,
则X的化学式是( )
A、NH3 B、NH4HCO3 C、NH3·H2O D、NH4NO3
B
D
A
9、现有下列物质:熟石灰、碳酸钠、氯化钠、碳酸钙、
碳酸氢钠、氢氧化铝、稀盐酸等在生产、生活中有广
泛的用途。
(1)请用化学式按下列要求填空:
①农业中用来降低土壤酸性,改良土壤结构的是 。
②天安门前的汉白玉华表的主要成分是 。
③用于造纸、玻璃、印染、洗涤剂的是 。
④用于维持人体正常生理活动的是 。
(2)写出符合下列要求的化学方程式:
①分解反应: 。
②复分解反应:酸与盐 。
碱与盐 。
Ca(OH)2
CaCO3
Na2CO3
NaCl
CaCO3 == CaO + CO2↑
高温
2HCl+Na2CO3 == 2NaCl+H2O+CO2↑
Ca(OH)2+Na2CO3 == CaCO3↓+2NaOH
10、下图所示:A为含三种元素的钠盐,B为食品袋中常用作干燥
剂的氧化物,C为相对分子质量为100白色不溶物,请填空:
(1)用化学式填空 A ;
B ;
C 。
(2)D中一定含有的溶质是 ;理由是(用化学方
程式表示) 。
(3)D还可能含的溶质是 。
Na2CO3
CaO
CaCO3
NaOH
CaO+H2O == Ca(OH)2、 Ca(OH)2+Na2CO3 == CaCO3↓+2NaOH
NaOH和Na2CO3或NaOH和Ca(OH)2
谢 谢
第3节 几种重要的盐
三、碳酸钠(Na2CO3 ) 碳酸氢钠(NaHCO3 ) 碳酸钙(CaCO3)
名 称 颜色、状态 主 要 用 途
碳酸钠 [苏打、纯碱]
碳酸氢钠 [小苏打]
碳酸钙
返回
白色、固体
白色、固体
白色、固体
发酵粉的主要成分、治疗胃酸过多的药剂
用于生产玻璃、造纸、纺织、洗涤剂
可作作补钙剂。石灰石、大理石作作建筑材料、也用于实验室制取二氧化碳
化学性质
CaCO3+2HCl=CaCl2+H2CO3
CO2 ↑+H2O
CaCO3+2HCl=CaCl2+ CO2 ↑ +H2O
Na2CO3+2HCl=2NaCl+H2CO3
CO2 ↑ +H2O
Na2CO3+2HCl=2NaCl+ CO2 ↑ +H2O
NaHCO3+HCl=NaCl+H2CO3
CO2↑ +H2O
NaHCO3+HCl=NaCl+ CO2 ↑ +H2O
归纳:这三个反应的共同特点
思考: 碳酸盐如何检验?
CaCO3+2HCl=CaCl2+ CO2 ↑ +H2O
Na2CO3+2HCl=2NaCl+ CO2 ↑ +H2O
NaHCO3+HCl=NaCl+ CO2 ↑ +H2O
碳酸盐(即CO32- 、HCO3-)的检验方法
实验操作 实验现象
实验结论
向少量样品中加入稀盐酸,将产生的气体通入澄清石灰水。 有无色气体生成,澄清石灰水变浑浊。 该样品是碳酸盐。
实验11-2 碳酸钠溶液+澄清石灰水
现象
分析
Na2CO3 + Ca(OH)2 = CaCO3 + 2NaOH
出现白色沉淀
二者发生反应,生成一种难溶物
返回
它们的性质有什么不同呢?
适宜的鉴别方法有…
1、厨房里有两瓶白色固体,一瓶是食盐,一瓶是纯碱。想想看,我们能用哪些方法鉴别它们呢?
探究思考题
探究:如何鉴别氯化钠溶液和碳酸钠溶液?
方法 实验现象、结论 原理
(用化学方程式表示)
1.
2.
3.
4.
Na2CO3+2HCl==2NaCl+H2O+CO2↑
Na2CO3+Ca(OH)2==CaCO3↓+2NaOH
酚酞试液
显红色的为碳酸钠溶液
无色的为氯化钠溶液
pH试纸
pH>7 ,碳酸钠溶液
pH=7,氯化钠溶液
稀盐酸
有大量气泡产生的是碳酸钠溶液
无明显现象的为氯化钠溶液
氢氧化钙
溶液
有白色沉淀产生的是碳酸钠溶液
无明显现象的为氯化钠溶液
它们的性质有什么不同呢?
鉴别的顺序…
2、不用其他试剂,如何区分出氯化钙溶液、氯化钠溶液、碳酸钠溶液和硫酸铜溶液?
探究思考题
1、下列物质中,全部是盐类的一组是( )
A、食盐、高锰酸钾、苏打、干冰
B、硫酸铜、纯碱、碳铵、亚硝酸钠
C、碳酸钙、烧碱、碳酸钠、食醋
D、氯化钡、硫酸、熟石灰、过氧化氢
2、为使馒头松软可口,常在揉面时加入食用碱。为了探究食用碱
的主要成分,向其中加入了稀盐酸,发现产生了一种能使澄清
的石灰水变浑浊的气体,则食用碱中可能含有 ( )
A、食盐 B、烧碱 C、纯碱 D、味精
3、食盐、食醋、纯碱均是家庭厨房中常用的物质,利用这些物
质,我能够完成的实验是 ( )
①检验自来水中是否含有氯离子;②除去热水瓶中的水垢;
③区分食盐和纯碱;④检验鸡蛋壳中是否含有碳酸钙。
A、①② B、①③ C、①④ D、②③④
学情检查:
B
C
D
4.用做鉴别碳酸根离子的试剂是 [ ]
A.稀硫酸 B.食盐水
C.石灰水 D.稀盐酸和澄清石灰水
5.在改进制碱法方面,曾做出杰出贡献的我国科学家是 [ ]
A.侯德榜 B.拉瓦锡 C.道尔顿 D.汤姆生
D
A
6、下列物质间不能发生复分解反应的是( )
A、碳酸钙和稀盐酸
B、硝酸钠溶液和氯化钾溶液
C、氯化钡溶液和硫酸钾溶液
D、氯化铁溶液和氢氧化钠溶液
8、下列化肥与碱混合后,能闻到氨气气味的是( )
A.硫酸铵 B.硫酸钾
C.氯化钠 D.硝酸钾
7、农业生产中有一种氮肥,若运输过程中受到猛烈撞击,会发生
爆炸性分解,其反应的化学方程式为:2X = 2N2↑+O2↑+4H2O,
则X的化学式是( )
A、NH3 B、NH4HCO3 C、NH3·H2O D、NH4NO3
B
D
A
9、现有下列物质:熟石灰、碳酸钠、氯化钠、碳酸钙、
碳酸氢钠、氢氧化铝、稀盐酸等在生产、生活中有广
泛的用途。
(1)请用化学式按下列要求填空:
①农业中用来降低土壤酸性,改良土壤结构的是 。
②天安门前的汉白玉华表的主要成分是 。
③用于造纸、玻璃、印染、洗涤剂的是 。
④用于维持人体正常生理活动的是 。
(2)写出符合下列要求的化学方程式:
①分解反应: 。
②复分解反应:酸与盐 。
碱与盐 。
Ca(OH)2
CaCO3
Na2CO3
NaCl
CaCO3 == CaO + CO2↑
高温
2HCl+Na2CO3 == 2NaCl+H2O+CO2↑
Ca(OH)2+Na2CO3 == CaCO3↓+2NaOH
10、下图所示:A为含三种元素的钠盐,B为食品袋中常用作干燥
剂的氧化物,C为相对分子质量为100白色不溶物,请填空:
(1)用化学式填空 A ;
B ;
C 。
(2)D中一定含有的溶质是 ;理由是(用化学方
程式表示) 。
(3)D还可能含的溶质是 。
Na2CO3
CaO
CaCO3
NaOH
CaO+H2O == Ca(OH)2、 Ca(OH)2+Na2CO3 == CaCO3↓+2NaOH
NaOH和Na2CO3或NaOH和Ca(OH)2
谢 谢
