沪教版化学九年级下册第7章应用广泛的酸·碱·盐基础实验8 酸与碱的化学性质课件(共11张PPT)
文档属性
| 名称 | 沪教版化学九年级下册第7章应用广泛的酸·碱·盐基础实验8 酸与碱的化学性质课件(共11张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-09-28 00:00:00 | ||
图片预览



文档简介
(共11张PPT)
基础实验8 酸与碱的化学性质
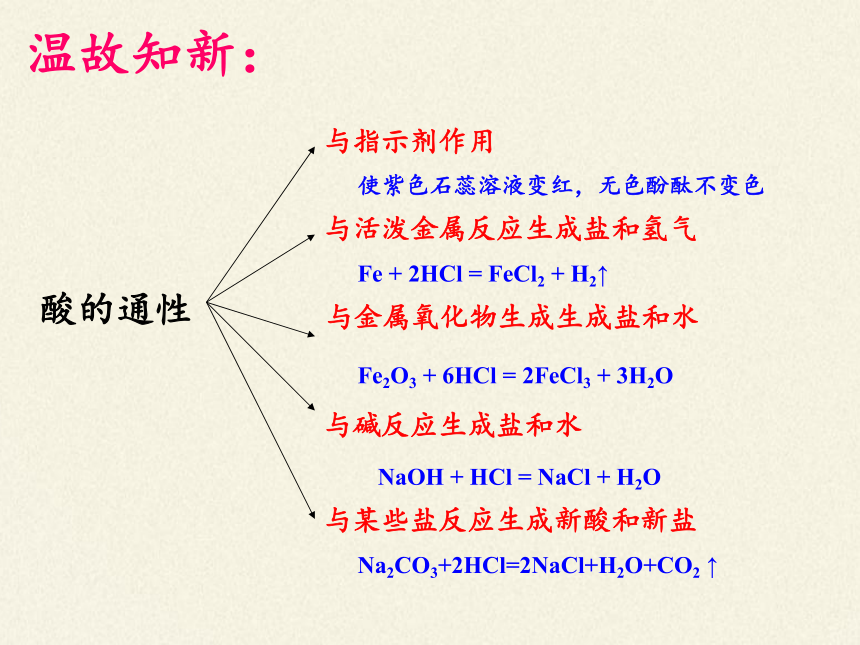
酸的通性
与指示剂作用
与活泼金属反应生成盐和氢气
与金属氧化物生成生成盐和水
与碱反应生成盐和水
与某些盐反应生成新酸和新盐
使紫色石蕊溶液变红,无色酚酞不变色
Fe + 2HCl = FeCl2 + H2↑
Fe2O3 + 6HCl = 2FeCl3 + 3H2O
NaOH + HCl = NaCl + H2O
Na2CO3+2HCl=2NaCl+H2O+CO2 ↑
温故知新:
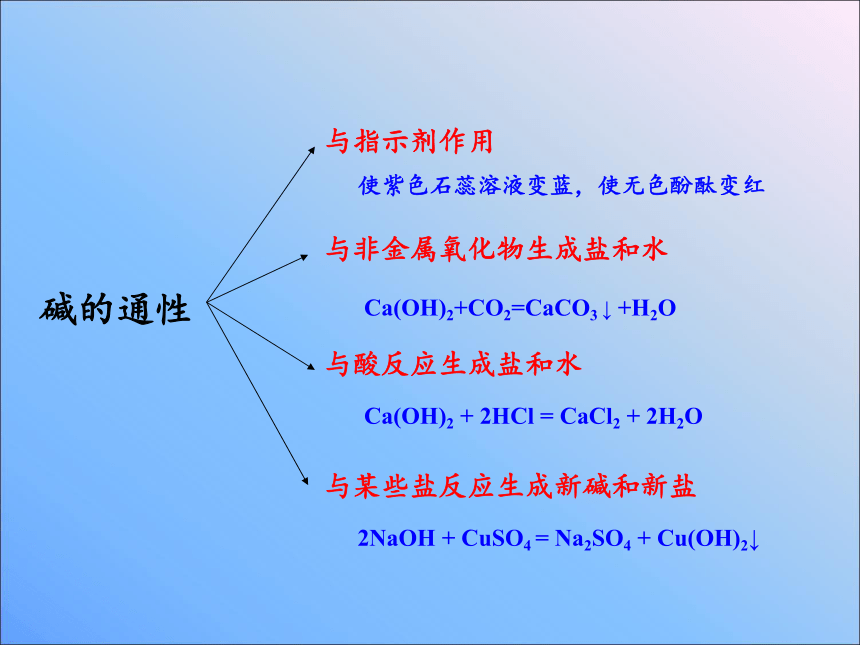
碱的通性
与指示剂作用
与非金属氧化物生成盐和水
与酸反应生成盐和水
与某些盐反应生成新碱和新盐
使紫色石蕊溶液变蓝,使无色酚酞变红
Ca(OH)2+CO2=CaCO3 ↓ +H2O
Ca(OH)2 + 2HCl = CaCl2 + 2H2O
2NaOH + CuSO4 = Na2SO4 + Cu(OH)2↓
实验目的:
1、比较常见的酸的化学性质,认识其特征;
2、认识常见碱的一些化学性质;
3、通过探究,认识酸碱中和反应。
实验用品:
稀盐酸、稀硫酸、稀氢氧化钠溶液、石灰水、镁条、锌粒、铜片、碳酸钠粉末、石灰石(或大理石)、生锈铁钉、硫酸铜溶液、蒸馏水等;
试管、镊子、药匙、烧杯、胶头滴管、玻璃棒、温度计等。
实验注意事项
酸和碱有腐蚀性,实验时应注意安全。若不小心有试剂粘在皮肤上或渐入眼睛中,应立即用大量水冲洗,严重时需紧急就医。不能触摸药品,不能尝药品的味道,不能直接闻药品的气味。实验时要不急不缓,保持心情平静,有条不紊的进行。药品没有确定用量时,按最少量原则。
(1)取三支试管,分别放入适量的镁条、锌粒和铜片,再各加入适量稀硫酸(稀盐酸),观察实验现象
(2)取一支试管,放入一枚生锈铁钉,再加入适量稀硫酸(稀盐酸),观察实验现象
(3)取两支试管,分别加入适量碳酸钠粉末、石灰石(或大理石),再各加入适量稀硫酸(稀盐酸),观察实验现象
实验过程:
1、常见酸的化学性质
2、常见碱的化学性质
取一支试管,加入2mL硫酸铜溶液,再逐滴加入石灰水(稀氢氧化钠溶液),观察实验现象
3、酸碱中和反应
(1)在小烧杯中加入适量氢氧化钠溶液,滴加2~3滴酚酞试液,插入1根温度计,测量溶液的温度
(2)用胶头滴管吸取稀盐酸逐滴加入上述小烧杯中,边加边用玻璃棒轻轻搅拌,当溶液刚好变成无色时,停止滴加盐酸,观察实验现象并测量溶液温度
(3)取实验(2)反应后的溶液少许,转移到另一试管中,再滴加1滴稀氢氧化钠溶液,观察溶液的颜色变化
实验小结:
1、常见酸的化学性质
实验过程 实验现象 实验结论
(1)取三支试管,分别放入适量的镁条、锌粒和铜片,再各加入适量稀硫酸(稀盐酸),观察实验现象
(2)取一支试管,放入一枚生锈铁钉,再加入适量稀硫酸(稀盐酸),观察实验现象
(3)取两支试管,分别加入适量碳酸钠粉末、石灰石(或大理石),再各加入适量稀硫酸(稀盐酸),观察实验现象
铁锈逐渐消失,溶液由无色变黄色
有气泡产生
镁条:剧烈反应, 产生大量气泡
锌粒:反应较剧烈,产生较多气泡
铜片:不反应
酸能与较活泼的金属反应产生氢气
酸能与金属氧化物反应生成水
酸能与某些盐反应生成新盐和新酸
2、常见碱的化学性质
实验过程 实验现象 实验结论
取一支试管,加入2mL硫酸铜溶液,再逐滴加入石灰水(稀氢氧化钠溶液),观察实验现象
产生蓝色沉淀,溶液由蓝色变为无色
碱能与某些盐反应生成新碱和新盐
3、酸碱中和反应
实验过程 实验现象 实验结论
(1)在小烧杯中加入适量氢氧化钠溶液,滴加2~3滴酚酞试液,插入1根温度计,测量溶液的温度
(2)用胶头滴管吸取稀盐酸逐滴加入上述小烧杯中,边加边用玻璃棒轻轻搅拌,当溶液刚好变成无色时,停止滴加盐酸,观察实验现象并测量溶液温度
(3)取实验(2)反应后的溶液少许,转移到另一试管中,再滴加1滴稀氢氧化钠溶液,观察溶液的颜色变化
溶液由红色变为无色,溶液温度逐渐升高
溶液由无色变为红色
溶液由无色变为红色
碱能使无色酚酞溶液变红
酸和碱恰好完全反应;中和反应是放热反应
氢氧化钠过量,溶液显碱性
1、用稀酸除去铁制品表面的铁锈,是否能将铁制品长期浸泡在酸溶液中?为什么?写出相关的化学方程式。
2、根据实验现象说明,在实验室为什么常用稀盐酸和大理石反应来制取CO2气体?
3、酸碱中和反应试验中,步骤(3)的目的是什么?
问题讨论:
谢 谢
基础实验8 酸与碱的化学性质
酸的通性
与指示剂作用
与活泼金属反应生成盐和氢气
与金属氧化物生成生成盐和水
与碱反应生成盐和水
与某些盐反应生成新酸和新盐
使紫色石蕊溶液变红,无色酚酞不变色
Fe + 2HCl = FeCl2 + H2↑
Fe2O3 + 6HCl = 2FeCl3 + 3H2O
NaOH + HCl = NaCl + H2O
Na2CO3+2HCl=2NaCl+H2O+CO2 ↑
温故知新:
碱的通性
与指示剂作用
与非金属氧化物生成盐和水
与酸反应生成盐和水
与某些盐反应生成新碱和新盐
使紫色石蕊溶液变蓝,使无色酚酞变红
Ca(OH)2+CO2=CaCO3 ↓ +H2O
Ca(OH)2 + 2HCl = CaCl2 + 2H2O
2NaOH + CuSO4 = Na2SO4 + Cu(OH)2↓
实验目的:
1、比较常见的酸的化学性质,认识其特征;
2、认识常见碱的一些化学性质;
3、通过探究,认识酸碱中和反应。
实验用品:
稀盐酸、稀硫酸、稀氢氧化钠溶液、石灰水、镁条、锌粒、铜片、碳酸钠粉末、石灰石(或大理石)、生锈铁钉、硫酸铜溶液、蒸馏水等;
试管、镊子、药匙、烧杯、胶头滴管、玻璃棒、温度计等。
实验注意事项
酸和碱有腐蚀性,实验时应注意安全。若不小心有试剂粘在皮肤上或渐入眼睛中,应立即用大量水冲洗,严重时需紧急就医。不能触摸药品,不能尝药品的味道,不能直接闻药品的气味。实验时要不急不缓,保持心情平静,有条不紊的进行。药品没有确定用量时,按最少量原则。
(1)取三支试管,分别放入适量的镁条、锌粒和铜片,再各加入适量稀硫酸(稀盐酸),观察实验现象
(2)取一支试管,放入一枚生锈铁钉,再加入适量稀硫酸(稀盐酸),观察实验现象
(3)取两支试管,分别加入适量碳酸钠粉末、石灰石(或大理石),再各加入适量稀硫酸(稀盐酸),观察实验现象
实验过程:
1、常见酸的化学性质
2、常见碱的化学性质
取一支试管,加入2mL硫酸铜溶液,再逐滴加入石灰水(稀氢氧化钠溶液),观察实验现象
3、酸碱中和反应
(1)在小烧杯中加入适量氢氧化钠溶液,滴加2~3滴酚酞试液,插入1根温度计,测量溶液的温度
(2)用胶头滴管吸取稀盐酸逐滴加入上述小烧杯中,边加边用玻璃棒轻轻搅拌,当溶液刚好变成无色时,停止滴加盐酸,观察实验现象并测量溶液温度
(3)取实验(2)反应后的溶液少许,转移到另一试管中,再滴加1滴稀氢氧化钠溶液,观察溶液的颜色变化
实验小结:
1、常见酸的化学性质
实验过程 实验现象 实验结论
(1)取三支试管,分别放入适量的镁条、锌粒和铜片,再各加入适量稀硫酸(稀盐酸),观察实验现象
(2)取一支试管,放入一枚生锈铁钉,再加入适量稀硫酸(稀盐酸),观察实验现象
(3)取两支试管,分别加入适量碳酸钠粉末、石灰石(或大理石),再各加入适量稀硫酸(稀盐酸),观察实验现象
铁锈逐渐消失,溶液由无色变黄色
有气泡产生
镁条:剧烈反应, 产生大量气泡
锌粒:反应较剧烈,产生较多气泡
铜片:不反应
酸能与较活泼的金属反应产生氢气
酸能与金属氧化物反应生成水
酸能与某些盐反应生成新盐和新酸
2、常见碱的化学性质
实验过程 实验现象 实验结论
取一支试管,加入2mL硫酸铜溶液,再逐滴加入石灰水(稀氢氧化钠溶液),观察实验现象
产生蓝色沉淀,溶液由蓝色变为无色
碱能与某些盐反应生成新碱和新盐
3、酸碱中和反应
实验过程 实验现象 实验结论
(1)在小烧杯中加入适量氢氧化钠溶液,滴加2~3滴酚酞试液,插入1根温度计,测量溶液的温度
(2)用胶头滴管吸取稀盐酸逐滴加入上述小烧杯中,边加边用玻璃棒轻轻搅拌,当溶液刚好变成无色时,停止滴加盐酸,观察实验现象并测量溶液温度
(3)取实验(2)反应后的溶液少许,转移到另一试管中,再滴加1滴稀氢氧化钠溶液,观察溶液的颜色变化
溶液由红色变为无色,溶液温度逐渐升高
溶液由无色变为红色
溶液由无色变为红色
碱能使无色酚酞溶液变红
酸和碱恰好完全反应;中和反应是放热反应
氢氧化钠过量,溶液显碱性
1、用稀酸除去铁制品表面的铁锈,是否能将铁制品长期浸泡在酸溶液中?为什么?写出相关的化学方程式。
2、根据实验现象说明,在实验室为什么常用稀盐酸和大理石反应来制取CO2气体?
3、酸碱中和反应试验中,步骤(3)的目的是什么?
问题讨论:
谢 谢
