生物人教版选择性必修3 2.2.1 动物细胞培养(共23张ppt)
文档属性
| 名称 | 生物人教版选择性必修3 2.2.1 动物细胞培养(共23张ppt) |
|
|
| 格式 | zip | ||
| 文件大小 | 6.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 生物学 | ||
| 更新时间 | 2022-10-03 00:00:00 | ||
图片预览





文档简介
(共23张PPT)
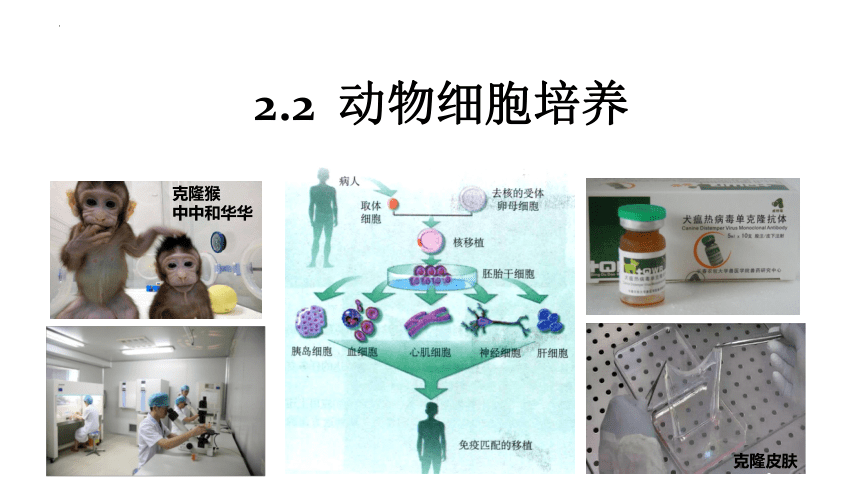
动物细胞工程(含胚胎工程)的发展历程
1890年,希普将安哥拉兔的胚胎移入比利时兔的输卵管内,得到了两只安哥拉兔,这是世界上胚胎移植成功的首例
1907年,哈里森用一滴淋巴液成功培养了蝌蚪的神经元,首创了动物组织体外培养法
1951年,张明觉等发现了哺乳动物精子的获能现象
1958年,格登用非洲爪蟾进行体细胞核移植实验,成功培育出性成熟个体,同一时期,我国科学家童第周等开展了鱼类细胞核移植工作
1959年,试管家兔诞生,之后,多种试管动物相继出生
1975年,米尔斯坦和科勒等创立了单克隆抗体技术
1978年,小鼠的桑椹胚被成功分割,次年,科学家分割绵羊胚胎获得了同卵羔羊
1981年,埃文斯等成功分离和培养了小鼠的胚胎干细胞
1996年,世界上第一只体细胞克隆羊多莉在英国诞生,随后多种克隆动物相继问世
2006年,山中伸弥等获得了诱导多能干细胞,我国科学家用这种细胞培育出了小鼠
2014年,世界上第一个用单细胞基因组测序进行遗传病筛查的试管婴儿在我国诞生
2017年,我国科学家首次培育了体细胞克隆猴
2.2 动物细胞工程
动物细胞培养
动物细胞核移植
动物细胞融合
生产单克隆抗体
其中动物细胞培养是最基础的技术。
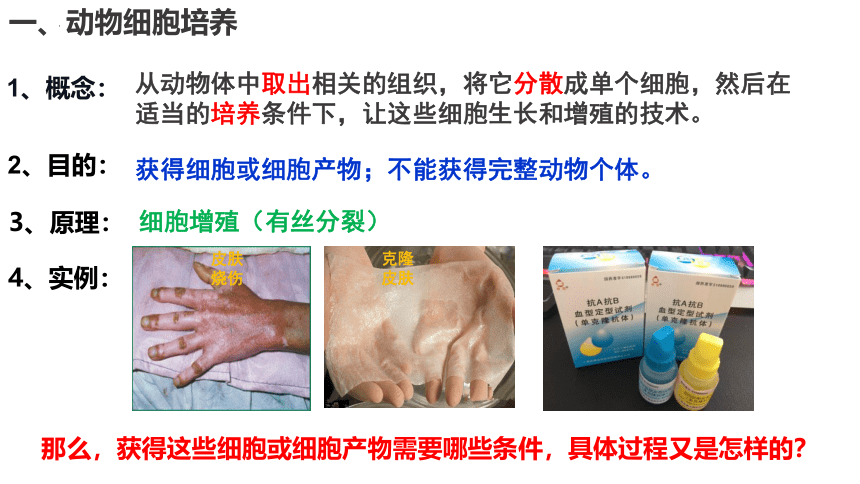
2.2 动物细胞培养
克隆猴
中中和华华
克隆皮肤
在治疗大面积烧伤时,通常采用的办法是取烧伤病人的健康皮肤进行自体移植。 但对这样的病人来说,自体健康皮肤非常有限,使用他人皮肤来源又不足,而且产生免疫排斥反应。
那么,怎样才能获得大量的自体健康皮肤?能不能用自体皮肤的单个细胞培养出可供移植的皮肤?
从社会中来
克隆皮肤
科学家通过动物细胞培养构建了人造皮肤
可以从病人身上取少量正常、健康的皮肤在体外进行培养、扩増。目前,科学家还在研究对皮肤干细胞进行培养,以获得适合临床上使用的人造皮肤。
一、动物细胞培养
1、概念:
从动物体中取出相关的组织,将它分散成单个细胞,然后在适当的培养条件下,让这些细胞生长和增殖的技术。
2、目的:
获得细胞或细胞产物;不能获得完整动物个体。
3、原理:
细胞增殖(有丝分裂)
4、实例:
那么,获得这些细胞或细胞产物需要哪些条件,具体过程又是怎样的?
克隆皮肤
皮肤烧伤
(一)、动物细胞培养的条件
1. 营养:
葡萄糖、氨基酸、无机盐、维生素、促生长因子、微量元素(合成培养基)+动物血清等
2. 无菌、无毒的环境:
①培养液和所有培养用具灭菌处理,无菌操作。
②添加一定量的抗生素?
③定期更换培养液,防止代谢物积累伤害细胞。
3. 温度、PH和渗透压:
温度36.5+0.5度,pH7.2~7.4,也需考虑渗透压因素。
4. 气体环境:
O2和CO2(95%空气和5% CO2 )
O2和CO2的作用分别是什么?
O2是细胞代谢所必需的
CO2的主要作用维持培养液的pH
为什么对动物细胞进行培养时通常要添加血清?
补充资料:
1、血清中含有蛋白质、氨基酸、葡萄糖、激素等,
2、氨基酸有多种,是细胞合成蛋白质的基本成分,其中有些氨基酸动物细胞本身不能合成(称为必需氨基酸),必须由培养液提供。
3、血清激素有胰岛素、生长激素等及多种生长因子;血清还含有多种未知的促细胞生长因子、促贴附因子及其他活性物质,能促进细胞的生长、增殖和贴附。
4、因此,细胞培养时,要保证细胞能够顺利生长和增殖,一般需添加10%~20%的血清。
血清中含有多种未知的促细胞生长因子等营养物质,这是细胞生长和增殖所必需的。
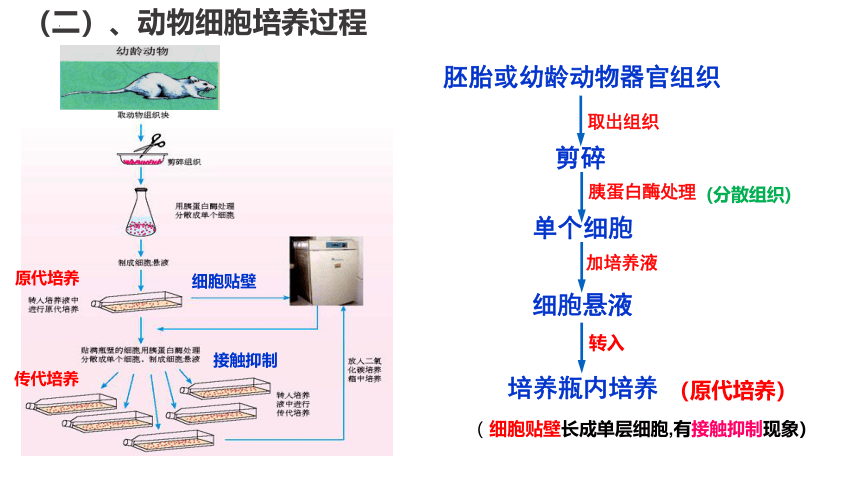
(二)、动物细胞培养过程
胚胎或幼龄动物器官组织
取出组织
剪碎
胰蛋白酶处理
单个细胞
细胞悬液
加培养液
培养瓶内培养
转入
( 细胞贴壁长成单层细胞,有接触抑制现象)
细胞贴壁
接触抑制
原代培养
传代培养
(原代培养)
(分散组织)
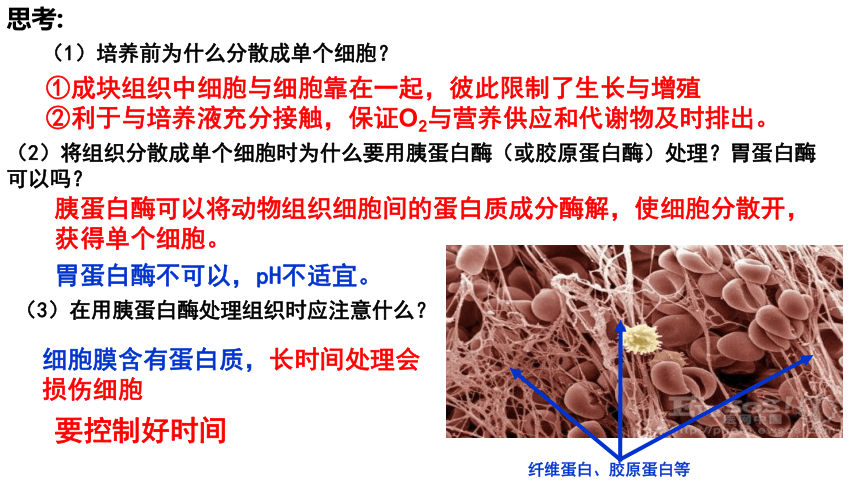
思考:
(1)培养前为什么分散成单个细胞?
①成块组织中细胞与细胞靠在一起,彼此限制了生长与增殖
②利于与培养液充分接触,保证O2与营养供应和代谢物及时排出。
(2)将组织分散成单个细胞时为什么要用胰蛋白酶(或胶原蛋白酶)处理?胃蛋白酶可以吗?
胰蛋白酶可以将动物组织细胞间的蛋白质成分酶解,使细胞分散开,获得单个细胞。
纤维蛋白、胶原蛋白等
胃蛋白酶不可以,pH不适宜。
(3)在用胰蛋白酶处理组织时应注意什么?
细胞膜含有蛋白质,长时间处理会损伤细胞
要控制好时间
原代培养——初次培养
传代培养——分瓶后的培养
拓展1:动物细胞培养过程中涉及到名词解释
1:细胞贴壁:
悬液中分散的细胞很快就贴附在瓶壁上(单层)。
要求:
培养瓶(皿)内表面光滑、无毒、易于贴附。
2:接触抑制:
当贴壁细胞分裂生长到表面相互接触时,细胞就会停止分裂增殖。
细胞的接触抑制
3:原代培养
把动物组织经处理后的初次培养统称为原代培养。
4:传代培养
将分瓶之后的细胞培养称为传代培养。
当原代培养的细胞生长停止,这时如果要使细胞继续生长,就要及时用胰蛋白酶等,使细胞从瓶壁上解离下来,然后加入新的培养液,将细胞分离稀释,并从原培养瓶内转接到新的培养瓶内的过程。
5:细胞株
从原代培养细胞群中筛选出进行传代培养的细胞,能传到40-50代,其遗传物质没有发生变化。
6:细胞系
传到40-50代后有部分细胞遗传物质发生了变化,具有癌细胞的特点,失去接触抑制,可能在培养条件下无限制的传代下去。
细胞系的遗传物质改变,具有癌细胞的特点,失去接触抑制,容易传代培养。
区别:
分瓶培养
10代细胞
50代细胞
无限增殖
保持细胞正常二倍体核型
部分细胞核型改变
遗传物质改变突破细胞寿限
危机1
危机2
(三) 动物细胞培养培养危机:
原代培养
传代培养
(遗传物质没改变)
(遗传物质有的改变)
拓展1:核型
核型是指一个体细胞中的全部染色体,按其大小、形态特征顺序排列所构成的图像。
在完全正常的情况下,一个体细胞的核型一般可代表该个体的核型。
思考·讨论 P45
1.幼龄动物的细胞与老龄动物的细胞比较,分化程度低的细胞与分化程度高的细胞比较,哪些细胞更易于培养?为什么?
细胞的增殖能力与供体的年龄有关,幼龄动物的细胞增殖能力强,有丝分裂旺盛,老龄动物的细胞则相反。所以,一般来说,幼龄动物的细胞比老龄动物的细胞易于培养。同样,分化程度越低的细胞,増殖能力越强,所以更容易培养。
动物胚胎或幼龄动物的组织、器官
细胞悬浮液
胰蛋白酶
10代细胞
50代细胞
无限传代
单个细胞
加培养液
离体的植物器官、组织或细胞
愈伤组织
根、芽
植物体
脱分化
再分化
接种至培养基
动物细胞培养
植物组织培养
思考:动物细胞培养与植物组织培养有什么相同和不同之处?
比较项目 植物组织培养 动物细胞培养
原理
培养基性质
培养基特有成分
培养结果
培养目的
获得细胞及代谢产物
细胞的全能性
细胞株、细胞系
植物体
快速繁殖、培育无病毒植株等
葡萄糖、动物血清
蔗糖、植物激素
液体培养基
固体培养基
细胞增殖
拓展2:植物组织培养和动物细胞培养的比较
二、干细胞培养及其应用
3、干细胞类型:
1、胚胎干细胞:
存在于早期胚胎中,具有分化成为成年动物体内任何一种类型的细胞,并进一步形成机体的所有组织和器官甚至个体的潜能。
2、干细胞分布:
早期胚胎、骨髓和脐带血等多种组织和器官中
胚胎干细胞
( ES细胞)
成体干细胞
全能干细胞
多能干细胞
专能干细胞
诱导多能干细胞
4、诱导多能干细胞应用
体外诱导小鼠成纤维细胞
诱导多能干细胞
iPS
临床治疗人类疾病
多种体细胞
定向诱导分化
如:白血病、帕金森病、阿而茨海默病等
人的核移植胚胎干细胞经诱导分化,形成相应的组织、器官后,可用于组织器官的移植。
干细胞将在再生医学、药物安全性与有效性检测等领域发挥大作用。
练习与应用
1.×× √ ×
2. A
拓展应用
(1)像建立骨髓库一样,有研究团队正在尝试建立HA(Human Leukocyte Antigen,人类白细胞抗原)多态性丰富的iPS细胞库,可以为需要的人找到HLA匹配度较高的iPS细胞,这样不仅可以节省时间、成本,还能减轻异体干细胞移植后发生的免疫排斥反应。
(2)该技术可能被用于治疗不孕症;获得足够量的生殖细胞来进行濒危物种的克隆研究;获得生殖细胞进行转基因操作,再经过受精、胚胎发育等过程来获得转基因动物。该技术可能带来一系列的伦理问题。例如,如果用同一个人的iPS细胞分别诱导形成精子和卵子,两者受精可能培育出“单亲”婴儿;有的人还可能有目的地选择iPS细胞,从而“设计”婴儿。
动物细胞工程(含胚胎工程)的发展历程
1890年,希普将安哥拉兔的胚胎移入比利时兔的输卵管内,得到了两只安哥拉兔,这是世界上胚胎移植成功的首例
1907年,哈里森用一滴淋巴液成功培养了蝌蚪的神经元,首创了动物组织体外培养法
1951年,张明觉等发现了哺乳动物精子的获能现象
1958年,格登用非洲爪蟾进行体细胞核移植实验,成功培育出性成熟个体,同一时期,我国科学家童第周等开展了鱼类细胞核移植工作
1959年,试管家兔诞生,之后,多种试管动物相继出生
1975年,米尔斯坦和科勒等创立了单克隆抗体技术
1978年,小鼠的桑椹胚被成功分割,次年,科学家分割绵羊胚胎获得了同卵羔羊
1981年,埃文斯等成功分离和培养了小鼠的胚胎干细胞
1996年,世界上第一只体细胞克隆羊多莉在英国诞生,随后多种克隆动物相继问世
2006年,山中伸弥等获得了诱导多能干细胞,我国科学家用这种细胞培育出了小鼠
2014年,世界上第一个用单细胞基因组测序进行遗传病筛查的试管婴儿在我国诞生
2017年,我国科学家首次培育了体细胞克隆猴
2.2 动物细胞工程
动物细胞培养
动物细胞核移植
动物细胞融合
生产单克隆抗体
其中动物细胞培养是最基础的技术。
2.2 动物细胞培养
克隆猴
中中和华华
克隆皮肤
在治疗大面积烧伤时,通常采用的办法是取烧伤病人的健康皮肤进行自体移植。 但对这样的病人来说,自体健康皮肤非常有限,使用他人皮肤来源又不足,而且产生免疫排斥反应。
那么,怎样才能获得大量的自体健康皮肤?能不能用自体皮肤的单个细胞培养出可供移植的皮肤?
从社会中来
克隆皮肤
科学家通过动物细胞培养构建了人造皮肤
可以从病人身上取少量正常、健康的皮肤在体外进行培养、扩増。目前,科学家还在研究对皮肤干细胞进行培养,以获得适合临床上使用的人造皮肤。
一、动物细胞培养
1、概念:
从动物体中取出相关的组织,将它分散成单个细胞,然后在适当的培养条件下,让这些细胞生长和增殖的技术。
2、目的:
获得细胞或细胞产物;不能获得完整动物个体。
3、原理:
细胞增殖(有丝分裂)
4、实例:
那么,获得这些细胞或细胞产物需要哪些条件,具体过程又是怎样的?
克隆皮肤
皮肤烧伤
(一)、动物细胞培养的条件
1. 营养:
葡萄糖、氨基酸、无机盐、维生素、促生长因子、微量元素(合成培养基)+动物血清等
2. 无菌、无毒的环境:
①培养液和所有培养用具灭菌处理,无菌操作。
②添加一定量的抗生素?
③定期更换培养液,防止代谢物积累伤害细胞。
3. 温度、PH和渗透压:
温度36.5+0.5度,pH7.2~7.4,也需考虑渗透压因素。
4. 气体环境:
O2和CO2(95%空气和5% CO2 )
O2和CO2的作用分别是什么?
O2是细胞代谢所必需的
CO2的主要作用维持培养液的pH
为什么对动物细胞进行培养时通常要添加血清?
补充资料:
1、血清中含有蛋白质、氨基酸、葡萄糖、激素等,
2、氨基酸有多种,是细胞合成蛋白质的基本成分,其中有些氨基酸动物细胞本身不能合成(称为必需氨基酸),必须由培养液提供。
3、血清激素有胰岛素、生长激素等及多种生长因子;血清还含有多种未知的促细胞生长因子、促贴附因子及其他活性物质,能促进细胞的生长、增殖和贴附。
4、因此,细胞培养时,要保证细胞能够顺利生长和增殖,一般需添加10%~20%的血清。
血清中含有多种未知的促细胞生长因子等营养物质,这是细胞生长和增殖所必需的。
(二)、动物细胞培养过程
胚胎或幼龄动物器官组织
取出组织
剪碎
胰蛋白酶处理
单个细胞
细胞悬液
加培养液
培养瓶内培养
转入
( 细胞贴壁长成单层细胞,有接触抑制现象)
细胞贴壁
接触抑制
原代培养
传代培养
(原代培养)
(分散组织)
思考:
(1)培养前为什么分散成单个细胞?
①成块组织中细胞与细胞靠在一起,彼此限制了生长与增殖
②利于与培养液充分接触,保证O2与营养供应和代谢物及时排出。
(2)将组织分散成单个细胞时为什么要用胰蛋白酶(或胶原蛋白酶)处理?胃蛋白酶可以吗?
胰蛋白酶可以将动物组织细胞间的蛋白质成分酶解,使细胞分散开,获得单个细胞。
纤维蛋白、胶原蛋白等
胃蛋白酶不可以,pH不适宜。
(3)在用胰蛋白酶处理组织时应注意什么?
细胞膜含有蛋白质,长时间处理会损伤细胞
要控制好时间
原代培养——初次培养
传代培养——分瓶后的培养
拓展1:动物细胞培养过程中涉及到名词解释
1:细胞贴壁:
悬液中分散的细胞很快就贴附在瓶壁上(单层)。
要求:
培养瓶(皿)内表面光滑、无毒、易于贴附。
2:接触抑制:
当贴壁细胞分裂生长到表面相互接触时,细胞就会停止分裂增殖。
细胞的接触抑制
3:原代培养
把动物组织经处理后的初次培养统称为原代培养。
4:传代培养
将分瓶之后的细胞培养称为传代培养。
当原代培养的细胞生长停止,这时如果要使细胞继续生长,就要及时用胰蛋白酶等,使细胞从瓶壁上解离下来,然后加入新的培养液,将细胞分离稀释,并从原培养瓶内转接到新的培养瓶内的过程。
5:细胞株
从原代培养细胞群中筛选出进行传代培养的细胞,能传到40-50代,其遗传物质没有发生变化。
6:细胞系
传到40-50代后有部分细胞遗传物质发生了变化,具有癌细胞的特点,失去接触抑制,可能在培养条件下无限制的传代下去。
细胞系的遗传物质改变,具有癌细胞的特点,失去接触抑制,容易传代培养。
区别:
分瓶培养
10代细胞
50代细胞
无限增殖
保持细胞正常二倍体核型
部分细胞核型改变
遗传物质改变突破细胞寿限
危机1
危机2
(三) 动物细胞培养培养危机:
原代培养
传代培养
(遗传物质没改变)
(遗传物质有的改变)
拓展1:核型
核型是指一个体细胞中的全部染色体,按其大小、形态特征顺序排列所构成的图像。
在完全正常的情况下,一个体细胞的核型一般可代表该个体的核型。
思考·讨论 P45
1.幼龄动物的细胞与老龄动物的细胞比较,分化程度低的细胞与分化程度高的细胞比较,哪些细胞更易于培养?为什么?
细胞的增殖能力与供体的年龄有关,幼龄动物的细胞增殖能力强,有丝分裂旺盛,老龄动物的细胞则相反。所以,一般来说,幼龄动物的细胞比老龄动物的细胞易于培养。同样,分化程度越低的细胞,増殖能力越强,所以更容易培养。
动物胚胎或幼龄动物的组织、器官
细胞悬浮液
胰蛋白酶
10代细胞
50代细胞
无限传代
单个细胞
加培养液
离体的植物器官、组织或细胞
愈伤组织
根、芽
植物体
脱分化
再分化
接种至培养基
动物细胞培养
植物组织培养
思考:动物细胞培养与植物组织培养有什么相同和不同之处?
比较项目 植物组织培养 动物细胞培养
原理
培养基性质
培养基特有成分
培养结果
培养目的
获得细胞及代谢产物
细胞的全能性
细胞株、细胞系
植物体
快速繁殖、培育无病毒植株等
葡萄糖、动物血清
蔗糖、植物激素
液体培养基
固体培养基
细胞增殖
拓展2:植物组织培养和动物细胞培养的比较
二、干细胞培养及其应用
3、干细胞类型:
1、胚胎干细胞:
存在于早期胚胎中,具有分化成为成年动物体内任何一种类型的细胞,并进一步形成机体的所有组织和器官甚至个体的潜能。
2、干细胞分布:
早期胚胎、骨髓和脐带血等多种组织和器官中
胚胎干细胞
( ES细胞)
成体干细胞
全能干细胞
多能干细胞
专能干细胞
诱导多能干细胞
4、诱导多能干细胞应用
体外诱导小鼠成纤维细胞
诱导多能干细胞
iPS
临床治疗人类疾病
多种体细胞
定向诱导分化
如:白血病、帕金森病、阿而茨海默病等
人的核移植胚胎干细胞经诱导分化,形成相应的组织、器官后,可用于组织器官的移植。
干细胞将在再生医学、药物安全性与有效性检测等领域发挥大作用。
练习与应用
1.×× √ ×
2. A
拓展应用
(1)像建立骨髓库一样,有研究团队正在尝试建立HA(Human Leukocyte Antigen,人类白细胞抗原)多态性丰富的iPS细胞库,可以为需要的人找到HLA匹配度较高的iPS细胞,这样不仅可以节省时间、成本,还能减轻异体干细胞移植后发生的免疫排斥反应。
(2)该技术可能被用于治疗不孕症;获得足够量的生殖细胞来进行濒危物种的克隆研究;获得生殖细胞进行转基因操作,再经过受精、胚胎发育等过程来获得转基因动物。该技术可能带来一系列的伦理问题。例如,如果用同一个人的iPS细胞分别诱导形成精子和卵子,两者受精可能培育出“单亲”婴儿;有的人还可能有目的地选择iPS细胞,从而“设计”婴儿。
