沪教版化学九年级下册 第6章 溶解现象 《溶解度及溶解度曲线》复习课教案(表格式)
文档属性
| 名称 | 沪教版化学九年级下册 第6章 溶解现象 《溶解度及溶解度曲线》复习课教案(表格式) |

|
|
| 格式 | docx | ||
| 文件大小 | 117.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-10-10 00:00:00 | ||
图片预览

文档简介
《溶解度及溶解度曲线》复习课教学设计
知识与技能:认识溶解度概念及溶解度曲线在生产生活中的应用,形成溶解度的基本概念。初步形成辨别饱和溶液与不饱和溶液和使其在一定条件下相互转化的基本技能。
过程与方法:通过引导学生思考有关溶液结晶的实际问题,增强学生科学探究意识。运用比较、分类、归纳、概括等方法,建立起知识梳理-互助巩固-互助提高-总结归纳的复习过程。养成良好的学习习惯和学习方法。
情感态度与价值观:增强学生对溶液这一生活中常见的化学现象的探究欲,发展学习化学的兴趣和善于合作、勤于思考、严谨求实、勇于创新和实践的科学精神。
教学方法:引导,比较,分类,归纳,总结。
教学过程
教学环节 教学设计内容 设计 意图
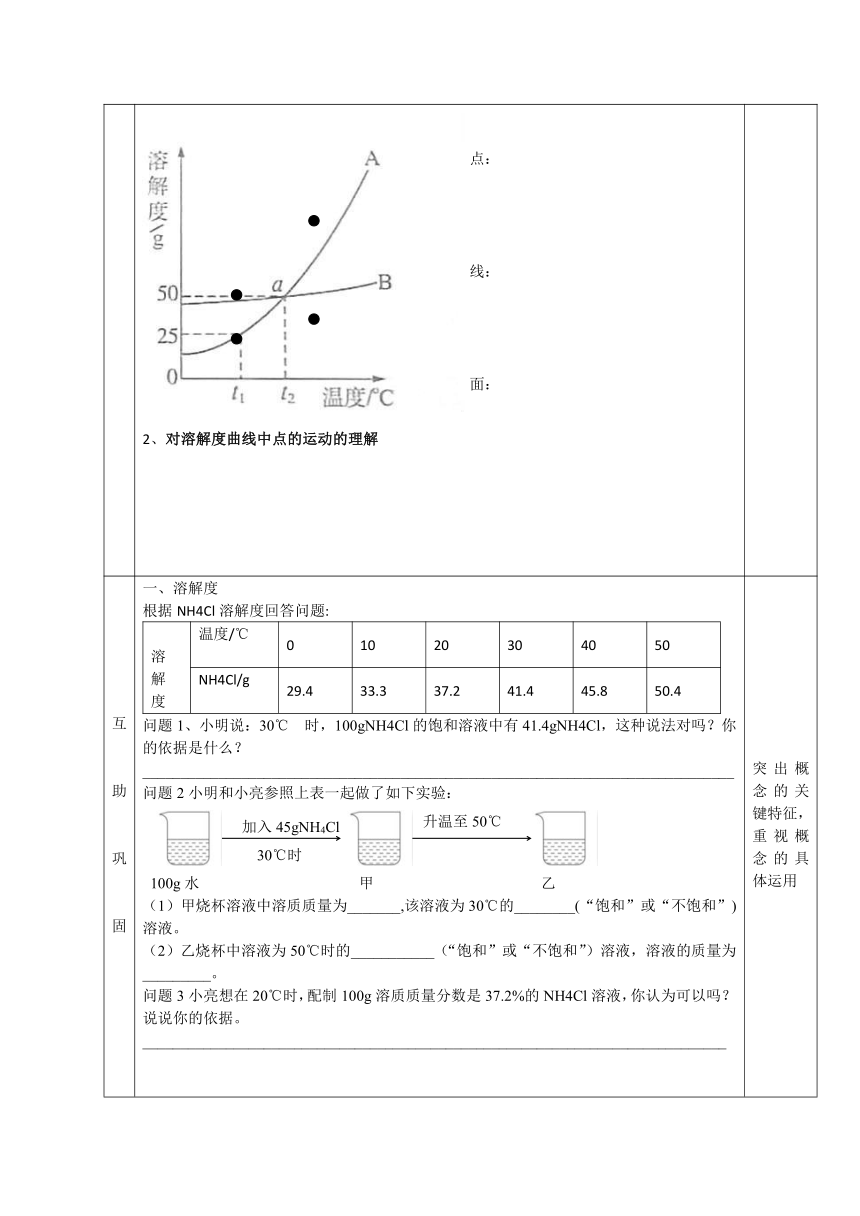
知 识 梳 理 引言:盐湖边上的人们有冬天捞碱,夏天晒盐的习惯,是什么道理呢?(学生各抒己见)本节课我们对溶解度以及溶解度曲线进行重点复习。 一 、理解溶解度概念 有关溶解度的知识点: 定义:在______下,某固态物质在_____溶剂里达到_____时所溶解的_____叫做这种物质在这种溶剂里的溶解度。 四要素: 影响固体物质溶解度的因素: 教师强调: 溶解度概念的四要素缺一不可,前两条是前提条件,第三条是状态,第四条是溶解的质量。 影响固体物质 内因:质、剂本身性质 溶解度的因素: 外因:温度 二、溶解度曲线的意义及其应用 【知识梳理】1、现有A、B两种物质的溶解度曲线,如图--1所示,由此图线可以得到哪些信息? (
点:
线:
面:
) 2、对溶解度曲线中点的运动的理解 通过学生自己重温相关知识点,突出概念的关键特征
互 助 巩 固 一、溶解度 根据NH4Cl溶解度回答问题: 溶 解 度温度/℃ 01020304050NH4Cl/g 29.433.337.241.445.850.4
问题1、小明说:30℃ 时,100gNH4Cl的饱和溶液中有41.4gNH4Cl,这种说法对吗?你的依据是什么? ______________________________________________________________________________ 问题2小明和小亮参照上表一起做了如下实验: (
加入
45gNH
4
Cl
) (
升温至
50
℃
) (
30
℃时
) 100g水 甲 乙 (1)甲烧杯溶液中溶质质量为_______,该溶液为30℃的________(“饱和”或“不饱和”)溶液。 (2)乙烧杯中溶液为50℃时的___________(“饱和”或“不饱和”)溶液,溶液的质量为_________。 问题3小亮想在20℃时,配制100g溶质质量分数是37.2%的NH4Cl溶液,你认为可以吗?说说你的依据。 _____________________________________________________________________________ 二、溶解度曲线 1、如图是甲、乙、丙三种物质的溶解度曲线,下列叙述正确的是( ) A.t2℃时,甲与丙两种物质的饱和溶液中溶质质量相同 B.t2℃时,20g丙溶解于50g水中能形成70g溶液 C.乙中混有少量甲时,应采用降温结晶的方法提纯乙 D.若要将组成在N点的甲溶液转变为M点的甲溶液, 可采取恒温蒸发溶剂的方法 2、某温度下某物质的饱和溶液,改变温度后,其溶质质量分数的变化 (
图
--2
t3
t
3
M
)根据图—2回答下列问题: ①将t1℃时A的饱和溶液,升温至t3℃,则A成为___________ (“饱和”或“不饱和”)溶液,升温后,溶液A中下列量没有 改变的是 ______________ a. 溶质质量 b. 溶剂质量 c. 溶液质量 d. 溶质质量分数 ②将t1℃时B的饱和溶液,升温至t3℃,则 B成为___________ (“饱和”或“不饱和”)溶液,升温后,溶液B中下列量没有 改变的是___________ 溶质质量 b. 溶剂质量 c. 溶液质量 d. 溶质质量分数 ③将t1℃时A、B的饱和溶液,升温至t3℃,则升温到t2℃时,溶质的质量分数A ______B, t3 ℃时A_________ B (填 “=”或“<”或“>”)。 突出概念的关键特征,重视概念的具体运用 对溶解度曲线的相关知识进行具体运用
拓 展 提 高 一、溶解度 如表是不同温度时硝酸钾的溶解度,有关说法正确的是( ) 温度/℃020406080100溶解度/克13.331.663.9110169246
A.20℃时硝酸钾的溶解度为31.6 B.40℃时,将65g硝酸钾溶于100g水中可得到165g溶液 C.100℃的水能溶解的硝酸钾一定比80℃的水能溶解的硝酸钾多 D.0℃的硝酸钾饱和溶液一定比60℃的硝酸钾饱和溶液的溶质质量分数小 突出概念的关键特征,重视概念的具体运用
直 击 中 考 溶解度曲线 如图是a、b、c三种固体物质的溶解度曲线,下列分析不正确的是( ) t2℃时a、b、c三种物质的溶解度由大到小的顺序是a>b>c t2℃时,将50g a物质放入100g 水中充分溶解得到 a的 饱和溶液(a物质不含结晶水) 将t2℃时a、b、c三种物质的饱和溶液降温到t1℃时, 所得溶液的溶质质量分数关系是 b>a=c 将 c的饱和溶液变为不饱和溶液,可采用降温的方法 明析中考考点,进行针对性练习。
课 后作业 1、硫酸镁在工农业以及医疗上有广泛应用,其溶解度如表所示.则下列说法正确的是 ( ) 温度/℃1030507090溶解度/g27.739.349.054.151.1
A.硫酸镁的溶解度随温度升高而增大 B.10℃时,27.7g硫酸镁和72.3g水可配制成质量分数为27.7%的硫酸镁溶液 C.50℃时,100g的硫酸镁饱和溶液中溶质和溶剂的质量比为49:100 D.70℃时的硫酸镁饱和溶液升温至90℃,溶液的溶质质量分数增大 2、如图是甲、乙两种固体物质(不含结晶水)的溶解度曲线,下列说法正确的是( ) A.甲的溶解度大于乙的溶解度 B.a1℃时,甲、乙的饱和溶液升温至a2℃时,均有固体析出 C.a2℃时,M点对应的甲溶液不饱和 D.a2℃时,乙饱和溶液的质量分数为20% 3、两个烧杯中分别盛装X、Y的饱和溶液,两只试管中分别装有NaOH和NH4NO3固体,向两只试管中分别滴加适量水,现象如图一所示,结合图二判断下列说法正确的是( ) A.Y的溶解度曲线为b曲线 B.降温可使X的饱和溶液变浑浊 C.X的饱和溶液从t2℃降温到t1℃,溶质的质量分数变大 D.t3℃时,X、Y的饱和溶液质量相等,则溶剂质量X>Y 4、处理图表信息是学习的一种重要方法。下表是氯化钠和硝酸钾在不同温度下的溶解度。 温度/℃20406080溶解度/gNaCl36.036.637.338.4KNO331.663.9110169
这两种固体物质在水中的溶解度曲线如右图所示: 请仔细阅读图表后回答下列问题: (1)A曲线表示的是______的溶解度曲线。(填“NaCl”或“KNO3”) (2)P点的含义是___________________________________ 。 (3)t2℃时,将等质量的A和B的饱和溶液降温至t1℃,所得 溶液的质量大小关系是A__________B。(填“<”、“>”或“=”) 对所复习的相关知识进一步巩固练习。
板书设计 溶解度及溶解度曲线 (复习课) 溶解度 二、溶解度曲线 定义 1、点: 四要素 线: 影响固体物质溶解度的因素 面: 2、由曲线总结溶液饱和状态的转变 能够清晰的呈现本节课复习的重点。
教 学 反 思 得意之处:通过引导学生思考“冬天捞碱,夏天晒盐”的实际问题,增强学生科学探究意识。运用比较、分类、归纳、概括等方法,建立起提出问题-初步探究-获取知识-实践运用的科学探究基本过程。养成良好的学习习惯和学习方法。在整节课中增强了学生对溶液这一生活中常见的化学现象的探究欲,发展学习化学的兴趣和善于合作、勤于思考、严谨求实、勇于创新和实践的科学精神。 2、不足之处:在知识的形成和发展过程中,为学生的个性特长和才能的发挥架设平台不够明显,虽然在意图上想让每个学生都能在不同程度上享受成功,但从课堂反馈看,有个别学生还是未享受到成功的喜悦,培养学生科学态度及获取科学方法有效途径还要加强。自主、合作、探究的学习方式还应突出,非智力因素的开发也要加强,比如应该将激励性语言贯穿课堂始终,挖掘学生内在潜能,使他们在科学知识的探求上乐此不疲。通过反馈小测得知,有一小部分的同学没能达到预期的学习目标,面对变式习题,还是表现出束手无策。说明自己在教学设计上没能充分考虑到学困生的能力问题,今后还要加强分层次教学,使分层次教学体现出实效性,真正面向全体学生,提高课堂吸收率。
知识与技能:认识溶解度概念及溶解度曲线在生产生活中的应用,形成溶解度的基本概念。初步形成辨别饱和溶液与不饱和溶液和使其在一定条件下相互转化的基本技能。
过程与方法:通过引导学生思考有关溶液结晶的实际问题,增强学生科学探究意识。运用比较、分类、归纳、概括等方法,建立起知识梳理-互助巩固-互助提高-总结归纳的复习过程。养成良好的学习习惯和学习方法。
情感态度与价值观:增强学生对溶液这一生活中常见的化学现象的探究欲,发展学习化学的兴趣和善于合作、勤于思考、严谨求实、勇于创新和实践的科学精神。
教学方法:引导,比较,分类,归纳,总结。
教学过程
教学环节 教学设计内容 设计 意图
知 识 梳 理 引言:盐湖边上的人们有冬天捞碱,夏天晒盐的习惯,是什么道理呢?(学生各抒己见)本节课我们对溶解度以及溶解度曲线进行重点复习。 一 、理解溶解度概念 有关溶解度的知识点: 定义:在______下,某固态物质在_____溶剂里达到_____时所溶解的_____叫做这种物质在这种溶剂里的溶解度。 四要素: 影响固体物质溶解度的因素: 教师强调: 溶解度概念的四要素缺一不可,前两条是前提条件,第三条是状态,第四条是溶解的质量。 影响固体物质 内因:质、剂本身性质 溶解度的因素: 外因:温度 二、溶解度曲线的意义及其应用 【知识梳理】1、现有A、B两种物质的溶解度曲线,如图--1所示,由此图线可以得到哪些信息? (
点:
线:
面:
) 2、对溶解度曲线中点的运动的理解 通过学生自己重温相关知识点,突出概念的关键特征
互 助 巩 固 一、溶解度 根据NH4Cl溶解度回答问题: 溶 解 度温度/℃ 01020304050NH4Cl/g 29.433.337.241.445.850.4
问题1、小明说:30℃ 时,100gNH4Cl的饱和溶液中有41.4gNH4Cl,这种说法对吗?你的依据是什么? ______________________________________________________________________________ 问题2小明和小亮参照上表一起做了如下实验: (
加入
45gNH
4
Cl
) (
升温至
50
℃
) (
30
℃时
) 100g水 甲 乙 (1)甲烧杯溶液中溶质质量为_______,该溶液为30℃的________(“饱和”或“不饱和”)溶液。 (2)乙烧杯中溶液为50℃时的___________(“饱和”或“不饱和”)溶液,溶液的质量为_________。 问题3小亮想在20℃时,配制100g溶质质量分数是37.2%的NH4Cl溶液,你认为可以吗?说说你的依据。 _____________________________________________________________________________ 二、溶解度曲线 1、如图是甲、乙、丙三种物质的溶解度曲线,下列叙述正确的是( ) A.t2℃时,甲与丙两种物质的饱和溶液中溶质质量相同 B.t2℃时,20g丙溶解于50g水中能形成70g溶液 C.乙中混有少量甲时,应采用降温结晶的方法提纯乙 D.若要将组成在N点的甲溶液转变为M点的甲溶液, 可采取恒温蒸发溶剂的方法 2、某温度下某物质的饱和溶液,改变温度后,其溶质质量分数的变化 (
图
--2
t3
t
3
M
)根据图—2回答下列问题: ①将t1℃时A的饱和溶液,升温至t3℃,则A成为___________ (“饱和”或“不饱和”)溶液,升温后,溶液A中下列量没有 改变的是 ______________ a. 溶质质量 b. 溶剂质量 c. 溶液质量 d. 溶质质量分数 ②将t1℃时B的饱和溶液,升温至t3℃,则 B成为___________ (“饱和”或“不饱和”)溶液,升温后,溶液B中下列量没有 改变的是___________ 溶质质量 b. 溶剂质量 c. 溶液质量 d. 溶质质量分数 ③将t1℃时A、B的饱和溶液,升温至t3℃,则升温到t2℃时,溶质的质量分数A ______B, t3 ℃时A_________ B (填 “=”或“<”或“>”)。 突出概念的关键特征,重视概念的具体运用 对溶解度曲线的相关知识进行具体运用
拓 展 提 高 一、溶解度 如表是不同温度时硝酸钾的溶解度,有关说法正确的是( ) 温度/℃020406080100溶解度/克13.331.663.9110169246
A.20℃时硝酸钾的溶解度为31.6 B.40℃时,将65g硝酸钾溶于100g水中可得到165g溶液 C.100℃的水能溶解的硝酸钾一定比80℃的水能溶解的硝酸钾多 D.0℃的硝酸钾饱和溶液一定比60℃的硝酸钾饱和溶液的溶质质量分数小 突出概念的关键特征,重视概念的具体运用
直 击 中 考 溶解度曲线 如图是a、b、c三种固体物质的溶解度曲线,下列分析不正确的是( ) t2℃时a、b、c三种物质的溶解度由大到小的顺序是a>b>c t2℃时,将50g a物质放入100g 水中充分溶解得到 a的 饱和溶液(a物质不含结晶水) 将t2℃时a、b、c三种物质的饱和溶液降温到t1℃时, 所得溶液的溶质质量分数关系是 b>a=c 将 c的饱和溶液变为不饱和溶液,可采用降温的方法 明析中考考点,进行针对性练习。
课 后作业 1、硫酸镁在工农业以及医疗上有广泛应用,其溶解度如表所示.则下列说法正确的是 ( ) 温度/℃1030507090溶解度/g27.739.349.054.151.1
A.硫酸镁的溶解度随温度升高而增大 B.10℃时,27.7g硫酸镁和72.3g水可配制成质量分数为27.7%的硫酸镁溶液 C.50℃时,100g的硫酸镁饱和溶液中溶质和溶剂的质量比为49:100 D.70℃时的硫酸镁饱和溶液升温至90℃,溶液的溶质质量分数增大 2、如图是甲、乙两种固体物质(不含结晶水)的溶解度曲线,下列说法正确的是( ) A.甲的溶解度大于乙的溶解度 B.a1℃时,甲、乙的饱和溶液升温至a2℃时,均有固体析出 C.a2℃时,M点对应的甲溶液不饱和 D.a2℃时,乙饱和溶液的质量分数为20% 3、两个烧杯中分别盛装X、Y的饱和溶液,两只试管中分别装有NaOH和NH4NO3固体,向两只试管中分别滴加适量水,现象如图一所示,结合图二判断下列说法正确的是( ) A.Y的溶解度曲线为b曲线 B.降温可使X的饱和溶液变浑浊 C.X的饱和溶液从t2℃降温到t1℃,溶质的质量分数变大 D.t3℃时,X、Y的饱和溶液质量相等,则溶剂质量X>Y 4、处理图表信息是学习的一种重要方法。下表是氯化钠和硝酸钾在不同温度下的溶解度。 温度/℃20406080溶解度/gNaCl36.036.637.338.4KNO331.663.9110169
这两种固体物质在水中的溶解度曲线如右图所示: 请仔细阅读图表后回答下列问题: (1)A曲线表示的是______的溶解度曲线。(填“NaCl”或“KNO3”) (2)P点的含义是___________________________________ 。 (3)t2℃时,将等质量的A和B的饱和溶液降温至t1℃,所得 溶液的质量大小关系是A__________B。(填“<”、“>”或“=”) 对所复习的相关知识进一步巩固练习。
板书设计 溶解度及溶解度曲线 (复习课) 溶解度 二、溶解度曲线 定义 1、点: 四要素 线: 影响固体物质溶解度的因素 面: 2、由曲线总结溶液饱和状态的转变 能够清晰的呈现本节课复习的重点。
教 学 反 思 得意之处:通过引导学生思考“冬天捞碱,夏天晒盐”的实际问题,增强学生科学探究意识。运用比较、分类、归纳、概括等方法,建立起提出问题-初步探究-获取知识-实践运用的科学探究基本过程。养成良好的学习习惯和学习方法。在整节课中增强了学生对溶液这一生活中常见的化学现象的探究欲,发展学习化学的兴趣和善于合作、勤于思考、严谨求实、勇于创新和实践的科学精神。 2、不足之处:在知识的形成和发展过程中,为学生的个性特长和才能的发挥架设平台不够明显,虽然在意图上想让每个学生都能在不同程度上享受成功,但从课堂反馈看,有个别学生还是未享受到成功的喜悦,培养学生科学态度及获取科学方法有效途径还要加强。自主、合作、探究的学习方式还应突出,非智力因素的开发也要加强,比如应该将激励性语言贯穿课堂始终,挖掘学生内在潜能,使他们在科学知识的探求上乐此不疲。通过反馈小测得知,有一小部分的同学没能达到预期的学习目标,面对变式习题,还是表现出束手无策。说明自己在教学设计上没能充分考虑到学困生的能力问题,今后还要加强分层次教学,使分层次教学体现出实效性,真正面向全体学生,提高课堂吸收率。
