第7章应用广泛的酸、碱、盐测试题九年级化学沪教版(全国)下册(含答案)
文档属性
| 名称 | 第7章应用广泛的酸、碱、盐测试题九年级化学沪教版(全国)下册(含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 149.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-12-19 00:00:00 | ||
图片预览



文档简介
第7章应用广泛的酸、碱、盐测试题 九年级化学沪教版(全国)下册
一、单选题
1.物质的性质决定其用途。固体氢氧化钠可用作干燥剂,是利用了它的哪种性质( )
A.白色固体
B.吸水性
C.腐蚀性
D.能与空气中的二氧化碳反应
2.下表为四种食物的近似pH,你认为胃酸过多的患者不宜多吃的食物是( )
食物 苹果汁 豆浆 玉米粥 鸡蛋清
pH 2.9-3.3 7.4-7.9 6.8-8.0 7.6-8.0
A.苹果汁 B.豆浆 C.玉米粥 D.鸡蛋清
3.下列能使紫色石蕊试液和无色酚酞试液均变色的是
A.pH=1的盐酸
B.pH=3的硫酸
C.pH=7的氯化钠溶液
D.pH=14的氢氧化钾溶液
4.关于复分解反应说法一定正确的是( )
A.反应物为酸和碱 B.伴随有明显现象
C.生成物为盐和水 D.元素化合价不变
5.下列有关盐的用途的说法错误的是
A.氯化钠是重要的调味品
B.可用亚硝酸钠代替食盐腌渍食品
C.小苏打可用于培制糕点
D.碳酸钾可用作化学肥料
6.某校化学小组在利用硫酸和氢氧化钾溶液探究酸碱中和反应时,利用数字化传感器测得烧杯中溶液pH的变化图象如图所示.下列说法正确的是
A.图中c点所示溶液呈碱性
B.图中a点所示溶液中,含有的溶质是K2SO4和H2SO4
C.该实验是将氢氧化钾溶液逐滴滴入到盛有硫酸的烧杯中
D.由b点到c点的变化过程中没有发生化学反应
7.有X、Y、Z三种金属,X在常温下就能与氧气反应,Y、Z在常温下几乎不与氧气反应;如果把Y和Z分别放入硝酸银溶液中,过一会儿,在Z表面有银析出,而Y没有变化。根据以上实验事实,判断X、Y、Z三种金属的活动性由强到弱的顺序正确的是
A.X、Y、Z B.X、Z、Y
C.Y、Z、X D.Z、Y、X
8.下列方法中,能达到目的是
选项 物质(括号内为杂质) 除去杂质的方法
A CuSO4溶液(H2SO4) 加足量铜粉,过滤
B CaO(CaCO3) 加足量水溶解、过滤
C CO2(CO) 点燃
D FeC12溶液(CuCl2) 加入过量铁粉,过滤
A.A B.B C.C D.D
9.硝酸铵(NH4NO3)是一种高效化肥,它属于
A.氮肥 B.磷肥 C.钾肥 D.复合肥
10.将质量相等的A、B、C三种金属,同时分别放入三份溶质质量分数相同且足量的稀盐酸中,反应生成H2的质量与反应时间的关系如图所示.根据图中所提供的信息,得出的结论正确的是(已知:A、B、C在生成物中均为+2价)
A.放出H2的质量是B>A>C
B.金属活动性顺序是A>B>C
C.反应速率最大的是A
D.相对原子质量是C>B>A
11.现有盐酸和CaCl2的混合溶液,向其中加入过量某物质X,溶液的pH随加入X的量的变化关系如图所示。则X是
A.石灰石 B.熟石灰 C.纯碱 D.烧碱
二、简答题
12.生活用品中蕴含着丰富的化学知识。
用品 管道通 石灰乳
有效成分 NaOH Ca(OH)2
(1)管道通在使用时禁止与皮肤接触,其原因是_____。
(2)使用石灰乳抹墙,一段时间后变硬的原因_____(用化学方程式回答)。
13.怎样鉴别石灰水和氢氧化钠溶液?
14.向一定量硝酸银、硝酸铜和硝酸亚铁的混合溶液中加入锌粉,充分反应后所得溶液的质量与加入锌粉的质量关系如图。
(1)写出ab段发生反应的化学方程式______。
(2)cd段溶液质量为什么增大______?
(3)e点得到的固体中有什么物质______?
三、推断题
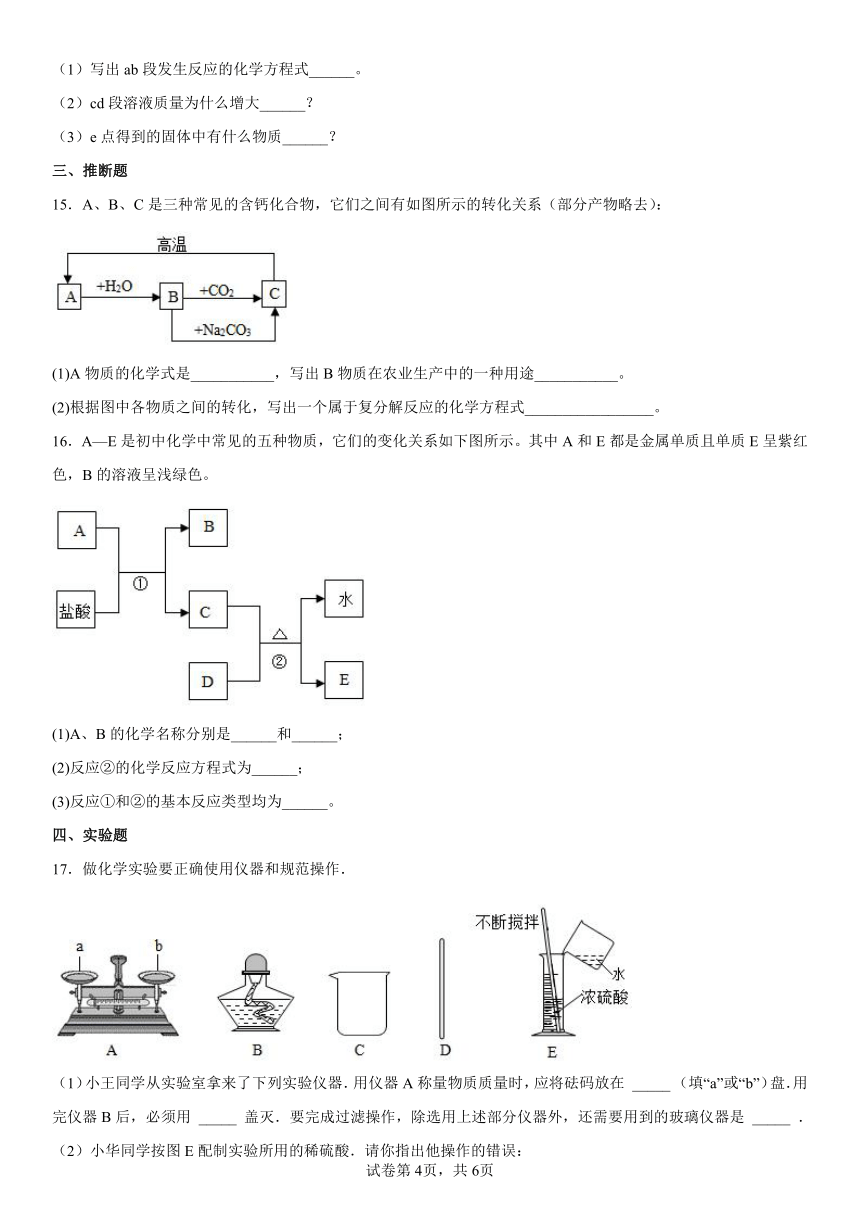
15.A、B、C是三种常见的含钙化合物,它们之间有如图所示的转化关系(部分产物略去):
(1)A物质的化学式是___________,写出B物质在农业生产中的一种用途___________。
(2)根据图中各物质之间的转化,写出一个属于复分解反应的化学方程式_________________。
16.A—E是初中化学中常见的五种物质,它们的变化关系如下图所示。其中A和E都是金属单质且单质E呈紫红色,B的溶液呈浅绿色。
(1)A、B的化学名称分别是______和______;
(2)反应②的化学反应方程式为______;
(3)反应①和②的基本反应类型均为______。
四、实验题
17.做化学实验要正确使用仪器和规范操作.
(1)小王同学从实验室拿来了下列实验仪器.用仪器A称量物质质量时,应将砝码放在 _____ (填“a”或“b”)盘.用完仪器B后,必须用 _____ 盖灭.要完成过滤操作,除选用上述部分仪器外,还需要用到的玻璃仪器是 _____ .
(2)小华同学按图E配制实验所用的稀硫酸.请你指出他操作的错误:
错误① _____ ;错误② _____ .
18.化学课堂上老师演示了如图所示的几个实验:
(1)上述实验中出现的现象,与CO2的物理性质和化学性质都有关的是:______(填序号);
(2)图A所示实验中,紫色干花(用石蕊溶液浸泡过)最终会变红,原因是:______(用化学方程式解释);
(3)图C所示实验中,经振荡后可观察到的实验现象有______(填序号).
①软塑料瓶变瘪 ②瓶内生成了白色的碳酸钙
③瓶内澄清石灰水变浑浊 ④瓶内溶液变红.
19.实验室部分装置如图所示,回答下列问题:
(1)仪器X的名称是________。
(2)实验室常用氯化铵固体与碱石灰固体共热来制取氨气(NH3),其发生装置为____。NH3是一种碱性气体,干燥时不能选用下列干燥剂中的______(填序号)。
A.氢氧化钠固体 B.浓硫酸 C.生石灰
(3)实验室用装置B制O2的化学方程式为_______。
(4)某同学欲用活泼金属单质和稀盐酸反应制取纯净干燥的H2,请从这些装置中选择并连接成一套组合装置,按照气流从左到右的流向,写出所选装置接口的连接顺序:______→______→______→______→______→______→______
五、计算题
20.计算6.5g锌粉与足量稀硫酸完全反应时,产生氢气的质量,并写出具体计算过程。
21.现有碳酸钠和氯化钠的混合物样品12.5g,将其放入干净的烧杯中,加100g水,使其完全溶解。向所得溶液中加入溶质质量分数为7.3%的稀盐酸,烧杯中溶液的质量与加入稀盐酸的质量关系曲线如图所示。请回答下列问题。
(1)在碳酸钠和氯化钠的混合物样品中,含碳酸钠的质量为______(结果精确至 0.1g)
(2)A点时,求此温度下所得不饱和溶液中溶质质量分数______(写出具体计算过程,计算结果精确至0.1%)。
22.某化肥厂生产的一种化肥包装袋上的说明如图所示,化学兴趣小组为测定其纯度,取样品5.6克,完全溶于水,向所得溶液中加入100克一定溶质质量分数的硝酸银溶液,恰好完全反应生成14.35克沉淀(杂质不与硝酸银溶液反应)。通过计算回答。
氯化铵净重25Kg 纯度≥95% XX化肥有限责任公司
(1)所用硝酸银溶液的溶质质量分数;_____。
(2)该化肥是否合格(结果精确到0.1%)。_____。
23.某纯碱样品中含有少量氯化钠杂质。称取该样品22.8g,加入到盛有一定质量稀盐酸的烧杯中,碳酸钠与稀盐酸恰好完全反应,气体完全逸出,得到不饱和NaCl溶液。反应过程中测得烧杯内混合物的质量(m)与反应时间(t)关系如图所示。试回答:
(1)生成CO2的质量_____。
(2)22.8g样品中氯化钠的质量为_____。
(3)计算所得溶液中溶质的质量分数_________。(写出解题过程,计算结果精确到0.1%)
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.B
2.A
3.D
4.D
5.B
6.D
7.B
8.D
9.A
10.D
11.C
12. 氢氧化钠具有强烈的腐蚀性 Ca(OH)2+CO2═CaCO3↓+H2O
13.取少量溶液于试管中,加入适量碳酸钠溶液,产生白色沉淀,则是石灰水,无明显现象,则是氢氧化钠溶液。
14. Zn+2AgNO3=Zn(NO3)2+2Ag 锌和硝酸亚铁反应生成硝酸锌和铁 锌、银、铜、铁
15.(1) CaO 中和酸性土壤
(2)Ca(OH)2+Na2CO3=CaCO3↓+2NaOH
16.(1) 铁 氯化亚铁
(2)CuO+H2Cu+H2O或Cu2O+H22Cu+H2O;
(3)置换反应
17. b 灯帽 漏斗 将水倒入浓硫酸中 在量筒中配制溶液
18. B H2O+CO2=H2CO3 ①③
19.(1)酒精灯
(2) A B
(3)
(4) b f e h g d c
20.解:设产生氢气的质量为x
x=0.2g
答:产生氢气的质量为0.2g。
21.(1)10.6g(2)6.5
22.解:设硝酸银的质量为x,氯化铵质量为y。
x=17g
y=5.35g
所用硝酸银溶液的溶质质量分数
样品的纯度为
故填:17%,合格
23.(1)由图象和质量守恒定律可知,生成二氧化碳的质量为:178.8g﹣170.0g=8.8g;
(2)设碳酸钠的质量为x,生成氯化钠的质量为y,
解得:x=21.2g,y=23.4g,
22.8g样品中氯化钠的质量为:22.8g﹣21.2g=1.6g
(3)完全反应后所得氯化钠溶液的溶质质量分数14.7%
故答为:(1)8.8;
(2)22.8g样品中氯化钠的质量为1.6g;
(3)所得溶液中溶质的质量分数为14.7%。
答案第1页,共2页
答案第1页,共2页
一、单选题
1.物质的性质决定其用途。固体氢氧化钠可用作干燥剂,是利用了它的哪种性质( )
A.白色固体
B.吸水性
C.腐蚀性
D.能与空气中的二氧化碳反应
2.下表为四种食物的近似pH,你认为胃酸过多的患者不宜多吃的食物是( )
食物 苹果汁 豆浆 玉米粥 鸡蛋清
pH 2.9-3.3 7.4-7.9 6.8-8.0 7.6-8.0
A.苹果汁 B.豆浆 C.玉米粥 D.鸡蛋清
3.下列能使紫色石蕊试液和无色酚酞试液均变色的是
A.pH=1的盐酸
B.pH=3的硫酸
C.pH=7的氯化钠溶液
D.pH=14的氢氧化钾溶液
4.关于复分解反应说法一定正确的是( )
A.反应物为酸和碱 B.伴随有明显现象
C.生成物为盐和水 D.元素化合价不变
5.下列有关盐的用途的说法错误的是
A.氯化钠是重要的调味品
B.可用亚硝酸钠代替食盐腌渍食品
C.小苏打可用于培制糕点
D.碳酸钾可用作化学肥料
6.某校化学小组在利用硫酸和氢氧化钾溶液探究酸碱中和反应时,利用数字化传感器测得烧杯中溶液pH的变化图象如图所示.下列说法正确的是
A.图中c点所示溶液呈碱性
B.图中a点所示溶液中,含有的溶质是K2SO4和H2SO4
C.该实验是将氢氧化钾溶液逐滴滴入到盛有硫酸的烧杯中
D.由b点到c点的变化过程中没有发生化学反应
7.有X、Y、Z三种金属,X在常温下就能与氧气反应,Y、Z在常温下几乎不与氧气反应;如果把Y和Z分别放入硝酸银溶液中,过一会儿,在Z表面有银析出,而Y没有变化。根据以上实验事实,判断X、Y、Z三种金属的活动性由强到弱的顺序正确的是
A.X、Y、Z B.X、Z、Y
C.Y、Z、X D.Z、Y、X
8.下列方法中,能达到目的是
选项 物质(括号内为杂质) 除去杂质的方法
A CuSO4溶液(H2SO4) 加足量铜粉,过滤
B CaO(CaCO3) 加足量水溶解、过滤
C CO2(CO) 点燃
D FeC12溶液(CuCl2) 加入过量铁粉,过滤
A.A B.B C.C D.D
9.硝酸铵(NH4NO3)是一种高效化肥,它属于
A.氮肥 B.磷肥 C.钾肥 D.复合肥
10.将质量相等的A、B、C三种金属,同时分别放入三份溶质质量分数相同且足量的稀盐酸中,反应生成H2的质量与反应时间的关系如图所示.根据图中所提供的信息,得出的结论正确的是(已知:A、B、C在生成物中均为+2价)
A.放出H2的质量是B>A>C
B.金属活动性顺序是A>B>C
C.反应速率最大的是A
D.相对原子质量是C>B>A
11.现有盐酸和CaCl2的混合溶液,向其中加入过量某物质X,溶液的pH随加入X的量的变化关系如图所示。则X是
A.石灰石 B.熟石灰 C.纯碱 D.烧碱
二、简答题
12.生活用品中蕴含着丰富的化学知识。
用品 管道通 石灰乳
有效成分 NaOH Ca(OH)2
(1)管道通在使用时禁止与皮肤接触,其原因是_____。
(2)使用石灰乳抹墙,一段时间后变硬的原因_____(用化学方程式回答)。
13.怎样鉴别石灰水和氢氧化钠溶液?
14.向一定量硝酸银、硝酸铜和硝酸亚铁的混合溶液中加入锌粉,充分反应后所得溶液的质量与加入锌粉的质量关系如图。
(1)写出ab段发生反应的化学方程式______。
(2)cd段溶液质量为什么增大______?
(3)e点得到的固体中有什么物质______?
三、推断题
15.A、B、C是三种常见的含钙化合物,它们之间有如图所示的转化关系(部分产物略去):
(1)A物质的化学式是___________,写出B物质在农业生产中的一种用途___________。
(2)根据图中各物质之间的转化,写出一个属于复分解反应的化学方程式_________________。
16.A—E是初中化学中常见的五种物质,它们的变化关系如下图所示。其中A和E都是金属单质且单质E呈紫红色,B的溶液呈浅绿色。
(1)A、B的化学名称分别是______和______;
(2)反应②的化学反应方程式为______;
(3)反应①和②的基本反应类型均为______。
四、实验题
17.做化学实验要正确使用仪器和规范操作.
(1)小王同学从实验室拿来了下列实验仪器.用仪器A称量物质质量时,应将砝码放在 _____ (填“a”或“b”)盘.用完仪器B后,必须用 _____ 盖灭.要完成过滤操作,除选用上述部分仪器外,还需要用到的玻璃仪器是 _____ .
(2)小华同学按图E配制实验所用的稀硫酸.请你指出他操作的错误:
错误① _____ ;错误② _____ .
18.化学课堂上老师演示了如图所示的几个实验:
(1)上述实验中出现的现象,与CO2的物理性质和化学性质都有关的是:______(填序号);
(2)图A所示实验中,紫色干花(用石蕊溶液浸泡过)最终会变红,原因是:______(用化学方程式解释);
(3)图C所示实验中,经振荡后可观察到的实验现象有______(填序号).
①软塑料瓶变瘪 ②瓶内生成了白色的碳酸钙
③瓶内澄清石灰水变浑浊 ④瓶内溶液变红.
19.实验室部分装置如图所示,回答下列问题:
(1)仪器X的名称是________。
(2)实验室常用氯化铵固体与碱石灰固体共热来制取氨气(NH3),其发生装置为____。NH3是一种碱性气体,干燥时不能选用下列干燥剂中的______(填序号)。
A.氢氧化钠固体 B.浓硫酸 C.生石灰
(3)实验室用装置B制O2的化学方程式为_______。
(4)某同学欲用活泼金属单质和稀盐酸反应制取纯净干燥的H2,请从这些装置中选择并连接成一套组合装置,按照气流从左到右的流向,写出所选装置接口的连接顺序:______→______→______→______→______→______→______
五、计算题
20.计算6.5g锌粉与足量稀硫酸完全反应时,产生氢气的质量,并写出具体计算过程。
21.现有碳酸钠和氯化钠的混合物样品12.5g,将其放入干净的烧杯中,加100g水,使其完全溶解。向所得溶液中加入溶质质量分数为7.3%的稀盐酸,烧杯中溶液的质量与加入稀盐酸的质量关系曲线如图所示。请回答下列问题。
(1)在碳酸钠和氯化钠的混合物样品中,含碳酸钠的质量为______(结果精确至 0.1g)
(2)A点时,求此温度下所得不饱和溶液中溶质质量分数______(写出具体计算过程,计算结果精确至0.1%)。
22.某化肥厂生产的一种化肥包装袋上的说明如图所示,化学兴趣小组为测定其纯度,取样品5.6克,完全溶于水,向所得溶液中加入100克一定溶质质量分数的硝酸银溶液,恰好完全反应生成14.35克沉淀(杂质不与硝酸银溶液反应)。通过计算回答。
氯化铵净重25Kg 纯度≥95% XX化肥有限责任公司
(1)所用硝酸银溶液的溶质质量分数;_____。
(2)该化肥是否合格(结果精确到0.1%)。_____。
23.某纯碱样品中含有少量氯化钠杂质。称取该样品22.8g,加入到盛有一定质量稀盐酸的烧杯中,碳酸钠与稀盐酸恰好完全反应,气体完全逸出,得到不饱和NaCl溶液。反应过程中测得烧杯内混合物的质量(m)与反应时间(t)关系如图所示。试回答:
(1)生成CO2的质量_____。
(2)22.8g样品中氯化钠的质量为_____。
(3)计算所得溶液中溶质的质量分数_________。(写出解题过程,计算结果精确到0.1%)
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.B
2.A
3.D
4.D
5.B
6.D
7.B
8.D
9.A
10.D
11.C
12. 氢氧化钠具有强烈的腐蚀性 Ca(OH)2+CO2═CaCO3↓+H2O
13.取少量溶液于试管中,加入适量碳酸钠溶液,产生白色沉淀,则是石灰水,无明显现象,则是氢氧化钠溶液。
14. Zn+2AgNO3=Zn(NO3)2+2Ag 锌和硝酸亚铁反应生成硝酸锌和铁 锌、银、铜、铁
15.(1) CaO 中和酸性土壤
(2)Ca(OH)2+Na2CO3=CaCO3↓+2NaOH
16.(1) 铁 氯化亚铁
(2)CuO+H2Cu+H2O或Cu2O+H22Cu+H2O;
(3)置换反应
17. b 灯帽 漏斗 将水倒入浓硫酸中 在量筒中配制溶液
18. B H2O+CO2=H2CO3 ①③
19.(1)酒精灯
(2) A B
(3)
(4) b f e h g d c
20.解:设产生氢气的质量为x
x=0.2g
答:产生氢气的质量为0.2g。
21.(1)10.6g(2)6.5
22.解:设硝酸银的质量为x,氯化铵质量为y。
x=17g
y=5.35g
所用硝酸银溶液的溶质质量分数
样品的纯度为
故填:17%,合格
23.(1)由图象和质量守恒定律可知,生成二氧化碳的质量为:178.8g﹣170.0g=8.8g;
(2)设碳酸钠的质量为x,生成氯化钠的质量为y,
解得:x=21.2g,y=23.4g,
22.8g样品中氯化钠的质量为:22.8g﹣21.2g=1.6g
(3)完全反应后所得氯化钠溶液的溶质质量分数14.7%
故答为:(1)8.8;
(2)22.8g样品中氯化钠的质量为1.6g;
(3)所得溶液中溶质的质量分数为14.7%。
答案第1页,共2页
答案第1页,共2页
