第7章应用广泛的酸、碱、盐训练九年级化学沪教版(全国)下册(含答案)
文档属性
| 名称 | 第7章应用广泛的酸、碱、盐训练九年级化学沪教版(全国)下册(含答案) |
|
|
| 格式 | docx | ||
| 文件大小 | 200.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-12-19 00:00:00 | ||
图片预览



文档简介
第7章应用广泛的酸、碱、盐训练 九年级化学沪教版(全国)下册
一、单选题
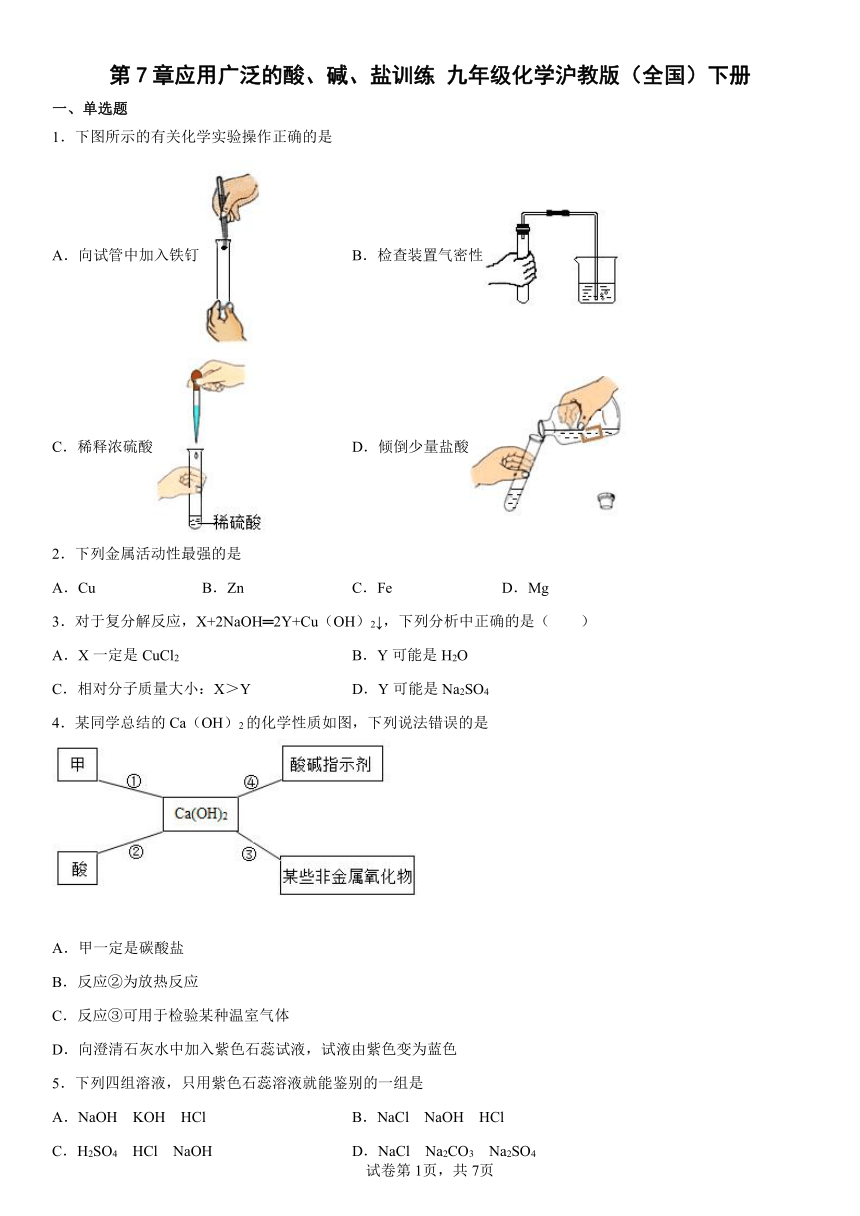
1.下图所示的有关化学实验操作正确的是
A.向试管中加入铁钉 B.检查装置气密性
C.稀释浓硫酸 D.倾倒少量盐酸
2.下列金属活动性最强的是
A.Cu B.Zn C.Fe D.Mg
3.对于复分解反应,X+2NaOH═2Y+Cu(OH)2↓,下列分析中正确的是( )
A.X一定是CuCl2 B.Y可能是H2O
C.相对分子质量大小:X>Y D.Y可能是Na2SO4
4.某同学总结的Ca(OH)2的化学性质如图,下列说法错误的是
A.甲一定是碳酸盐
B.反应②为放热反应
C.反应③可用于检验某种温室气体
D.向澄清石灰水中加入紫色石蕊试液,试液由紫色变为蓝色
5.下列四组溶液,只用紫色石蕊溶液就能鉴别的一组是
A.NaOH KOH HCl B.NaCl NaOH HCl
C.H2SO4 HCl NaOH D.NaCl Na2CO3 Na2SO4
6.下列对宏观事实的微观解释错误的是
选项 事 实 解 释
A 自然界的水循环 水分子的不断运动
B 气体容易压缩,液体、固体不易压缩 液体、固体中分子间无间隔
C 一氧化碳有毒,二氧化碳无毒 构成两者的分子不同
D 碳酸钠、碳酸钾都能与盐酸反应生成二氧化碳 两种盐中都含碳酸根离子
A.A B.B C.C D.D
7.下列实验操作能达到实验目的的是
选项 实验目的 实验操作
A 分离KCl和MnO2的固体混合物 加足量的水溶解,过滤
B 鉴别NaNO3和NH4HCO3两种氮肥 取样,闻气味
C 除去CO中的CO2 将混合气体通过红热的铜网
D 探究铁钉生锈的条件 将两根铁钉分别密封在盛有干燥空气和盛满水的试管中一周并观察现象
A.A B.B C.C D.D
8.某农技站货架上待售的化肥有NH4NO3、NH4H2PO4、CO(NH2)2,其中缺少的肥料品种是( )
A.氮肥 B.磷肥 C.钾肥 D.复合肥料
9.某工厂排出的废水pH小于7,并含有较多的Cu2+,对环境污染严重。从环保及回收利用考虑,较切合实际的治理方案是应适量加入
A.烧碱和纯碱 B.盐酸和铁粉
C.生石灰和铁粉 D.熟石灰和金属银
10.观察下列图像,所得结论不正确的是
A.图1:向一定量的氢氧化钠溶液中滴加pH=3的稀盐酸
B.图2:在饱和石灰水中加入少量生石灰
C.图3:将一定体积的空气通过灼热的铜网充分反应,可知氧气的体积约占空气体积的1/5
D.图4:将CO2通入一定量的澄清石灰水中,先变浑浊,后生成Ca(HCO3)2而变澄清
11.下列实验目的与所用试剂相符的是
A.证明NaOH溶液中含有Na2CO3――酚酞试剂
B.证明NaOH溶液中含有Na2CO3――澄清石灰水
C.除去NaOH溶液中的Na2CO3杂质――稀盐酸
D.除去NaOH溶液中的Na2CO3杂质――CaCl2溶液
12.有一不纯的Na2CO3样品,杂质可能是K2CO3、CaCO3、FeCl3和NaCl中的一种或几种,取该样品10.6g,加入足量稀盐酸完全反应后得到无色溶液,同时产生4.4g气体,下列判断正确的是
A.杂质一定有FeCl3和CaCO3
B.杂质一定没有NaCl
C.杂质可能是K2CO3、CaCO3、NaCl组成的
D.杂质可能是K2CO3和NaCl组成的
二、简答题
13.在宏观、微观和符号之间建立联系是化学学科的特点.
(1)硫酸和盐酸都能用于除铁锈,是因为都存在 _____ 粒子(填微粒符号).
(2)钠元素与氯元素的本质区别为 _____ (微观解释).
(3)如图1所示为某化学反应的微观模拟示意图,其中表示氧原子,表示铜原子,表示氢原子.
请写出该反应的化学方程式 _____ 。
(4)在氢氧化钠溶液中滴加盐酸,恰好完全反应时其微观示意图如图2所示,请在图中补充反应后溶液中存在的粒子 _____ .
14.请回答生活中的化学问题:
(1)长期饮用硬水对健康不利,生活中常用_____的方法将硬水转化为软水。
(2)把磨好的豆浆倒在纱布袋中将渣和浆分离,相当于化学实验中的_____操作。
(3)干粉灭火器主要用来扑灭油、气等燃烧引起的失火,干粉主要成分是碳酸氢钠,干粉受热后生成一种碳酸盐和两种氧化物,请写出该反应的化学方程式_____。
15.物质的性质和用途是化学的重要研究内容。
(1)浓硫酸具有吸水性,在实验室中常用它做_____________剂。
(2)用石灰浆粉刷墙壁,干燥后墙面就变硬了,用化学原理解释该现象______________。
(3)图中,用滤纸做成的小花喷洒某溶液后放在烧杯上方,片刻后变成红色。请推测喷洒液和烧杯中溶液可能是什么?_____________(写出一组即可)
三、推断题
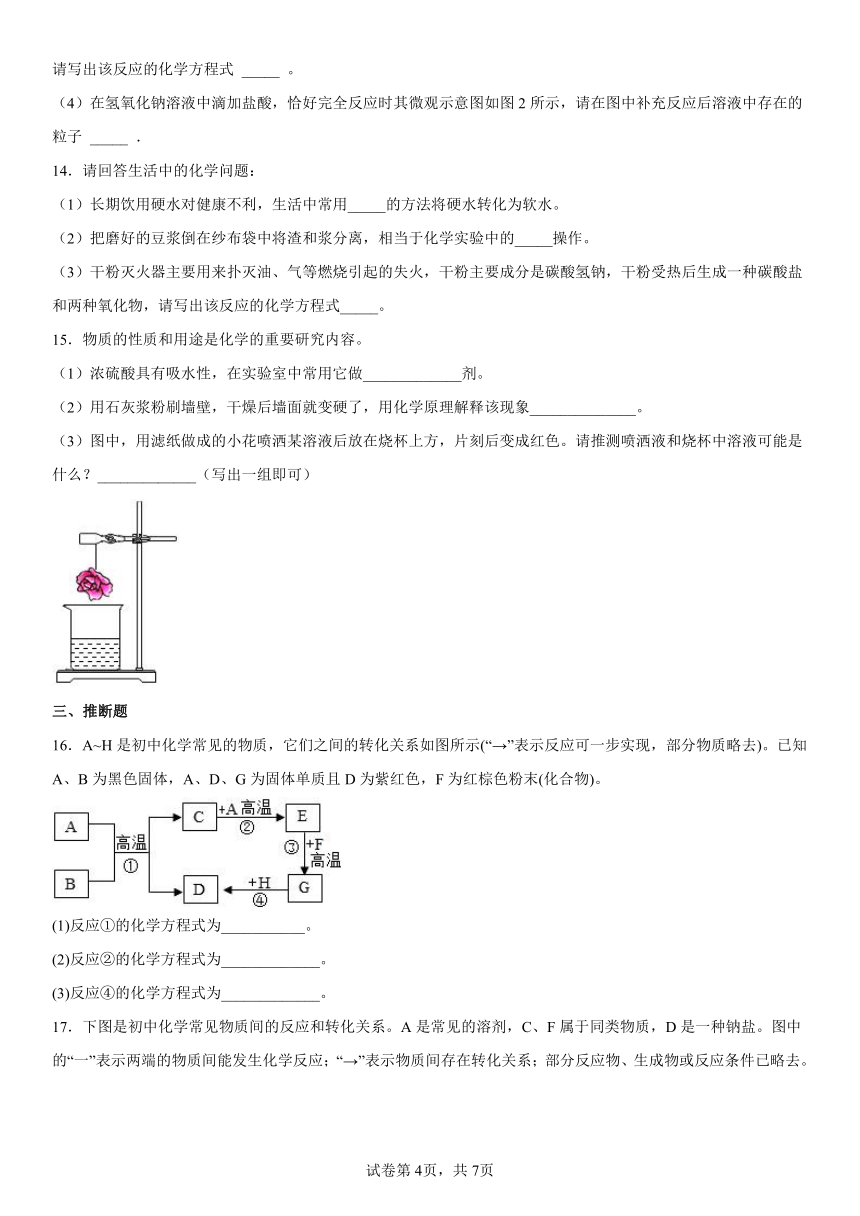
16.A~H是初中化学常见的物质,它们之间的转化关系如图所示(“→”表示反应可一步实现,部分物质略去)。已知A、B为黑色固体,A、D、G为固体单质且D为紫红色,F为红棕色粉末(化合物)。
(1)反应①的化学方程式为___________。
(2)反应②的化学方程式为_____________。
(3)反应④的化学方程式为_____________。
17.下图是初中化学常见物质间的反应和转化关系。A是常见的溶剂,C、F属于同类物质,D是一种钠盐。图中的“一”表示两端的物质间能发生化学反应;“→”表示物质间存在转化关系;部分反应物、生成物或反应条件已略去。
(1)写出物质C的化学式______。
(2)若B由三种元素组成,则其化学式为______。
(3)D→F反应的化学方程式为______。
(4)A与E反应的化学方程式为______。
四、实验题
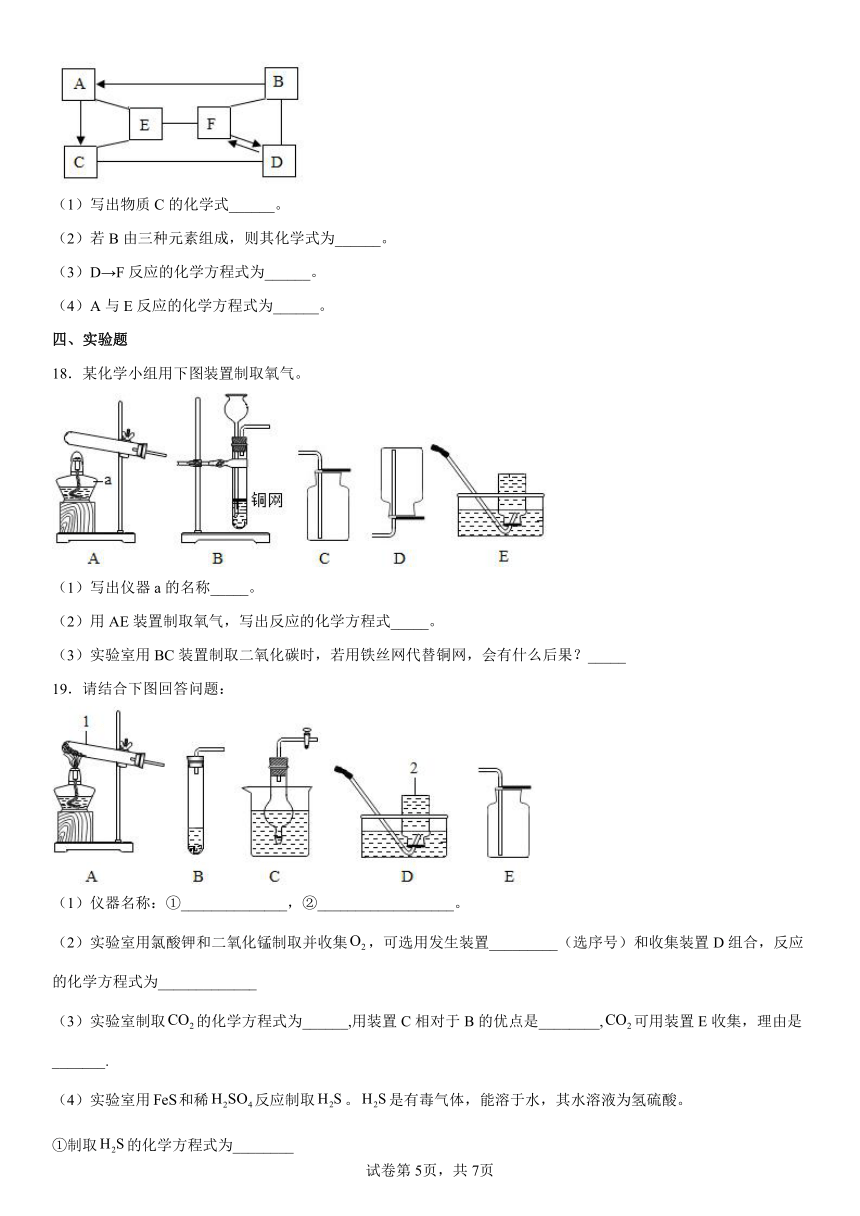
18.某化学小组用下图装置制取氧气。
(1)写出仪器a的名称_____。
(2)用AE装置制取氧气,写出反应的化学方程式_____。
(3)实验室用BC装置制取二氧化碳时,若用铁丝网代替铜网,会有什么后果?_____
19.请结合下图回答问题:
(1)仪器名称:①______________,②__________________。
(2)实验室用氯酸钾和二氧化锰制取并收集,可选用发生装置_________(选序号)和收集装置D组合,反应的化学方程式为_____________
(3)实验室制取的化学方程式为______,用装置C相对于B的优点是________,可用装置E收集,理由是_______.
(4)实验室用和稀反应制取。是有毒气体,能溶于水,其水溶液为氢硫酸。
①制取的化学方程式为________
②图中“防倒吸装置”应选择______________(选填“甲”或“乙”)
③溶液的作用是____________________.
20.中和反应是一类重要的化学反应。某同学利用图1装置研究稀盐酸与氢氧化钠液反应的过程,并用pH和温度传感器测量反应过程中相关物理量的变化情况,得到图2和图3。
(1)烧杯中发生反应的化学方程式为____________________;
(2)仪器A中溶液的溶质是_________________(填化学式);
(3)图3中V的数值最接近_______(填“6”、“12”或“16”);
(4)下列说法错误的是____________。
A 图2中b点所示溶液中的溶质是NaCl和NaOH;
B 取图2中c点所示溶液加热蒸干所得固体为纯净物
C 图2中c→d所示溶液中NaCl的质量不断增加;
D 通过图3中f→g变化趋势可说明该反应的热量变化。
(5)通过图3可知,中和反应是_________反应(填“放热”或“吸热”)。如果改用固体氢氧化钠与稀盐酸反应来探究中和反应中能量的变化情况,你认为该方案____________(填“合理”或“不合理”)。理由是_________________。
五、计算题
21.取100g一定质量分数的Ba(OH)2溶液于烧杯中,逐渐加入质量分数为20%的H2SO4溶液.实验过程中,溶液的pH与加入H2SO4溶液的质量关系如图所示。请计算Ba(OH)2溶液中溶质的质量分数。( 反应的方程式为:Ba(OH)2 + H2SO4 = BaSO4↓+ 2H2O)
22.某铁合金5.8g,与足量的稀硫酸充分反应,得到0.2g的氢气。请计算:
(1)该合金中铁的质量是多少克?
(2)该合金是生铁还是钢?(已知:生铁的含碳量是2%—4.3%,钢的含碳量是0.03%—2%)
23.为了测定某粉末状黄铜(铜、锌合金)样品中铜的质量分数,阳阳同学取一定质量的黄铜样品放入烧杯中,再取40g稀盐酸分四次加入烧杯中,均充分反应,实验数据如下:
第一次 第二次 第三次 第四次
加入稀盐酸质量/g 10 10 10 10
剩余固体的质量/g 9.10 8.45 7.80 7.80
请你计算:
(1)所用稀盐酸中溶质的质量分数。
(2)用36.5%的浓盐酸配制40g上述稀盐酸,需要浓盐酸的质量。
(3)黄铜样品中铜的质量分数。
24.某化学兴趣小组为测定某石灰石样品(杂质不溶于水,也不与酸反应)中碳酸钙的质量分数,进行如图所示的实验。请根据以上信息回答下列问题:
(1)写出反应的化学方程式 ;
(2)该反应中产生二氧化碳的总质量为 g;
(3)列出求解该样品中参加反应的碳酸钙质量(x)的比例式 ;
(4)石灰石样品中碳酸钙的质量分数为 ;
(5)某同学想用上述石灰石样品250t,可制得含杂质的生石灰的质量是 。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.B
2.D
3.C
4.A
5.B
6.B
7.B
8.C
9.C
10.A
11.B
12.C
13. H+ 原子的质子数不同(或核电荷数不同) CuO+H2Cu+H2O
14. 加热煮沸 过滤 2NaHCO3Na2CO3+CO2↑+H2O 。
15. 干燥 石灰浆中含有Ca(OH)2,干燥过程中与CO2反应.生成难溶于水的CaCO3 石蕊溶液和浓盐酸。(或酚酞溶液和浓氨水)
16.(1)
(2)
(3)(合理即可)
17. Ca(OH)2 H2SO4(答案合理即可)
18. 酒精灯 2KClO32KCl+3O2↑ 制取的二氧化碳中会混有氢气
19. 试管 集气瓶 A 能控制反应的进行和停止 二氧化碳的密度大于空气 FeS+H2SO4=FeSO4+H2S↑ 乙 吸收H2S,防止污染空气
20. NaOH+HCl=NaCl+H2O HCl 12 CD 放热 不合理 固体氢氧化钠溶于水放热
21.6.48%
22.解:(1)设该合金中铁的质量是
=5.6g
答:该合金中铁的质量是5.6g。
(2)该合金中碳的质量分数为
该合金的含碳量在2%—4.3%之间,故为生铁。
答:该合金是生铁。
23.
(1)设参加反应的HCl的质量为x
第二次加入10g盐酸,消耗锌的质量为9.10g-8.45g=0.65g
第三次加入10g盐酸,消耗锌的质量为8.45g-7.80g=0.65g
故Zn的质量=0.65g×3=1.95g
x=2.19g
稀盐酸中溶质HCl的质量分数=。
(2)需要浓盐酸的质量==8g
(3)黄铜中铜的质量分数=×100%=80%
答:稀盐酸中溶质HCl的质量分数为7.3%,需要浓盐酸的质量为8g,黄铜中铜的质量分数为80%。
24.(1)(2)8.8(3)20g(4)80%(5)162t
答案第1页,共2页
答案第1页,共2页
一、单选题
1.下图所示的有关化学实验操作正确的是
A.向试管中加入铁钉 B.检查装置气密性
C.稀释浓硫酸 D.倾倒少量盐酸
2.下列金属活动性最强的是
A.Cu B.Zn C.Fe D.Mg
3.对于复分解反应,X+2NaOH═2Y+Cu(OH)2↓,下列分析中正确的是( )
A.X一定是CuCl2 B.Y可能是H2O
C.相对分子质量大小:X>Y D.Y可能是Na2SO4
4.某同学总结的Ca(OH)2的化学性质如图,下列说法错误的是
A.甲一定是碳酸盐
B.反应②为放热反应
C.反应③可用于检验某种温室气体
D.向澄清石灰水中加入紫色石蕊试液,试液由紫色变为蓝色
5.下列四组溶液,只用紫色石蕊溶液就能鉴别的一组是
A.NaOH KOH HCl B.NaCl NaOH HCl
C.H2SO4 HCl NaOH D.NaCl Na2CO3 Na2SO4
6.下列对宏观事实的微观解释错误的是
选项 事 实 解 释
A 自然界的水循环 水分子的不断运动
B 气体容易压缩,液体、固体不易压缩 液体、固体中分子间无间隔
C 一氧化碳有毒,二氧化碳无毒 构成两者的分子不同
D 碳酸钠、碳酸钾都能与盐酸反应生成二氧化碳 两种盐中都含碳酸根离子
A.A B.B C.C D.D
7.下列实验操作能达到实验目的的是
选项 实验目的 实验操作
A 分离KCl和MnO2的固体混合物 加足量的水溶解,过滤
B 鉴别NaNO3和NH4HCO3两种氮肥 取样,闻气味
C 除去CO中的CO2 将混合气体通过红热的铜网
D 探究铁钉生锈的条件 将两根铁钉分别密封在盛有干燥空气和盛满水的试管中一周并观察现象
A.A B.B C.C D.D
8.某农技站货架上待售的化肥有NH4NO3、NH4H2PO4、CO(NH2)2,其中缺少的肥料品种是( )
A.氮肥 B.磷肥 C.钾肥 D.复合肥料
9.某工厂排出的废水pH小于7,并含有较多的Cu2+,对环境污染严重。从环保及回收利用考虑,较切合实际的治理方案是应适量加入
A.烧碱和纯碱 B.盐酸和铁粉
C.生石灰和铁粉 D.熟石灰和金属银
10.观察下列图像,所得结论不正确的是
A.图1:向一定量的氢氧化钠溶液中滴加pH=3的稀盐酸
B.图2:在饱和石灰水中加入少量生石灰
C.图3:将一定体积的空气通过灼热的铜网充分反应,可知氧气的体积约占空气体积的1/5
D.图4:将CO2通入一定量的澄清石灰水中,先变浑浊,后生成Ca(HCO3)2而变澄清
11.下列实验目的与所用试剂相符的是
A.证明NaOH溶液中含有Na2CO3――酚酞试剂
B.证明NaOH溶液中含有Na2CO3――澄清石灰水
C.除去NaOH溶液中的Na2CO3杂质――稀盐酸
D.除去NaOH溶液中的Na2CO3杂质――CaCl2溶液
12.有一不纯的Na2CO3样品,杂质可能是K2CO3、CaCO3、FeCl3和NaCl中的一种或几种,取该样品10.6g,加入足量稀盐酸完全反应后得到无色溶液,同时产生4.4g气体,下列判断正确的是
A.杂质一定有FeCl3和CaCO3
B.杂质一定没有NaCl
C.杂质可能是K2CO3、CaCO3、NaCl组成的
D.杂质可能是K2CO3和NaCl组成的
二、简答题
13.在宏观、微观和符号之间建立联系是化学学科的特点.
(1)硫酸和盐酸都能用于除铁锈,是因为都存在 _____ 粒子(填微粒符号).
(2)钠元素与氯元素的本质区别为 _____ (微观解释).
(3)如图1所示为某化学反应的微观模拟示意图,其中表示氧原子,表示铜原子,表示氢原子.
请写出该反应的化学方程式 _____ 。
(4)在氢氧化钠溶液中滴加盐酸,恰好完全反应时其微观示意图如图2所示,请在图中补充反应后溶液中存在的粒子 _____ .
14.请回答生活中的化学问题:
(1)长期饮用硬水对健康不利,生活中常用_____的方法将硬水转化为软水。
(2)把磨好的豆浆倒在纱布袋中将渣和浆分离,相当于化学实验中的_____操作。
(3)干粉灭火器主要用来扑灭油、气等燃烧引起的失火,干粉主要成分是碳酸氢钠,干粉受热后生成一种碳酸盐和两种氧化物,请写出该反应的化学方程式_____。
15.物质的性质和用途是化学的重要研究内容。
(1)浓硫酸具有吸水性,在实验室中常用它做_____________剂。
(2)用石灰浆粉刷墙壁,干燥后墙面就变硬了,用化学原理解释该现象______________。
(3)图中,用滤纸做成的小花喷洒某溶液后放在烧杯上方,片刻后变成红色。请推测喷洒液和烧杯中溶液可能是什么?_____________(写出一组即可)
三、推断题
16.A~H是初中化学常见的物质,它们之间的转化关系如图所示(“→”表示反应可一步实现,部分物质略去)。已知A、B为黑色固体,A、D、G为固体单质且D为紫红色,F为红棕色粉末(化合物)。
(1)反应①的化学方程式为___________。
(2)反应②的化学方程式为_____________。
(3)反应④的化学方程式为_____________。
17.下图是初中化学常见物质间的反应和转化关系。A是常见的溶剂,C、F属于同类物质,D是一种钠盐。图中的“一”表示两端的物质间能发生化学反应;“→”表示物质间存在转化关系;部分反应物、生成物或反应条件已略去。
(1)写出物质C的化学式______。
(2)若B由三种元素组成,则其化学式为______。
(3)D→F反应的化学方程式为______。
(4)A与E反应的化学方程式为______。
四、实验题
18.某化学小组用下图装置制取氧气。
(1)写出仪器a的名称_____。
(2)用AE装置制取氧气,写出反应的化学方程式_____。
(3)实验室用BC装置制取二氧化碳时,若用铁丝网代替铜网,会有什么后果?_____
19.请结合下图回答问题:
(1)仪器名称:①______________,②__________________。
(2)实验室用氯酸钾和二氧化锰制取并收集,可选用发生装置_________(选序号)和收集装置D组合,反应的化学方程式为_____________
(3)实验室制取的化学方程式为______,用装置C相对于B的优点是________,可用装置E收集,理由是_______.
(4)实验室用和稀反应制取。是有毒气体,能溶于水,其水溶液为氢硫酸。
①制取的化学方程式为________
②图中“防倒吸装置”应选择______________(选填“甲”或“乙”)
③溶液的作用是____________________.
20.中和反应是一类重要的化学反应。某同学利用图1装置研究稀盐酸与氢氧化钠液反应的过程,并用pH和温度传感器测量反应过程中相关物理量的变化情况,得到图2和图3。
(1)烧杯中发生反应的化学方程式为____________________;
(2)仪器A中溶液的溶质是_________________(填化学式);
(3)图3中V的数值最接近_______(填“6”、“12”或“16”);
(4)下列说法错误的是____________。
A 图2中b点所示溶液中的溶质是NaCl和NaOH;
B 取图2中c点所示溶液加热蒸干所得固体为纯净物
C 图2中c→d所示溶液中NaCl的质量不断增加;
D 通过图3中f→g变化趋势可说明该反应的热量变化。
(5)通过图3可知,中和反应是_________反应(填“放热”或“吸热”)。如果改用固体氢氧化钠与稀盐酸反应来探究中和反应中能量的变化情况,你认为该方案____________(填“合理”或“不合理”)。理由是_________________。
五、计算题
21.取100g一定质量分数的Ba(OH)2溶液于烧杯中,逐渐加入质量分数为20%的H2SO4溶液.实验过程中,溶液的pH与加入H2SO4溶液的质量关系如图所示。请计算Ba(OH)2溶液中溶质的质量分数。( 反应的方程式为:Ba(OH)2 + H2SO4 = BaSO4↓+ 2H2O)
22.某铁合金5.8g,与足量的稀硫酸充分反应,得到0.2g的氢气。请计算:
(1)该合金中铁的质量是多少克?
(2)该合金是生铁还是钢?(已知:生铁的含碳量是2%—4.3%,钢的含碳量是0.03%—2%)
23.为了测定某粉末状黄铜(铜、锌合金)样品中铜的质量分数,阳阳同学取一定质量的黄铜样品放入烧杯中,再取40g稀盐酸分四次加入烧杯中,均充分反应,实验数据如下:
第一次 第二次 第三次 第四次
加入稀盐酸质量/g 10 10 10 10
剩余固体的质量/g 9.10 8.45 7.80 7.80
请你计算:
(1)所用稀盐酸中溶质的质量分数。
(2)用36.5%的浓盐酸配制40g上述稀盐酸,需要浓盐酸的质量。
(3)黄铜样品中铜的质量分数。
24.某化学兴趣小组为测定某石灰石样品(杂质不溶于水,也不与酸反应)中碳酸钙的质量分数,进行如图所示的实验。请根据以上信息回答下列问题:
(1)写出反应的化学方程式 ;
(2)该反应中产生二氧化碳的总质量为 g;
(3)列出求解该样品中参加反应的碳酸钙质量(x)的比例式 ;
(4)石灰石样品中碳酸钙的质量分数为 ;
(5)某同学想用上述石灰石样品250t,可制得含杂质的生石灰的质量是 。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.B
2.D
3.C
4.A
5.B
6.B
7.B
8.C
9.C
10.A
11.B
12.C
13. H+ 原子的质子数不同(或核电荷数不同) CuO+H2Cu+H2O
14. 加热煮沸 过滤 2NaHCO3Na2CO3+CO2↑+H2O 。
15. 干燥 石灰浆中含有Ca(OH)2,干燥过程中与CO2反应.生成难溶于水的CaCO3 石蕊溶液和浓盐酸。(或酚酞溶液和浓氨水)
16.(1)
(2)
(3)(合理即可)
17. Ca(OH)2 H2SO4(答案合理即可)
18. 酒精灯 2KClO32KCl+3O2↑ 制取的二氧化碳中会混有氢气
19. 试管 集气瓶 A 能控制反应的进行和停止 二氧化碳的密度大于空气 FeS+H2SO4=FeSO4+H2S↑ 乙 吸收H2S,防止污染空气
20. NaOH+HCl=NaCl+H2O HCl 12 CD 放热 不合理 固体氢氧化钠溶于水放热
21.6.48%
22.解:(1)设该合金中铁的质量是
=5.6g
答:该合金中铁的质量是5.6g。
(2)该合金中碳的质量分数为
该合金的含碳量在2%—4.3%之间,故为生铁。
答:该合金是生铁。
23.
(1)设参加反应的HCl的质量为x
第二次加入10g盐酸,消耗锌的质量为9.10g-8.45g=0.65g
第三次加入10g盐酸,消耗锌的质量为8.45g-7.80g=0.65g
故Zn的质量=0.65g×3=1.95g
x=2.19g
稀盐酸中溶质HCl的质量分数=。
(2)需要浓盐酸的质量==8g
(3)黄铜中铜的质量分数=×100%=80%
答:稀盐酸中溶质HCl的质量分数为7.3%,需要浓盐酸的质量为8g,黄铜中铜的质量分数为80%。
24.(1)(2)8.8(3)20g(4)80%(5)162t
答案第1页,共2页
答案第1页,共2页
