2022—2023学年化学沪教版(全国)九年级下册第6章 溶解现象 章末自检题(有答案)
文档属性
| 名称 | 2022—2023学年化学沪教版(全国)九年级下册第6章 溶解现象 章末自检题(有答案) |

|
|
| 格式 | zip | ||
| 文件大小 | 347.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-01-04 00:00:00 | ||
图片预览




文档简介
2022—2023学年化学沪教版(全国)九年级下册第6章 溶解现象 章末自检题含答案
沪教版(全国)第6章 溶解现象
一、选择题。
1、如图所示,往烧杯中加入一定量的某固体,会引起试管内白磷燃烧,该固体可能是( )
A.氢氧化钠 B.硝酸铵 C.氯化钠 D.碳酸钙
2、用硝酸钾固体配制溶质的质量分数为10%的硝酸钾溶液50g。下列做法不正确的是( )
A.称量:用天平称量硝酸钾5g B.量取:用量筒量取蒸馏水45mL
C.溶解:将硝酸钾倒入量筒中溶解 D.转移:将配好的溶液转移至试剂瓶
3、下列关于溶液的说法正确的是( )
A.从一杯质量分数为10%的食盐溶液中倒出一半,余下的溶液质量分数为5%
B.某饱和溶液降温后析出晶体,此时它就变成不饱和溶液
C.向某物质的饱和溶液中加少量该物质,恒温下放置一定时间后,溶液中的溶质质量分数变大
D.稀溶液可能是饱和溶液,浓溶液也可能是不饱和溶液
4、某同学选用氢氧化钠固体与水配制20g溶质质量分数为10%的氢氧化钠溶液,下列说法错误的是( )
①需称取氢氧化钠固体2.0g
②称量前托盘天平应先检查游码是否归零,并调节平衡
③用托盘天平称量氢氧化钠固体时,为防止污染托盘,可将氢氧化钠放在纸上称量
④选用250mL量筒量取18mL的水
⑤存放溶液时,为确保数据准确,将试剂瓶用蒸馏水清洗后,立即倒入所配溶液封存
A. B. C. D.
5、下列物质不属于溶液的是( )
A.冰水 B.碘酒 C.食盐水 D.浓盐酸
6、实验室用氯化钠配制50g质量分数为6%的氯化钠溶液。下列说法中不正确的是( )
A.所需氯化钠的质量为3g
B.氯化钠放在托盘天平的左盘称量
C.俯视量筒读数会使所配溶液偏稀
D.所需玻璃仪器有烧杯、玻璃棒、量筒等
7、甲、乙两种固体物质的溶解度曲线如图所示。下列说法中正确的是( )
A.甲的溶解度比乙大
B.t2℃时,甲、乙饱和溶液的溶质质量分数都为30%
C.t3℃时,甲、乙的饱和溶液分别降温至t1℃,甲溶液饱和,乙溶液不饱和
D.t2℃时,质量相同的甲、乙饱和溶液分别升温至t3℃,为达饱和状态,需加入甲的质量大于乙
8、在配制一定溶质质量分数的蔗糖溶液时,导致溶液中蔗糖的质量分数偏大的可能原因有( )
A.用量筒量取水时俯视读数
B.用来配制溶液的烧杯刚用少量蒸馏水润洗过
C.用托盘天平称取蔗糖时,将蔗糖放在右盘,且称量时使用了游码
D.用了含少量杂质的蔗糖配制溶液
9、下列液体去除油污效果最好的是( )
A.洗洁精 B.食盐水 C.白醋 D.自来水
10、实验室用蔗糖配制50.0g溶质的质量分数为10%的蔗糖溶液,下列说法错误的是( )
A.用托盘天平称取5.0g蔗糖
B.用量程为10mL的量筒量取所需的水
C.溶解蔗糖时,使用的玻璃仪器有烧杯、玻璃棒
D.将配制好的溶液装入细口瓶中,塞好瓶塞并贴上标签
11、a、b、c三种不含结晶水的物质的溶解度曲线如图,下列说法正确的是( )
A.a的溶解度大于b的溶解度
B.将a的溶液由降温到,一定有晶体析出
C.时,50g的a溶于50g水,溶液的质量分数为
D.c的饱和溶液由降温到,溶液的质量分数不变
12、20℃时,NaCl的溶解度为36g。配制此温度下20g质量分数为5%的NaCl溶液,下列说法正确的是( )
A.配制该溶液需要5g NaCl
B.该溶液为饱和溶液
C.将该溶液长时间敞口放置,最终有晶体析出
D.配溶液时,量取所需体积的水倒入烧杯,有少量水洒出,则所配溶液浓度小于5%
13、向如图装置的试管中加入某种物质后,U形管右边支管的红墨水液面降低,左边支管的红墨水液面上升,则加入的物质是( )
A.氢氧化钠 B.生石灰 C.浓硫酸 D.硝酸铵
14、在配制一定溶质质量分数的氯化钠溶液时,出现下列失误操作,一定会使所配溶液的溶质质量分数偏低的是( )
A.用托盘天平称量氯化钠时,砝码放在左盘,未使用游码
B.量取蒸馏水,仰视量筒读数
C.将量筒中的水倒入烧杯时,有水洒出
D.将配好的溶液转移到细口瓶里,不慎洒出部分溶液
15、如图所示,向烧杯中加入某物质能使试管中的饱和石灰水变浑浊,该物质可能是( )
A.冰 B.硝酸铵固体 C.氯化钠固体 D.氢氧化钠固体
二、填空题。
16、将少量①橄榄油②醋③冰块④白糖⑤肥皂水⑥面粉,分别加入水中振荡,其中 形成乳浊液, 形成溶液(写序号)。
17、分别填写下列溶液中溶质和溶剂的名称:
(1)蔗糖溶液:溶质_______;溶剂________。
(2)碘酒(即碘的酒精溶液):溶质_______;溶剂________。
(3)乙醇的水溶液:溶质_______;溶剂________。
(4)0.9%的生理盐水:溶质_______;溶剂________。
18、回答下列问题
(1)固体的溶解度指在一定______下,某固态物质在______溶剂里达到______状态所溶解的______。
(2)20℃时,氯化钠在水中的溶解度为36 g,意思是20℃时,______水中达到______状态时溶解氯化钠的质量为______;或者20℃时,______水中______可溶解氯化钠的质量为36 g。
(3)物质的溶解性是根据______℃时的溶解度规定的,当该温度下物质的溶解度______10 g时,为易溶物质。
a.固体的溶解度从几个要素进行规定?______
b.要比较两种物质的溶解度,需要注意什么问题?______
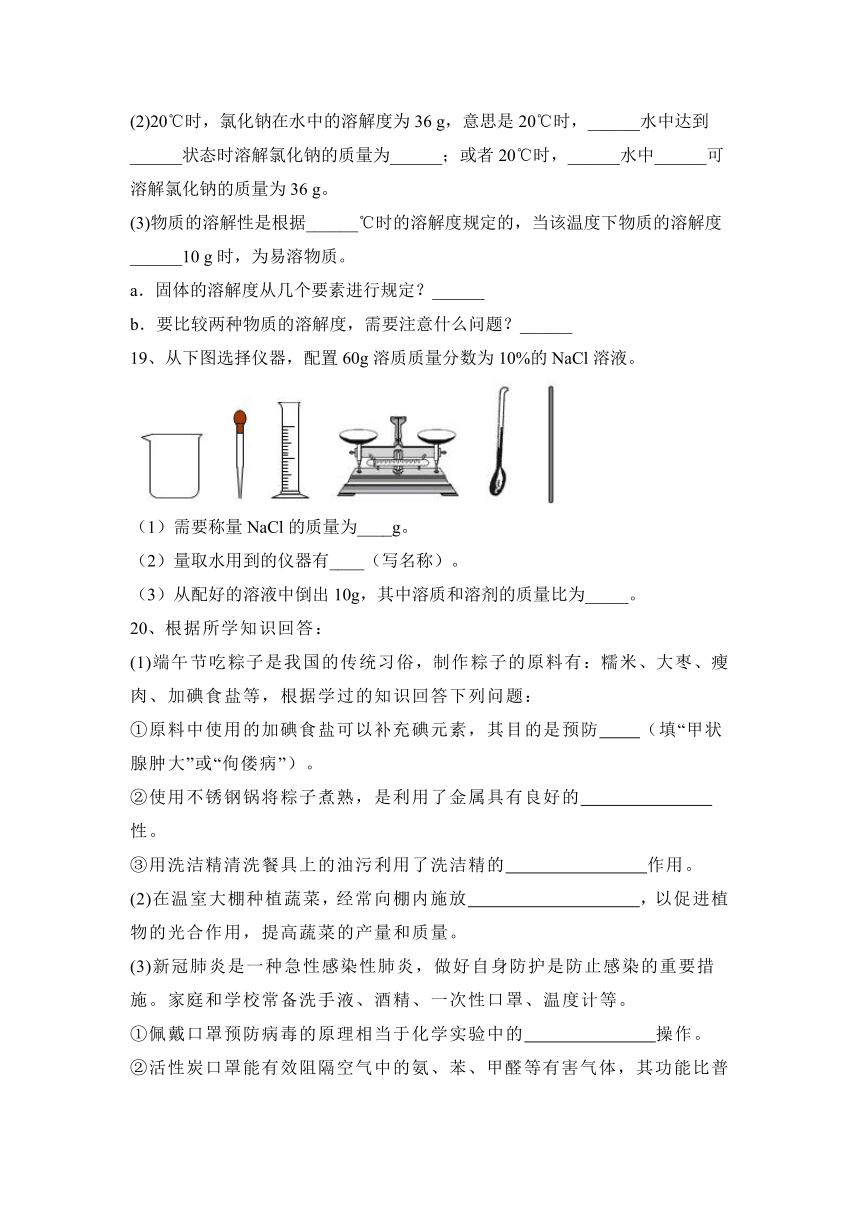
19、从下图选择仪器,配置60g溶质质量分数为10%的NaCl溶液。
(1)需要称量NaCl的质量为____g。
(2)量取水用到的仪器有____(写名称)。
(3)从配好的溶液中倒出10g,其中溶质和溶剂的质量比为_____。
20、根据所学知识回答:
(1)端午节吃粽子是我国的传统习俗,制作粽子的原料有:糯米、大枣、瘦肉、加碘食盐等,根据学过的知识回答下列问题:
①原料中使用的加碘食盐可以补充碘元素,其目的是预防 (填“甲状腺肿大”或“佝偻病”)。
②使用不锈钢锅将粽子煮熟,是利用了金属具有良好的 性。
③用洗洁精清洗餐具上的油污利用了洗洁精的 作用。
(2)在温室大棚种植蔬菜,经常向棚内施放 ,以促进植物的光合作用,提高蔬菜的产量和质量。
(3)新冠肺炎是一种急性感染性肺炎,做好自身防护是防止感染的重要措施。家庭和学校常备洗手液、酒精、一次性口罩、温度计等。
①佩戴口罩预防病毒的原理相当于化学实验中的 操作。
②活性炭口罩能有效阻隔空气中的氨、苯、甲醛等有害气体,其功能比普通口罩强大,原因是活性炭具有 性。
③医用酒精是75%酒精溶液,其溶剂是 。
④温度计有多种,常用的体温计有水银温度计,温度升高,水银柱会上升,从微观角度来解释是 。
21、若6.5克锌与100克稀硫酸恰好完全反应。
(1)在100克稀硫酸中,溶质的化学式是____,其质量是_____,溶剂的化学式是______,其质量为_____。
(2)完全反应后,所得溶液的质量为____,其中溶质的化学式为______,其质量为______。
22、交点的含义:
如图所示,P点表示______,此时两种物质的饱和溶液中一定相等的是______。
23、某同学配制50g质量分数为6%的NaC1溶液,整个操作过程如下图所示。
回答下列问题:
(1)配制溶液的正确操作顺序为___________(填序号),其中有错误的操作是___________(填序号)。
(2)用量筒量取液体时,读数时视线要与量筒内___________保持水平。
(3)改正上图中的错误操作后,经检测该同学配制的溶液质量分数偏小,可能的原因是___________(填一个原因即可)。
三、实验题。
24、请结合如图所示的实验,回答下列与燃烧有关的问题。
(1)甲实验中,能观察到的现象是 。
(2)乙实验中,向烧杯中加入一定量下列物质,不能使试管中白磷燃烧的是 。
ANaCl BNH4NO3 C浓H2SO4 DNaOH
(3)家用罐装燃气是液化石油气,它是石油化工的一种产品。石油属于(选填“可再生”或“不可再生” 能源,若厨房失火,要移走燃气罐,这样做利用的灭火原理是 。
四、综合应用题。
25、溶液与人们的生产、生活密切相关。
(1)向澄清石灰水中通入二氧化碳直至过量的全过程中,下列转变关系正确的是______(填字母)。
A.溶液、乳浊液、溶液 B.溶液、悬溶液、乳浊液
C.悬溶液、乳浊液、溶液 D.溶液、悬浊液、溶液
(2)在盛有水的烧杯中加入以下某种物质,在形成溶液的过程中,溶液温度明显升高的是______(填字母)。
A.烧碱 B.硝酸铵 C.氯化钠
(3)如图为甲、乙两种固体物质的溶解度曲线。
①溶解度随温度升高而增大的物质是______(填“甲”或“乙”)。
②将t1℃时的甲、乙两种物质的饱和溶液升温至t2℃,所得溶液中溶质的质量分数甲______乙(填“<”、“=”或“>”)
③在t2℃时,某同学向128.5g甲溶液中加入1.5g甲固体恰好得到t2℃时甲的饱和溶液,则原甲溶液溶质的质量分数为______(结果精确到0.1%)。
(4)t2℃时,同学们在实验室配制一定量10%的甲溶液(已知水的密度为1g/cm3)。
①用8.0g甲(不含结晶水)固体配制10%的甲溶液,需要水______mL。
②将配好的溶液倒入洁净的______中(填容器名称),盖好塞子贴上标签。
③下列操作会导致配制的甲溶液的溶质质量分数偏低的是______。
A.甲固体中含有杂质
B.烧杯未干燥直接用于配制溶液
C.用量筒量取水时采用俯视方法读数
五、计算类题。
26、化学兴趣小组的同学用46g稀硫酸与一定质量的氧化铜恰好完全反应,反应后得到的溶液质量为50g。求:
(1)氧化铜的质量为:___________g。
(2)反应后所得溶液中溶质的质量分数。
【提示:CuO+H2SO4═CuSO4+H2O】
2022—2023学年化学沪教版(全国)九年级下册第6章 溶解现象 章末自检题含答案
沪教版(全国)第6章 溶解现象
一、选择题。
1、如图所示,往烧杯中加入一定量的某固体,会引起试管内白磷燃烧,该固体可能是( )
A.氢氧化钠 B.硝酸铵 C.氯化钠 D.碳酸钙
【答案】A
2、用硝酸钾固体配制溶质的质量分数为10%的硝酸钾溶液50g。下列做法不正确的是( )
A.称量:用天平称量硝酸钾5g B.量取:用量筒量取蒸馏水45mL
C.溶解:将硝酸钾倒入量筒中溶解 D.转移:将配好的溶液转移至试剂瓶
【答案】C
3、下列关于溶液的说法正确的是( )
A.从一杯质量分数为10%的食盐溶液中倒出一半,余下的溶液质量分数为5%
B.某饱和溶液降温后析出晶体,此时它就变成不饱和溶液
C.向某物质的饱和溶液中加少量该物质,恒温下放置一定时间后,溶液中的溶质质量分数变大
D.稀溶液可能是饱和溶液,浓溶液也可能是不饱和溶液
【答案】D
4、某同学选用氢氧化钠固体与水配制20g溶质质量分数为10%的氢氧化钠溶液,下列说法错误的是( )
①需称取氢氧化钠固体2.0g
②称量前托盘天平应先检查游码是否归零,并调节平衡
③用托盘天平称量氢氧化钠固体时,为防止污染托盘,可将氢氧化钠放在纸上称量
④选用250mL量筒量取18mL的水
⑤存放溶液时,为确保数据准确,将试剂瓶用蒸馏水清洗后,立即倒入所配溶液封存
A. B. C. D.
【答案】B
5、下列物质不属于溶液的是( )
A.冰水 B.碘酒 C.食盐水 D.浓盐酸
【答案】A
6、实验室用氯化钠配制50g质量分数为6%的氯化钠溶液。下列说法中不正确的是( )
A.所需氯化钠的质量为3g
B.氯化钠放在托盘天平的左盘称量
C.俯视量筒读数会使所配溶液偏稀
D.所需玻璃仪器有烧杯、玻璃棒、量筒等
【答案】C
7、甲、乙两种固体物质的溶解度曲线如图所示。下列说法中正确的是( )
A.甲的溶解度比乙大
B.t2℃时,甲、乙饱和溶液的溶质质量分数都为30%
C.t3℃时,甲、乙的饱和溶液分别降温至t1℃,甲溶液饱和,乙溶液不饱和
D.t2℃时,质量相同的甲、乙饱和溶液分别升温至t3℃,为达饱和状态,需加入甲的质量大于乙
【答案】D
8、在配制一定溶质质量分数的蔗糖溶液时,导致溶液中蔗糖的质量分数偏大的可能原因有( )
A.用量筒量取水时俯视读数
B.用来配制溶液的烧杯刚用少量蒸馏水润洗过
C.用托盘天平称取蔗糖时,将蔗糖放在右盘,且称量时使用了游码
D.用了含少量杂质的蔗糖配制溶液
【答案】A
9、下列液体去除油污效果最好的是( )
A.洗洁精 B.食盐水 C.白醋 D.自来水
【答案】A
10、实验室用蔗糖配制50.0g溶质的质量分数为10%的蔗糖溶液,下列说法错误的是( )
A.用托盘天平称取5.0g蔗糖
B.用量程为10mL的量筒量取所需的水
C.溶解蔗糖时,使用的玻璃仪器有烧杯、玻璃棒
D.将配制好的溶液装入细口瓶中,塞好瓶塞并贴上标签
【答案】B
11、a、b、c三种不含结晶水的物质的溶解度曲线如图,下列说法正确的是( )
A.a的溶解度大于b的溶解度
B.将a的溶液由降温到,一定有晶体析出
C.时,50g的a溶于50g水,溶液的质量分数为
D.c的饱和溶液由降温到,溶液的质量分数不变
【答案】D
12、20℃时,NaCl的溶解度为36g。配制此温度下20g质量分数为5%的NaCl溶液,下列说法正确的是( )
A.配制该溶液需要5g NaCl
B.该溶液为饱和溶液
C.将该溶液长时间敞口放置,最终有晶体析出
D.配溶液时,量取所需体积的水倒入烧杯,有少量水洒出,则所配溶液浓度小于5%
【答案】C
13、向如图装置的试管中加入某种物质后,U形管右边支管的红墨水液面降低,左边支管的红墨水液面上升,则加入的物质是( )
A.氢氧化钠 B.生石灰 C.浓硫酸 D.硝酸铵
【答案】D
14、在配制一定溶质质量分数的氯化钠溶液时,出现下列失误操作,一定会使所配溶液的溶质质量分数偏低的是( )
A.用托盘天平称量氯化钠时,砝码放在左盘,未使用游码
B.量取蒸馏水,仰视量筒读数
C.将量筒中的水倒入烧杯时,有水洒出
D.将配好的溶液转移到细口瓶里,不慎洒出部分溶液
【答案】B
15、如图所示,向烧杯中加入某物质能使试管中的饱和石灰水变浑浊,该物质可能是( )
A.冰 B.硝酸铵固体 C.氯化钠固体 D.氢氧化钠固体
【答案】D
二、填空题。
16、将少量①橄榄油②醋③冰块④白糖⑤肥皂水⑥面粉,分别加入水中振荡,其中 形成乳浊液, 形成溶液(写序号)。
【答案】; ①⑤; ②④
17、分别填写下列溶液中溶质和溶剂的名称:
(1)蔗糖溶液:溶质_______;溶剂________。
(2)碘酒(即碘的酒精溶液):溶质_______;溶剂________。
(3)乙醇的水溶液:溶质_______;溶剂________。
(4)0.9%的生理盐水:溶质_______;溶剂________。
【答案】(1) 蔗糖 水 (2) 碘 酒精
(3) 乙醇 水 (4) 氯化钠 水
18、回答下列问题
(1)固体的溶解度指在一定______下,某固态物质在______溶剂里达到______状态所溶解的______。
(2)20℃时,氯化钠在水中的溶解度为36 g,意思是20℃时,______水中达到______状态时溶解氯化钠的质量为______;或者20℃时,______水中______可溶解氯化钠的质量为36 g。
(3)物质的溶解性是根据______℃时的溶解度规定的,当该温度下物质的溶解度______10 g时,为易溶物质。
a.固体的溶解度从几个要素进行规定?______
b.要比较两种物质的溶解度,需要注意什么问题?______
【答案】(1) 温度 100g 饱和 质量
(2) 100g 饱和 36g 100g 最多
(3) 20 大于 一定温度、溶剂质量100g、饱和溶液、溶解质量 温度相同
19、从下图选择仪器,配置60g溶质质量分数为10%的NaCl溶液。
(1)需要称量NaCl的质量为____g。
(2)量取水用到的仪器有____(写名称)。
(3)从配好的溶液中倒出10g,其中溶质和溶剂的质量比为_____。
【答案】6 100mL量筒、胶头滴管(顺序可变) 1:9
20、根据所学知识回答:
(1)端午节吃粽子是我国的传统习俗,制作粽子的原料有:糯米、大枣、瘦肉、加碘食盐等,根据学过的知识回答下列问题:
①原料中使用的加碘食盐可以补充碘元素,其目的是预防 (填“甲状腺肿大”或“佝偻病”)。
②使用不锈钢锅将粽子煮熟,是利用了金属具有良好的 性。
③用洗洁精清洗餐具上的油污利用了洗洁精的 作用。
(2)在温室大棚种植蔬菜,经常向棚内施放 ,以促进植物的光合作用,提高蔬菜的产量和质量。
(3)新冠肺炎是一种急性感染性肺炎,做好自身防护是防止感染的重要措施。家庭和学校常备洗手液、酒精、一次性口罩、温度计等。
①佩戴口罩预防病毒的原理相当于化学实验中的 操作。
②活性炭口罩能有效阻隔空气中的氨、苯、甲醛等有害气体,其功能比普通口罩强大,原因是活性炭具有 性。
③医用酒精是75%酒精溶液,其溶剂是 。
④温度计有多种,常用的体温计有水银温度计,温度升高,水银柱会上升,从微观角度来解释是 。
【答案】(1) 甲状腺肿大; 导热; 乳化; (2)二氧化碳(CO2);
(3) 过滤; 吸附; 水(H2O); 温度升高,汞原子之间的间隔变大
21、若6.5克锌与100克稀硫酸恰好完全反应。
(1)在100克稀硫酸中,溶质的化学式是____,其质量是_____,溶剂的化学式是______,其质量为_____。
(2)完全反应后,所得溶液的质量为____,其中溶质的化学式为______,其质量为______。
【答案】H2SO4 9.8 H2O 90.2 106.3 ZnSO4 16.1
22、交点的含义:
如图所示,P点表示______,此时两种物质的饱和溶液中一定相等的是______。
【答案】t3℃时甲、乙的溶解度相等 溶解度、溶质质量分数
23、某同学配制50g质量分数为6%的NaC1溶液,整个操作过程如下图所示。
回答下列问题:
(1)配制溶液的正确操作顺序为___________(填序号),其中有错误的操作是___________(填序号)。
(2)用量筒量取液体时,读数时视线要与量筒内___________保持水平。
(3)改正上图中的错误操作后,经检测该同学配制的溶液质量分数偏小,可能的原因是___________(填一个原因即可)。
【答案】(1) ②①⑤③④ ①
(2)凹液面的最低处 (3)量取水时仰视读数(合理即可)
三、实验题。
24、请结合如图所示的实验,回答下列与燃烧有关的问题。
(1)甲实验中,能观察到的现象是 。
(2)乙实验中,向烧杯中加入一定量下列物质,不能使试管中白磷燃烧的是 。
ANaCl BNH4NO3 C浓H2SO4 DNaOH
(3)家用罐装燃气是液化石油气,它是石油化工的一种产品。石油属于(选填“可再生”或“不可再生” 能源,若厨房失火,要移走燃气罐,这样做利用的灭火原理是 。
【答案】(1)白磷燃烧,产生大量的白烟
(2)A、B (3)不可再生 移走可燃物
四、综合应用题。
25、溶液与人们的生产、生活密切相关。
(1)向澄清石灰水中通入二氧化碳直至过量的全过程中,下列转变关系正确的是______(填字母)。
A.溶液、乳浊液、溶液 B.溶液、悬溶液、乳浊液
C.悬溶液、乳浊液、溶液 D.溶液、悬浊液、溶液
(2)在盛有水的烧杯中加入以下某种物质,在形成溶液的过程中,溶液温度明显升高的是______(填字母)。
A.烧碱 B.硝酸铵 C.氯化钠
(3)如图为甲、乙两种固体物质的溶解度曲线。
①溶解度随温度升高而增大的物质是______(填“甲”或“乙”)。
②将t1℃时的甲、乙两种物质的饱和溶液升温至t2℃,所得溶液中溶质的质量分数甲______乙(填“<”、“=”或“>”)
③在t2℃时,某同学向128.5g甲溶液中加入1.5g甲固体恰好得到t2℃时甲的饱和溶液,则原甲溶液溶质的质量分数为______(结果精确到0.1%)。
(4)t2℃时,同学们在实验室配制一定量10%的甲溶液(已知水的密度为1g/cm3)。
①用8.0g甲(不含结晶水)固体配制10%的甲溶液,需要水______mL。
②将配好的溶液倒入洁净的______中(填容器名称),盖好塞子贴上标签。
③下列操作会导致配制的甲溶液的溶质质量分数偏低的是______。
A.甲固体中含有杂质
B.烧杯未干燥直接用于配制溶液
C.用量筒量取水时采用俯视方法读数
【答案】D A 甲 > 22.2% 72 细口瓶 AB
五、计算类题。
26、化学兴趣小组的同学用46g稀硫酸与一定质量的氧化铜恰好完全反应,反应后得到的溶液质量为50g。求:
(1)氧化铜的质量为:___________g。
(2)反应后所得溶液中溶质的质量分数。
【提示:CuO+H2SO4═CuSO4+H2O】
【答案】(1)4g。
(2)设反应后所得溶液中溶质的质量为x
解得:x=8g
反应后所得溶液中溶质的质量分数为:=16%
答:反应后所得溶液中溶质的质量分数为16%。
沪教版(全国)第6章 溶解现象
一、选择题。
1、如图所示,往烧杯中加入一定量的某固体,会引起试管内白磷燃烧,该固体可能是( )
A.氢氧化钠 B.硝酸铵 C.氯化钠 D.碳酸钙
2、用硝酸钾固体配制溶质的质量分数为10%的硝酸钾溶液50g。下列做法不正确的是( )
A.称量:用天平称量硝酸钾5g B.量取:用量筒量取蒸馏水45mL
C.溶解:将硝酸钾倒入量筒中溶解 D.转移:将配好的溶液转移至试剂瓶
3、下列关于溶液的说法正确的是( )
A.从一杯质量分数为10%的食盐溶液中倒出一半,余下的溶液质量分数为5%
B.某饱和溶液降温后析出晶体,此时它就变成不饱和溶液
C.向某物质的饱和溶液中加少量该物质,恒温下放置一定时间后,溶液中的溶质质量分数变大
D.稀溶液可能是饱和溶液,浓溶液也可能是不饱和溶液
4、某同学选用氢氧化钠固体与水配制20g溶质质量分数为10%的氢氧化钠溶液,下列说法错误的是( )
①需称取氢氧化钠固体2.0g
②称量前托盘天平应先检查游码是否归零,并调节平衡
③用托盘天平称量氢氧化钠固体时,为防止污染托盘,可将氢氧化钠放在纸上称量
④选用250mL量筒量取18mL的水
⑤存放溶液时,为确保数据准确,将试剂瓶用蒸馏水清洗后,立即倒入所配溶液封存
A. B. C. D.
5、下列物质不属于溶液的是( )
A.冰水 B.碘酒 C.食盐水 D.浓盐酸
6、实验室用氯化钠配制50g质量分数为6%的氯化钠溶液。下列说法中不正确的是( )
A.所需氯化钠的质量为3g
B.氯化钠放在托盘天平的左盘称量
C.俯视量筒读数会使所配溶液偏稀
D.所需玻璃仪器有烧杯、玻璃棒、量筒等
7、甲、乙两种固体物质的溶解度曲线如图所示。下列说法中正确的是( )
A.甲的溶解度比乙大
B.t2℃时,甲、乙饱和溶液的溶质质量分数都为30%
C.t3℃时,甲、乙的饱和溶液分别降温至t1℃,甲溶液饱和,乙溶液不饱和
D.t2℃时,质量相同的甲、乙饱和溶液分别升温至t3℃,为达饱和状态,需加入甲的质量大于乙
8、在配制一定溶质质量分数的蔗糖溶液时,导致溶液中蔗糖的质量分数偏大的可能原因有( )
A.用量筒量取水时俯视读数
B.用来配制溶液的烧杯刚用少量蒸馏水润洗过
C.用托盘天平称取蔗糖时,将蔗糖放在右盘,且称量时使用了游码
D.用了含少量杂质的蔗糖配制溶液
9、下列液体去除油污效果最好的是( )
A.洗洁精 B.食盐水 C.白醋 D.自来水
10、实验室用蔗糖配制50.0g溶质的质量分数为10%的蔗糖溶液,下列说法错误的是( )
A.用托盘天平称取5.0g蔗糖
B.用量程为10mL的量筒量取所需的水
C.溶解蔗糖时,使用的玻璃仪器有烧杯、玻璃棒
D.将配制好的溶液装入细口瓶中,塞好瓶塞并贴上标签
11、a、b、c三种不含结晶水的物质的溶解度曲线如图,下列说法正确的是( )
A.a的溶解度大于b的溶解度
B.将a的溶液由降温到,一定有晶体析出
C.时,50g的a溶于50g水,溶液的质量分数为
D.c的饱和溶液由降温到,溶液的质量分数不变
12、20℃时,NaCl的溶解度为36g。配制此温度下20g质量分数为5%的NaCl溶液,下列说法正确的是( )
A.配制该溶液需要5g NaCl
B.该溶液为饱和溶液
C.将该溶液长时间敞口放置,最终有晶体析出
D.配溶液时,量取所需体积的水倒入烧杯,有少量水洒出,则所配溶液浓度小于5%
13、向如图装置的试管中加入某种物质后,U形管右边支管的红墨水液面降低,左边支管的红墨水液面上升,则加入的物质是( )
A.氢氧化钠 B.生石灰 C.浓硫酸 D.硝酸铵
14、在配制一定溶质质量分数的氯化钠溶液时,出现下列失误操作,一定会使所配溶液的溶质质量分数偏低的是( )
A.用托盘天平称量氯化钠时,砝码放在左盘,未使用游码
B.量取蒸馏水,仰视量筒读数
C.将量筒中的水倒入烧杯时,有水洒出
D.将配好的溶液转移到细口瓶里,不慎洒出部分溶液
15、如图所示,向烧杯中加入某物质能使试管中的饱和石灰水变浑浊,该物质可能是( )
A.冰 B.硝酸铵固体 C.氯化钠固体 D.氢氧化钠固体
二、填空题。
16、将少量①橄榄油②醋③冰块④白糖⑤肥皂水⑥面粉,分别加入水中振荡,其中 形成乳浊液, 形成溶液(写序号)。
17、分别填写下列溶液中溶质和溶剂的名称:
(1)蔗糖溶液:溶质_______;溶剂________。
(2)碘酒(即碘的酒精溶液):溶质_______;溶剂________。
(3)乙醇的水溶液:溶质_______;溶剂________。
(4)0.9%的生理盐水:溶质_______;溶剂________。
18、回答下列问题
(1)固体的溶解度指在一定______下,某固态物质在______溶剂里达到______状态所溶解的______。
(2)20℃时,氯化钠在水中的溶解度为36 g,意思是20℃时,______水中达到______状态时溶解氯化钠的质量为______;或者20℃时,______水中______可溶解氯化钠的质量为36 g。
(3)物质的溶解性是根据______℃时的溶解度规定的,当该温度下物质的溶解度______10 g时,为易溶物质。
a.固体的溶解度从几个要素进行规定?______
b.要比较两种物质的溶解度,需要注意什么问题?______
19、从下图选择仪器,配置60g溶质质量分数为10%的NaCl溶液。
(1)需要称量NaCl的质量为____g。
(2)量取水用到的仪器有____(写名称)。
(3)从配好的溶液中倒出10g,其中溶质和溶剂的质量比为_____。
20、根据所学知识回答:
(1)端午节吃粽子是我国的传统习俗,制作粽子的原料有:糯米、大枣、瘦肉、加碘食盐等,根据学过的知识回答下列问题:
①原料中使用的加碘食盐可以补充碘元素,其目的是预防 (填“甲状腺肿大”或“佝偻病”)。
②使用不锈钢锅将粽子煮熟,是利用了金属具有良好的 性。
③用洗洁精清洗餐具上的油污利用了洗洁精的 作用。
(2)在温室大棚种植蔬菜,经常向棚内施放 ,以促进植物的光合作用,提高蔬菜的产量和质量。
(3)新冠肺炎是一种急性感染性肺炎,做好自身防护是防止感染的重要措施。家庭和学校常备洗手液、酒精、一次性口罩、温度计等。
①佩戴口罩预防病毒的原理相当于化学实验中的 操作。
②活性炭口罩能有效阻隔空气中的氨、苯、甲醛等有害气体,其功能比普通口罩强大,原因是活性炭具有 性。
③医用酒精是75%酒精溶液,其溶剂是 。
④温度计有多种,常用的体温计有水银温度计,温度升高,水银柱会上升,从微观角度来解释是 。
21、若6.5克锌与100克稀硫酸恰好完全反应。
(1)在100克稀硫酸中,溶质的化学式是____,其质量是_____,溶剂的化学式是______,其质量为_____。
(2)完全反应后,所得溶液的质量为____,其中溶质的化学式为______,其质量为______。
22、交点的含义:
如图所示,P点表示______,此时两种物质的饱和溶液中一定相等的是______。
23、某同学配制50g质量分数为6%的NaC1溶液,整个操作过程如下图所示。
回答下列问题:
(1)配制溶液的正确操作顺序为___________(填序号),其中有错误的操作是___________(填序号)。
(2)用量筒量取液体时,读数时视线要与量筒内___________保持水平。
(3)改正上图中的错误操作后,经检测该同学配制的溶液质量分数偏小,可能的原因是___________(填一个原因即可)。
三、实验题。
24、请结合如图所示的实验,回答下列与燃烧有关的问题。
(1)甲实验中,能观察到的现象是 。
(2)乙实验中,向烧杯中加入一定量下列物质,不能使试管中白磷燃烧的是 。
ANaCl BNH4NO3 C浓H2SO4 DNaOH
(3)家用罐装燃气是液化石油气,它是石油化工的一种产品。石油属于(选填“可再生”或“不可再生” 能源,若厨房失火,要移走燃气罐,这样做利用的灭火原理是 。
四、综合应用题。
25、溶液与人们的生产、生活密切相关。
(1)向澄清石灰水中通入二氧化碳直至过量的全过程中,下列转变关系正确的是______(填字母)。
A.溶液、乳浊液、溶液 B.溶液、悬溶液、乳浊液
C.悬溶液、乳浊液、溶液 D.溶液、悬浊液、溶液
(2)在盛有水的烧杯中加入以下某种物质,在形成溶液的过程中,溶液温度明显升高的是______(填字母)。
A.烧碱 B.硝酸铵 C.氯化钠
(3)如图为甲、乙两种固体物质的溶解度曲线。
①溶解度随温度升高而增大的物质是______(填“甲”或“乙”)。
②将t1℃时的甲、乙两种物质的饱和溶液升温至t2℃,所得溶液中溶质的质量分数甲______乙(填“<”、“=”或“>”)
③在t2℃时,某同学向128.5g甲溶液中加入1.5g甲固体恰好得到t2℃时甲的饱和溶液,则原甲溶液溶质的质量分数为______(结果精确到0.1%)。
(4)t2℃时,同学们在实验室配制一定量10%的甲溶液(已知水的密度为1g/cm3)。
①用8.0g甲(不含结晶水)固体配制10%的甲溶液,需要水______mL。
②将配好的溶液倒入洁净的______中(填容器名称),盖好塞子贴上标签。
③下列操作会导致配制的甲溶液的溶质质量分数偏低的是______。
A.甲固体中含有杂质
B.烧杯未干燥直接用于配制溶液
C.用量筒量取水时采用俯视方法读数
五、计算类题。
26、化学兴趣小组的同学用46g稀硫酸与一定质量的氧化铜恰好完全反应,反应后得到的溶液质量为50g。求:
(1)氧化铜的质量为:___________g。
(2)反应后所得溶液中溶质的质量分数。
【提示:CuO+H2SO4═CuSO4+H2O】
2022—2023学年化学沪教版(全国)九年级下册第6章 溶解现象 章末自检题含答案
沪教版(全国)第6章 溶解现象
一、选择题。
1、如图所示,往烧杯中加入一定量的某固体,会引起试管内白磷燃烧,该固体可能是( )
A.氢氧化钠 B.硝酸铵 C.氯化钠 D.碳酸钙
【答案】A
2、用硝酸钾固体配制溶质的质量分数为10%的硝酸钾溶液50g。下列做法不正确的是( )
A.称量:用天平称量硝酸钾5g B.量取:用量筒量取蒸馏水45mL
C.溶解:将硝酸钾倒入量筒中溶解 D.转移:将配好的溶液转移至试剂瓶
【答案】C
3、下列关于溶液的说法正确的是( )
A.从一杯质量分数为10%的食盐溶液中倒出一半,余下的溶液质量分数为5%
B.某饱和溶液降温后析出晶体,此时它就变成不饱和溶液
C.向某物质的饱和溶液中加少量该物质,恒温下放置一定时间后,溶液中的溶质质量分数变大
D.稀溶液可能是饱和溶液,浓溶液也可能是不饱和溶液
【答案】D
4、某同学选用氢氧化钠固体与水配制20g溶质质量分数为10%的氢氧化钠溶液,下列说法错误的是( )
①需称取氢氧化钠固体2.0g
②称量前托盘天平应先检查游码是否归零,并调节平衡
③用托盘天平称量氢氧化钠固体时,为防止污染托盘,可将氢氧化钠放在纸上称量
④选用250mL量筒量取18mL的水
⑤存放溶液时,为确保数据准确,将试剂瓶用蒸馏水清洗后,立即倒入所配溶液封存
A. B. C. D.
【答案】B
5、下列物质不属于溶液的是( )
A.冰水 B.碘酒 C.食盐水 D.浓盐酸
【答案】A
6、实验室用氯化钠配制50g质量分数为6%的氯化钠溶液。下列说法中不正确的是( )
A.所需氯化钠的质量为3g
B.氯化钠放在托盘天平的左盘称量
C.俯视量筒读数会使所配溶液偏稀
D.所需玻璃仪器有烧杯、玻璃棒、量筒等
【答案】C
7、甲、乙两种固体物质的溶解度曲线如图所示。下列说法中正确的是( )
A.甲的溶解度比乙大
B.t2℃时,甲、乙饱和溶液的溶质质量分数都为30%
C.t3℃时,甲、乙的饱和溶液分别降温至t1℃,甲溶液饱和,乙溶液不饱和
D.t2℃时,质量相同的甲、乙饱和溶液分别升温至t3℃,为达饱和状态,需加入甲的质量大于乙
【答案】D
8、在配制一定溶质质量分数的蔗糖溶液时,导致溶液中蔗糖的质量分数偏大的可能原因有( )
A.用量筒量取水时俯视读数
B.用来配制溶液的烧杯刚用少量蒸馏水润洗过
C.用托盘天平称取蔗糖时,将蔗糖放在右盘,且称量时使用了游码
D.用了含少量杂质的蔗糖配制溶液
【答案】A
9、下列液体去除油污效果最好的是( )
A.洗洁精 B.食盐水 C.白醋 D.自来水
【答案】A
10、实验室用蔗糖配制50.0g溶质的质量分数为10%的蔗糖溶液,下列说法错误的是( )
A.用托盘天平称取5.0g蔗糖
B.用量程为10mL的量筒量取所需的水
C.溶解蔗糖时,使用的玻璃仪器有烧杯、玻璃棒
D.将配制好的溶液装入细口瓶中,塞好瓶塞并贴上标签
【答案】B
11、a、b、c三种不含结晶水的物质的溶解度曲线如图,下列说法正确的是( )
A.a的溶解度大于b的溶解度
B.将a的溶液由降温到,一定有晶体析出
C.时,50g的a溶于50g水,溶液的质量分数为
D.c的饱和溶液由降温到,溶液的质量分数不变
【答案】D
12、20℃时,NaCl的溶解度为36g。配制此温度下20g质量分数为5%的NaCl溶液,下列说法正确的是( )
A.配制该溶液需要5g NaCl
B.该溶液为饱和溶液
C.将该溶液长时间敞口放置,最终有晶体析出
D.配溶液时,量取所需体积的水倒入烧杯,有少量水洒出,则所配溶液浓度小于5%
【答案】C
13、向如图装置的试管中加入某种物质后,U形管右边支管的红墨水液面降低,左边支管的红墨水液面上升,则加入的物质是( )
A.氢氧化钠 B.生石灰 C.浓硫酸 D.硝酸铵
【答案】D
14、在配制一定溶质质量分数的氯化钠溶液时,出现下列失误操作,一定会使所配溶液的溶质质量分数偏低的是( )
A.用托盘天平称量氯化钠时,砝码放在左盘,未使用游码
B.量取蒸馏水,仰视量筒读数
C.将量筒中的水倒入烧杯时,有水洒出
D.将配好的溶液转移到细口瓶里,不慎洒出部分溶液
【答案】B
15、如图所示,向烧杯中加入某物质能使试管中的饱和石灰水变浑浊,该物质可能是( )
A.冰 B.硝酸铵固体 C.氯化钠固体 D.氢氧化钠固体
【答案】D
二、填空题。
16、将少量①橄榄油②醋③冰块④白糖⑤肥皂水⑥面粉,分别加入水中振荡,其中 形成乳浊液, 形成溶液(写序号)。
【答案】; ①⑤; ②④
17、分别填写下列溶液中溶质和溶剂的名称:
(1)蔗糖溶液:溶质_______;溶剂________。
(2)碘酒(即碘的酒精溶液):溶质_______;溶剂________。
(3)乙醇的水溶液:溶质_______;溶剂________。
(4)0.9%的生理盐水:溶质_______;溶剂________。
【答案】(1) 蔗糖 水 (2) 碘 酒精
(3) 乙醇 水 (4) 氯化钠 水
18、回答下列问题
(1)固体的溶解度指在一定______下,某固态物质在______溶剂里达到______状态所溶解的______。
(2)20℃时,氯化钠在水中的溶解度为36 g,意思是20℃时,______水中达到______状态时溶解氯化钠的质量为______;或者20℃时,______水中______可溶解氯化钠的质量为36 g。
(3)物质的溶解性是根据______℃时的溶解度规定的,当该温度下物质的溶解度______10 g时,为易溶物质。
a.固体的溶解度从几个要素进行规定?______
b.要比较两种物质的溶解度,需要注意什么问题?______
【答案】(1) 温度 100g 饱和 质量
(2) 100g 饱和 36g 100g 最多
(3) 20 大于 一定温度、溶剂质量100g、饱和溶液、溶解质量 温度相同
19、从下图选择仪器,配置60g溶质质量分数为10%的NaCl溶液。
(1)需要称量NaCl的质量为____g。
(2)量取水用到的仪器有____(写名称)。
(3)从配好的溶液中倒出10g,其中溶质和溶剂的质量比为_____。
【答案】6 100mL量筒、胶头滴管(顺序可变) 1:9
20、根据所学知识回答:
(1)端午节吃粽子是我国的传统习俗,制作粽子的原料有:糯米、大枣、瘦肉、加碘食盐等,根据学过的知识回答下列问题:
①原料中使用的加碘食盐可以补充碘元素,其目的是预防 (填“甲状腺肿大”或“佝偻病”)。
②使用不锈钢锅将粽子煮熟,是利用了金属具有良好的 性。
③用洗洁精清洗餐具上的油污利用了洗洁精的 作用。
(2)在温室大棚种植蔬菜,经常向棚内施放 ,以促进植物的光合作用,提高蔬菜的产量和质量。
(3)新冠肺炎是一种急性感染性肺炎,做好自身防护是防止感染的重要措施。家庭和学校常备洗手液、酒精、一次性口罩、温度计等。
①佩戴口罩预防病毒的原理相当于化学实验中的 操作。
②活性炭口罩能有效阻隔空气中的氨、苯、甲醛等有害气体,其功能比普通口罩强大,原因是活性炭具有 性。
③医用酒精是75%酒精溶液,其溶剂是 。
④温度计有多种,常用的体温计有水银温度计,温度升高,水银柱会上升,从微观角度来解释是 。
【答案】(1) 甲状腺肿大; 导热; 乳化; (2)二氧化碳(CO2);
(3) 过滤; 吸附; 水(H2O); 温度升高,汞原子之间的间隔变大
21、若6.5克锌与100克稀硫酸恰好完全反应。
(1)在100克稀硫酸中,溶质的化学式是____,其质量是_____,溶剂的化学式是______,其质量为_____。
(2)完全反应后,所得溶液的质量为____,其中溶质的化学式为______,其质量为______。
【答案】H2SO4 9.8 H2O 90.2 106.3 ZnSO4 16.1
22、交点的含义:
如图所示,P点表示______,此时两种物质的饱和溶液中一定相等的是______。
【答案】t3℃时甲、乙的溶解度相等 溶解度、溶质质量分数
23、某同学配制50g质量分数为6%的NaC1溶液,整个操作过程如下图所示。
回答下列问题:
(1)配制溶液的正确操作顺序为___________(填序号),其中有错误的操作是___________(填序号)。
(2)用量筒量取液体时,读数时视线要与量筒内___________保持水平。
(3)改正上图中的错误操作后,经检测该同学配制的溶液质量分数偏小,可能的原因是___________(填一个原因即可)。
【答案】(1) ②①⑤③④ ①
(2)凹液面的最低处 (3)量取水时仰视读数(合理即可)
三、实验题。
24、请结合如图所示的实验,回答下列与燃烧有关的问题。
(1)甲实验中,能观察到的现象是 。
(2)乙实验中,向烧杯中加入一定量下列物质,不能使试管中白磷燃烧的是 。
ANaCl BNH4NO3 C浓H2SO4 DNaOH
(3)家用罐装燃气是液化石油气,它是石油化工的一种产品。石油属于(选填“可再生”或“不可再生” 能源,若厨房失火,要移走燃气罐,这样做利用的灭火原理是 。
【答案】(1)白磷燃烧,产生大量的白烟
(2)A、B (3)不可再生 移走可燃物
四、综合应用题。
25、溶液与人们的生产、生活密切相关。
(1)向澄清石灰水中通入二氧化碳直至过量的全过程中,下列转变关系正确的是______(填字母)。
A.溶液、乳浊液、溶液 B.溶液、悬溶液、乳浊液
C.悬溶液、乳浊液、溶液 D.溶液、悬浊液、溶液
(2)在盛有水的烧杯中加入以下某种物质,在形成溶液的过程中,溶液温度明显升高的是______(填字母)。
A.烧碱 B.硝酸铵 C.氯化钠
(3)如图为甲、乙两种固体物质的溶解度曲线。
①溶解度随温度升高而增大的物质是______(填“甲”或“乙”)。
②将t1℃时的甲、乙两种物质的饱和溶液升温至t2℃,所得溶液中溶质的质量分数甲______乙(填“<”、“=”或“>”)
③在t2℃时,某同学向128.5g甲溶液中加入1.5g甲固体恰好得到t2℃时甲的饱和溶液,则原甲溶液溶质的质量分数为______(结果精确到0.1%)。
(4)t2℃时,同学们在实验室配制一定量10%的甲溶液(已知水的密度为1g/cm3)。
①用8.0g甲(不含结晶水)固体配制10%的甲溶液,需要水______mL。
②将配好的溶液倒入洁净的______中(填容器名称),盖好塞子贴上标签。
③下列操作会导致配制的甲溶液的溶质质量分数偏低的是______。
A.甲固体中含有杂质
B.烧杯未干燥直接用于配制溶液
C.用量筒量取水时采用俯视方法读数
【答案】D A 甲 > 22.2% 72 细口瓶 AB
五、计算类题。
26、化学兴趣小组的同学用46g稀硫酸与一定质量的氧化铜恰好完全反应,反应后得到的溶液质量为50g。求:
(1)氧化铜的质量为:___________g。
(2)反应后所得溶液中溶质的质量分数。
【提示:CuO+H2SO4═CuSO4+H2O】
【答案】(1)4g。
(2)设反应后所得溶液中溶质的质量为x
解得:x=8g
反应后所得溶液中溶质的质量分数为:=16%
答:反应后所得溶液中溶质的质量分数为16%。
