化学九年级下册同步测试:6.3 物质的溶解性(含答案)
文档属性
| 名称 | 化学九年级下册同步测试:6.3 物质的溶解性(含答案) |

|
|
| 格式 | doc | ||
| 文件大小 | 244.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-02-10 00:00:00 | ||
图片预览


文档简介
第6单元 溶解现象
6.3 物质的溶解性
一、单选题(共14题;共28分)
1.下列说法中正确的是( )
A. 溶液一定是均一、无色、稳定的 B. 一种溶剂只能溶解一种溶质
C. 饱和溶液的溶质质量分数一定大于不饱和溶液 D. 海水晒盐属于蒸发结晶
2.关于生活中的化学,下列说法正确的是( )
A. 用厨房清洁剂除水垢
B. 喝完汽水打嗝是因为压强增大气体溶解度减小
C. 施用大量的化肥农药以提高农作物的产量
D. 人被蚊虫叮咬后常抹牙膏、肥皂水
3.据《说文解字》记载,我们的祖先在神农氏时代就开始利用海水晒盐。海水晒盐的原理是( )
A. 利用日晒,使海水分解
B. 利用日晒,使氯化钠的溶解能力变小
C. 利用阳光和风力,使海水中的水分蒸发
D. 利用阳光和风力,使海水中的氯化钠蒸发
4.下列条件下的氢氧化钙溶液,质量分数最大的是( )
A. 80℃的饱和溶液 B. 20℃的饱和溶液 C. 80℃的不饱和溶液 D. 20℃的不饱和溶液
5.下列有关饱和溶液的说法正确的是( )
A. 在一定量溶剂里,不能再溶解任何物质的溶液
B. 很浓的溶液
C. 不是稀溶液,也不是浓溶液
D. 在一定温度下,在一定量的溶剂里,不能再溶解某种溶质的溶液
6.新制的凉开水不宜养鱼,其主要原因是凉开水中几乎不含( )
A. 氧分子 B. 氧原子 C. 氧元素 D. 病菌
7.通常情况下,将一杯不饱和的蔗糖溶液变成饱和溶液,最适宜的方法是( )
A. 加蔗糖 B. 加水 C. 升温 D. 增大压强
8.20℃时,氯化钠的溶解度为36 g。对这句话理解错误的是( )
A. 20℃时,100 g水中最多能溶解氯化钠36 g
B. 20℃时,100 g氯化钠饱和溶液中含氯化钠36 g
C. 20℃时,氯化钠饱和溶液中水与氯化钠的质量比为100:36
D. 20℃时,将36 g氯化钠溶解于100 g水中,所得溶液为该温度下氯化钠的饱和溶液
9.60℃时,化合物甲的溶解度比乙的大。分别取等质量60℃时的甲、乙饱和液,降温至20℃后,析出甲和乙的质量分别为a g和b g(甲、乙均无结晶水)。以下叙述中正确的是( )
A. 60℃时等质量的甲饱和溶液与乙饱和溶液相比,前者所含溶质的质量小
B. a一定大于b
C. 20℃时,若甲的溶解度比乙的小,则a一定大于b
D. 20℃时,若甲的溶解度仍比乙的大,则a一定小于b
10.下列有关溶液的知识中,不正确的是( )
A. 析出晶体后的溶液,是该温度下该物质的饱和溶液
B. 固体物质的溶解度都是随着温度的升高而增大
C. 在同一温度下同种溶质的饱和溶液一定比它的不饱和溶液的浓度大
D. 溶液都是均一、稳定的
11.如图是甲、乙两种固体物质的溶解度曲线.下列说法错误的是( )
A. T℃时,甲、乙两物质的溶解度相等
B. 乙的饱和溶液降温时,溶质质量分数保持不变
C. 甲中混有少量乙,可采用降温结晶的方法提纯甲
D. T℃时,甲的饱和溶液溶质质量分数为20%
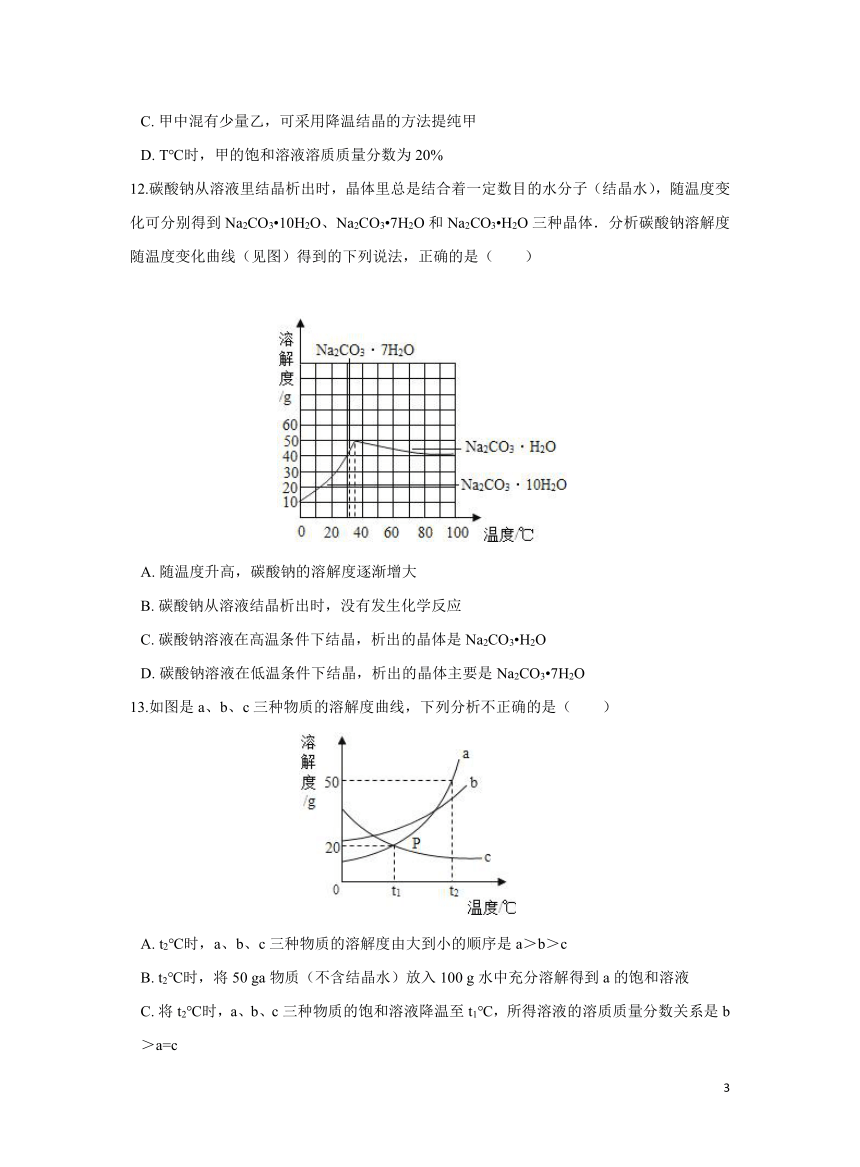
12.碳酸钠从溶液里结晶析出时,晶体里总是结合着一定数目的水分子(结晶水),随温度变化可分别得到Na2CO3 10H2O、Na2CO3 7H2O和Na2CO3 H2O三种晶体.分析碳酸钠溶解度随温度变化曲线(见图)得到的下列说法,正确的是( )
A. 随温度升高,碳酸钠的溶解度逐渐增大
B. 碳酸钠从溶液结晶析出时,没有发生化学反应
C. 碳酸钠溶液在高温条件下结晶,析出的晶体是Na2CO3 H2O
D. 碳酸钠溶液在低温条件下结晶,析出的晶体主要是Na2CO3 7H2O
13.如图是a、b、c三种物质的溶解度曲线,下列分析不正确的是( )
A. t2℃时,a、b、c三种物质的溶解度由大到小的顺序是a>b>c
B. t2℃时,将50 ga物质(不含结晶水)放入100 g水中充分溶解得到a的饱和溶液
C. 将t2℃时,a、b、c三种物质的饱和溶液降温至t1℃,所得溶液的溶质质量分数关系是b>a=c
D. 将c的饱和溶液变为不饱和溶液,可采用降温的方法
14.20℃时,将等质量的a、b两种固体,分别加入到盛有100 g水的烧杯中,充分搅拌后现象如图甲,升温到50℃时,现象如图乙,a、b两种固体的溶解度曲线如图丙。下列说法正确的是( )
A. 图丙中M表示b的溶解度曲线 B. 图甲溶液中溶质的质量分数a大于b
C. 图乙中a、b溶液一定是不饱和溶液 D. 30℃时a、b溶液溶质质量分数不相等
二、填空题(共1题;共3分)
15.如图为甲、乙两种固体物质在水中的溶解度曲线,据此回答下列问题:
(1)在40℃时甲、乙两种固体物质的溶解度________(填“相同”或“不同”)。
(2)两种物质中________物质的溶解度随温度的升高而降低。(填“甲”或“乙”)。
(3)若要从甲的60℃的饱和溶液中得到甲(固态),应该采用________ 的方法。(填序号)
A.升高温度到70℃ B.降低温度 C.加入一定量的水
三、解答题(共1题;共8分)
16.水与溶液在生产生活中有着广泛的用途。请你结合所学知识回答下列问题:
(1)镜湖是临河区的一个重要的旅游景点,“五 一”期间小明一家去镜湖旅游。
①小明带去“自热米饭”的加热原理是饭盒夹层中的水与生石灰反应生成氢氧化钙,放出大量的热,该反应的化学方程式为________。
②小明从镜湖中取回一瓶水,为检验这瓶水的硬度,可向水中加入________。生活中,常采用________的方法来降低水的硬度。
③回家后,小明用洗洁精清洗餐县上的油污,是因为洗洁精具有________作用。
(2)如图一所示:不含结晶水的甲、乙、丙三种固体物质的溶解度曲线,看图并回答下列问题。
M点表示的含义是________(合理即可)。
②t3℃时,将35 g甲物质加入到50 g水中,充分溶解后所得溶液的质量是________g。
③t3℃时,将等质量的甲、乙、丙三种物质的饱和溶液分别降温至t1℃,所得溶液中溶质质量分数由大到小的顺序是________。
(3)如图二所示,20℃时,把试管放入盛有X的饱和溶液的烧杯中,在试管中加入一小块生石灰,再加入适量的水,烧杯中的溶液逐渐变浑浊,则X可能为________(填“甲”或“乙”或“丙”)固体物质。
四、综合题(共1题;共5分)
17.硝酸钾和氯化钾两种物质的溶解度曲线见下图,这两种物质的溶解度见下表。
温度/℃ 10 20 30 40 50 60
溶解度/g 甲 20.9 31.6 45.8 63.9 85.5 110
乙 31.0 34.0 37.0 40.0 42.6 45.5
请回答下列问题:
(1)观察溶解度曲线和溶解度表,判断物质乙是指________(填写化学式)。
(2)60℃时,饱和KNO3溶液中混有少量KCl,应采用________的方法提纯KNO3(填写“蒸发溶剂”或“冷却结晶”)。
(3)60℃时,分别将等质量的KNO3和KCl两种物质的饱和溶液温度降至t ℃,析出晶体的质量关系为:KNO3________ KCl(填写“>”“=”或“<”)。
(4)如图所示,20℃时,将一定质量的KNO3固体放入盛水的试管中,发现有少量固体未溶解,向烧杯的水中加入某物质后,试管内固体能完全溶解。则加入的物质可以是________(填写字母标号)。
①冰块 ②生石灰固体 ③硝酸铵固体 ④干冰 ⑤浓硫酸 ⑥氢氧化钠固体
A.①③④ B.②⑤⑥ C.①③⑤ D.②④⑥
(5)60 ℃时,将45 g KCl固体溶解于100 g水中,降温至20 ℃,析出晶体的质量是________。
参考答案
一、单选题
1.D 2.D 3. C 4.B 5.D 6.A 7.A 8.B 9.C 10.B 11.D 12.C 13.C 14.C
二、填空题(共1题;共3分)
15.【答案】 相同 ;乙 ;B
三、解答题(共1题;共8分)
16.【答案】 (1);肥皂水;煮沸;乳化 (2)t2℃时,甲、丙物质的溶解度相等;80;乙>丙>甲 (3)丙
四、综合题(共1题;共5分)
17.【答案】 (1)KCl (2)冷却结晶 (3)> (4)B (5)11 g (或11.0 g,漏写单位不得分)
1
6.3 物质的溶解性
一、单选题(共14题;共28分)
1.下列说法中正确的是( )
A. 溶液一定是均一、无色、稳定的 B. 一种溶剂只能溶解一种溶质
C. 饱和溶液的溶质质量分数一定大于不饱和溶液 D. 海水晒盐属于蒸发结晶
2.关于生活中的化学,下列说法正确的是( )
A. 用厨房清洁剂除水垢
B. 喝完汽水打嗝是因为压强增大气体溶解度减小
C. 施用大量的化肥农药以提高农作物的产量
D. 人被蚊虫叮咬后常抹牙膏、肥皂水
3.据《说文解字》记载,我们的祖先在神农氏时代就开始利用海水晒盐。海水晒盐的原理是( )
A. 利用日晒,使海水分解
B. 利用日晒,使氯化钠的溶解能力变小
C. 利用阳光和风力,使海水中的水分蒸发
D. 利用阳光和风力,使海水中的氯化钠蒸发
4.下列条件下的氢氧化钙溶液,质量分数最大的是( )
A. 80℃的饱和溶液 B. 20℃的饱和溶液 C. 80℃的不饱和溶液 D. 20℃的不饱和溶液
5.下列有关饱和溶液的说法正确的是( )
A. 在一定量溶剂里,不能再溶解任何物质的溶液
B. 很浓的溶液
C. 不是稀溶液,也不是浓溶液
D. 在一定温度下,在一定量的溶剂里,不能再溶解某种溶质的溶液
6.新制的凉开水不宜养鱼,其主要原因是凉开水中几乎不含( )
A. 氧分子 B. 氧原子 C. 氧元素 D. 病菌
7.通常情况下,将一杯不饱和的蔗糖溶液变成饱和溶液,最适宜的方法是( )
A. 加蔗糖 B. 加水 C. 升温 D. 增大压强
8.20℃时,氯化钠的溶解度为36 g。对这句话理解错误的是( )
A. 20℃时,100 g水中最多能溶解氯化钠36 g
B. 20℃时,100 g氯化钠饱和溶液中含氯化钠36 g
C. 20℃时,氯化钠饱和溶液中水与氯化钠的质量比为100:36
D. 20℃时,将36 g氯化钠溶解于100 g水中,所得溶液为该温度下氯化钠的饱和溶液
9.60℃时,化合物甲的溶解度比乙的大。分别取等质量60℃时的甲、乙饱和液,降温至20℃后,析出甲和乙的质量分别为a g和b g(甲、乙均无结晶水)。以下叙述中正确的是( )
A. 60℃时等质量的甲饱和溶液与乙饱和溶液相比,前者所含溶质的质量小
B. a一定大于b
C. 20℃时,若甲的溶解度比乙的小,则a一定大于b
D. 20℃时,若甲的溶解度仍比乙的大,则a一定小于b
10.下列有关溶液的知识中,不正确的是( )
A. 析出晶体后的溶液,是该温度下该物质的饱和溶液
B. 固体物质的溶解度都是随着温度的升高而增大
C. 在同一温度下同种溶质的饱和溶液一定比它的不饱和溶液的浓度大
D. 溶液都是均一、稳定的
11.如图是甲、乙两种固体物质的溶解度曲线.下列说法错误的是( )
A. T℃时,甲、乙两物质的溶解度相等
B. 乙的饱和溶液降温时,溶质质量分数保持不变
C. 甲中混有少量乙,可采用降温结晶的方法提纯甲
D. T℃时,甲的饱和溶液溶质质量分数为20%
12.碳酸钠从溶液里结晶析出时,晶体里总是结合着一定数目的水分子(结晶水),随温度变化可分别得到Na2CO3 10H2O、Na2CO3 7H2O和Na2CO3 H2O三种晶体.分析碳酸钠溶解度随温度变化曲线(见图)得到的下列说法,正确的是( )
A. 随温度升高,碳酸钠的溶解度逐渐增大
B. 碳酸钠从溶液结晶析出时,没有发生化学反应
C. 碳酸钠溶液在高温条件下结晶,析出的晶体是Na2CO3 H2O
D. 碳酸钠溶液在低温条件下结晶,析出的晶体主要是Na2CO3 7H2O
13.如图是a、b、c三种物质的溶解度曲线,下列分析不正确的是( )
A. t2℃时,a、b、c三种物质的溶解度由大到小的顺序是a>b>c
B. t2℃时,将50 ga物质(不含结晶水)放入100 g水中充分溶解得到a的饱和溶液
C. 将t2℃时,a、b、c三种物质的饱和溶液降温至t1℃,所得溶液的溶质质量分数关系是b>a=c
D. 将c的饱和溶液变为不饱和溶液,可采用降温的方法
14.20℃时,将等质量的a、b两种固体,分别加入到盛有100 g水的烧杯中,充分搅拌后现象如图甲,升温到50℃时,现象如图乙,a、b两种固体的溶解度曲线如图丙。下列说法正确的是( )
A. 图丙中M表示b的溶解度曲线 B. 图甲溶液中溶质的质量分数a大于b
C. 图乙中a、b溶液一定是不饱和溶液 D. 30℃时a、b溶液溶质质量分数不相等
二、填空题(共1题;共3分)
15.如图为甲、乙两种固体物质在水中的溶解度曲线,据此回答下列问题:
(1)在40℃时甲、乙两种固体物质的溶解度________(填“相同”或“不同”)。
(2)两种物质中________物质的溶解度随温度的升高而降低。(填“甲”或“乙”)。
(3)若要从甲的60℃的饱和溶液中得到甲(固态),应该采用________ 的方法。(填序号)
A.升高温度到70℃ B.降低温度 C.加入一定量的水
三、解答题(共1题;共8分)
16.水与溶液在生产生活中有着广泛的用途。请你结合所学知识回答下列问题:
(1)镜湖是临河区的一个重要的旅游景点,“五 一”期间小明一家去镜湖旅游。
①小明带去“自热米饭”的加热原理是饭盒夹层中的水与生石灰反应生成氢氧化钙,放出大量的热,该反应的化学方程式为________。
②小明从镜湖中取回一瓶水,为检验这瓶水的硬度,可向水中加入________。生活中,常采用________的方法来降低水的硬度。
③回家后,小明用洗洁精清洗餐县上的油污,是因为洗洁精具有________作用。
(2)如图一所示:不含结晶水的甲、乙、丙三种固体物质的溶解度曲线,看图并回答下列问题。
M点表示的含义是________(合理即可)。
②t3℃时,将35 g甲物质加入到50 g水中,充分溶解后所得溶液的质量是________g。
③t3℃时,将等质量的甲、乙、丙三种物质的饱和溶液分别降温至t1℃,所得溶液中溶质质量分数由大到小的顺序是________。
(3)如图二所示,20℃时,把试管放入盛有X的饱和溶液的烧杯中,在试管中加入一小块生石灰,再加入适量的水,烧杯中的溶液逐渐变浑浊,则X可能为________(填“甲”或“乙”或“丙”)固体物质。
四、综合题(共1题;共5分)
17.硝酸钾和氯化钾两种物质的溶解度曲线见下图,这两种物质的溶解度见下表。
温度/℃ 10 20 30 40 50 60
溶解度/g 甲 20.9 31.6 45.8 63.9 85.5 110
乙 31.0 34.0 37.0 40.0 42.6 45.5
请回答下列问题:
(1)观察溶解度曲线和溶解度表,判断物质乙是指________(填写化学式)。
(2)60℃时,饱和KNO3溶液中混有少量KCl,应采用________的方法提纯KNO3(填写“蒸发溶剂”或“冷却结晶”)。
(3)60℃时,分别将等质量的KNO3和KCl两种物质的饱和溶液温度降至t ℃,析出晶体的质量关系为:KNO3________ KCl(填写“>”“=”或“<”)。
(4)如图所示,20℃时,将一定质量的KNO3固体放入盛水的试管中,发现有少量固体未溶解,向烧杯的水中加入某物质后,试管内固体能完全溶解。则加入的物质可以是________(填写字母标号)。
①冰块 ②生石灰固体 ③硝酸铵固体 ④干冰 ⑤浓硫酸 ⑥氢氧化钠固体
A.①③④ B.②⑤⑥ C.①③⑤ D.②④⑥
(5)60 ℃时,将45 g KCl固体溶解于100 g水中,降温至20 ℃,析出晶体的质量是________。
参考答案
一、单选题
1.D 2.D 3. C 4.B 5.D 6.A 7.A 8.B 9.C 10.B 11.D 12.C 13.C 14.C
二、填空题(共1题;共3分)
15.【答案】 相同 ;乙 ;B
三、解答题(共1题;共8分)
16.【答案】 (1);肥皂水;煮沸;乳化 (2)t2℃时,甲、丙物质的溶解度相等;80;乙>丙>甲 (3)丙
四、综合题(共1题;共5分)
17.【答案】 (1)KCl (2)冷却结晶 (3)> (4)B (5)11 g (或11.0 g,漏写单位不得分)
1
