原子结构的模型(第2课时)
图片预览





文档简介
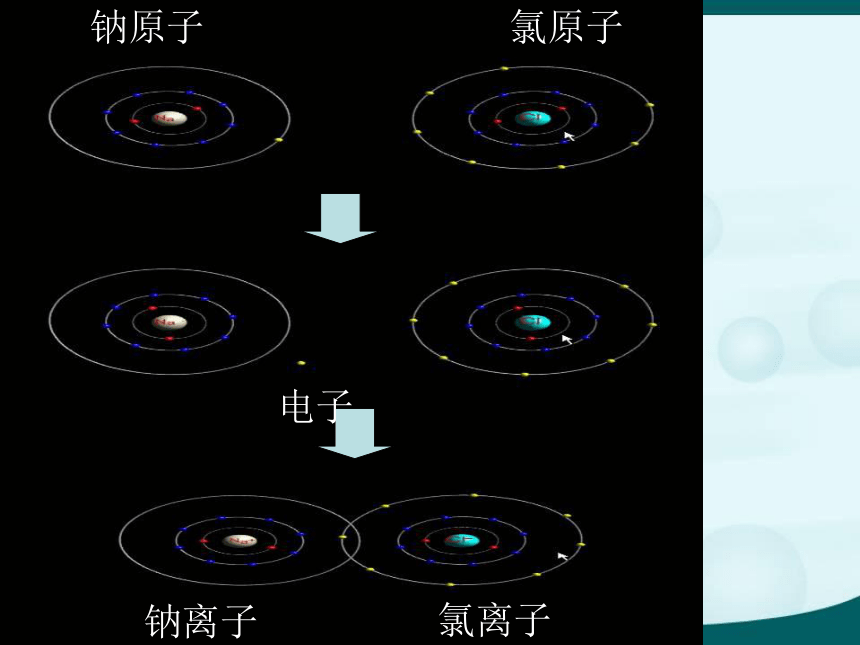
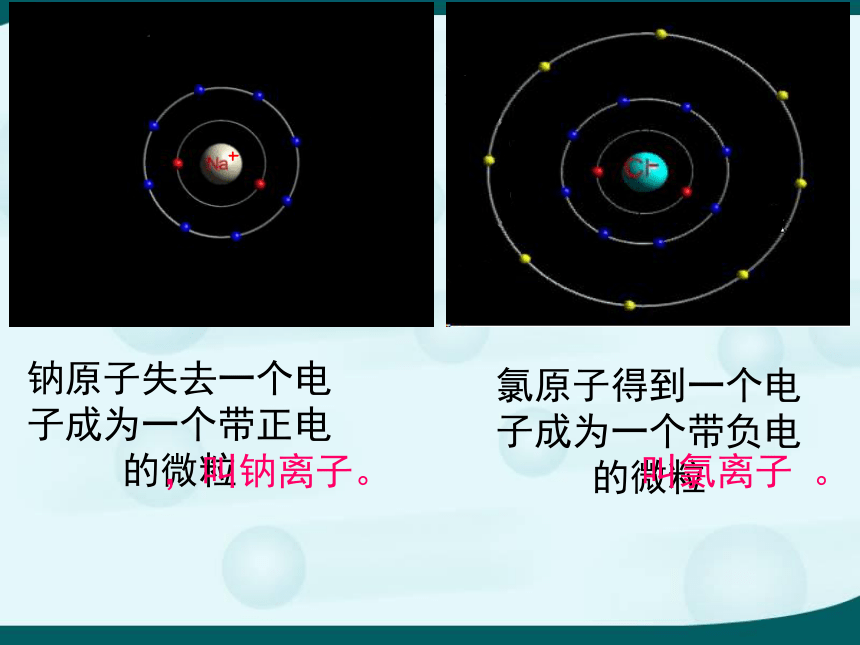
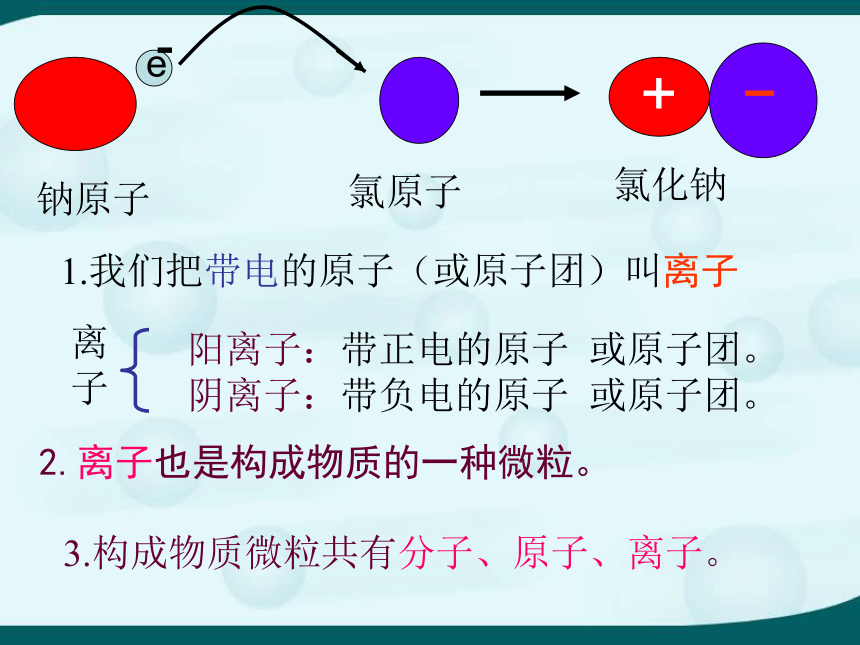
课件29张PPT。一、温故知新1、大量科学实验证明:原子是由———与————构成的,————在原子核周围作高速运动。电子带———电荷,整个原子不显电性的原因是——————————————。原子核核外电子核外电子负电原子核所带正电核与核外电子所带负电荷数目相等,电性相反2、回忆卢瑟福实验,该实验不能证明的是( )A、原子核极其微小B、原子不是实心球体,大部分空间是空的C、а粒子发生偏转是因为同种电荷互相排斥D、原子核质量比电子大D第三节 原子结构的模型(2)三、带电的原子——离子黄绿色气体银白色实验现象:钠继续燃烧,产生黄色火焰,燃烧后剩下白色粉末物质(氯化钠),放出大量的热。这个化学反应如何用粒子知识来解释呢?钠原子氯原子电子钠离子氯离子钠原子失去一个电子成为一个带正电的微粒氯原子得到一个电子成为一个带负电的微粒 ,叫钠离子。 叫氯离子 。 e+钠原子氯原子氯化钠1.我们把带电的原子(或原子团)叫离子2.离子也是构成物质的一种微粒。3.构成物质微粒共有分子、原子、离子。阳离子:带正电的原子 或原子团。
阴离子:带负电的原子 或原子团。离子硫酸铜晶体是由_______________、
_____________和____________构成铜离子硫酸根离子结晶水原子团:
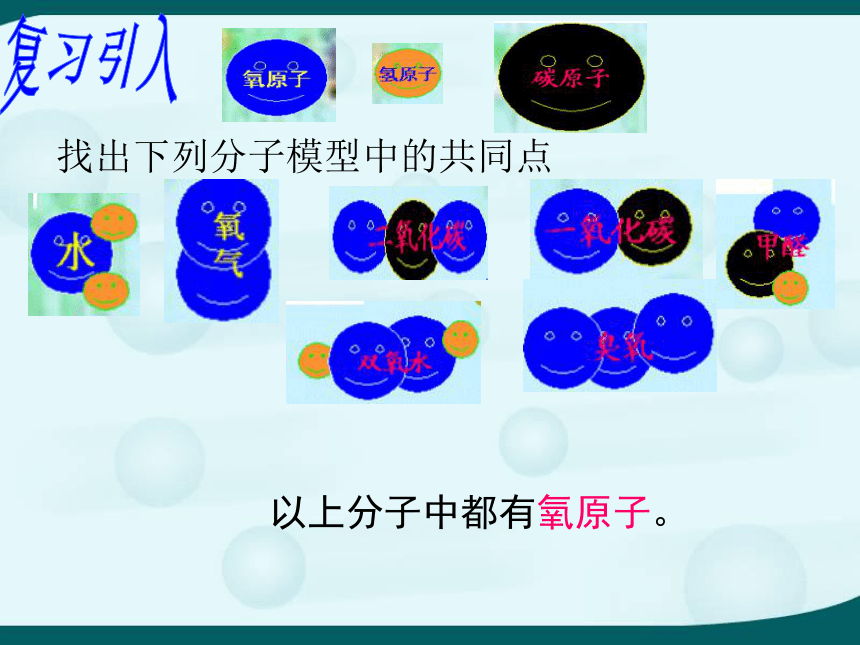
几个原子结合在一起,在许多化学反应中做为一个整体参加,好像一个原子一样,这样的原子的集团叫做原子团。硫酸根离子SO42-复习引入找出下列分子模型中的共同点以上分子中都有氧原子。下面氧的三种原子的原子核有什么不同?A原子核中有( )个质子,( )中子;B原子核中有( )个质子,( )个中子;C原子核中有( )个质子,( )个中子。8889810C思考:1、A、B、C 三种原子中,核外电子数分别是多少? 2、这三种原子的原子核内质子数、中子数关系如何?板书四、同位素1、元素的定义:具有相同核电荷数(即质子数)的同一类原子总称为元素。说明:元素的分类是以质子数(核电荷数)为依据的。 由中子数关系可知,同样是氧原子,氧原子的核内中子数可以不一样。将上述三种氧原子互称为氧的同位素原子。 这些氧原子的原子核中都有8个质子数,核电荷数也为8,这些氧原子总称为氧元素。 板书2、同位素原子:
(1)概念:同类元素中质子数相同而中子数不相同的原子称为同位素原子。例:见课本中氧的三种原子。思考1:同位素原子如何表示?如三种氧原子是否是氧A、氧B、氧C呢?H11H21H31同样是氢元素,其核内的中子数也不一样,统称为氢的三种同位素原子。(2)表示:氢的同位素原子还可表示为:
氕 1H 氘 2 H 氚 3 H111方法1、中子数、质子数之和质子数元素符号方法2、元素符号质子数、中子数之和如:C 12 Na 23元素与同位素原子的区别:
元素是互为同位素原子的总称,
同位素原子是一种元素的不同种原子。同位素原子在工业、农业、医疗、国防等方面有着广泛的应用利用碳-14同位素测定年代(3)、常见元素的同位素及其符号和用途 示踪三、带电的原子——离子小结:四、元素和同位素1、元素的定义:具有相同核电荷数(即质子数)的同一类原子总称为元素。2、在同一个原子中
核电荷数 = 质子数 = 核外电子数 ≠中子数3、同位素原子的定义:原子中原子核内质子数相同、中子数不同的同类原子统称为同位素原子。4、常见元素的同位素及其符号和用途 1. 列表比较氢的3种同位素原子。1 0 11 1 11 2 12. 以氧原子为例,说明构成原子的粒子有哪几种,它们是怎样构成原子的?为什么整个原子不显电性?构成氧原子的粒子有原子核内的质子、中子和核外电子,其中质子带正电荷、中子不带电、电子带负电荷。由于原子核内质子所带的正电荷数与核外电子所带的负电荷数在数值上相等,所以整个原子不显电性。4. 有3种不同的原子,甲原子核内有6个质子和6个中子,乙原子核内有6个质子和8个中子,丙原子核内有7个质子和7个中子。下列说法正确的是( )
A. 甲和乙是同一种元素
B. 甲和乙的核电荷数不同
C. 乙和丙核外电子数相等
D. 乙和丙互为同位素原子A将物质与直接构成物质的粒子用线连起来:
金属铜 原子
硫酸铜晶体
干 冰(固体二氧化碳) 离子
金刚石(碳)
水蒸气 分子练习:1、 我国发射的一颗绕月探测卫星,其任务之一是寻找一种新能源——氦3。氦3的原子核是由一个中子和两个质子构成的,其原子核外电子数为( )
A、1 B、2 C、3 D、6B3.有两种原子,所含的质子数相同,下列说法正确的是( )
A.它们属于同种元素
B.它们属于不同种元素
C.它们属于同种原子
D.以上叙述都不对
4.氕、氘、氚三种原子的______相同,互为____________。 A质子数同位素原子5.具有相同_________的同类原子总称为元素,铁钉、铁锈中都含有________。
6.元素的种类决定于原子的( )
A.中子数 B.质子数
C.相对原子质量 D.电子数核电荷数铁元素B7.下列有关氯化钠的叙述正确的是( )
A.氯化钠由氯化钠分子构成
B.氯化钠由钠原子和氯原子构成
C.氯化钠由钠离子和氯离子构成
D.以上叙述都不对 C10.下列叙述正确的是( )
A.二氧化碳是由碳和氧气组成的
B.1个二氧化碳分子是由2个氧原子和1个碳原子构成的
C.二氧化碳是由碳原子和氧原子组成的
D.二氧化碳由2个氧原子和1个碳原子构成B11.下列有关原子的说法正确的是 ( )
A.原子是不可再分的最小微粒
B.原子都是由质子、中子和电子构成的
C.原子的类别是由原子核内的质子数决定的
D.以上说法都不确切 C12.下列叙述正确的是( )
A、属于同位素不同原子即其核电荷数相同但核外电子数不同。
B、属于同位素不同原子即其核电荷数相同但中子数不同。
C、属于同位素不同原子即其核外电子数相同但核电荷数不同。
D、属于同位素不同原子即其中子数相同但核外电子数不同。B
阴离子:带负电的原子 或原子团。离子硫酸铜晶体是由_______________、
_____________和____________构成铜离子硫酸根离子结晶水原子团:
几个原子结合在一起,在许多化学反应中做为一个整体参加,好像一个原子一样,这样的原子的集团叫做原子团。硫酸根离子SO42-复习引入找出下列分子模型中的共同点以上分子中都有氧原子。下面氧的三种原子的原子核有什么不同?A原子核中有( )个质子,( )中子;B原子核中有( )个质子,( )个中子;C原子核中有( )个质子,( )个中子。8889810C思考:1、A、B、C 三种原子中,核外电子数分别是多少? 2、这三种原子的原子核内质子数、中子数关系如何?板书四、同位素1、元素的定义:具有相同核电荷数(即质子数)的同一类原子总称为元素。说明:元素的分类是以质子数(核电荷数)为依据的。 由中子数关系可知,同样是氧原子,氧原子的核内中子数可以不一样。将上述三种氧原子互称为氧的同位素原子。 这些氧原子的原子核中都有8个质子数,核电荷数也为8,这些氧原子总称为氧元素。 板书2、同位素原子:
(1)概念:同类元素中质子数相同而中子数不相同的原子称为同位素原子。例:见课本中氧的三种原子。思考1:同位素原子如何表示?如三种氧原子是否是氧A、氧B、氧C呢?H11H21H31同样是氢元素,其核内的中子数也不一样,统称为氢的三种同位素原子。(2)表示:氢的同位素原子还可表示为:
氕 1H 氘 2 H 氚 3 H111方法1、中子数、质子数之和质子数元素符号方法2、元素符号质子数、中子数之和如:C 12 Na 23元素与同位素原子的区别:
元素是互为同位素原子的总称,
同位素原子是一种元素的不同种原子。同位素原子在工业、农业、医疗、国防等方面有着广泛的应用利用碳-14同位素测定年代(3)、常见元素的同位素及其符号和用途 示踪三、带电的原子——离子小结:四、元素和同位素1、元素的定义:具有相同核电荷数(即质子数)的同一类原子总称为元素。2、在同一个原子中
核电荷数 = 质子数 = 核外电子数 ≠中子数3、同位素原子的定义:原子中原子核内质子数相同、中子数不同的同类原子统称为同位素原子。4、常见元素的同位素及其符号和用途 1. 列表比较氢的3种同位素原子。1 0 11 1 11 2 12. 以氧原子为例,说明构成原子的粒子有哪几种,它们是怎样构成原子的?为什么整个原子不显电性?构成氧原子的粒子有原子核内的质子、中子和核外电子,其中质子带正电荷、中子不带电、电子带负电荷。由于原子核内质子所带的正电荷数与核外电子所带的负电荷数在数值上相等,所以整个原子不显电性。4. 有3种不同的原子,甲原子核内有6个质子和6个中子,乙原子核内有6个质子和8个中子,丙原子核内有7个质子和7个中子。下列说法正确的是( )
A. 甲和乙是同一种元素
B. 甲和乙的核电荷数不同
C. 乙和丙核外电子数相等
D. 乙和丙互为同位素原子A将物质与直接构成物质的粒子用线连起来:
金属铜 原子
硫酸铜晶体
干 冰(固体二氧化碳) 离子
金刚石(碳)
水蒸气 分子练习:1、 我国发射的一颗绕月探测卫星,其任务之一是寻找一种新能源——氦3。氦3的原子核是由一个中子和两个质子构成的,其原子核外电子数为( )
A、1 B、2 C、3 D、6B3.有两种原子,所含的质子数相同,下列说法正确的是( )
A.它们属于同种元素
B.它们属于不同种元素
C.它们属于同种原子
D.以上叙述都不对
4.氕、氘、氚三种原子的______相同,互为____________。 A质子数同位素原子5.具有相同_________的同类原子总称为元素,铁钉、铁锈中都含有________。
6.元素的种类决定于原子的( )
A.中子数 B.质子数
C.相对原子质量 D.电子数核电荷数铁元素B7.下列有关氯化钠的叙述正确的是( )
A.氯化钠由氯化钠分子构成
B.氯化钠由钠原子和氯原子构成
C.氯化钠由钠离子和氯离子构成
D.以上叙述都不对 C10.下列叙述正确的是( )
A.二氧化碳是由碳和氧气组成的
B.1个二氧化碳分子是由2个氧原子和1个碳原子构成的
C.二氧化碳是由碳原子和氧原子组成的
D.二氧化碳由2个氧原子和1个碳原子构成B11.下列有关原子的说法正确的是 ( )
A.原子是不可再分的最小微粒
B.原子都是由质子、中子和电子构成的
C.原子的类别是由原子核内的质子数决定的
D.以上说法都不确切 C12.下列叙述正确的是( )
A、属于同位素不同原子即其核电荷数相同但核外电子数不同。
B、属于同位素不同原子即其核电荷数相同但中子数不同。
C、属于同位素不同原子即其核外电子数相同但核电荷数不同。
D、属于同位素不同原子即其中子数相同但核外电子数不同。B
同课章节目录
- 第1章 电与磁
- 第1节 指南针为什么能指方向
- 第2节 电生磁
- 第3节 电磁铁的应用
- 第4节 电动机
- 第5节 磁生电
- 第6节 家庭用电
- 第7节 电的安全使用
- 第2章 微粒的模型与符号
- 第1节 模型、符号的建立与作用
- 第2节 物质的微观粒子模型
- 第3节 原子结构的模型
- 第4节 组成物质的元素
- 第5节 表示元素的符号
- 第6节 表示物质的符号
- 第7节 元素符号表示的量
- 第3章 空气与生命
- 第1节 空气与氧气
- 第2节 氧化和燃烧
- 第3节 化学方程式
- 第4节 二氧化碳
- 第5节 生物的呼吸和呼吸作用
- 第6节 光合作用
- 第7节 自然界中的氧循环和碳循环
- 第8节 空气污染与保护
- 第4章 植物与土壤
- 第1节 土壤的成分
- 第2节 各种各样的土壤
- 第3节 植物的根与物质吸收
- 第4节 植物的茎与物质运输
- 第5节 植物的叶与蒸腾作用
- 第6节 保护土壤
- 研究性学习课题
- 一 设计简单的电磁控制电路
- 二 化学反应中质量守恒的研究
- 三 研究植物的呼吸
- 四 当地水土状况调查
