化学九年级下册同步测试:7.1 溶液的酸碱性(含答案)
文档属性
| 名称 | 化学九年级下册同步测试:7.1 溶液的酸碱性(含答案) |

|
|
| 格式 | doc | ||
| 文件大小 | 294.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-02-13 00:00:00 | ||
图片预览


文档简介
第七章 应用广泛的酸、碱、盐
7.1 溶液的酸碱性
一、单选题(共10题;共20分)
1.下表是人体内一些液体的正常pH范围,其中酸性最强的是( )
名称 胃液 唾液 胰液 胆汁
pH 0.9-1.5 6.6-7.1 7.5-8.0 7.1-7.3
A. 胃液 B. 唾液 C. 胰液 D. 胆汁
2.某同学用pH试纸测定某酸性溶液的pH时,他先用蒸馏水将试纸湿润,然后再测定,则他所测得的溶液pH将( )
A. 偏大 B. 偏小 C. 无影响 D. 无法确定
3.下列说法错误的是( )
A. 有一种溶液能使无色的酚酞试液变红,则该溶液呈碱性
B. 有一种溶液能使紫色的石蕊试液变蓝,则该溶液呈碱性
C. 有一种溶液不能使无色的酚酞试液变色,则该溶液呈酸性
D. 有一种溶液能使紫色的石蕊试液变红,则该溶液呈酸性
4.用pH计测得一些物质的pH,下列说法正确的是( )
物质 苹果汁 西瓜汁 牛奶 鸡蛋清 炉具清洁剂
pH 2.9 5.8 6.4 7.6 12.5
A. 牛奶放置一段时间后变酸,pH变大 B. 炉具清洁剂的碱性比鸡蛋清的碱性强
C. 等量的西瓜汁比苹果汁所含氢离子数多 D. 胃酸过多的人应该多喝苹果汁
5.下列说法正确的是( )
A. C、H、O三种元素在人体中的含量逐渐增加
B. HCl、NaCl、NaOH三者饱和溶液的pH逐渐变大
C. K2MnO4、KMnO4、MnO2三者中Mn的化合价逐渐升高
D. NaOH、NaCl、NH4NO3三种物质溶于水所形成溶液的温度是依次升高的
6.取一滤纸条,等间距滴入10滴紫色石蕊溶液,装入玻璃管中,然后从玻璃管的两端同时放入分别蘸有浓氨水和浓盐酸的棉球,并迅速封闭两端管口,很快可观察到管内有白烟产生,待白烟消失后还可观察到如图所示的现象.则下列说法中正确的是( )
A. 氨水和盐酸都属于易挥发性物质 B. 该过程中没有化学反应发生
C. 所有气体分子的运动速率都相同 D. 图示黑点表示石蕊溶液变成了红色
7.下列说法正确的是( )
A. 酸能使紫色石蕊溶液变红.通入CO2后的紫色石蕊溶液变红,所以CO2是酸
B. 碱性溶液的pH大于7.石灰水是碱性溶液,所以石灰水的pH大于7
C. 将植物油与水混合,充分搅拌,得到的是溶液
D. 配制溶液时,搅拌溶液可以增大溶质的溶解度
8.下列图象能正确反映其对应的实验操作的是( )
A B B D
A. 向盛有一定质量MnO2的烧杯中加入H2O2溶液
B. 向两份完全相同的稀盐酸中分别加入过量Zn粉、Fe粉
C. 向盛有一定质量的NaOH溶液的烧杯中逐滴滴加稀H2SO4至过量
D. 向稀盐酸与MgCl2的混合溶液中滴加NaOH溶液至过量
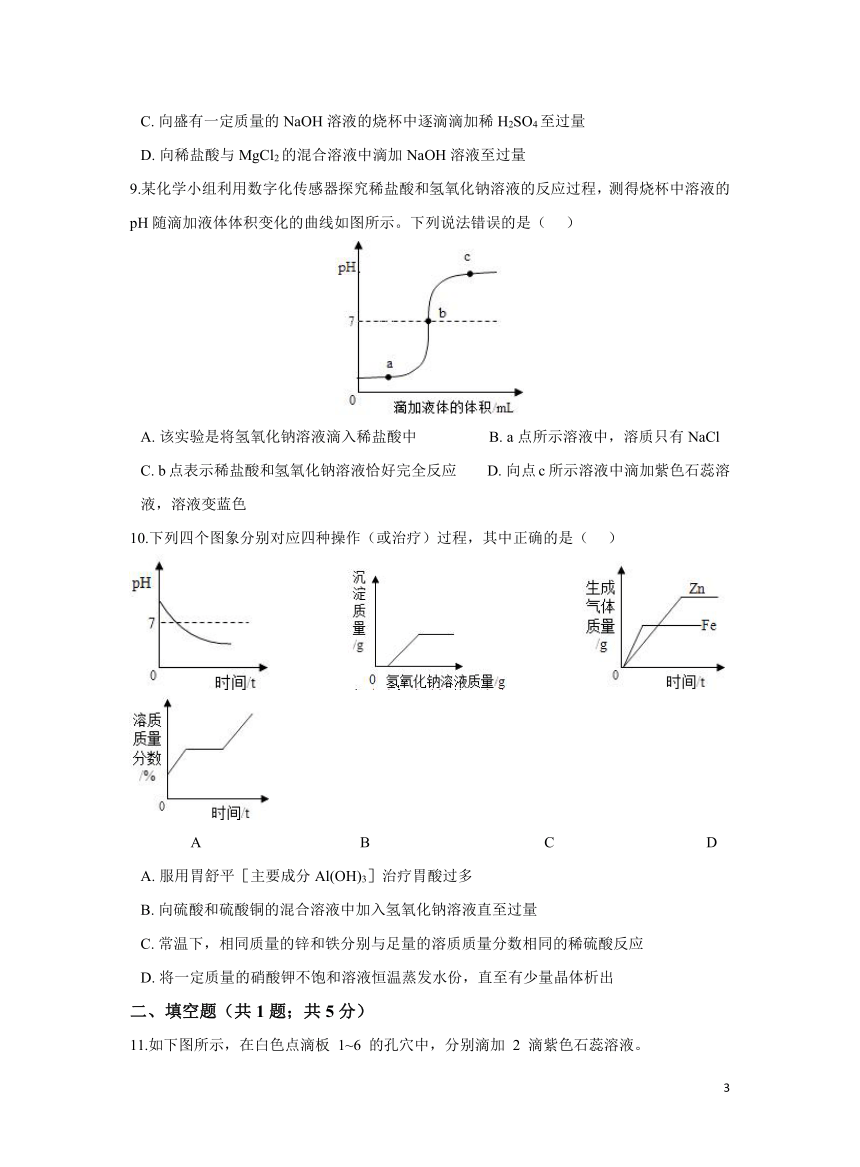
9.某化学小组利用数字化传感器探究稀盐酸和氢氧化钠溶液的反应过程,测得烧杯中溶液的pH随滴加液体体积变化的曲线如图所示。下列说法错误的是( )
A. 该实验是将氢氧化钠溶液滴入稀盐酸中 B. a点所示溶液中,溶质只有NaCl
C. b点表示稀盐酸和氢氧化钠溶液恰好完全反应 D. 向点c所示溶液中滴加紫色石蕊溶液,溶液变蓝色
10.下列四个图象分别对应四种操作(或治疗)过程,其中正确的是( )
A B C D
A. 服用胃舒平[主要成分Al(OH)3]治疗胃酸过多
B. 向硫酸和硫酸铜的混合溶液中加入氢氧化钠溶液直至过量
C. 常温下,相同质量的锌和铁分别与足量的溶质质量分数相同的稀硫酸反应
D. 将一定质量的硝酸钾不饱和溶液恒温蒸发水份,直至有少量晶体析出
二、填空题(共1题;共5分)
11.如下图所示,在白色点滴板 1~6 的孔穴中,分别滴加 2 滴紫色石蕊溶液。
(1)pH<7的孔穴有________(填孔穴序号,下同)。
(2)孔穴6中溶液变为蓝色,说明碳酸钾溶液显________(填“酸性”或“碱性”)。
(3)溶液变为红色的孔穴有________。
(4)作为空白对照实验的孔穴是________。
(5)再向孔穴4中滴加稀硫酸,溶液变为紫色,用化学方程式解释其原因:________。
三、实验探究题(共2题;共11分)
12.为了探究物质的化学性质,研究小组做了如图1所示实验。
请回答下列问题
(1)若取A所得溶液少许,加入石蕊试液,溶液显红色,故A所得溶液中一定含有的溶质是________(写化学式)。
(2)B试管中的实验现象________,B中所发生反应的化学方程式:________。
(3)若取B所得溶液少许,加入酚酞试液,溶液显红色,由此可知,B所得溶液中一定含有的溶质是________(写化学式)。
(4)反应结束后,小组同学将反应后A、B试管中的上层清液倒入洁净的烧杯中。往烧杯中滴加紫色石蕊溶液,溶液变红,然后将烧杯内的物质过滤。为了确定滤液中溶质的成分,小组同学进行了如下探究。
【作出猜想】猜想一:NaCl 猜想二:NaCl、HCl 猜想三:NaCl、HCl、CaCl2
【评价交流】你认为以上猜想________不合理。
【实验验证】同学们对可能含有的物质进行确定。小组同学取一定量清液于试管中,向溶液中逐滴加入碳酸钠溶液,看到先产生大量的气体后生成沉淀。
【结论】根据现象得出,猜想________正确。产生气体的化学方程式:________。
(5)【拓展提高】根据以上反应现象得到如图2所示的图象。
小组同学对图象进行了分析,下列说法错误的是 。
A.O至A过程中,生成了气体 B.O至A过程中,溶液的pH变大
C.C点时对应的溶液中只有两种溶质 D.整个过程只发生了复分解反应
13.某同学用如图所示装置进行实验。
已知:浓氨水易释放出氨气。
(1)该实验能说明分子具有的性质 。
(2)若该实验能说明“氨气能与水发生化学反应”,则相应的实验现象是 。
参考答案
一、单选题
1.A 2.A 3. C 4.B 5.B 6.A 7.B 8.B 9.B 10.B
二、填空题(共1题;共5分)
11.【答案】 (1)2和5 (2)碱性 (3)2和5 (4)3
(5)2NaOH+H2SO4 =Na2SO4+2H2O
三、实验探究题(共2题;共11分)
12.【答案】 (1)CaCl2、HCl (2)有白色沉淀产生;Na2CO3+Ca(OH)2=CaCO3↓+2NaOH
(3)NaOH (4)一;三;2HCl+Na2CO3=2NaCl+H2O+CO2↑ (5)C
13.【答案】 (1)分子在不断运动
(2)湿润的酚酞滤纸条变红,干燥的酚酞滤纸条无明显变化
1
7.1 溶液的酸碱性
一、单选题(共10题;共20分)
1.下表是人体内一些液体的正常pH范围,其中酸性最强的是( )
名称 胃液 唾液 胰液 胆汁
pH 0.9-1.5 6.6-7.1 7.5-8.0 7.1-7.3
A. 胃液 B. 唾液 C. 胰液 D. 胆汁
2.某同学用pH试纸测定某酸性溶液的pH时,他先用蒸馏水将试纸湿润,然后再测定,则他所测得的溶液pH将( )
A. 偏大 B. 偏小 C. 无影响 D. 无法确定
3.下列说法错误的是( )
A. 有一种溶液能使无色的酚酞试液变红,则该溶液呈碱性
B. 有一种溶液能使紫色的石蕊试液变蓝,则该溶液呈碱性
C. 有一种溶液不能使无色的酚酞试液变色,则该溶液呈酸性
D. 有一种溶液能使紫色的石蕊试液变红,则该溶液呈酸性
4.用pH计测得一些物质的pH,下列说法正确的是( )
物质 苹果汁 西瓜汁 牛奶 鸡蛋清 炉具清洁剂
pH 2.9 5.8 6.4 7.6 12.5
A. 牛奶放置一段时间后变酸,pH变大 B. 炉具清洁剂的碱性比鸡蛋清的碱性强
C. 等量的西瓜汁比苹果汁所含氢离子数多 D. 胃酸过多的人应该多喝苹果汁
5.下列说法正确的是( )
A. C、H、O三种元素在人体中的含量逐渐增加
B. HCl、NaCl、NaOH三者饱和溶液的pH逐渐变大
C. K2MnO4、KMnO4、MnO2三者中Mn的化合价逐渐升高
D. NaOH、NaCl、NH4NO3三种物质溶于水所形成溶液的温度是依次升高的
6.取一滤纸条,等间距滴入10滴紫色石蕊溶液,装入玻璃管中,然后从玻璃管的两端同时放入分别蘸有浓氨水和浓盐酸的棉球,并迅速封闭两端管口,很快可观察到管内有白烟产生,待白烟消失后还可观察到如图所示的现象.则下列说法中正确的是( )
A. 氨水和盐酸都属于易挥发性物质 B. 该过程中没有化学反应发生
C. 所有气体分子的运动速率都相同 D. 图示黑点表示石蕊溶液变成了红色
7.下列说法正确的是( )
A. 酸能使紫色石蕊溶液变红.通入CO2后的紫色石蕊溶液变红,所以CO2是酸
B. 碱性溶液的pH大于7.石灰水是碱性溶液,所以石灰水的pH大于7
C. 将植物油与水混合,充分搅拌,得到的是溶液
D. 配制溶液时,搅拌溶液可以增大溶质的溶解度
8.下列图象能正确反映其对应的实验操作的是( )
A B B D
A. 向盛有一定质量MnO2的烧杯中加入H2O2溶液
B. 向两份完全相同的稀盐酸中分别加入过量Zn粉、Fe粉
C. 向盛有一定质量的NaOH溶液的烧杯中逐滴滴加稀H2SO4至过量
D. 向稀盐酸与MgCl2的混合溶液中滴加NaOH溶液至过量
9.某化学小组利用数字化传感器探究稀盐酸和氢氧化钠溶液的反应过程,测得烧杯中溶液的pH随滴加液体体积变化的曲线如图所示。下列说法错误的是( )
A. 该实验是将氢氧化钠溶液滴入稀盐酸中 B. a点所示溶液中,溶质只有NaCl
C. b点表示稀盐酸和氢氧化钠溶液恰好完全反应 D. 向点c所示溶液中滴加紫色石蕊溶液,溶液变蓝色
10.下列四个图象分别对应四种操作(或治疗)过程,其中正确的是( )
A B C D
A. 服用胃舒平[主要成分Al(OH)3]治疗胃酸过多
B. 向硫酸和硫酸铜的混合溶液中加入氢氧化钠溶液直至过量
C. 常温下,相同质量的锌和铁分别与足量的溶质质量分数相同的稀硫酸反应
D. 将一定质量的硝酸钾不饱和溶液恒温蒸发水份,直至有少量晶体析出
二、填空题(共1题;共5分)
11.如下图所示,在白色点滴板 1~6 的孔穴中,分别滴加 2 滴紫色石蕊溶液。
(1)pH<7的孔穴有________(填孔穴序号,下同)。
(2)孔穴6中溶液变为蓝色,说明碳酸钾溶液显________(填“酸性”或“碱性”)。
(3)溶液变为红色的孔穴有________。
(4)作为空白对照实验的孔穴是________。
(5)再向孔穴4中滴加稀硫酸,溶液变为紫色,用化学方程式解释其原因:________。
三、实验探究题(共2题;共11分)
12.为了探究物质的化学性质,研究小组做了如图1所示实验。
请回答下列问题
(1)若取A所得溶液少许,加入石蕊试液,溶液显红色,故A所得溶液中一定含有的溶质是________(写化学式)。
(2)B试管中的实验现象________,B中所发生反应的化学方程式:________。
(3)若取B所得溶液少许,加入酚酞试液,溶液显红色,由此可知,B所得溶液中一定含有的溶质是________(写化学式)。
(4)反应结束后,小组同学将反应后A、B试管中的上层清液倒入洁净的烧杯中。往烧杯中滴加紫色石蕊溶液,溶液变红,然后将烧杯内的物质过滤。为了确定滤液中溶质的成分,小组同学进行了如下探究。
【作出猜想】猜想一:NaCl 猜想二:NaCl、HCl 猜想三:NaCl、HCl、CaCl2
【评价交流】你认为以上猜想________不合理。
【实验验证】同学们对可能含有的物质进行确定。小组同学取一定量清液于试管中,向溶液中逐滴加入碳酸钠溶液,看到先产生大量的气体后生成沉淀。
【结论】根据现象得出,猜想________正确。产生气体的化学方程式:________。
(5)【拓展提高】根据以上反应现象得到如图2所示的图象。
小组同学对图象进行了分析,下列说法错误的是 。
A.O至A过程中,生成了气体 B.O至A过程中,溶液的pH变大
C.C点时对应的溶液中只有两种溶质 D.整个过程只发生了复分解反应
13.某同学用如图所示装置进行实验。
已知:浓氨水易释放出氨气。
(1)该实验能说明分子具有的性质 。
(2)若该实验能说明“氨气能与水发生化学反应”,则相应的实验现象是 。
参考答案
一、单选题
1.A 2.A 3. C 4.B 5.B 6.A 7.B 8.B 9.B 10.B
二、填空题(共1题;共5分)
11.【答案】 (1)2和5 (2)碱性 (3)2和5 (4)3
(5)2NaOH+H2SO4 =Na2SO4+2H2O
三、实验探究题(共2题;共11分)
12.【答案】 (1)CaCl2、HCl (2)有白色沉淀产生;Na2CO3+Ca(OH)2=CaCO3↓+2NaOH
(3)NaOH (4)一;三;2HCl+Na2CO3=2NaCl+H2O+CO2↑ (5)C
13.【答案】 (1)分子在不断运动
(2)湿润的酚酞滤纸条变红,干燥的酚酞滤纸条无明显变化
1
