化学沪教版九下课件:6.2 溶液组成的表示(共25张PPT)
文档属性
| 名称 | 化学沪教版九下课件:6.2 溶液组成的表示(共25张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.0MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-02-17 00:00:00 | ||
图片预览







文档简介
(共25张PPT)
第6章 溶解现象
第2节 溶液组成的表示
课堂导入
标签上的10%、5%是代表什么?
溶液的组成
(2)溶剂:能溶解其他物质的物质叫做溶剂。
蔗糖
溶质
水
溶剂
溶液
溶液的组成:
溶液由溶质和溶剂组成
(1)溶质:被溶解的物质叫做溶质。
(3)m溶液= m溶质+ m溶剂
溶液的组成
思考:溶剂只可以是水吗?溶质只能是固体吗
最常用的溶剂是水;但溶剂可以是汽油、酒精等液体,甚至是固体或气体
溶质可以是固体、液体或气体
溶液的组成
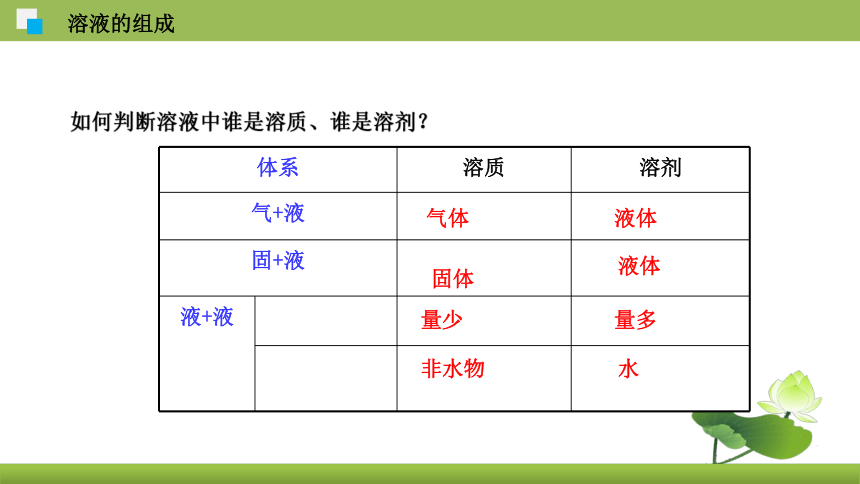
如何判断溶液中谁是溶质、谁是溶剂?
体系 溶质 溶剂
气+液
固+液
液+液
液体
固体
气体
液体
量少
量多
非水物
水
溶液的组成
溶液的命名
某某的某某溶液
加入水中的物质 溶质 溶剂 溶液名称
蔗 糖
食 盐
高锰酸钾
蔗糖
水
水
水
食盐
高锰酸钾
蔗糖的水溶液或蔗糖溶液
食盐的水溶液或食盐溶液
高锰酸钾的水溶液或高锰酸钾溶液
注: 溶剂为水时,可以简称为某溶液如氯化钠溶液
溶液浓度的表示
完成下列实验,将观察到的实验现象记录在表6—6中
[实验3]
烧杯1:称取3g蔗糖加入到烧杯中,再用量筒量取20mL水加入烧杯中,搅拌使蔗糖完全溶解。
烧杯2:称取5g蔗糖加入到烧杯中,再用量筒量取50mL水加入烧杯中,搅拌使蔗糖完全溶解。问:烧杯
1、2谁更甜?你能通过有关数据的比值来说明吗?
常温下配制蔗糖溶液
想一想:
如何更准确地表示溶液的组成?
溶液浓度的表示
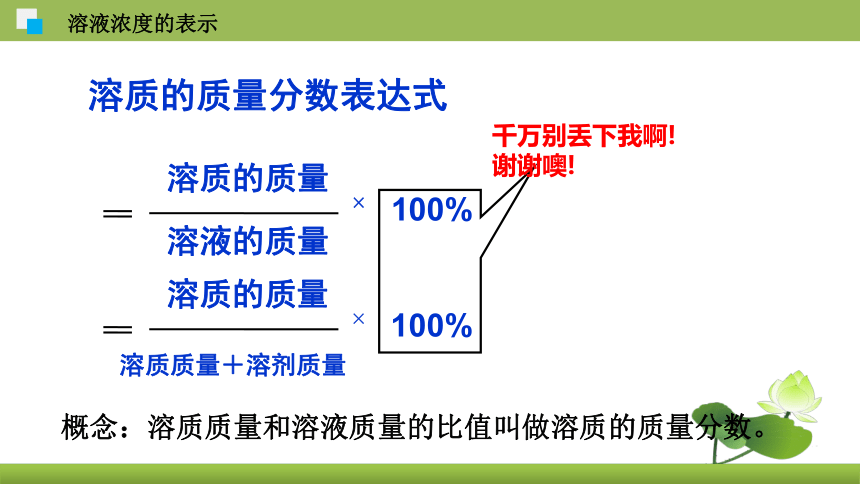
溶质的质量分数表达式
溶质的质量
溶液的质量
×
100%
溶质的质量
溶质质量+溶剂质量
×
100%
千万别丢下我啊! 谢谢噢!
概念:溶质质量和溶液质量的比值叫做溶质的质量分数。
溶液浓度的表示
注意:
①溶质的质量:被溶解的那部分质量,没有被溶解的那部分不能计入溶质质量和溶液质量。
②溶液的质量 = 溶质的质量 + 溶剂的质量
③溶质质量、溶剂质量、溶液质量的单位要统一。
④溶质的质量分数用百分数表示。
溶液浓度的表示
溶质质量分数的含义
5 % 的食盐溶液
①5g食盐溶于95g水形成的溶液。
②食盐的质量占整个食盐溶液的5%。
③将100g食盐溶液蒸干可以得到食盐5g。
④组成:M(食盐):M(水):M(食盐溶液) =5 : 95 : 100
溶质质量
溶液质量
溶液浓度的表示
溶质的质量分数
溶质质量
溶液质量
×100%
溶质的质量=
溶液的质量=
溶质的质量
溶质的质量分数
溶液的质量×溶质的质量分数
变形公式:
溶液浓度的表示
下表是NaCl溶液中的有关质量,请填表:
食盐 水 食盐水 食盐水的溶质质量分数
100克 5%
8克 92克
5克
8%
95克
100克
应用公式计算
溶液浓度的表示
例1.在农业生产上,常需要用质量分数为16%的氯化
钠 溶液来选种。现要配制150 kg的这种溶液,需要
氯化钠和水的质量各是多少?
解:溶质NaCl = 150kg×16% = 24kg
含溶剂水 = 溶液质量 — 溶质质量
= 150kg— 24kg
=126kg
答:需要24 kg氯化钠,126 kg的水。
有关溶液的计算
溶液浓度的表示
【练习】蒸干40 g某氯化钠溶液得到8 g氯化钠。试确定这瓶溶液中溶质的质量分数。
解:这瓶溶液中溶质的质量分数为
答:这瓶溶液中氯化钾的质量分数为20%。
8g
40g
×100%= 20%
溶液浓度的表示
溶液稀释问题的计算
计算的依据 :
稀释前溶质质量 = 稀释后溶质质量
公式:
m浓×c浓%= m稀×c稀%
浓缩前溶质质量 = 浓缩后溶质质量
溶液浓度的表示
例题:化学实验室现有98%的浓硫酸,但在实验中常需要用较稀的硫酸溶液。要把50 g质量分数为98%的浓硫酸稀释为质量分数为20%的 硫酸溶液需要多少克水?
溶液稀释问题的计算
溶液浓度的表示
解:设稀释后溶液的质量为x。因为溶液稀释前后溶质的质量不变,所以:
50g×98%= x ×20%
x =
50 g×98%
20%
=250 g
需要水的质量为:250 g-50 g=200 g
答:稀释需要水的质量为200 g。
溶液浓度的表示
知识点1 固体药品配制溶液
配制50 g质量分数为6%的氯化钠溶液
实验步骤:
1.计算:按配制要求计算出所需要的溶质和溶剂的量 (固体计算出质量,液体计算出体积)。
水的质量:50 g – 3 g= 47 g
氯化钠的质量:50g 6%= 3 g
溶液浓度的表示
2.称取氯化钠:用托盘天平称量所需的氯化钠,放入烧杯中。
溶液浓度的表示
用量筒量取所需的水,倒入盛有氯化钠的烧杯中。
平视
液面凹面最低点与47刻度持平
3.量取水:
溶液浓度的表示
4.溶解:用玻璃棒搅拌,使氯化钠溶解。
5.转移:将配置好的溶液装入试剂瓶中,贴上标签,标签上应包括药品的名称、化学式、溶液的质量分数。
典例讲解
名称 溶质 溶剂
白酒 ________ _______
碘酒 ________ ___________
食盐水 _________________ ____
氢氧化钠溶液 _________________ ____
酒精
水
碘
酒精
食盐(或氯化钠)
水
氢氧化钠
水
1. 写出下列物质的溶质和溶剂
典例讲解
2. 冬天,人们可在皮肤上擦甘油溶液,使皮肤保持湿润。当甘油溶液中溶质的质量分数为80%时护肤效果最佳。欲配制50 g这种甘油溶液,需甘油的质量是多少?水的质量是多少?
解:溶质的质量=50g×80%
=40g
所需水为50g-40g=10g
答:所需甘油40g,水10g。
典例讲解
3.现有100 g 溶质质量分数为10%的食盐溶液,若使溶液的溶质质量分数增加一倍,应蒸发掉多少水?
解:设应蒸发掉水x
答:应蒸发掉水40g水。
典例讲解
4. 配制500 mL20%的硫酸需要98%的硫酸多少毫升
(查硫酸密度和溶质质量分数对照表得出:20%的硫酸的密
度为1.14 g/cm3,98%的硫酸的密度为1.84 g/cm3。)
设:需98%的硫酸的体积为x。
稀释前后溶质质量在不变!
x × 1.84g/cm3 × 98% = 500 cm3 × 1.14g/cm3 × 20%
稀释前溶液中所含溶质
稀释后溶液中所含溶质
x = 63.2 cm3
答:配制500mL20%的硫酸需要63.2 mL98%的硫酸。
第6章 溶解现象
第2节 溶液组成的表示
课堂导入
标签上的10%、5%是代表什么?
溶液的组成
(2)溶剂:能溶解其他物质的物质叫做溶剂。
蔗糖
溶质
水
溶剂
溶液
溶液的组成:
溶液由溶质和溶剂组成
(1)溶质:被溶解的物质叫做溶质。
(3)m溶液= m溶质+ m溶剂
溶液的组成
思考:溶剂只可以是水吗?溶质只能是固体吗
最常用的溶剂是水;但溶剂可以是汽油、酒精等液体,甚至是固体或气体
溶质可以是固体、液体或气体
溶液的组成
如何判断溶液中谁是溶质、谁是溶剂?
体系 溶质 溶剂
气+液
固+液
液+液
液体
固体
气体
液体
量少
量多
非水物
水
溶液的组成
溶液的命名
某某的某某溶液
加入水中的物质 溶质 溶剂 溶液名称
蔗 糖
食 盐
高锰酸钾
蔗糖
水
水
水
食盐
高锰酸钾
蔗糖的水溶液或蔗糖溶液
食盐的水溶液或食盐溶液
高锰酸钾的水溶液或高锰酸钾溶液
注: 溶剂为水时,可以简称为某溶液如氯化钠溶液
溶液浓度的表示
完成下列实验,将观察到的实验现象记录在表6—6中
[实验3]
烧杯1:称取3g蔗糖加入到烧杯中,再用量筒量取20mL水加入烧杯中,搅拌使蔗糖完全溶解。
烧杯2:称取5g蔗糖加入到烧杯中,再用量筒量取50mL水加入烧杯中,搅拌使蔗糖完全溶解。问:烧杯
1、2谁更甜?你能通过有关数据的比值来说明吗?
常温下配制蔗糖溶液
想一想:
如何更准确地表示溶液的组成?
溶液浓度的表示
溶质的质量分数表达式
溶质的质量
溶液的质量
×
100%
溶质的质量
溶质质量+溶剂质量
×
100%
千万别丢下我啊! 谢谢噢!
概念:溶质质量和溶液质量的比值叫做溶质的质量分数。
溶液浓度的表示
注意:
①溶质的质量:被溶解的那部分质量,没有被溶解的那部分不能计入溶质质量和溶液质量。
②溶液的质量 = 溶质的质量 + 溶剂的质量
③溶质质量、溶剂质量、溶液质量的单位要统一。
④溶质的质量分数用百分数表示。
溶液浓度的表示
溶质质量分数的含义
5 % 的食盐溶液
①5g食盐溶于95g水形成的溶液。
②食盐的质量占整个食盐溶液的5%。
③将100g食盐溶液蒸干可以得到食盐5g。
④组成:M(食盐):M(水):M(食盐溶液) =5 : 95 : 100
溶质质量
溶液质量
溶液浓度的表示
溶质的质量分数
溶质质量
溶液质量
×100%
溶质的质量=
溶液的质量=
溶质的质量
溶质的质量分数
溶液的质量×溶质的质量分数
变形公式:
溶液浓度的表示
下表是NaCl溶液中的有关质量,请填表:
食盐 水 食盐水 食盐水的溶质质量分数
100克 5%
8克 92克
5克
8%
95克
100克
应用公式计算
溶液浓度的表示
例1.在农业生产上,常需要用质量分数为16%的氯化
钠 溶液来选种。现要配制150 kg的这种溶液,需要
氯化钠和水的质量各是多少?
解:溶质NaCl = 150kg×16% = 24kg
含溶剂水 = 溶液质量 — 溶质质量
= 150kg— 24kg
=126kg
答:需要24 kg氯化钠,126 kg的水。
有关溶液的计算
溶液浓度的表示
【练习】蒸干40 g某氯化钠溶液得到8 g氯化钠。试确定这瓶溶液中溶质的质量分数。
解:这瓶溶液中溶质的质量分数为
答:这瓶溶液中氯化钾的质量分数为20%。
8g
40g
×100%= 20%
溶液浓度的表示
溶液稀释问题的计算
计算的依据 :
稀释前溶质质量 = 稀释后溶质质量
公式:
m浓×c浓%= m稀×c稀%
浓缩前溶质质量 = 浓缩后溶质质量
溶液浓度的表示
例题:化学实验室现有98%的浓硫酸,但在实验中常需要用较稀的硫酸溶液。要把50 g质量分数为98%的浓硫酸稀释为质量分数为20%的 硫酸溶液需要多少克水?
溶液稀释问题的计算
溶液浓度的表示
解:设稀释后溶液的质量为x。因为溶液稀释前后溶质的质量不变,所以:
50g×98%= x ×20%
x =
50 g×98%
20%
=250 g
需要水的质量为:250 g-50 g=200 g
答:稀释需要水的质量为200 g。
溶液浓度的表示
知识点1 固体药品配制溶液
配制50 g质量分数为6%的氯化钠溶液
实验步骤:
1.计算:按配制要求计算出所需要的溶质和溶剂的量 (固体计算出质量,液体计算出体积)。
水的质量:50 g – 3 g= 47 g
氯化钠的质量:50g 6%= 3 g
溶液浓度的表示
2.称取氯化钠:用托盘天平称量所需的氯化钠,放入烧杯中。
溶液浓度的表示
用量筒量取所需的水,倒入盛有氯化钠的烧杯中。
平视
液面凹面最低点与47刻度持平
3.量取水:
溶液浓度的表示
4.溶解:用玻璃棒搅拌,使氯化钠溶解。
5.转移:将配置好的溶液装入试剂瓶中,贴上标签,标签上应包括药品的名称、化学式、溶液的质量分数。
典例讲解
名称 溶质 溶剂
白酒 ________ _______
碘酒 ________ ___________
食盐水 _________________ ____
氢氧化钠溶液 _________________ ____
酒精
水
碘
酒精
食盐(或氯化钠)
水
氢氧化钠
水
1. 写出下列物质的溶质和溶剂
典例讲解
2. 冬天,人们可在皮肤上擦甘油溶液,使皮肤保持湿润。当甘油溶液中溶质的质量分数为80%时护肤效果最佳。欲配制50 g这种甘油溶液,需甘油的质量是多少?水的质量是多少?
解:溶质的质量=50g×80%
=40g
所需水为50g-40g=10g
答:所需甘油40g,水10g。
典例讲解
3.现有100 g 溶质质量分数为10%的食盐溶液,若使溶液的溶质质量分数增加一倍,应蒸发掉多少水?
解:设应蒸发掉水x
答:应蒸发掉水40g水。
典例讲解
4. 配制500 mL20%的硫酸需要98%的硫酸多少毫升
(查硫酸密度和溶质质量分数对照表得出:20%的硫酸的密
度为1.14 g/cm3,98%的硫酸的密度为1.84 g/cm3。)
设:需98%的硫酸的体积为x。
稀释前后溶质质量在不变!
x × 1.84g/cm3 × 98% = 500 cm3 × 1.14g/cm3 × 20%
稀释前溶液中所含溶质
稀释后溶液中所含溶质
x = 63.2 cm3
答:配制500mL20%的硫酸需要63.2 mL98%的硫酸。
