化学沪教版九下:7.1 溶液的酸碱性课件(共24张PPT)
文档属性
| 名称 | 化学沪教版九下:7.1 溶液的酸碱性课件(共24张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 2.0MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-02-20 00:00:00 | ||
图片预览








文档简介
(共24张PPT)
第7章
应用广泛的酸、碱、盐
第1节 溶液的酸碱性
课堂导入
品尝
有什么感觉
请说出生活中具有酸味的物质名称
山楂
酸性溶液和碱性溶液
通常禁止对实验室中的化学试剂采用“尝味试验法”了解其味道 。
一种溶液是否有酸味即是否显酸性,如何通过化学手段去了解呢?
在前面的学习中我们是否接触过酸性、碱性物质的有关检验呢?
酸性溶液和碱性溶液
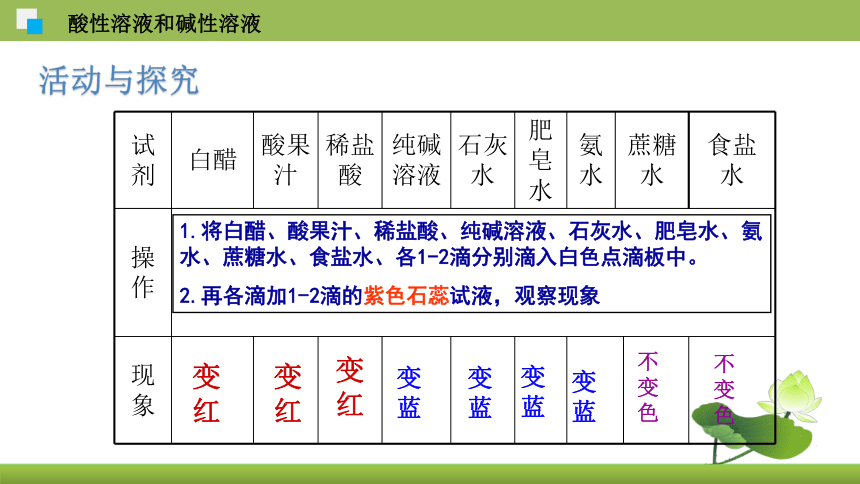
活动与探究
试剂 白醋 酸果汁 稀盐酸 纯碱 溶液 石灰水 肥皂水 氨水 蔗糖水 食盐水
操作 现象
变红
变红
变蓝
变蓝
不变色
不变色
变
红
变蓝
变蓝
1.将白醋、酸果汁、稀盐酸、纯碱溶液、石灰水、肥皂水、氨水、蔗糖水、食盐水、各1-2滴分别滴入白色点滴板中。
2.再各滴加1-2滴的紫色石蕊试液,观察现象
酸性溶液和碱性溶液
1. 能使紫色石蕊试液变红的溶液呈酸性。
2. 能使紫色石蕊试液变蓝的溶液呈碱性。
3. 不能使紫色石蕊试液变色的溶液,既不显酸性,也不显碱性,呈中性。
结
论:
1. 像石蕊这样 能检验溶液酸、碱性的试液,称为酸碱指示剂。
常用指示剂:
紫色石蕊溶液
无色酚酞溶液
酸性溶液和碱性溶液
变红
变蓝
不变色
变红
2. 紫色石蕊溶液
遇酸溶液
遇碱溶液
遇酸溶液
遇碱溶液
3. 无色酚酞溶液
变色规律:
酸性溶液和碱性溶液
检验酸碱溶液的操作步骤:
① 取样
② 滴加指示剂
③ 观察现象
④ 得出结论
答:将两种试剂各取少许于试管中,分别滴加紫色石蕊试液,振荡,如果溶液变红,则原溶液是盐酸;如果溶液变蓝,则原溶液是氢氧化钠溶液。
例:如何鉴别两瓶无色液体:稀盐酸、氢氧化钠溶液。
酸性溶液和碱性溶液
注意:酸碱指示剂与酸或碱的溶液反应时,
变色的是指示剂,而不是酸、碱溶液
酸性或碱性溶液
两者关系:
酸溶液一定显酸性,显酸性不一定是酸溶液
碱溶液一定显碱性,显碱性不一定是碱溶液
酸性溶液和碱性溶液
酸性溶液使蓝色石蕊试纸变红
碱性溶液使红色石蕊试纸变蓝
用紫色石蕊试液可以区分酸和碱,但实验较麻烦,还可以用石蕊试纸进行区分。试纸比酸碱指示剂更易于携带,操作较方便。
酸性溶液和碱性溶液
日常生活中,在我们吃食醋、橘子、葡萄等水果时,会感到它们酸的程度是不一样的,那么,如何表示物质酸性的强弱呢
溶液酸碱性的强弱
溶液的酸碱度是表示酸碱性的强弱程度。
稀溶液的酸碱度可用pH表示,用pH试纸测定。
pH试纸
溶液酸碱性的强弱
溶液的酸碱度常用pH表示, pH的范围通常在0~14之间。
酸性溶液pH < 7
碱性溶液pH > 7
中性溶液pH = 7
pH越小,酸性越强
pH越大,碱性越强
(如NaCl溶液、Na2SO4溶液的pH=7)
溶液酸碱性的强弱
1. pH的测定——用pH试纸测定(最简便的方法)
在白瓷板或玻璃片上放一小片pH 试纸,用干净的玻璃棒蘸取被测液滴到试纸上,把试纸显示的颜色与标准比色卡比较,即可得出被测液的pH 。
测定方法:
溶液酸碱性的强弱
【注意事项】
1. 不能把pH试纸放到待测溶液中测pH,以免带入杂质,污染试剂。
2. pH试纸不能用蒸馏水润湿后再测定,否则测定的是稀释后的溶液酸碱度,导致测定结果不准确。
3. 读数只能整数。
4. 检验气体酸性碱性润湿在用。
原溶液为酸性,会使pH变大;
原溶液为碱性,会使pH变小;
原溶液为中性,会对pH影响;
溶液酸碱性的强弱
更精确的pH测试仪器——pH计
溶液酸碱性的强弱
溶液的浓度与pH的关系
浓度越小,酸性越弱,pH越大;
浓度越小,碱性越弱,pH越小;
浓度越大,酸性越强,pH越小。
浓度越大,碱性越强,pH越大。
问:NaCl 的水溶液呢?浓度对pH有什么影响?
氯化钠溶液是中性的, pH =7,所以不管溶液的浓度高低,溶液的pH都是7,因此无影响。
酸溶液
碱溶液
溶液酸碱性的强弱
⑴加碱: pH增大至=或﹥ 7
若pH
﹤7
﹥7
若pH
⑵加水: pH增大至≈7
⑴加酸: pH减小到=或﹤ 7
⑵加水: pH减小至≈7
调节溶液pH的方法
溶液酸碱性与生命活动的关关系
人体中几种重要体液的正常pH范围
体液 血液 唾液 胃液 乳汁 尿液
pH 7.35-7.45 6.6-7.1 0.9-1.5 6.6-7.6 4.7-8.4
人的体液的pH必须维持在一定范围内,如果超越正常范围,会导致生理功能失调或发生疾病,甚至出现酸中毒或碱中毒。
如果胃酸分泌过多,使胃液pH降到正常水平以下,容易出现胃痛等症状。
溶液酸碱性与生命活动的关关系
阅读资料:
大多数农作物适宜在接近中性(pH在6.5—7.5之间)的土壤中生长,酸性太强(pH小于4)或碱性太强(pH大于8)的土壤都不适宜作物的生长。
溶液酸碱性与生命活动的关关系
雨水一般呈弱酸性(由于空气中的二氧化碳溶解在雨水中),人们一般把pH小于5.6 的雨水称为酸雨。
酸雨的危害
典例讲解
1. 生活中会接触到各种各样的溶液,其中不可能显酸性的是 ( )
A . 酸雨 C. 果珍饮料
B. 汽水 D. 肥皂水
2.某溶液中,加入酚酞试液后,呈现红色,如果加入紫色的石蕊试液,则呈现的颜色是 ( )
A.黄色 B.红色
C.蓝色 D.紫色
D
C
典例讲解
3.光明中学的小方同学在学习酸碱指示剂与常见酸、碱溶液的作用时,归纳出如图所示的关系,图中A、B、C、D是两圆相交的部分,表示指示剂与酸、碱溶液作用时所显示的颜色,则其中表示不正确的是( )
A.紫色 B.蓝色
C.红色 D.无色
A
典例讲解
4. 把纯水、稀硫酸和氢氧化钠三 种无色溶液区别开的最简单的方法是( )
A. 滴入酚酞试液
B. 滴入石蕊试液
C. 滴入氯化钡溶液
D. 通入二氧化碳气体
B
典例讲解
5.下表是一些食物的pH,胃酸过多的病人空腹时最宜食用的是 ( )
A. 柠檬 B. 苹果 C. 牛奶 D. 玉米粥
6. 将pH=10的氢氧化钠溶液加水稀释后,所得溶液的pH可能是( )
A.6 B.8 C.11 D.14
D
B
第7章
应用广泛的酸、碱、盐
第1节 溶液的酸碱性
课堂导入
品尝
有什么感觉
请说出生活中具有酸味的物质名称
山楂
酸性溶液和碱性溶液
通常禁止对实验室中的化学试剂采用“尝味试验法”了解其味道 。
一种溶液是否有酸味即是否显酸性,如何通过化学手段去了解呢?
在前面的学习中我们是否接触过酸性、碱性物质的有关检验呢?
酸性溶液和碱性溶液
活动与探究
试剂 白醋 酸果汁 稀盐酸 纯碱 溶液 石灰水 肥皂水 氨水 蔗糖水 食盐水
操作 现象
变红
变红
变蓝
变蓝
不变色
不变色
变
红
变蓝
变蓝
1.将白醋、酸果汁、稀盐酸、纯碱溶液、石灰水、肥皂水、氨水、蔗糖水、食盐水、各1-2滴分别滴入白色点滴板中。
2.再各滴加1-2滴的紫色石蕊试液,观察现象
酸性溶液和碱性溶液
1. 能使紫色石蕊试液变红的溶液呈酸性。
2. 能使紫色石蕊试液变蓝的溶液呈碱性。
3. 不能使紫色石蕊试液变色的溶液,既不显酸性,也不显碱性,呈中性。
结
论:
1. 像石蕊这样 能检验溶液酸、碱性的试液,称为酸碱指示剂。
常用指示剂:
紫色石蕊溶液
无色酚酞溶液
酸性溶液和碱性溶液
变红
变蓝
不变色
变红
2. 紫色石蕊溶液
遇酸溶液
遇碱溶液
遇酸溶液
遇碱溶液
3. 无色酚酞溶液
变色规律:
酸性溶液和碱性溶液
检验酸碱溶液的操作步骤:
① 取样
② 滴加指示剂
③ 观察现象
④ 得出结论
答:将两种试剂各取少许于试管中,分别滴加紫色石蕊试液,振荡,如果溶液变红,则原溶液是盐酸;如果溶液变蓝,则原溶液是氢氧化钠溶液。
例:如何鉴别两瓶无色液体:稀盐酸、氢氧化钠溶液。
酸性溶液和碱性溶液
注意:酸碱指示剂与酸或碱的溶液反应时,
变色的是指示剂,而不是酸、碱溶液
酸性或碱性溶液
两者关系:
酸溶液一定显酸性,显酸性不一定是酸溶液
碱溶液一定显碱性,显碱性不一定是碱溶液
酸性溶液和碱性溶液
酸性溶液使蓝色石蕊试纸变红
碱性溶液使红色石蕊试纸变蓝
用紫色石蕊试液可以区分酸和碱,但实验较麻烦,还可以用石蕊试纸进行区分。试纸比酸碱指示剂更易于携带,操作较方便。
酸性溶液和碱性溶液
日常生活中,在我们吃食醋、橘子、葡萄等水果时,会感到它们酸的程度是不一样的,那么,如何表示物质酸性的强弱呢
溶液酸碱性的强弱
溶液的酸碱度是表示酸碱性的强弱程度。
稀溶液的酸碱度可用pH表示,用pH试纸测定。
pH试纸
溶液酸碱性的强弱
溶液的酸碱度常用pH表示, pH的范围通常在0~14之间。
酸性溶液pH < 7
碱性溶液pH > 7
中性溶液pH = 7
pH越小,酸性越强
pH越大,碱性越强
(如NaCl溶液、Na2SO4溶液的pH=7)
溶液酸碱性的强弱
1. pH的测定——用pH试纸测定(最简便的方法)
在白瓷板或玻璃片上放一小片pH 试纸,用干净的玻璃棒蘸取被测液滴到试纸上,把试纸显示的颜色与标准比色卡比较,即可得出被测液的pH 。
测定方法:
溶液酸碱性的强弱
【注意事项】
1. 不能把pH试纸放到待测溶液中测pH,以免带入杂质,污染试剂。
2. pH试纸不能用蒸馏水润湿后再测定,否则测定的是稀释后的溶液酸碱度,导致测定结果不准确。
3. 读数只能整数。
4. 检验气体酸性碱性润湿在用。
原溶液为酸性,会使pH变大;
原溶液为碱性,会使pH变小;
原溶液为中性,会对pH影响;
溶液酸碱性的强弱
更精确的pH测试仪器——pH计
溶液酸碱性的强弱
溶液的浓度与pH的关系
浓度越小,酸性越弱,pH越大;
浓度越小,碱性越弱,pH越小;
浓度越大,酸性越强,pH越小。
浓度越大,碱性越强,pH越大。
问:NaCl 的水溶液呢?浓度对pH有什么影响?
氯化钠溶液是中性的, pH =7,所以不管溶液的浓度高低,溶液的pH都是7,因此无影响。
酸溶液
碱溶液
溶液酸碱性的强弱
⑴加碱: pH增大至=或﹥ 7
若pH
﹤7
﹥7
若pH
⑵加水: pH增大至≈7
⑴加酸: pH减小到=或﹤ 7
⑵加水: pH减小至≈7
调节溶液pH的方法
溶液酸碱性与生命活动的关关系
人体中几种重要体液的正常pH范围
体液 血液 唾液 胃液 乳汁 尿液
pH 7.35-7.45 6.6-7.1 0.9-1.5 6.6-7.6 4.7-8.4
人的体液的pH必须维持在一定范围内,如果超越正常范围,会导致生理功能失调或发生疾病,甚至出现酸中毒或碱中毒。
如果胃酸分泌过多,使胃液pH降到正常水平以下,容易出现胃痛等症状。
溶液酸碱性与生命活动的关关系
阅读资料:
大多数农作物适宜在接近中性(pH在6.5—7.5之间)的土壤中生长,酸性太强(pH小于4)或碱性太强(pH大于8)的土壤都不适宜作物的生长。
溶液酸碱性与生命活动的关关系
雨水一般呈弱酸性(由于空气中的二氧化碳溶解在雨水中),人们一般把pH小于5.6 的雨水称为酸雨。
酸雨的危害
典例讲解
1. 生活中会接触到各种各样的溶液,其中不可能显酸性的是 ( )
A . 酸雨 C. 果珍饮料
B. 汽水 D. 肥皂水
2.某溶液中,加入酚酞试液后,呈现红色,如果加入紫色的石蕊试液,则呈现的颜色是 ( )
A.黄色 B.红色
C.蓝色 D.紫色
D
C
典例讲解
3.光明中学的小方同学在学习酸碱指示剂与常见酸、碱溶液的作用时,归纳出如图所示的关系,图中A、B、C、D是两圆相交的部分,表示指示剂与酸、碱溶液作用时所显示的颜色,则其中表示不正确的是( )
A.紫色 B.蓝色
C.红色 D.无色
A
典例讲解
4. 把纯水、稀硫酸和氢氧化钠三 种无色溶液区别开的最简单的方法是( )
A. 滴入酚酞试液
B. 滴入石蕊试液
C. 滴入氯化钡溶液
D. 通入二氧化碳气体
B
典例讲解
5.下表是一些食物的pH,胃酸过多的病人空腹时最宜食用的是 ( )
A. 柠檬 B. 苹果 C. 牛奶 D. 玉米粥
6. 将pH=10的氢氧化钠溶液加水稀释后,所得溶液的pH可能是( )
A.6 B.8 C.11 D.14
D
B
