7.1 溶液的酸碱性 同步练习(含答案) 2022-2023学年 九年级下册化学沪教版(全国)
文档属性
| 名称 | 7.1 溶液的酸碱性 同步练习(含答案) 2022-2023学年 九年级下册化学沪教版(全国) |
|
|
| 格式 | zip | ||
| 文件大小 | 97.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-02-24 00:00:00 | ||
图片预览




文档简介
7.1 溶液的酸碱性 同步练习
一、单选题
1.推理法是化学学习方法中常见的一种,下列有关推理正确的是( )
选项 具体事例 推理总结
A 酸雨一定呈酸性 呈酸性的雨水一定是酸雨
B 金属离子和酸根离子构成盐 盐溶液中一定含有金属离子和酸根离子
C 单质是由同种元素组成的物质 同种元素组成的纯净物一定是单质
D 碱溶液能使无色酚酞溶液变红 能使无色酚酞溶液变红的一定是碱溶液
A.A B.B C.C D.D
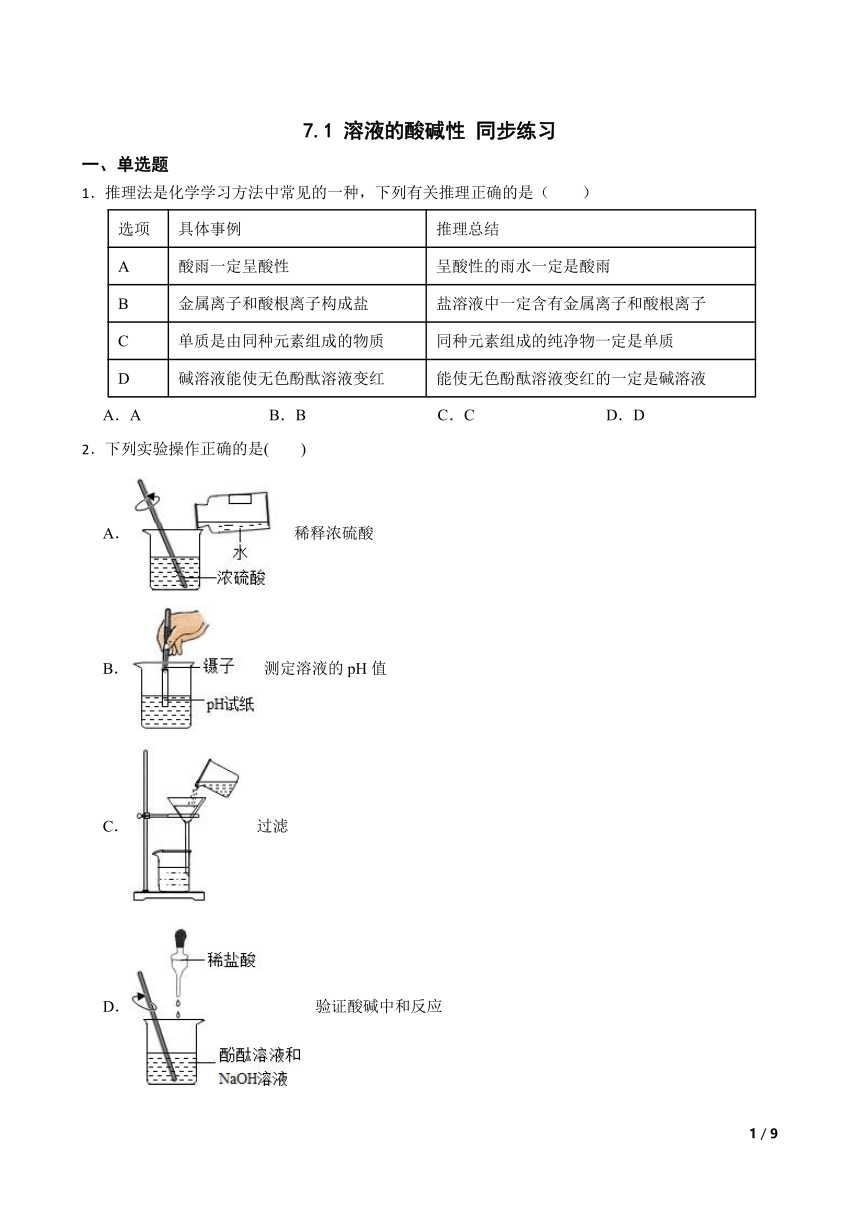
2.下列实验操作正确的是( )
A. 稀释浓硫酸
B. 测定溶液的pH值
C. 过滤
D. 验证酸碱中和反应
3.下列四个图象能正确反映对应变化关系的是( )
A.一定温度下,气体的溶解度与压强的关系
B.向一定质量的稀盐酸中逐滴滴加氢氧化钠溶液
C.加热一定质量氯酸钾和二氧化锰的混合物
D.相同质量的铁粉和锌粉,分别与质量分数相同的足量稀盐酸反应
4.下表列出了生活中一些常见物质的pH,其中碱性最强的物质是( )
物质 食醋 酱油 雨水 鲜牛奶 矿泉水 肥皂液
pH 2~3 4~5 约5.6 6.3~6.6 6.5~7.5 9.5~10.5
A.食醋 B.雨水 C.矿泉水 D.肥皂液
5.关注健康,预防疾病。下列叙述错误的是()
A.人体胃液正常的pH范围在0.9﹣1.5之间
B.人体缺乏维生素C会引起坏血病
C.香烟的烟气中含多种对人体有害的物质
D.人体缺氟会引起氟斑牙、氟骨病,氟过量会引起龋齿
6.以下“水”能使酚酞变红的是( )
A.糖水 B.盐水 C.氨水 D.汽水
7.学习要善于分析比较,去伪存真。下列说法中正确的一项是()
A.不能使酚酞变色的溶液的pH一定等于7
B.已知NaHSO4在溶液中离解出Na+、H+和SO42-,其pH<7,但不是酸
C.上网查资料得知水也能离解出极少量H+和OH-,所以水既可看作酸也可看作碱
D.甲用石蕊试液测知某果汁液变红色;乙改用pH试纸测知pH=8.2
8.下列各组物质能在pH=1的溶液中大量共存,且得到无色透明溶液的是( )
A.Na2CO3 NaCl KNO3 NH4Cl
B.NaCl Cu(NO3)2 H2SO4 KNO3
C.BaCl2 NaNO3 MgCl2 KOH
D.ZnSO4 Mg(NO3)2 NaNO3 KCl
9.取三种植物的花瓣分别放在研钵中,加入酒精研磨,得到花汁.各取少许花汁,用稀酸和稀碱进行检验,结果如下表所示:
花的种类 花汁在酒精中的颜色 花汁在酸溶液中的颜色 花汁在碱溶液中的颜色
大红花 粉红色 橙色 绿色
万寿菊 黄色 黄色 黄色
雏菊 无色 无色 黄色
则下列说法不正确的是( )
A.研磨花瓣时加入酒精是为了溶解其中的色素
B.在pH=10的溶液中大红花汁会变成橙色
C.万寿菊花汁不能用作酸碱指示剂
D.可用雏菊花汁来区别稀盐酸和氢氧化钠溶液
10.已知胃酸的主要成分是盐酸,胃液的正常pH范围是0.9﹣1.5,如果不断加水把胃液稀释,则胃液的pH值与加水量关系图正确的是( )
A. B.
C. D.
11.某校化学小组在利用盐酸和氢氧化钠溶液探究酸碱中和反应时,利用数字化传感器测得烧杯中溶液pH的变化图象,如图所示。下列说法正确的是()
A.由a点到b点的pH变化过程证明酸和碱发生中和反应
B.图中a点所示溶液中,含有的溶质是NaCl和NaOH
C.该实验是将盐酸溶液逐滴滴入到盛有氢氧化钠的烧杯中
D.图中c点所示溶液呈酸性了
12.下列有关盐酸的说法正确的是( )
A.稀盐酸的溶质是一种气体
B.打开浓盐酸瓶塞,可看到大量白烟
C.镁和稀盐酸的反应是一个吸热反应
D.向稀盐酸中逐滴加入氢氧化钠溶液,溶液的pH先增大后减小
二、填空题
13.柠檬酸(C6H8O7)是一种工业原料,广泛应用于食品、医疗等行业,柠檬酸中碳元素的质量分数为 ,将紫色石蕊溶液滴加到柠檬酸中,溶液变红色,说明柠檬酸的pH值 7(填“>”“=”或“<”)
14.通过实验,我们测得了石灰水、碳酸饮料、食醋及食盐水的pH,则在图(溶液pH逐渐增大)中表示石灰水的是 ,表示食盐水的是 。
15.如图所示的化学反应中溶液颜色变化体现了“魔法世界,魅力化学”。请回答:
(1)若A是一种指示剂,则试剂A的名称是 。
(2)若X是稀硫酸,B是红色的氧化物,则X与B的反应的化学方程式 。
(3)若X是稀盐酸,D是碱,则X与D反应的化学方程式 。
16.重庆奉节盛产脐橙。脐橙适宜生长在pH为5.5~6.5的土壤环境中。为了防治脐橙在生长过程中发生“脐橙炭疽病”,可喷洒农药波尔多液(由硫酸铜、石灰加水配制而成)。根据上述材料回答下列问题:
(1)脐橙适宜生长在 (填“酸性”、“碱性”或“中性”)的土壤里;
(2)果农们在配制农药波尔多液时,均使用塑料桶或木桶,而不使用铁桶,其原因是(用化学方程式表示): ;
(3)脐橙生长过程中,叶色发黄,你建议农民伯伯们施用哪种化肥?____________(填字母)
A.CO(NH2)2 B.KCl C.Ca3(PO4)2
三、综合题
17.学习了盐酸的性质后,小军归纳出盐酸的五条化学性质(如图)。
(1)为了验证性质①,小军将紫色石蕊溶液滴加到盐酸溶液中,溶液变 色;
(2)图中A所表示的物质类别是 ;试写出一个盐酸与该类别物质发生反应的化学方程式 ;
(3)为了验证性质⑤,可选用的物质是 (填一种即可);
(4)镁和锌可以用来验证盐酸的性质②。现在小军要探究镁和锌与盐酸反应的快慢,下列因素不影响镁和锌与盐酸反应快慢的是 (填序号);
A.盐酸的质量分数
B.温度
C.反应容器的大小
D.两种金属的形状
写出锌与盐酸发生反应的化学方程式 。
18.“杂交水稻之父”袁隆平“一稻济天下”,在不断培育高产杂交水稻的同时,还成功培育出了适宜在盐碱地上种植的“海水稻”。
(1)“杂交水稻”富含淀粉,淀粉属于六大基本营养素中的 。
(2)“海水稻”富含硒,硒是人体必需的 (选填“微量”“常量”)元素。
(3)海水稻在我国首种成功。海水呈弱碱性,其pH 7(填“>”、“=”或“<”)。
(4)提高粮食产量,离不开化肥。碳酸氢铵(NH4HCO3)是目前应用最广泛、最安全的氮肥,但易分解生成两种气体和一种液体,有较浓的氨味,试写出其分解的化学方程式 。
19.日常生活中,人们利用碳酸钠溶液具有碱性,清洗餐具上的油污,碱性越强,去油污的效果越好,小菁决定对影响碳酸钠溶液碱性的因素展开探究,请你参与。
用不同温度的水,配制溶质质量分数分别为2%、6%和10%的碳酸钠溶液,依次测量溶液的pH,记录数据如下表:
实验编号 a1 a2 a3 b1 b2 b3 c1 c2 c3
溶质质量分数 2% 2% 2% 6% 6% 6% 10% 10% 10%
水的温度(℃) 20 40 60 20 50 60 20 40 70
溶液pH 10.90 11.18 11.26 11.08 11.27 11.30 11.22 11.46 11.50
请你分析表中数据回答:
(1)要得出碳酸钠溶液的溶质质量分数变化与pH变化关系的结论,可选择的一组实验是 (填实验编号),结论是 。
(2)在一定温度范围内,温度的变化与碳酸钠溶液的pH变化关系是 。
(3)将10%的碳酸钠溶液从20℃持续升温到70℃,所测得的pH如下表:
温度(℃) 20 30 40 50 60 70
溶液pH 11.22 11.35 11.46 11.48 11.50 11.50
①当温度介于20℃~40℃时,温度对碳酸钠溶液的pH影响比较 (选填“大”或“小”)。
②小菁将适量碳酸钠粉末洒在沾有油污的餐具上,并冲入适量的热水,再进行擦洗,达到较好的洗涤效果,这是因为 。
(4)碳酸钠溶于水,有部分碳酸钠能与水发生反应生成氢氧化钠,致使溶液呈碱性。欲使碳酸钠溶液中的碳酸钠完全转化为烧碱,可在溶液中加入适量的物质(写名称) ,并充分搅拌,有关反应的化学方程式为 。
20.某氧化铜矿石主要成分是CuO、Cu(OH)2、CuCO3、Fe2O3及不溶于酸的杂质,用该矿石制备硫酸铜晶体和硫酸亚铁晶体的工艺流程如图。
(资料)Cu2+、Fe3+以氢氧化物形式沉淀时溶液的pH见下表:
沉淀物 Fe(OH)3 Cu(OH)2
开始沉淀的pH 1.5 4.2
沉淀完全的pH 3.7 6.7
请回答问题:
(1)酸溶前粉碎氧化铜矿石的作用是 。
(2)写出往氧化铜矿粉中加入足量硫酸发生中和反应的化学方程式 。溶液1中溶质有CuSO4、 (写出一种的化学式)。
(3)调pH不高于 ,调pH选用的最佳化合物为 (填序号)。
A.Na2CO3 B.CuO C.NaCl D.H2SO4
(4)往溶液3中加入过量的铁粉,其中一个反应是铁与铁盐反应生成是硫酸亚铁,请写出反应方程式 。
(5)FeSO4 7H2O可部分脱水制备FeSO4 xH2O,x与加热温度和时间的关系如下表,则得到FeSO4 3H2O适宜的工艺条件为温度 ℃、时间 h。
序号 ① ② ③ ④ ⑤ ⑥
时间/h 2 3 3.5 4 4.2 4.3
温度℃ 50 80 100 130 150 230
x的数值 6 5 4 3 2 1
答案解析部分
1.【答案】C
2.【答案】D
3.【答案】D
4.【答案】D
5.【答案】D
6.【答案】C
7.【答案】B
8.【答案】D
9.【答案】B
10.【答案】B
11.【答案】A
12.【答案】A
13.【答案】37.5%;<
14.【答案】D;C
15.【答案】(1)石蕊试液
(2)Fe2O3+3H2SO4=Fe2(SO4)3+3H2O
(3)H2SO4+Cu(OH)2=CuSO4+2H2O
16.【答案】(1)酸性
(2)Fe+CuSO4═FeSO4+Cu
(3)A
17.【答案】(1)红
(2)碱;NaOH+HCl=NaCl+H2O(符合条件即可)
(3)符合条件的盐即可
(4)C;Zn + 2HCl = ZnCl2 + H2↑
18.【答案】(1)糖类
(2)微量
(3)>
(4)
19.【答案】(1)a1、b1、c1(或a2、b2、c2;或a3、b3、c3);在水温度相同的条件下碳酸钠溶液的溶质质量分数越大溶液pH越大
(2)温度越高溶液pH越大
(3)大;温度越高,碳酸钠溶液的pH越大,碱性越强
(4)熟石灰(或氢氧化钙);
20.【答案】(1)增大反应物接触面积,加快反应速率
(2)Cu(OH)2+H2SO4═CuSO4+2H2O;H2SO4或Fe2(SO4)3
(3)3.7;B
(4)Fe2(SO4)3+Fe=3FeSO4
(5)130;4
1 / 1
一、单选题
1.推理法是化学学习方法中常见的一种,下列有关推理正确的是( )
选项 具体事例 推理总结
A 酸雨一定呈酸性 呈酸性的雨水一定是酸雨
B 金属离子和酸根离子构成盐 盐溶液中一定含有金属离子和酸根离子
C 单质是由同种元素组成的物质 同种元素组成的纯净物一定是单质
D 碱溶液能使无色酚酞溶液变红 能使无色酚酞溶液变红的一定是碱溶液
A.A B.B C.C D.D
2.下列实验操作正确的是( )
A. 稀释浓硫酸
B. 测定溶液的pH值
C. 过滤
D. 验证酸碱中和反应
3.下列四个图象能正确反映对应变化关系的是( )
A.一定温度下,气体的溶解度与压强的关系
B.向一定质量的稀盐酸中逐滴滴加氢氧化钠溶液
C.加热一定质量氯酸钾和二氧化锰的混合物
D.相同质量的铁粉和锌粉,分别与质量分数相同的足量稀盐酸反应
4.下表列出了生活中一些常见物质的pH,其中碱性最强的物质是( )
物质 食醋 酱油 雨水 鲜牛奶 矿泉水 肥皂液
pH 2~3 4~5 约5.6 6.3~6.6 6.5~7.5 9.5~10.5
A.食醋 B.雨水 C.矿泉水 D.肥皂液
5.关注健康,预防疾病。下列叙述错误的是()
A.人体胃液正常的pH范围在0.9﹣1.5之间
B.人体缺乏维生素C会引起坏血病
C.香烟的烟气中含多种对人体有害的物质
D.人体缺氟会引起氟斑牙、氟骨病,氟过量会引起龋齿
6.以下“水”能使酚酞变红的是( )
A.糖水 B.盐水 C.氨水 D.汽水
7.学习要善于分析比较,去伪存真。下列说法中正确的一项是()
A.不能使酚酞变色的溶液的pH一定等于7
B.已知NaHSO4在溶液中离解出Na+、H+和SO42-,其pH<7,但不是酸
C.上网查资料得知水也能离解出极少量H+和OH-,所以水既可看作酸也可看作碱
D.甲用石蕊试液测知某果汁液变红色;乙改用pH试纸测知pH=8.2
8.下列各组物质能在pH=1的溶液中大量共存,且得到无色透明溶液的是( )
A.Na2CO3 NaCl KNO3 NH4Cl
B.NaCl Cu(NO3)2 H2SO4 KNO3
C.BaCl2 NaNO3 MgCl2 KOH
D.ZnSO4 Mg(NO3)2 NaNO3 KCl
9.取三种植物的花瓣分别放在研钵中,加入酒精研磨,得到花汁.各取少许花汁,用稀酸和稀碱进行检验,结果如下表所示:
花的种类 花汁在酒精中的颜色 花汁在酸溶液中的颜色 花汁在碱溶液中的颜色
大红花 粉红色 橙色 绿色
万寿菊 黄色 黄色 黄色
雏菊 无色 无色 黄色
则下列说法不正确的是( )
A.研磨花瓣时加入酒精是为了溶解其中的色素
B.在pH=10的溶液中大红花汁会变成橙色
C.万寿菊花汁不能用作酸碱指示剂
D.可用雏菊花汁来区别稀盐酸和氢氧化钠溶液
10.已知胃酸的主要成分是盐酸,胃液的正常pH范围是0.9﹣1.5,如果不断加水把胃液稀释,则胃液的pH值与加水量关系图正确的是( )
A. B.
C. D.
11.某校化学小组在利用盐酸和氢氧化钠溶液探究酸碱中和反应时,利用数字化传感器测得烧杯中溶液pH的变化图象,如图所示。下列说法正确的是()
A.由a点到b点的pH变化过程证明酸和碱发生中和反应
B.图中a点所示溶液中,含有的溶质是NaCl和NaOH
C.该实验是将盐酸溶液逐滴滴入到盛有氢氧化钠的烧杯中
D.图中c点所示溶液呈酸性了
12.下列有关盐酸的说法正确的是( )
A.稀盐酸的溶质是一种气体
B.打开浓盐酸瓶塞,可看到大量白烟
C.镁和稀盐酸的反应是一个吸热反应
D.向稀盐酸中逐滴加入氢氧化钠溶液,溶液的pH先增大后减小
二、填空题
13.柠檬酸(C6H8O7)是一种工业原料,广泛应用于食品、医疗等行业,柠檬酸中碳元素的质量分数为 ,将紫色石蕊溶液滴加到柠檬酸中,溶液变红色,说明柠檬酸的pH值 7(填“>”“=”或“<”)
14.通过实验,我们测得了石灰水、碳酸饮料、食醋及食盐水的pH,则在图(溶液pH逐渐增大)中表示石灰水的是 ,表示食盐水的是 。
15.如图所示的化学反应中溶液颜色变化体现了“魔法世界,魅力化学”。请回答:
(1)若A是一种指示剂,则试剂A的名称是 。
(2)若X是稀硫酸,B是红色的氧化物,则X与B的反应的化学方程式 。
(3)若X是稀盐酸,D是碱,则X与D反应的化学方程式 。
16.重庆奉节盛产脐橙。脐橙适宜生长在pH为5.5~6.5的土壤环境中。为了防治脐橙在生长过程中发生“脐橙炭疽病”,可喷洒农药波尔多液(由硫酸铜、石灰加水配制而成)。根据上述材料回答下列问题:
(1)脐橙适宜生长在 (填“酸性”、“碱性”或“中性”)的土壤里;
(2)果农们在配制农药波尔多液时,均使用塑料桶或木桶,而不使用铁桶,其原因是(用化学方程式表示): ;
(3)脐橙生长过程中,叶色发黄,你建议农民伯伯们施用哪种化肥?____________(填字母)
A.CO(NH2)2 B.KCl C.Ca3(PO4)2
三、综合题
17.学习了盐酸的性质后,小军归纳出盐酸的五条化学性质(如图)。
(1)为了验证性质①,小军将紫色石蕊溶液滴加到盐酸溶液中,溶液变 色;
(2)图中A所表示的物质类别是 ;试写出一个盐酸与该类别物质发生反应的化学方程式 ;
(3)为了验证性质⑤,可选用的物质是 (填一种即可);
(4)镁和锌可以用来验证盐酸的性质②。现在小军要探究镁和锌与盐酸反应的快慢,下列因素不影响镁和锌与盐酸反应快慢的是 (填序号);
A.盐酸的质量分数
B.温度
C.反应容器的大小
D.两种金属的形状
写出锌与盐酸发生反应的化学方程式 。
18.“杂交水稻之父”袁隆平“一稻济天下”,在不断培育高产杂交水稻的同时,还成功培育出了适宜在盐碱地上种植的“海水稻”。
(1)“杂交水稻”富含淀粉,淀粉属于六大基本营养素中的 。
(2)“海水稻”富含硒,硒是人体必需的 (选填“微量”“常量”)元素。
(3)海水稻在我国首种成功。海水呈弱碱性,其pH 7(填“>”、“=”或“<”)。
(4)提高粮食产量,离不开化肥。碳酸氢铵(NH4HCO3)是目前应用最广泛、最安全的氮肥,但易分解生成两种气体和一种液体,有较浓的氨味,试写出其分解的化学方程式 。
19.日常生活中,人们利用碳酸钠溶液具有碱性,清洗餐具上的油污,碱性越强,去油污的效果越好,小菁决定对影响碳酸钠溶液碱性的因素展开探究,请你参与。
用不同温度的水,配制溶质质量分数分别为2%、6%和10%的碳酸钠溶液,依次测量溶液的pH,记录数据如下表:
实验编号 a1 a2 a3 b1 b2 b3 c1 c2 c3
溶质质量分数 2% 2% 2% 6% 6% 6% 10% 10% 10%
水的温度(℃) 20 40 60 20 50 60 20 40 70
溶液pH 10.90 11.18 11.26 11.08 11.27 11.30 11.22 11.46 11.50
请你分析表中数据回答:
(1)要得出碳酸钠溶液的溶质质量分数变化与pH变化关系的结论,可选择的一组实验是 (填实验编号),结论是 。
(2)在一定温度范围内,温度的变化与碳酸钠溶液的pH变化关系是 。
(3)将10%的碳酸钠溶液从20℃持续升温到70℃,所测得的pH如下表:
温度(℃) 20 30 40 50 60 70
溶液pH 11.22 11.35 11.46 11.48 11.50 11.50
①当温度介于20℃~40℃时,温度对碳酸钠溶液的pH影响比较 (选填“大”或“小”)。
②小菁将适量碳酸钠粉末洒在沾有油污的餐具上,并冲入适量的热水,再进行擦洗,达到较好的洗涤效果,这是因为 。
(4)碳酸钠溶于水,有部分碳酸钠能与水发生反应生成氢氧化钠,致使溶液呈碱性。欲使碳酸钠溶液中的碳酸钠完全转化为烧碱,可在溶液中加入适量的物质(写名称) ,并充分搅拌,有关反应的化学方程式为 。
20.某氧化铜矿石主要成分是CuO、Cu(OH)2、CuCO3、Fe2O3及不溶于酸的杂质,用该矿石制备硫酸铜晶体和硫酸亚铁晶体的工艺流程如图。
(资料)Cu2+、Fe3+以氢氧化物形式沉淀时溶液的pH见下表:
沉淀物 Fe(OH)3 Cu(OH)2
开始沉淀的pH 1.5 4.2
沉淀完全的pH 3.7 6.7
请回答问题:
(1)酸溶前粉碎氧化铜矿石的作用是 。
(2)写出往氧化铜矿粉中加入足量硫酸发生中和反应的化学方程式 。溶液1中溶质有CuSO4、 (写出一种的化学式)。
(3)调pH不高于 ,调pH选用的最佳化合物为 (填序号)。
A.Na2CO3 B.CuO C.NaCl D.H2SO4
(4)往溶液3中加入过量的铁粉,其中一个反应是铁与铁盐反应生成是硫酸亚铁,请写出反应方程式 。
(5)FeSO4 7H2O可部分脱水制备FeSO4 xH2O,x与加热温度和时间的关系如下表,则得到FeSO4 3H2O适宜的工艺条件为温度 ℃、时间 h。
序号 ① ② ③ ④ ⑤ ⑥
时间/h 2 3 3.5 4 4.2 4.3
温度℃ 50 80 100 130 150 230
x的数值 6 5 4 3 2 1
答案解析部分
1.【答案】C
2.【答案】D
3.【答案】D
4.【答案】D
5.【答案】D
6.【答案】C
7.【答案】B
8.【答案】D
9.【答案】B
10.【答案】B
11.【答案】A
12.【答案】A
13.【答案】37.5%;<
14.【答案】D;C
15.【答案】(1)石蕊试液
(2)Fe2O3+3H2SO4=Fe2(SO4)3+3H2O
(3)H2SO4+Cu(OH)2=CuSO4+2H2O
16.【答案】(1)酸性
(2)Fe+CuSO4═FeSO4+Cu
(3)A
17.【答案】(1)红
(2)碱;NaOH+HCl=NaCl+H2O(符合条件即可)
(3)符合条件的盐即可
(4)C;Zn + 2HCl = ZnCl2 + H2↑
18.【答案】(1)糖类
(2)微量
(3)>
(4)
19.【答案】(1)a1、b1、c1(或a2、b2、c2;或a3、b3、c3);在水温度相同的条件下碳酸钠溶液的溶质质量分数越大溶液pH越大
(2)温度越高溶液pH越大
(3)大;温度越高,碳酸钠溶液的pH越大,碱性越强
(4)熟石灰(或氢氧化钙);
20.【答案】(1)增大反应物接触面积,加快反应速率
(2)Cu(OH)2+H2SO4═CuSO4+2H2O;H2SO4或Fe2(SO4)3
(3)3.7;B
(4)Fe2(SO4)3+Fe=3FeSO4
(5)130;4
1 / 1
