7.2 常见的酸和碱 同步练习 (含答案)2022-2023学年 九年级下册化学沪教版(全国)
文档属性
| 名称 | 7.2 常见的酸和碱 同步练习 (含答案)2022-2023学年 九年级下册化学沪教版(全国) |

|
|
| 格式 | zip | ||
| 文件大小 | 175.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-02-24 00:00:00 | ||
图片预览


文档简介
7.2 常见的酸和碱 同步练习
一、单选题
1.下列说法中,正确的是( )
A.某物质能与稀盐酸反应产生气体,则该物质中一定含有碳酸根离子
B.向某溶液中加入氯化钡溶液,产生白色沉淀,则该物质中一定含有硫酸根离子
C.将一种碱溶液和一种盐溶液混合,它们可能相互反应生成两种沉淀
D.反应物和生成物均为两种化合物的反应,一定是复分解反应
2.化学是一门以实验为基础的学科,下列实验操作正确的是( )
A.过滤浑浊河水 B.量取水的体积
C.加热食盐水 D.稀释浓硫酸
3.2017年春季,在张献忠沉银现场,考古学家发现了金币、银币、铜币和银锭,还有铁刀、铁矛等兵器,金币银币光亮如初,铁刀铁矛锈迹斑斑。下列说法错误的是( )
A.金银铜铁都是重要的金属资源
B.金银的化学性质比铜铁更稳定
C.自然界中,金、银、铜、铁主要以单质的形式存在
D.可以用银、铁、硫酸铜溶液验证银、铁、铜三种金属的活动性顺序
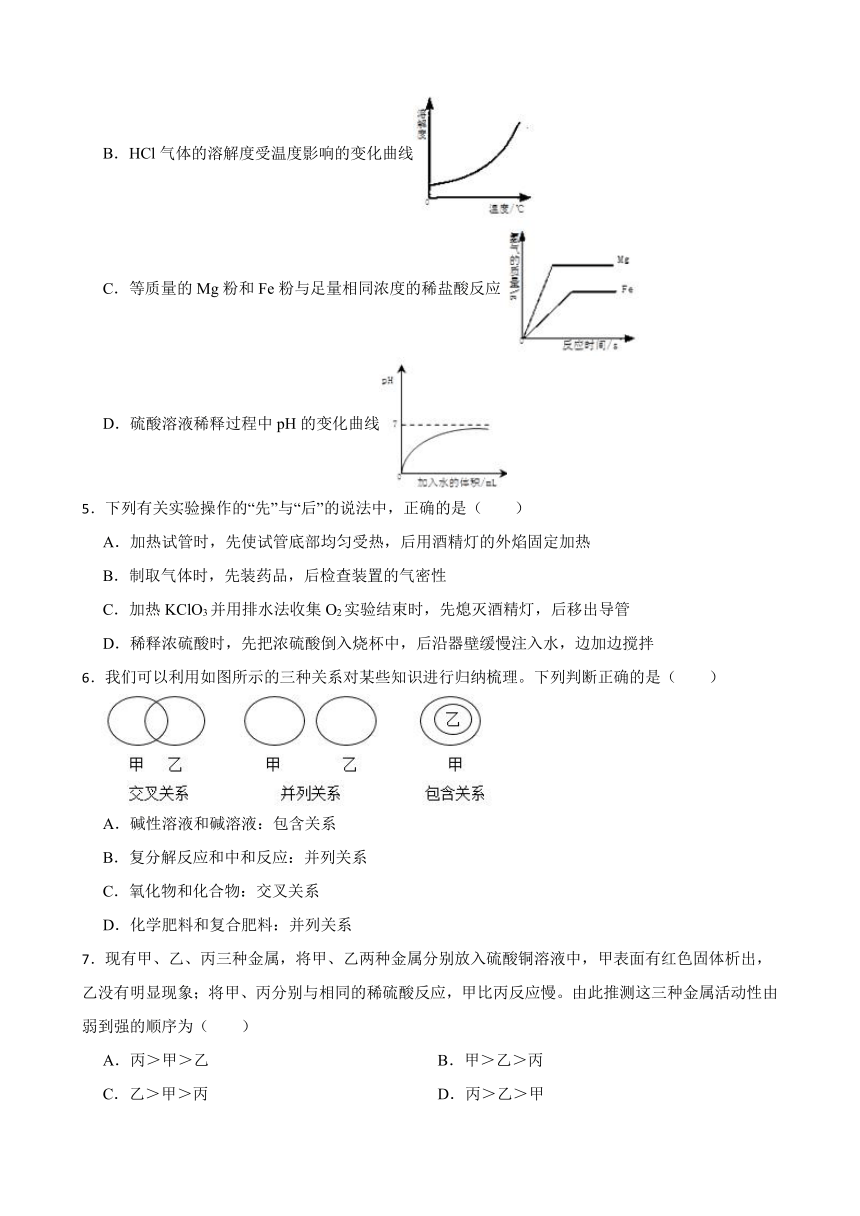
4.下列四个图像反映了对应实验过程中相关量的变化,其中错误的是( )
A.部分变质的NaOH溶液中滴加稀盐酸
B.HCl气体的溶解度受温度影响的变化曲线
C.等质量的Mg粉和Fe粉与足量相同浓度的稀盐酸反应
D.硫酸溶液稀释过程中pH的变化曲线
5.下列有关实验操作的“先”与“后”的说法中,正确的是( )
A.加热试管时,先使试管底部均匀受热,后用酒精灯的外焰固定加热
B.制取气体时,先装药品,后检查装置的气密性
C.加热KClO3并用排水法收集O2实验结束时,先熄灭酒精灯,后移出导管
D.稀释浓硫酸时,先把浓硫酸倒入烧杯中,后沿器壁缓慢注入水,边加边搅拌
6.我们可以利用如图所示的三种关系对某些知识进行归纳梳理。下列判断正确的是( )
A.碱性溶液和碱溶液:包含关系
B.复分解反应和中和反应:并列关系
C.氧化物和化合物:交叉关系
D.化学肥料和复合肥料:并列关系
7.现有甲、乙、丙三种金属,将甲、乙两种金属分别放入硫酸铜溶液中,甲表面有红色固体析出,乙没有明显现象;将甲、丙分别与相同的稀硫酸反应,甲比丙反应慢。由此推测这三种金属活动性由弱到强的顺序为( )
A.丙>甲>乙 B.甲>乙>丙
C.乙>甲>丙 D.丙>乙>甲
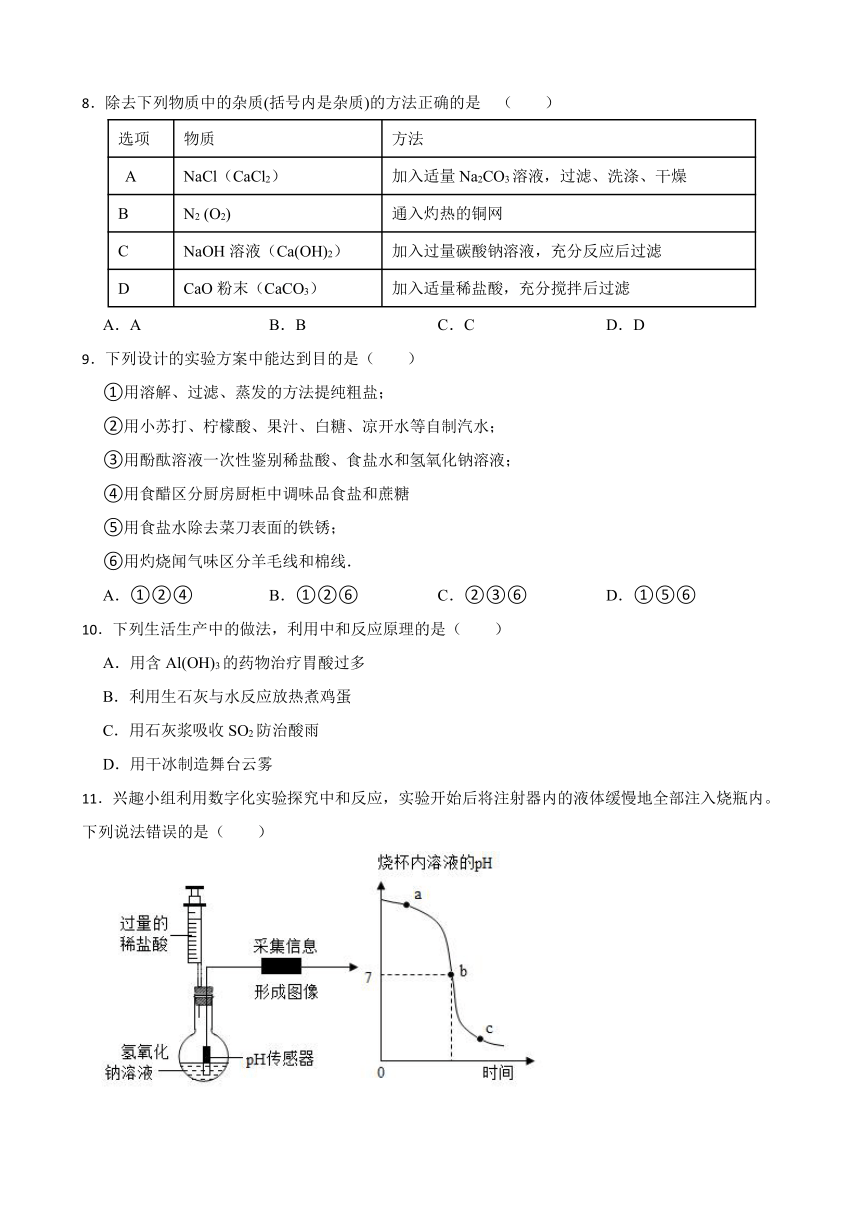
8.除去下列物质中的杂质(括号内是杂质)的方法正确的是 ( )
选项 物质 方法
A NaCl(CaCl2) 加入适量Na2CO3溶液,过滤、洗涤、干燥
B N2 (O2) 通入灼热的铜网
C NaOH溶液(Ca(OH)2) 加入过量碳酸钠溶液,充分反应后过滤
D CaO粉末(CaCO3) 加入适量稀盐酸,充分搅拌后过滤
A.A B.B C.C D.D
9.下列设计的实验方案中能达到目的是( )
①用溶解、过滤、蒸发的方法提纯粗盐;
②用小苏打、柠檬酸、果汁、白糖、凉开水等自制汽水;
③用酚酞溶液一次性鉴别稀盐酸、食盐水和氢氧化钠溶液;
④用食醋区分厨房厨柜中调味品食盐和蔗糖
⑤用食盐水除去菜刀表面的铁锈;
⑥用灼烧闻气味区分羊毛线和棉线.
A.①②④ B.①②⑥ C.②③⑥ D.①⑤⑥
10.下列生活生产中的做法,利用中和反应原理的是( )
A.用含Al(OH)3的药物治疗胃酸过多
B.利用生石灰与水反应放热煮鸡蛋
C.用石灰浆吸收SO2防治酸雨
D.用干冰制造舞台云雾
11.兴趣小组利用数字化实验探究中和反应,实验开始后将注射器内的液体缓慢地全部注入烧瓶内。下列说法错误的是( )
A.a点所示溶液滴加无色酚酞试液,液体变成红色
B.a、c两点所示溶液倒在一起,溶液中的溶质可能变成三种
C.a、b两点对应的溶液中,参加反应的两种物质的质量比相等
D.c点所示溶液加热蒸干所得固体是纯净物
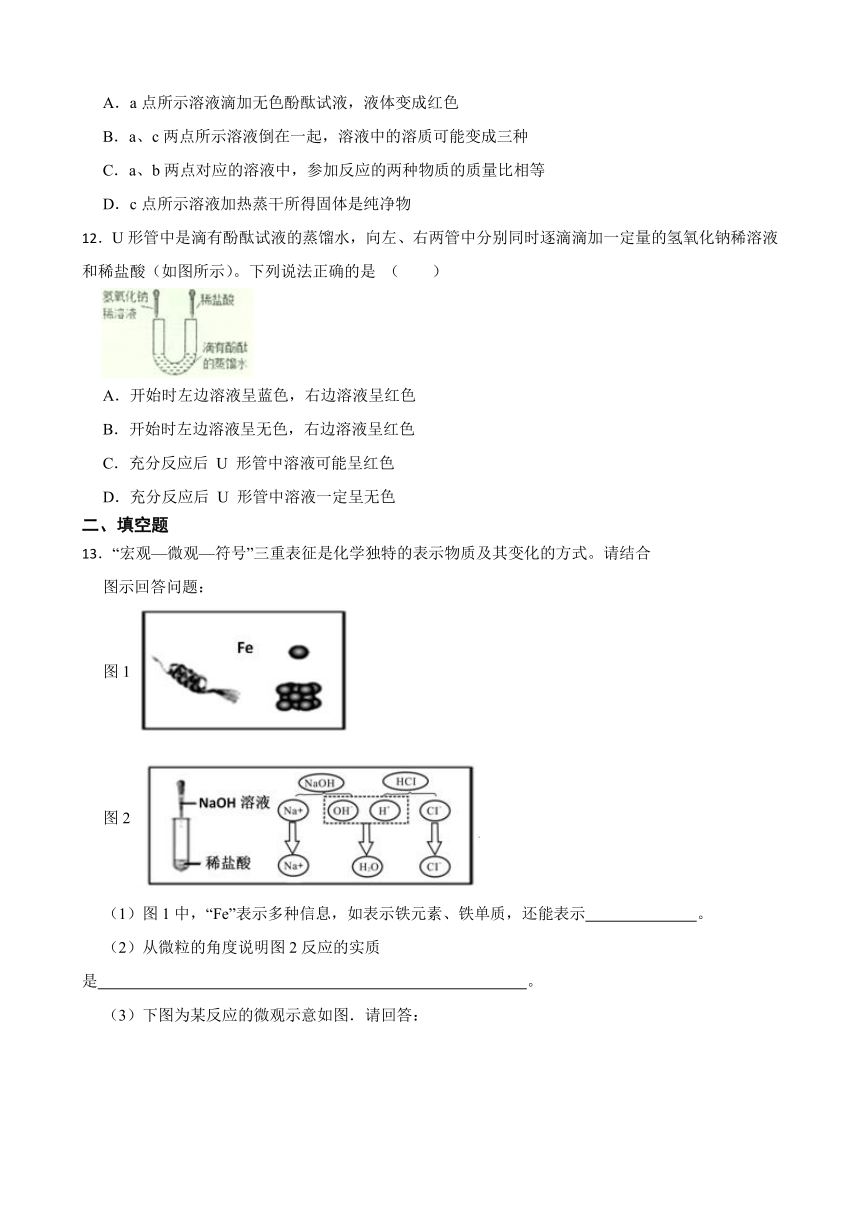
12.U形管中是滴有酚酞试液的蒸馏水,向左、右两管中分别同时逐滴滴加一定量的氢氧化钠稀溶液和稀盐酸(如图所示)。下列说法正确的是 ( )
A.开始时左边溶液呈蓝色,右边溶液呈红色
B.开始时左边溶液呈无色,右边溶液呈红色
C.充分反应后 U 形管中溶液可能呈红色
D.充分反应后 U 形管中溶液一定呈无色
二、填空题
13.“宏观—微观—符号”三重表征是化学独特的表示物质及其变化的方式。请结合
图示回答问题:
图1
图2
(1)图1中,“Fe”表示多种信息,如表示铁元素、铁单质,还能表示 。
(2)从微粒的角度说明图2反应的实质是 。
(3)下图为某反应的微观示意如图.请回答:
①反应前后的物质中属于单质的化学式: ;
②该反应的化学方程式为: 。
14.如图,在盛有少量石灰石的试管中加入适量的稀盐酸.
实验中出现的现象是: ;
烧杯内导管口出现气泡的原因是:石灰石与稀盐酸反应,生成了 导致管中的气体 ,导致内部压强 , 于外界大气压,在压强差的作用下气体从导管口被压出.
15.金属在生产生活中有广泛应用
(1)铝合金与纯铝相比,其硬度更 (填“大”或“小”)铝制品耐腐蚀是因其表面生成了致密的氧化铝薄膜,该反应的化学方程式为 ;
(2)铜丝作导线是利用了其良好的 性;
(3)铁生锈的条件是 ,可以采取的防锈措施是 ;
(4)真金不怕火炼是因为 ;
(5)为了验证Fe、Cu、Ag三种金属的活动性顺序,下列选用的药品可行的是 (填序号)
①Fe、CuSO4溶液、Ag ②FeSO4溶液、Cu、Ag
③FeSO4溶液、Cu、AgNO3溶液 ④FeSO4溶液、CuSO4溶液、Ag
16.酸、碱、盐在工农业生产、生活中应用广泛。请回答相关问题:
(1)盐酸和硫酸都是重要的酸,它们具有相似化学性质的原因是在水溶液中都能解离出酸根离子和 (填写符号);它们在工业上常用于金属除锈,请写出用盐酸除去铁锈的化学方程式 。
(2)酸和碱的中和反应在实际中应用广泛。我市某校化学实验室废液中有残留的硫酸,用pH试纸测定该废液的pH 7.若直接排放会导致环境污染,从经济可行的角度考虑,选用熟石灰处理该废液,有关化学方程式为 。
(3)小苏打是焙制糕点所用的发酵粉的主要成分之一,在医疗上也是治疗胃酸过多症的一种药剂,请写出该反应的化学方程式 。
(4)现有Ba(NO3)2溶液、稀硫酸、Na2CO3溶液、KOH溶液和CuSO4溶液。请从下列选项中,选择能够与上述物质发生复分解反应、并有气体生成的物质 ,写出反应的化学方程式 。
A.稀盐酸
B.烧碱溶液
C.硝酸钾溶液
三、综合题
17.金属材料在人类的生产、生活中有着十分重要的作用。
(1)多种金属可以压成薄片、抽成细丝,说明金属具有 性。
(2)实验室有打磨过的铝片、铁片和硫酸铜溶液。兴趣小组同学欲验证铝、铁和铜的活动性顺序,进行如下操作:
①取少量硫酸铜溶液于试管A中,将铁片(足量)插入硫酸铜溶液中,充分反应后将铁片取出,观察到的实验现象是 ;
② (请补充实验具体操作);
③取少量硫酸铜溶液于试管B中,将铝片插入硫酸铜溶液中,充分反应。写出该反应的化学方程式 。结论:三种金属的活动性由强到弱的顺序是 。
(3)金属腐蚀造成的损失巨大,对金属腐蚀的控制尤为重要。下列对金属的防护措施不合理的是 填序号)。
a.齿轮表面涂油
b.将钢材深埋保存
c.将钢刀浸泡在盐水中
d.车圈镀铬
18.实验小组研究盐酸、氢氧化钙两种物质的化学性质,做了如下图所示实验。
(1)实验后某试管中为红色溶液,向其中加入足量的 ,溶液变为无色。由此推断,该试管中最初盛有的物质是 。
(2)实验后某试管的底部有白色固体,过滤后向滤液中滴加稀盐酸,一段时间后有气泡出现。由此推断,该试管中最初发生反应的化学方程为 。
(3)实验后某试管中只得到无色溶液,向其中加入足量的Na2CO3溶液,无明显现象。由此推断,原试管所得无色溶液中的溶质一定有 。
19.能源利用与社会可持续发展密切相关.请回答:
(1)目前使用的燃料大多来自化石燃料.化石燃料包括天然气、煤、 .
(2)利用和开发新能源可以解决化石能源耗尽和环境污染问题.
①人类正在利用和开发的新能源有氢能、生物质能、核能、 等.
②氢气是理想的清洁、高能燃料.氢化锂在军事上常用于氢气的发生来源,它是无色晶体,熔点很高,导热性随温度升高而下降,与水剧烈反应生成 和氢气,常温下在干燥空气中能稳定存在,高温则分解为氢气和锂.其中属于氢化锂化学性质的是 (写出一条即可).
(3)如图为干电池的结构示意图,请利用所学知识完成下列问题.
①石墨可用作干电池的电极,是利用了石墨的 性.
②干电池中用到了铜和锌两种金属,请你写出一种证明两种金属活动性强弱的方案
20.金属在生产、生活和社会发展中的应用较为广泛。
(1)2020年11月24日,长征五号遥五运载火箭成功将嫦娥五号探测器运送至地月转移轨道。火箭、飞机的制造常使用钛合金,钛合金有很多优良性能,如______(填字母)。
A.熔点低,易加工
B.强度大,机械性能好
C.密度大,易腐蚀
(2)“折戟沉沙铁未销,自将磨洗认前朝”描述的是铁制兵器埋没在沙土中没有完全锈蚀,除了“磨洗”,实验室还可用稀盐酸除铁锈,该反应的方程式 。
(3)为探究锌、铁、铜的金属活动顺序,小明设计如图四个实验。
①某同学认为只需要两个实验即可达到目的,则不需要进行的实验是 (填字母)。由此得出这三种金属的活动性由强到弱的顺序为 。
②反应完成后,将四支试管中的废液全部倒入同一废液缸中,充分反应后过滤,得到滤液和滤渣,向滤液中加入铁粉,无明显现象,则滤液中一定含有 ,滤渣的成分可能有 种情况。
答案解析部分
1.【答案】C
2.【答案】A
3.【答案】C
4.【答案】B
5.【答案】A
6.【答案】A
7.【答案】A
8.【答案】B
9.【答案】B
10.【答案】A
11.【答案】B
12.【答案】C
13.【答案】(1)1个铁原子
(2)H++OH- =H2O(或“氢离子和氢氧根离子结合成水分子”)
(3)O2;2SO2+O2 2SO3
14.【答案】试管中有大量的气泡,澄清石灰水变浑浊;二氧化碳;增多;变大;大
15.【答案】(1)大;4Al+3O2=2Al2O3
(2)导电
(3)与氧气和水接触;刷漆,涂油,保持环境干燥等
(4)金在高温下也不与其它物质反应
(5)①③
16.【答案】(1)H+;
(2)小于;
(3)
(4)A;
17.【答案】(1)延展
(2)铁表面有红色固体析出;将铝片插入上述试管A中;2Al+3CuSO4=Al2(SO4)3+3Cu;铝>铁>铜
(3)bc
18.【答案】(1)稀盐酸;无色酚酞溶液
(2)Na2CO3+Ca(OH)2=CaCO3↓+2NaOH
(3)NaCl
19.【答案】(1)石油
(2)太阳能;氢氧化锂;与水剧烈反应
(3)导电;分别将两种金属与稀硫酸混合,观察能否反应
20.【答案】(1)B
(2)
(3)BD;Zn>Fe>Cu;ZnSO4、FeSO4;2
一、单选题
1.下列说法中,正确的是( )
A.某物质能与稀盐酸反应产生气体,则该物质中一定含有碳酸根离子
B.向某溶液中加入氯化钡溶液,产生白色沉淀,则该物质中一定含有硫酸根离子
C.将一种碱溶液和一种盐溶液混合,它们可能相互反应生成两种沉淀
D.反应物和生成物均为两种化合物的反应,一定是复分解反应
2.化学是一门以实验为基础的学科,下列实验操作正确的是( )
A.过滤浑浊河水 B.量取水的体积
C.加热食盐水 D.稀释浓硫酸
3.2017年春季,在张献忠沉银现场,考古学家发现了金币、银币、铜币和银锭,还有铁刀、铁矛等兵器,金币银币光亮如初,铁刀铁矛锈迹斑斑。下列说法错误的是( )
A.金银铜铁都是重要的金属资源
B.金银的化学性质比铜铁更稳定
C.自然界中,金、银、铜、铁主要以单质的形式存在
D.可以用银、铁、硫酸铜溶液验证银、铁、铜三种金属的活动性顺序
4.下列四个图像反映了对应实验过程中相关量的变化,其中错误的是( )
A.部分变质的NaOH溶液中滴加稀盐酸
B.HCl气体的溶解度受温度影响的变化曲线
C.等质量的Mg粉和Fe粉与足量相同浓度的稀盐酸反应
D.硫酸溶液稀释过程中pH的变化曲线
5.下列有关实验操作的“先”与“后”的说法中,正确的是( )
A.加热试管时,先使试管底部均匀受热,后用酒精灯的外焰固定加热
B.制取气体时,先装药品,后检查装置的气密性
C.加热KClO3并用排水法收集O2实验结束时,先熄灭酒精灯,后移出导管
D.稀释浓硫酸时,先把浓硫酸倒入烧杯中,后沿器壁缓慢注入水,边加边搅拌
6.我们可以利用如图所示的三种关系对某些知识进行归纳梳理。下列判断正确的是( )
A.碱性溶液和碱溶液:包含关系
B.复分解反应和中和反应:并列关系
C.氧化物和化合物:交叉关系
D.化学肥料和复合肥料:并列关系
7.现有甲、乙、丙三种金属,将甲、乙两种金属分别放入硫酸铜溶液中,甲表面有红色固体析出,乙没有明显现象;将甲、丙分别与相同的稀硫酸反应,甲比丙反应慢。由此推测这三种金属活动性由弱到强的顺序为( )
A.丙>甲>乙 B.甲>乙>丙
C.乙>甲>丙 D.丙>乙>甲
8.除去下列物质中的杂质(括号内是杂质)的方法正确的是 ( )
选项 物质 方法
A NaCl(CaCl2) 加入适量Na2CO3溶液,过滤、洗涤、干燥
B N2 (O2) 通入灼热的铜网
C NaOH溶液(Ca(OH)2) 加入过量碳酸钠溶液,充分反应后过滤
D CaO粉末(CaCO3) 加入适量稀盐酸,充分搅拌后过滤
A.A B.B C.C D.D
9.下列设计的实验方案中能达到目的是( )
①用溶解、过滤、蒸发的方法提纯粗盐;
②用小苏打、柠檬酸、果汁、白糖、凉开水等自制汽水;
③用酚酞溶液一次性鉴别稀盐酸、食盐水和氢氧化钠溶液;
④用食醋区分厨房厨柜中调味品食盐和蔗糖
⑤用食盐水除去菜刀表面的铁锈;
⑥用灼烧闻气味区分羊毛线和棉线.
A.①②④ B.①②⑥ C.②③⑥ D.①⑤⑥
10.下列生活生产中的做法,利用中和反应原理的是( )
A.用含Al(OH)3的药物治疗胃酸过多
B.利用生石灰与水反应放热煮鸡蛋
C.用石灰浆吸收SO2防治酸雨
D.用干冰制造舞台云雾
11.兴趣小组利用数字化实验探究中和反应,实验开始后将注射器内的液体缓慢地全部注入烧瓶内。下列说法错误的是( )
A.a点所示溶液滴加无色酚酞试液,液体变成红色
B.a、c两点所示溶液倒在一起,溶液中的溶质可能变成三种
C.a、b两点对应的溶液中,参加反应的两种物质的质量比相等
D.c点所示溶液加热蒸干所得固体是纯净物
12.U形管中是滴有酚酞试液的蒸馏水,向左、右两管中分别同时逐滴滴加一定量的氢氧化钠稀溶液和稀盐酸(如图所示)。下列说法正确的是 ( )
A.开始时左边溶液呈蓝色,右边溶液呈红色
B.开始时左边溶液呈无色,右边溶液呈红色
C.充分反应后 U 形管中溶液可能呈红色
D.充分反应后 U 形管中溶液一定呈无色
二、填空题
13.“宏观—微观—符号”三重表征是化学独特的表示物质及其变化的方式。请结合
图示回答问题:
图1
图2
(1)图1中,“Fe”表示多种信息,如表示铁元素、铁单质,还能表示 。
(2)从微粒的角度说明图2反应的实质是 。
(3)下图为某反应的微观示意如图.请回答:
①反应前后的物质中属于单质的化学式: ;
②该反应的化学方程式为: 。
14.如图,在盛有少量石灰石的试管中加入适量的稀盐酸.
实验中出现的现象是: ;
烧杯内导管口出现气泡的原因是:石灰石与稀盐酸反应,生成了 导致管中的气体 ,导致内部压强 , 于外界大气压,在压强差的作用下气体从导管口被压出.
15.金属在生产生活中有广泛应用
(1)铝合金与纯铝相比,其硬度更 (填“大”或“小”)铝制品耐腐蚀是因其表面生成了致密的氧化铝薄膜,该反应的化学方程式为 ;
(2)铜丝作导线是利用了其良好的 性;
(3)铁生锈的条件是 ,可以采取的防锈措施是 ;
(4)真金不怕火炼是因为 ;
(5)为了验证Fe、Cu、Ag三种金属的活动性顺序,下列选用的药品可行的是 (填序号)
①Fe、CuSO4溶液、Ag ②FeSO4溶液、Cu、Ag
③FeSO4溶液、Cu、AgNO3溶液 ④FeSO4溶液、CuSO4溶液、Ag
16.酸、碱、盐在工农业生产、生活中应用广泛。请回答相关问题:
(1)盐酸和硫酸都是重要的酸,它们具有相似化学性质的原因是在水溶液中都能解离出酸根离子和 (填写符号);它们在工业上常用于金属除锈,请写出用盐酸除去铁锈的化学方程式 。
(2)酸和碱的中和反应在实际中应用广泛。我市某校化学实验室废液中有残留的硫酸,用pH试纸测定该废液的pH 7.若直接排放会导致环境污染,从经济可行的角度考虑,选用熟石灰处理该废液,有关化学方程式为 。
(3)小苏打是焙制糕点所用的发酵粉的主要成分之一,在医疗上也是治疗胃酸过多症的一种药剂,请写出该反应的化学方程式 。
(4)现有Ba(NO3)2溶液、稀硫酸、Na2CO3溶液、KOH溶液和CuSO4溶液。请从下列选项中,选择能够与上述物质发生复分解反应、并有气体生成的物质 ,写出反应的化学方程式 。
A.稀盐酸
B.烧碱溶液
C.硝酸钾溶液
三、综合题
17.金属材料在人类的生产、生活中有着十分重要的作用。
(1)多种金属可以压成薄片、抽成细丝,说明金属具有 性。
(2)实验室有打磨过的铝片、铁片和硫酸铜溶液。兴趣小组同学欲验证铝、铁和铜的活动性顺序,进行如下操作:
①取少量硫酸铜溶液于试管A中,将铁片(足量)插入硫酸铜溶液中,充分反应后将铁片取出,观察到的实验现象是 ;
② (请补充实验具体操作);
③取少量硫酸铜溶液于试管B中,将铝片插入硫酸铜溶液中,充分反应。写出该反应的化学方程式 。结论:三种金属的活动性由强到弱的顺序是 。
(3)金属腐蚀造成的损失巨大,对金属腐蚀的控制尤为重要。下列对金属的防护措施不合理的是 填序号)。
a.齿轮表面涂油
b.将钢材深埋保存
c.将钢刀浸泡在盐水中
d.车圈镀铬
18.实验小组研究盐酸、氢氧化钙两种物质的化学性质,做了如下图所示实验。
(1)实验后某试管中为红色溶液,向其中加入足量的 ,溶液变为无色。由此推断,该试管中最初盛有的物质是 。
(2)实验后某试管的底部有白色固体,过滤后向滤液中滴加稀盐酸,一段时间后有气泡出现。由此推断,该试管中最初发生反应的化学方程为 。
(3)实验后某试管中只得到无色溶液,向其中加入足量的Na2CO3溶液,无明显现象。由此推断,原试管所得无色溶液中的溶质一定有 。
19.能源利用与社会可持续发展密切相关.请回答:
(1)目前使用的燃料大多来自化石燃料.化石燃料包括天然气、煤、 .
(2)利用和开发新能源可以解决化石能源耗尽和环境污染问题.
①人类正在利用和开发的新能源有氢能、生物质能、核能、 等.
②氢气是理想的清洁、高能燃料.氢化锂在军事上常用于氢气的发生来源,它是无色晶体,熔点很高,导热性随温度升高而下降,与水剧烈反应生成 和氢气,常温下在干燥空气中能稳定存在,高温则分解为氢气和锂.其中属于氢化锂化学性质的是 (写出一条即可).
(3)如图为干电池的结构示意图,请利用所学知识完成下列问题.
①石墨可用作干电池的电极,是利用了石墨的 性.
②干电池中用到了铜和锌两种金属,请你写出一种证明两种金属活动性强弱的方案
20.金属在生产、生活和社会发展中的应用较为广泛。
(1)2020年11月24日,长征五号遥五运载火箭成功将嫦娥五号探测器运送至地月转移轨道。火箭、飞机的制造常使用钛合金,钛合金有很多优良性能,如______(填字母)。
A.熔点低,易加工
B.强度大,机械性能好
C.密度大,易腐蚀
(2)“折戟沉沙铁未销,自将磨洗认前朝”描述的是铁制兵器埋没在沙土中没有完全锈蚀,除了“磨洗”,实验室还可用稀盐酸除铁锈,该反应的方程式 。
(3)为探究锌、铁、铜的金属活动顺序,小明设计如图四个实验。
①某同学认为只需要两个实验即可达到目的,则不需要进行的实验是 (填字母)。由此得出这三种金属的活动性由强到弱的顺序为 。
②反应完成后,将四支试管中的废液全部倒入同一废液缸中,充分反应后过滤,得到滤液和滤渣,向滤液中加入铁粉,无明显现象,则滤液中一定含有 ,滤渣的成分可能有 种情况。
答案解析部分
1.【答案】C
2.【答案】A
3.【答案】C
4.【答案】B
5.【答案】A
6.【答案】A
7.【答案】A
8.【答案】B
9.【答案】B
10.【答案】A
11.【答案】B
12.【答案】C
13.【答案】(1)1个铁原子
(2)H++OH- =H2O(或“氢离子和氢氧根离子结合成水分子”)
(3)O2;2SO2+O2 2SO3
14.【答案】试管中有大量的气泡,澄清石灰水变浑浊;二氧化碳;增多;变大;大
15.【答案】(1)大;4Al+3O2=2Al2O3
(2)导电
(3)与氧气和水接触;刷漆,涂油,保持环境干燥等
(4)金在高温下也不与其它物质反应
(5)①③
16.【答案】(1)H+;
(2)小于;
(3)
(4)A;
17.【答案】(1)延展
(2)铁表面有红色固体析出;将铝片插入上述试管A中;2Al+3CuSO4=Al2(SO4)3+3Cu;铝>铁>铜
(3)bc
18.【答案】(1)稀盐酸;无色酚酞溶液
(2)Na2CO3+Ca(OH)2=CaCO3↓+2NaOH
(3)NaCl
19.【答案】(1)石油
(2)太阳能;氢氧化锂;与水剧烈反应
(3)导电;分别将两种金属与稀硫酸混合,观察能否反应
20.【答案】(1)B
(2)
(3)BD;Zn>Fe>Cu;ZnSO4、FeSO4;2
