6.3 物质的溶解性 同步练习(含答案) 2022-2023学年沪教版(全国)九年级下册化学
文档属性
| 名称 | 6.3 物质的溶解性 同步练习(含答案) 2022-2023学年沪教版(全国)九年级下册化学 |

|
|
| 格式 | zip | ||
| 文件大小 | 121.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-02-27 00:00:00 | ||
图片预览


文档简介
6.3 物质的溶解性 同步练习
一、单选题
1.图表资料可以为我们提供很多信息,下列关于图表提供的信息或应用的说法中,不正确的是( )
A.根据相对原子质量表,可查找元素的相对原子质量
B.根据酸、碱、盐的溶解性表,可判断各种酸、碱、盐的溶解度大小
C.根据溶解度曲线图,可选择从溶液中获得晶体的方法
D.根据空气质量周报,可知道空气质量级别和首要污染物
2.李克强总理在2022年3月的全国两会报告中指出:持续改善生态环境,推动绿色低碳发展。下列有关二氧化碳的说法错误的是( )
A.二氧化碳通入紫色石蕊溶液中,试液变成红色的原因是二氧化碳具有酸性
B.打开汽水瓶盖有大量气泡冒出说明二氧化碳的溶解度随压强的减小而减小
C.图书馆内的图书起火用二氧化碳灭火器灭火
D.大力植树造林,严禁乱砍滥伐森林,以控制二氧化碳的排放量
3.如图是A、B两种固体物质的溶解度曲线,下列说法一定正确的是( )
A.物质A的溶解度大于B的溶解度
B.36 C时,A的饱和溶液溶质量分数为60%
C.若A中含少量的B杂质,可通过降温结晶提纯A
D.18 C时,A,B的饱和溶液中所含溶质的质量相等
4.t℃时,A物质的饱和溶液中A的质量分数为15%,B物质的溶解度是25g,C物质的10g饱和溶液蒸干后可得1.5gC.若取等质量的3种物质的饱和溶液,则3种溶液中所含溶质的质量大小顺序是( )
A.A>C>B B.C>A>B C.B>C=A D.A>B>C
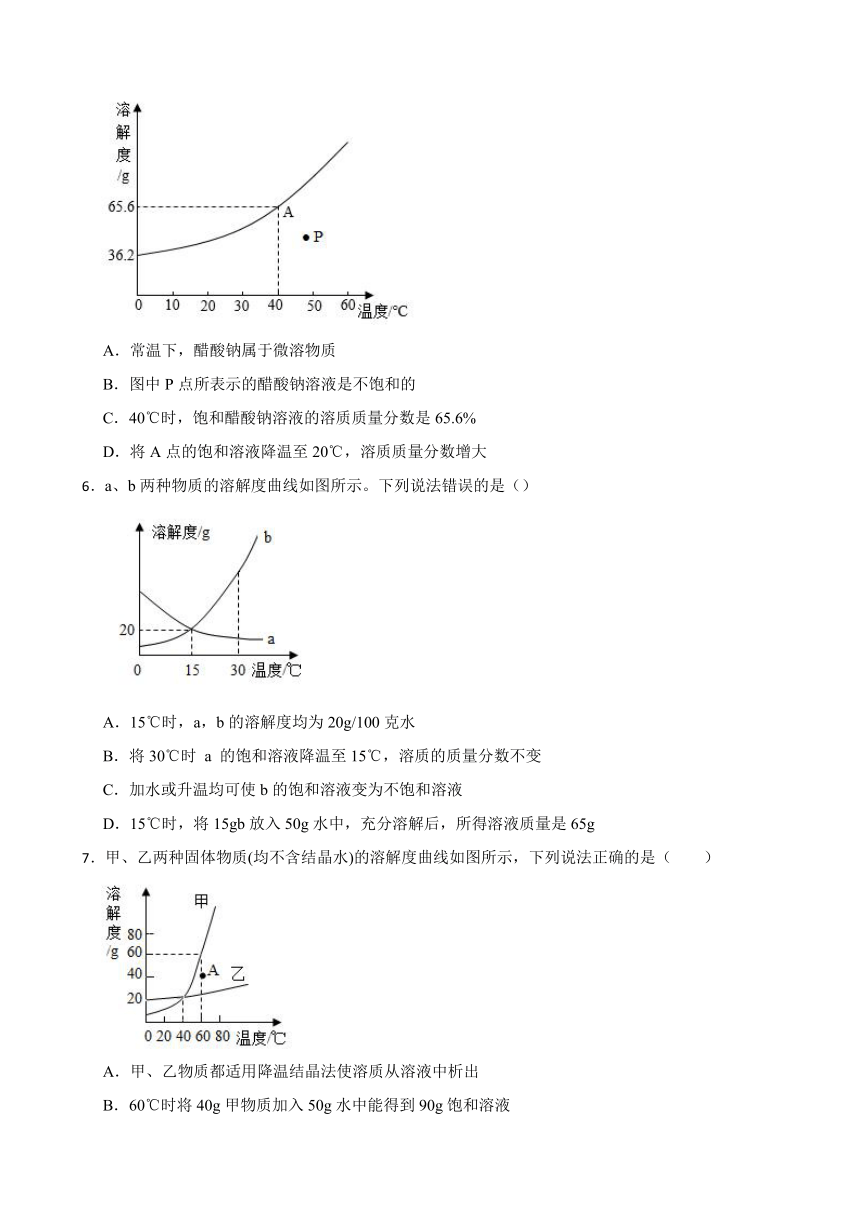
5.我国航天员王亚平在太空演示“冰雪”实验时用到了过饱和醋酸钠溶液。如图是醋酸钠的溶解度曲线,下列说法正确的是( )
A.常温下,醋酸钠属于微溶物质
B.图中P点所表示的醋酸钠溶液是不饱和的
C.40℃时,饱和醋酸钠溶液的溶质质量分数是65.6%
D.将A点的饱和溶液降温至20℃,溶质质量分数增大
6.a、b两种物质的溶解度曲线如图所示。下列说法错误的是()
A.15℃时,a,b的溶解度均为20g/100克水
B.将30℃时 a 的饱和溶液降温至15℃,溶质的质量分数不变
C.加水或升温均可使b的饱和溶液变为不饱和溶液
D.15℃时,将15gb放入50g水中,充分溶解后,所得溶液质量是65g
7.甲、乙两种固体物质(均不含结晶水)的溶解度曲线如图所示,下列说法正确的是( )
A.甲、乙物质都适用降温结晶法使溶质从溶液中析出
B.60℃时将40g甲物质加入50g水中能得到90g饱和溶液
C.通过降温能使A点甲的不饱和溶液变为饱和溶液
D.分别将甲、乙物质饱和溶液从60℃降至20℃,甲析出晶体较多
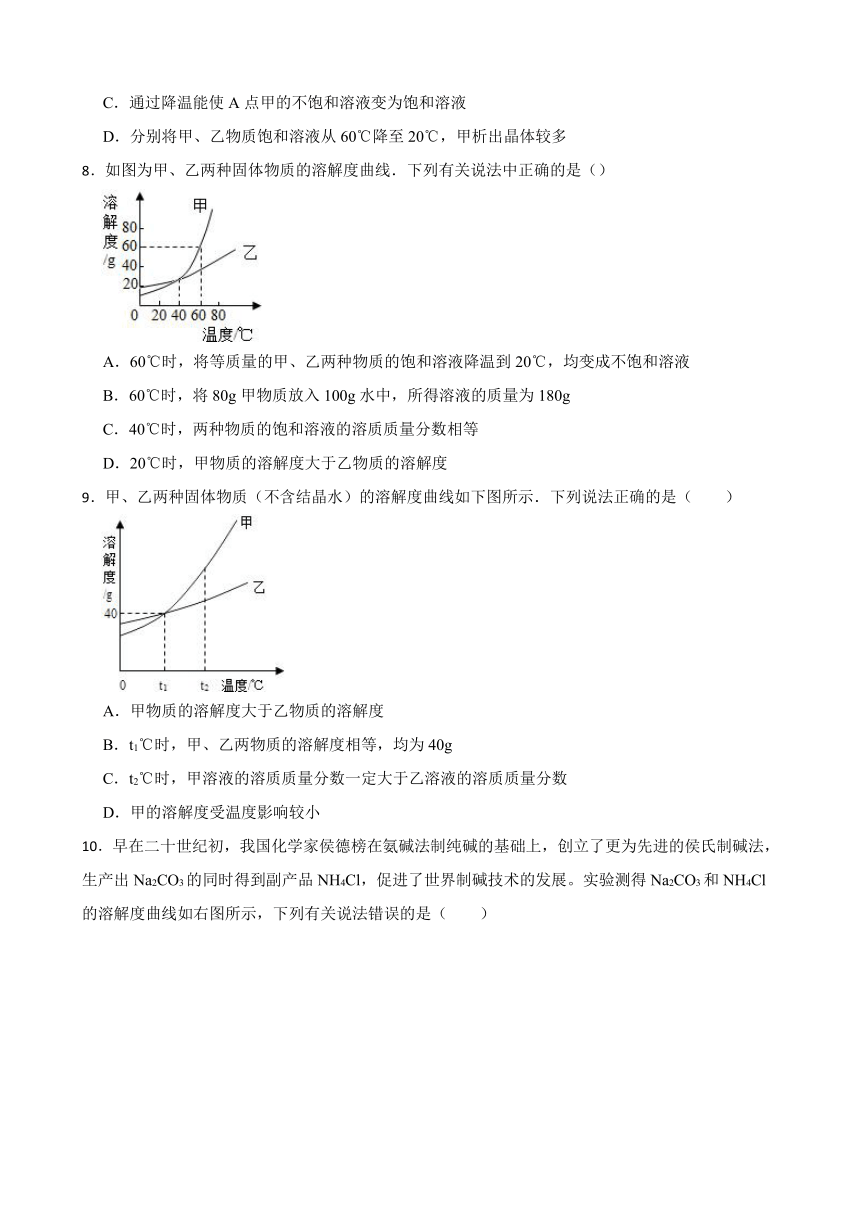
8.如图为甲、乙两种固体物质的溶解度曲线.下列有关说法中正确的是()
A.60℃时,将等质量的甲、乙两种物质的饱和溶液降温到20℃,均变成不饱和溶液
B.60℃时,将80g甲物质放入100g水中,所得溶液的质量为180g
C.40℃时,两种物质的饱和溶液的溶质质量分数相等
D.20℃时,甲物质的溶解度大于乙物质的溶解度
9.甲、乙两种固体物质(不含结晶水)的溶解度曲线如下图所示.下列说法正确的是( )
A.甲物质的溶解度大于乙物质的溶解度
B.t1℃时,甲、乙两物质的溶解度相等,均为40g
C.t2℃时,甲溶液的溶质质量分数一定大于乙溶液的溶质质量分数
D.甲的溶解度受温度影响较小
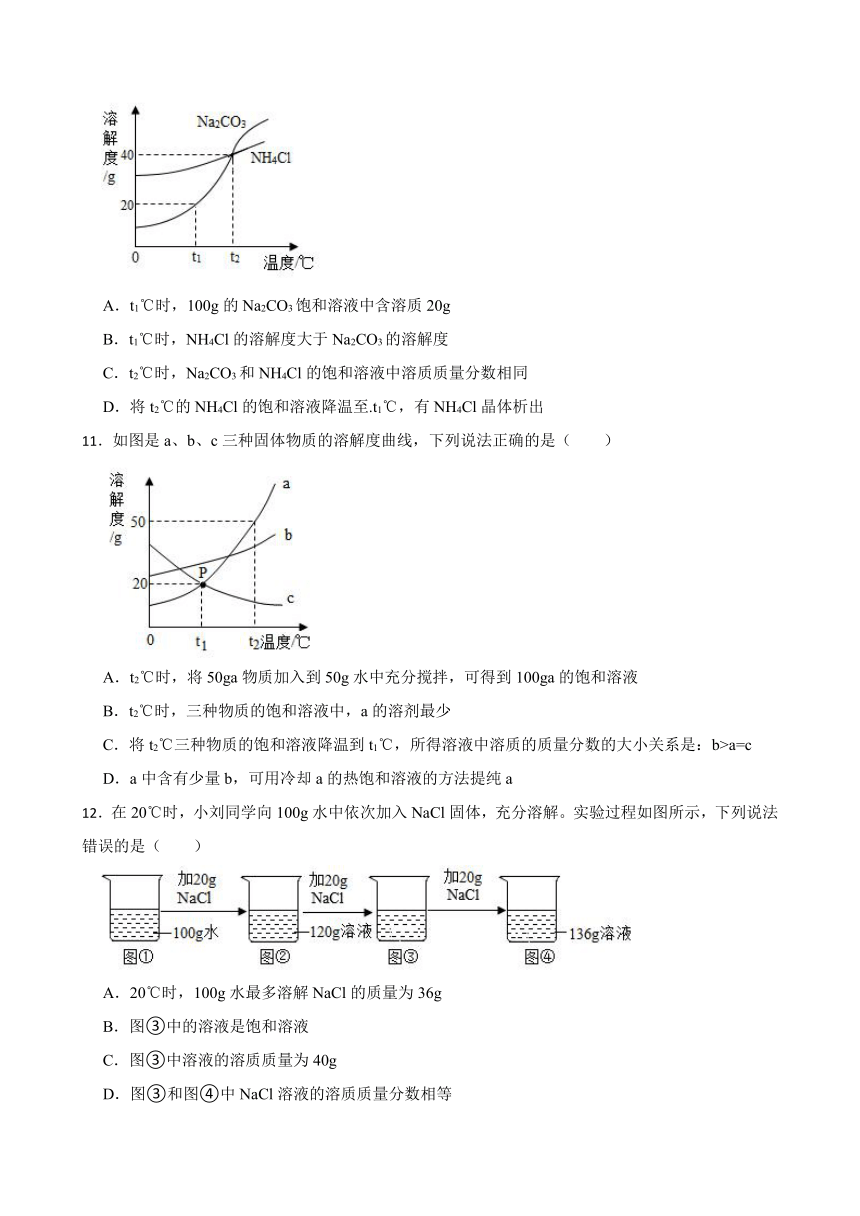
10.早在二十世纪初,我国化学家侯德榜在氨碱法制纯碱的基础上,创立了更为先进的侯氏制碱法,生产出Na2CO3的同时得到副产品NH4Cl,促进了世界制碱技术的发展。实验测得Na2CO3和NH4Cl的溶解度曲线如右图所示,下列有关说法错误的是( )
A.t1℃时,100g的Na2CO3饱和溶液中含溶质20g
B.t1℃时,NH4Cl的溶解度大于Na2CO3的溶解度
C.t2℃时,Na2CO3和NH4Cl的饱和溶液中溶质质量分数相同
D.将t2℃的NH4Cl的饱和溶液降温至.t1℃,有NH4Cl晶体析出
11.如图是a、b、c三种固体物质的溶解度曲线,下列说法正确的是( )
A.t2℃时,将50ga物质加入到50g水中充分搅拌,可得到100ga的饱和溶液
B.t2℃时,三种物质的饱和溶液中,a的溶剂最少
C.将t2℃三种物质的饱和溶液降温到t1℃,所得溶液中溶质的质量分数的大小关系是:b>a=c
D.a中含有少量b,可用冷却a的热饱和溶液的方法提纯a
12.在20℃时,小刘同学向100g水中依次加入NaCl固体,充分溶解。实验过程如图所示,下列说法错误的是( )
A.20℃时,100g水最多溶解NaCl的质量为36g
B.图③中的溶液是饱和溶液
C.图③中溶液的溶质质量为40g
D.图③和图④中NaCl溶液的溶质质量分数相等
二、填空题
13.下表是NaCl、KNO3在不同温度时的溶解度,根据数据回答。
温度/℃ 0 10 20 30 40 50 60
溶解度 NaCl 35.7 35.8 36.0 36.3 36.6 37.0 37.3
(g/100g水) KNO3 13.3 20.9 31.6 45.8 63.9 85.5 110
①氯化钠的溶解度受温度变化的影响 (填“很大”或“很小”)。
②50℃时,KNO3的溶解度 (填“<”、“>”或“=”)NaCl的溶解度;向烧杯中加入100g水和49.0gKNO3固体配成50℃的溶液,再冷却到20℃,烧杯中析出固体的质量为 g。
③KNO3中混有少量的NaCl,提纯的方法是 (填“降温结晶”或“蒸发结晶”)。
④要比较NaCl和KNO3在水中的溶解性强弱,测定的数据可以是:相同温度下,等质量的溶质完全溶解达到饱和时所需水的质量;或 。
⑤如图是有关硝酸钾溶液的实验操作及变化情况,说法正确的是 (填编号)。
A 操作I一定是降温
B a与b的溶剂质量可能相等
C a与c的溶质质量一定相等
D b与c的溶质质量分数一定相等
14.如图是A、B的溶解度曲线.t2℃时分别将100gA、B的饱和溶液降温至t1℃,析出固体质量A B(填“>”、“<”或“=”);把t2℃时150gA的饱和溶液稀释为20%,需加水 g.
15.甲、乙、丙三种固体(均不含结晶水)的部分溶解度见下表。
温度
t1 t2 t3
溶解度 (g/100g
水) 甲 44.9 54.2 107.5
乙 13.0 9.6 5.3
丙 5.0 10.0 40.0
①t2℃时,乙的溶解度是 g。
②如图一所示,t1℃时,甲、乙、丙三种物质各
25g 放入烧杯中,分别倒入 100g 水,保持温度不变,充分溶解。
I甲溶液的溶质质量分数是 。
II将三个烧杯中的混合物分别升温至 t3℃。溶液质量减少的是 溶液(选填“甲”“乙”或“丙”)。在图二中,绘制丙溶液溶质质量随温度变化的曲线 。
16.如图,是A、B、C三种物质的溶解度曲线,据图回答:
(1)t1℃时A、B、C三种物质的溶解度由大到小的顺序是 (填写序号,下同).
(2)t1℃时30gA物质加入到50g水中不断搅拌,形成的溶液质量是 g.
(3)将t1℃时A、B、C三种物质饱和溶液的温度升高到t2℃时,三种溶液的溶质质量分数由大小关系是 .
17.60℃时,硝酸钾的溶解度为110g,这说明在 时, 水中最多可溶解 硝酸钾.
18.甲、乙、丙三种物质的溶解度曲线如图所示。
(1)t1℃时,甲、乙、丙三种物质的溶解度由小到大顺序为 。
(2)当乙中混有少量的甲时,可采用 (填“降温结晶”或“蒸发结晶")的方法提纯乙。
(3)将t2℃时90 g甲的饱和溶液降温到t1℃,析出晶体的质量为 g。
(4)t2℃时将甲、乙、丙三种物质的饱和溶液降温到t1℃,所得溶液的溶质质量分数由大到小顺序为 。
三、综合题
19.结合KNO3和NaCl的溶解度表,回答下列问题。
温度/℃ 0 20 40 60 80 100
溶解度/g NaCl 35.7 36.0 36.6 37.3 38.4 39.8
KNO3 13.3 31.6 63.9 110 169 246
(1)0℃时,KNO3溶解度是 g
(2)根据NaCl的溶解度表可知,从海水中提取氯化钠,通常采用的结晶方法是 。
(3)在60℃时,将60gKNO3加入到50g水中充分溶解后所得溶液降温到40℃,对溶液的分析正确的是 。
A 降温前后溶液都是饱和溶液
B 溶液中溶质减少
C 溶液中溶质的质量分数不变
20.甲、乙两物质的溶解度曲线如图所示,请据图回答下列问题。
(1)20℃时,甲物质的溶解度是 g;
(2)从甲的饱和溶液中获得甲,可采用 方法。
(3)欲将40℃时乙物质的饱和溶液变为不饱和溶液,可采用的方法是 ;(写一种即可)
(4)40℃时,将甲、乙两物质的饱和溶液分别降温至20℃,所得溶液的溶质质量分数的大小关系是 。
21.如图是几种固体的溶解度曲线.
(1)10℃ 时,这几种固体中 的溶解度最小.
(2)向烧杯中加入100g水,将含160g硝酸钾和10g氯化钠的混合物加入该烧杯中,溶解配成80℃的溶液,再冷却到10℃,烧杯中析出的固体的名称是 ,质量是 g.当硝酸钾中含有少量氯化钠时,可采用 (填“降温”或“蒸发”)结晶的方法提纯硝酸钾.
(3)如图是配制溶质质量分数为10%的NaCl溶液的实验操作示意图:
用如图2表示的序号表示配制溶液的正确操作顺序 ,如图所示的配制过程还有两种仪器未画出,它们是 .将100g氯化钠溶液的溶质质量分数由10%增大为20%,若保持溶剂质量不变,需加氯化钠固体的质量是 g.
22.如图是甲、乙、丙的溶解度曲线,回答下列问题。
(1)P点的含义是 。
(2)在t1℃时,将30g甲物质加入到50g水中,充分搅拌后溶液的质量为 g。
(3)N点表示t2℃时乙的 溶液(填“饱和”或“不饱和”)。
(4)将甲、乙、丙三种物质的饱和溶液分别由t1℃升温到t2℃,所得溶液中溶质的质量分数最大的物质是 。
(5)t2℃时,将甲物质的不饱和溶液转变成饱和溶液可采取的方法有 (填一种即可)。
答案解析部分
1.【答案】B
2.【答案】A
3.【答案】C
4.【答案】C
5.【答案】B
6.【答案】D
7.【答案】C
8.【答案】C
9.【答案】B
10.【答案】A
11.【答案】D
12.【答案】C
13.【答案】很小;>;17.4;降温结晶;相同温度下,等质量的溶剂完全溶解达到饱和时所需溶质的质量;BD
14.【答案】>;100
15.【答案】9.6;20%;乙;
16.【答案】BCA;65;BCA
17.【答案】60℃;100g;110g
18.【答案】(1)甲=丙<乙
(2)蒸发结晶
(3)27.5g
(4)乙>甲>丙
19.【答案】(1)13.3
(2)蒸发结晶
(3)AB
20.【答案】(1)40
(2)降温结晶
(3)降低温度(合理即可)
(4)甲>乙
21.【答案】(1)硝酸钾
(2)硝酸钾;140;降温
(3)③②④⑤①;药匙、胶头滴管;12.5
22.【答案】(1)在t1℃时,甲、丙的溶解度相等,为40g
(2)70
(3)不饱和
(4)乙
(5)降温或增加溶质、蒸发溶剂
一、单选题
1.图表资料可以为我们提供很多信息,下列关于图表提供的信息或应用的说法中,不正确的是( )
A.根据相对原子质量表,可查找元素的相对原子质量
B.根据酸、碱、盐的溶解性表,可判断各种酸、碱、盐的溶解度大小
C.根据溶解度曲线图,可选择从溶液中获得晶体的方法
D.根据空气质量周报,可知道空气质量级别和首要污染物
2.李克强总理在2022年3月的全国两会报告中指出:持续改善生态环境,推动绿色低碳发展。下列有关二氧化碳的说法错误的是( )
A.二氧化碳通入紫色石蕊溶液中,试液变成红色的原因是二氧化碳具有酸性
B.打开汽水瓶盖有大量气泡冒出说明二氧化碳的溶解度随压强的减小而减小
C.图书馆内的图书起火用二氧化碳灭火器灭火
D.大力植树造林,严禁乱砍滥伐森林,以控制二氧化碳的排放量
3.如图是A、B两种固体物质的溶解度曲线,下列说法一定正确的是( )
A.物质A的溶解度大于B的溶解度
B.36 C时,A的饱和溶液溶质量分数为60%
C.若A中含少量的B杂质,可通过降温结晶提纯A
D.18 C时,A,B的饱和溶液中所含溶质的质量相等
4.t℃时,A物质的饱和溶液中A的质量分数为15%,B物质的溶解度是25g,C物质的10g饱和溶液蒸干后可得1.5gC.若取等质量的3种物质的饱和溶液,则3种溶液中所含溶质的质量大小顺序是( )
A.A>C>B B.C>A>B C.B>C=A D.A>B>C
5.我国航天员王亚平在太空演示“冰雪”实验时用到了过饱和醋酸钠溶液。如图是醋酸钠的溶解度曲线,下列说法正确的是( )
A.常温下,醋酸钠属于微溶物质
B.图中P点所表示的醋酸钠溶液是不饱和的
C.40℃时,饱和醋酸钠溶液的溶质质量分数是65.6%
D.将A点的饱和溶液降温至20℃,溶质质量分数增大
6.a、b两种物质的溶解度曲线如图所示。下列说法错误的是()
A.15℃时,a,b的溶解度均为20g/100克水
B.将30℃时 a 的饱和溶液降温至15℃,溶质的质量分数不变
C.加水或升温均可使b的饱和溶液变为不饱和溶液
D.15℃时,将15gb放入50g水中,充分溶解后,所得溶液质量是65g
7.甲、乙两种固体物质(均不含结晶水)的溶解度曲线如图所示,下列说法正确的是( )
A.甲、乙物质都适用降温结晶法使溶质从溶液中析出
B.60℃时将40g甲物质加入50g水中能得到90g饱和溶液
C.通过降温能使A点甲的不饱和溶液变为饱和溶液
D.分别将甲、乙物质饱和溶液从60℃降至20℃,甲析出晶体较多
8.如图为甲、乙两种固体物质的溶解度曲线.下列有关说法中正确的是()
A.60℃时,将等质量的甲、乙两种物质的饱和溶液降温到20℃,均变成不饱和溶液
B.60℃时,将80g甲物质放入100g水中,所得溶液的质量为180g
C.40℃时,两种物质的饱和溶液的溶质质量分数相等
D.20℃时,甲物质的溶解度大于乙物质的溶解度
9.甲、乙两种固体物质(不含结晶水)的溶解度曲线如下图所示.下列说法正确的是( )
A.甲物质的溶解度大于乙物质的溶解度
B.t1℃时,甲、乙两物质的溶解度相等,均为40g
C.t2℃时,甲溶液的溶质质量分数一定大于乙溶液的溶质质量分数
D.甲的溶解度受温度影响较小
10.早在二十世纪初,我国化学家侯德榜在氨碱法制纯碱的基础上,创立了更为先进的侯氏制碱法,生产出Na2CO3的同时得到副产品NH4Cl,促进了世界制碱技术的发展。实验测得Na2CO3和NH4Cl的溶解度曲线如右图所示,下列有关说法错误的是( )
A.t1℃时,100g的Na2CO3饱和溶液中含溶质20g
B.t1℃时,NH4Cl的溶解度大于Na2CO3的溶解度
C.t2℃时,Na2CO3和NH4Cl的饱和溶液中溶质质量分数相同
D.将t2℃的NH4Cl的饱和溶液降温至.t1℃,有NH4Cl晶体析出
11.如图是a、b、c三种固体物质的溶解度曲线,下列说法正确的是( )
A.t2℃时,将50ga物质加入到50g水中充分搅拌,可得到100ga的饱和溶液
B.t2℃时,三种物质的饱和溶液中,a的溶剂最少
C.将t2℃三种物质的饱和溶液降温到t1℃,所得溶液中溶质的质量分数的大小关系是:b>a=c
D.a中含有少量b,可用冷却a的热饱和溶液的方法提纯a
12.在20℃时,小刘同学向100g水中依次加入NaCl固体,充分溶解。实验过程如图所示,下列说法错误的是( )
A.20℃时,100g水最多溶解NaCl的质量为36g
B.图③中的溶液是饱和溶液
C.图③中溶液的溶质质量为40g
D.图③和图④中NaCl溶液的溶质质量分数相等
二、填空题
13.下表是NaCl、KNO3在不同温度时的溶解度,根据数据回答。
温度/℃ 0 10 20 30 40 50 60
溶解度 NaCl 35.7 35.8 36.0 36.3 36.6 37.0 37.3
(g/100g水) KNO3 13.3 20.9 31.6 45.8 63.9 85.5 110
①氯化钠的溶解度受温度变化的影响 (填“很大”或“很小”)。
②50℃时,KNO3的溶解度 (填“<”、“>”或“=”)NaCl的溶解度;向烧杯中加入100g水和49.0gKNO3固体配成50℃的溶液,再冷却到20℃,烧杯中析出固体的质量为 g。
③KNO3中混有少量的NaCl,提纯的方法是 (填“降温结晶”或“蒸发结晶”)。
④要比较NaCl和KNO3在水中的溶解性强弱,测定的数据可以是:相同温度下,等质量的溶质完全溶解达到饱和时所需水的质量;或 。
⑤如图是有关硝酸钾溶液的实验操作及变化情况,说法正确的是 (填编号)。
A 操作I一定是降温
B a与b的溶剂质量可能相等
C a与c的溶质质量一定相等
D b与c的溶质质量分数一定相等
14.如图是A、B的溶解度曲线.t2℃时分别将100gA、B的饱和溶液降温至t1℃,析出固体质量A B(填“>”、“<”或“=”);把t2℃时150gA的饱和溶液稀释为20%,需加水 g.
15.甲、乙、丙三种固体(均不含结晶水)的部分溶解度见下表。
温度
t1 t2 t3
溶解度 (g/100g
水) 甲 44.9 54.2 107.5
乙 13.0 9.6 5.3
丙 5.0 10.0 40.0
①t2℃时,乙的溶解度是 g。
②如图一所示,t1℃时,甲、乙、丙三种物质各
25g 放入烧杯中,分别倒入 100g 水,保持温度不变,充分溶解。
I甲溶液的溶质质量分数是 。
II将三个烧杯中的混合物分别升温至 t3℃。溶液质量减少的是 溶液(选填“甲”“乙”或“丙”)。在图二中,绘制丙溶液溶质质量随温度变化的曲线 。
16.如图,是A、B、C三种物质的溶解度曲线,据图回答:
(1)t1℃时A、B、C三种物质的溶解度由大到小的顺序是 (填写序号,下同).
(2)t1℃时30gA物质加入到50g水中不断搅拌,形成的溶液质量是 g.
(3)将t1℃时A、B、C三种物质饱和溶液的温度升高到t2℃时,三种溶液的溶质质量分数由大小关系是 .
17.60℃时,硝酸钾的溶解度为110g,这说明在 时, 水中最多可溶解 硝酸钾.
18.甲、乙、丙三种物质的溶解度曲线如图所示。
(1)t1℃时,甲、乙、丙三种物质的溶解度由小到大顺序为 。
(2)当乙中混有少量的甲时,可采用 (填“降温结晶”或“蒸发结晶")的方法提纯乙。
(3)将t2℃时90 g甲的饱和溶液降温到t1℃,析出晶体的质量为 g。
(4)t2℃时将甲、乙、丙三种物质的饱和溶液降温到t1℃,所得溶液的溶质质量分数由大到小顺序为 。
三、综合题
19.结合KNO3和NaCl的溶解度表,回答下列问题。
温度/℃ 0 20 40 60 80 100
溶解度/g NaCl 35.7 36.0 36.6 37.3 38.4 39.8
KNO3 13.3 31.6 63.9 110 169 246
(1)0℃时,KNO3溶解度是 g
(2)根据NaCl的溶解度表可知,从海水中提取氯化钠,通常采用的结晶方法是 。
(3)在60℃时,将60gKNO3加入到50g水中充分溶解后所得溶液降温到40℃,对溶液的分析正确的是 。
A 降温前后溶液都是饱和溶液
B 溶液中溶质减少
C 溶液中溶质的质量分数不变
20.甲、乙两物质的溶解度曲线如图所示,请据图回答下列问题。
(1)20℃时,甲物质的溶解度是 g;
(2)从甲的饱和溶液中获得甲,可采用 方法。
(3)欲将40℃时乙物质的饱和溶液变为不饱和溶液,可采用的方法是 ;(写一种即可)
(4)40℃时,将甲、乙两物质的饱和溶液分别降温至20℃,所得溶液的溶质质量分数的大小关系是 。
21.如图是几种固体的溶解度曲线.
(1)10℃ 时,这几种固体中 的溶解度最小.
(2)向烧杯中加入100g水,将含160g硝酸钾和10g氯化钠的混合物加入该烧杯中,溶解配成80℃的溶液,再冷却到10℃,烧杯中析出的固体的名称是 ,质量是 g.当硝酸钾中含有少量氯化钠时,可采用 (填“降温”或“蒸发”)结晶的方法提纯硝酸钾.
(3)如图是配制溶质质量分数为10%的NaCl溶液的实验操作示意图:
用如图2表示的序号表示配制溶液的正确操作顺序 ,如图所示的配制过程还有两种仪器未画出,它们是 .将100g氯化钠溶液的溶质质量分数由10%增大为20%,若保持溶剂质量不变,需加氯化钠固体的质量是 g.
22.如图是甲、乙、丙的溶解度曲线,回答下列问题。
(1)P点的含义是 。
(2)在t1℃时,将30g甲物质加入到50g水中,充分搅拌后溶液的质量为 g。
(3)N点表示t2℃时乙的 溶液(填“饱和”或“不饱和”)。
(4)将甲、乙、丙三种物质的饱和溶液分别由t1℃升温到t2℃,所得溶液中溶质的质量分数最大的物质是 。
(5)t2℃时,将甲物质的不饱和溶液转变成饱和溶液可采取的方法有 (填一种即可)。
答案解析部分
1.【答案】B
2.【答案】A
3.【答案】C
4.【答案】C
5.【答案】B
6.【答案】D
7.【答案】C
8.【答案】C
9.【答案】B
10.【答案】A
11.【答案】D
12.【答案】C
13.【答案】很小;>;17.4;降温结晶;相同温度下,等质量的溶剂完全溶解达到饱和时所需溶质的质量;BD
14.【答案】>;100
15.【答案】9.6;20%;乙;
16.【答案】BCA;65;BCA
17.【答案】60℃;100g;110g
18.【答案】(1)甲=丙<乙
(2)蒸发结晶
(3)27.5g
(4)乙>甲>丙
19.【答案】(1)13.3
(2)蒸发结晶
(3)AB
20.【答案】(1)40
(2)降温结晶
(3)降低温度(合理即可)
(4)甲>乙
21.【答案】(1)硝酸钾
(2)硝酸钾;140;降温
(3)③②④⑤①;药匙、胶头滴管;12.5
22.【答案】(1)在t1℃时,甲、丙的溶解度相等,为40g
(2)70
(3)不饱和
(4)乙
(5)降温或增加溶质、蒸发溶剂
