7.1 溶液的酸碱性 同步练习(含答案) 2022-2023学年沪教版(全国)九年级下册化学
文档属性
| 名称 | 7.1 溶液的酸碱性 同步练习(含答案) 2022-2023学年沪教版(全国)九年级下册化学 |

|
|
| 格式 | zip | ||
| 文件大小 | 56.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-03-01 00:00:00 | ||
图片预览



文档简介
7.1 溶液的酸碱性 同步练习
一、单选题
1.向下列物质的水溶液中滴加酚酞,溶液变红的是( )
A.二氧化碳的水溶液 B.食盐的水溶液
C.氢氧化钙的水溶液 D.氯化氢气体的水溶液
2.在柠檬汁中滴入酚酞试液不变色,滴入石蕊试液变成红色,由此可知,柠檬汁( )
A.显酸性 B.显碱性 C.显中性 D.酸碱性不定
3.20g溶质质量分数为20%的氢氧化钠溶液和20g溶质质量分数为20%的稀硫酸充分反应后,滴入紫色石蕊溶液显( )。
A.蓝色 B.红色 C.无色 D.紫色
4.分析推理是化学学习中常用的思维方法,下列分析推理正确的是( )
A.氢氧化镁可治疗胃酸过多,故氢氧化钠也可治疗胃酸过多
B.O2和O3的分子构成不同,所以它们的化学性质不同
C.烧碱属于碱,故纯碱也属于碱
D.酸雨的pH小于7,所以pH小于7的雨水一定是酸雨
5.铜能与硝酸反应,但不产生H2.根据反应方程式:3Cu+8HNO3(稀)=3Cu(NO3)2+2X↑+4H2O,推测 X 的化学式是( )
A.N2O3 B.NO2 C.NO D.N2O
6.不同品牌的洗手液pH一般不同,25℃时四种洗手液的pH如图所示。下列说法不正确的是( )
A.洗手液a用蒸馏水稀释后pH减小
B.洗手液b的酸性比a弱
C.洗手液c能使石蕊试液变蓝色
D.洗手液d和a混合液的pH可能等于7
7.阅读下列84消毒液和洁厕灵等消毒液内容,判断下列说法错误的是( )
产品品名 84消毒液
主要原料 有效成分次氯酸钠(NaClO)
主要性能 无色或淡黄色液体,有刺激性味道,pH=11,具有漂白性、挥发性等
主要功能 高效消毒剂
注意事项 不能与洁厕灵混合[产生有毒物质氯气(Cl2 )]
产品品名 洁厕灵
主要原料 有效成分为盐酸(HCl)
主要性能 无色液体、有刺激性气味
主要功能 有效清除污垢、除异味
注意事项 密封、置于阴凉处
A.①次氯酸钠、②盐酸、③氯气三种物质按氯元素化合价由高到低顺序是:①>③>②
B.石蕊试液遇84消毒液变蓝,遇洁厕灵变红
C.洁厕灵不能用来清洗以大理石为原料做成的物品
D.将酚酞试液染成的小花放入84消毒液中,小花最终呈红色
8.分别向甲、乙、丙三种无色溶液中滴加紫色石蕊试液、观察到甲溶液变红色,乙溶液变蓝色,丙溶液变紫色。则它们的pH由小到大的排列是( )
A.甲、乙、丙 B.甲、丙、乙 C.乙、甲、丙 D.丙、甲、乙
9.下列对宏微观现象的观察、思考、推理的说法错误的是( )
A.水蒸发变成水蒸气体积变大,说明水分子间隔变大
B.过氧化氢分解生成水和氧气,说明过氧化氢是由水分子和氧分子构成的
C.将紫色石蕊溶液滴入某稀溶液中,溶液显红色,说明该稀溶液显酸性
D.氢氧化钠、氢氧化钙具有相似的化学性质,说明它们的溶液中都含有氢氧根离子
10.归纳法是学习化学的重要方法之一,下列归納正确的是( )
A. pH和溶液的酸碱性
B. 氟离子的结构示意图
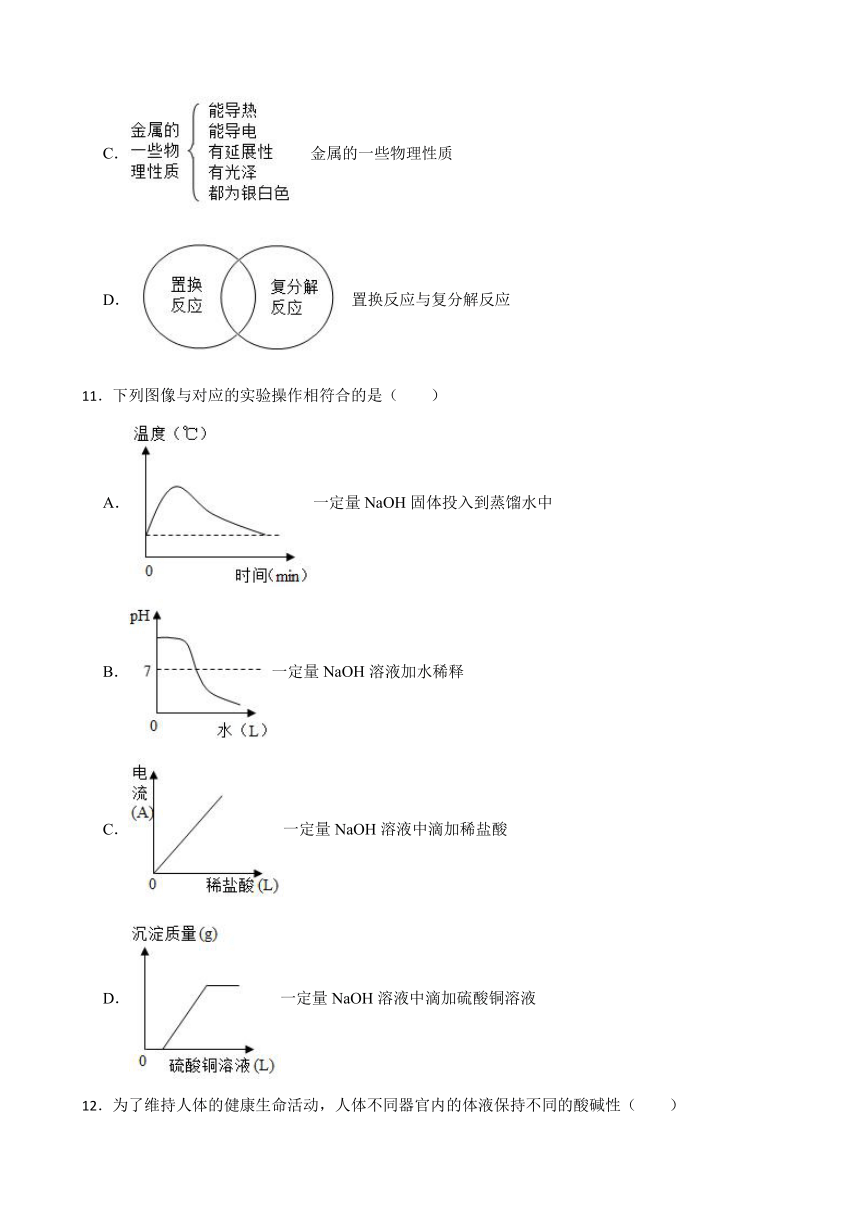
C. 金属的一些物理性质
D. 置换反应与复分解反应
11.下列图像与对应的实验操作相符合的是( )
A.一定量NaOH固体投入到蒸馏水中
B.一定量NaOH溶液加水稀释
C.一定量NaOH溶液中滴加稀盐酸
D.一定量NaOH溶液中滴加硫酸铜溶液
12.为了维持人体的健康生命活动,人体不同器官内的体液保持不同的酸碱性( )
体液 尿液 胃液 血液
pH 4.7﹣8.4 0.9﹣1.5 7.35﹣7.45
A.人体的尿液一定呈酸性
B.人体的血液一定呈碱性
C.人体的胃液能使紫色石蕊试液变蓝色
D.pH试纸可精确测得以上体液的pH
二、填空题
13.将7.3%的稀盐酸逐滴加入50g滴有少量酚酞的NaOH溶液中,溶液的pH和加入稀盐酸的质量关系如图。
a点处溶液呈 色,滴加稀盐酸后,酸与碱发生 反应,溶液的pH不断 ,b点表示 ,此处溶液的pH 7,至c点处时,溶液中的溶质为 ,原NaOH溶液的质量分数为 。
14.请将下列物质按一定的要求从大到小(由高到低或由多到少)排列(填序号)
(1)氮元素的化合价:a.NH3 b.NaNO3 c.NO2 。
(2)溶解性:a.CuO b.Ca(OH)2 c.NaNO3 。
(3)溶液的pH:a.KCl b.CH3COOH c.NaHCO3 。
(4)含铁质量分数:a.Fe2O3 b.FeO c.Fe3O4
15.“低碳经济”的理想形态是充分发展“阳光经济”、“风能经济”、“氢能经济”、“生物质能经济”.请根据所学知识回答下列问题:
(1)太阳能的特点是 .
(2)氢能指氢气燃烧释放的能量,试写出氢气在空气中燃烧的化学方程式: .
(3)“低碳经济”、“低碳生活”的重要含义之一,就是节约化石能源的消耗,为新能源的普及利用提供时间保障.化石能源主要指煤、石油、 .它们燃烧后的产物之一 ,是温室效应气体,它“让地球发烧”
(4)随着“低碳”意识的不断深入,低碳生活已经成为我们初中生积极提倡并去实践的生活方式.作为初中生的我们应从点滴做起,以下做法不符合科学的低碳生活方式的是:
A、家里的白炽灯将其更换为节能灯.
B、为了节约洗涤餐具时用的水,我们应尽量使用一次性筷子和餐盒.
C、家中的水进行二次利用,比如洗脸水可以冲洗厕所.
D、家中的用电器不使用时应断开电源,以避免待机时消耗的电能.
16.中和一定质量的稀硫酸,需用20克氢氧化钠,若改用20克氢氧化钾时,反应后溶液的pH应当是 .(填大于7 或等于7 或小于7 )
17.向盛有氢氧化钠溶液的锥形瓶里滴入几滴酚酞溶液,溶液变成 色,pH (填“>”、“<”或“=”),逐滴向锥形瓶中滴入盐酸并振荡,观察到的现象是 ,溶液的pH (填“增大”或“减小”).盐酸过量后此时溶液中的溶质有 .
18.现有下列八种物质:①NaHCO3;②Na2CO3;③Ca(OH)2;④CaO;⑤KNO3;⑥甲醛;⑦SO2⑧CO.请用上述物质的序号填空.
(1)俗名叫纯碱的是 ,可用于改良酸性土壤的碱是 ,可做食品干燥剂的是 .
(2)可用于治疗胃酸过多的是 ,在空气中会导致酸雨形成的是 ,能与血液中的血红蛋白结合导致生物体中毒的是 ,其水溶液可用于浸泡动物标本的是 .某作物叶片发黄且易倒伏需使用 (3)属于盐类的是 .
三、综合题
19.碳酸钠溶液具有碱性,可以清洗餐具上的油污,碱性越强,效果越好。用2%、6%和10%的碳酸钠溶液进行实验,研究碳酸钠溶液碱性的影响因素。
浓度 2% 2% 2% 6% 6% 6% 10% 10% 10%
温度 20 40 60 20 40 60 20 40 60
pH 10.09 11.13 11.18 11.10 11.19 11.30 11.15 11.23 11.35
(1)溶液碱性最强的是 。
(2)分析表中数据得出的结论是 。
20.用氢氧化钙中和一定量的盐酸时,溶液的pH与加入的氢氧化钙质量的关系如图所示。
(1)氢氧化钙与盐酸反应的化学方程式为
(2)当加入氢氧化钙mg时,溶液中的溶质为
(3)若改用ng氢氧化钠与相同量盐酸反应,所得溶液的 7(填“>”“<”或“=”)。
21.有一包白色固体可能含碳酸钠、硫酸钠、氯化钾、硝酸钡、氢氧化钠中的一种或几种.某化学兴趣小组为探究其成分做了以下实验:
Ⅰ.取少量固体于烧杯中,逐渐加水并不断搅拌,烧杯内固体的质量随加入水的质量的变化如图1所示;
Ⅱ.取少量B点时的清液于试管中,滴加酚酞溶液,酚酞溶液不变色;
Ⅲ.继续向烧杯中滴加稀硝酸并不断搅拌,烧杯内固体的质量随加入稀硝酸的质量的变化如图2所示.
请回答下列问题:
(1)BC段可观察到的现象是 ,从C到D液体的pH (填“增大”、“减小”或“不变”);
(2)原白色固体中一定含有 ,可能含有 ;
(3)D点时,溶液中一定含有的溶质是 ;
(4)为进一步探究该白色固体的成分,该组同学取少量原固体样品于试管中,加足量水溶解,加 ,过滤;再向滤液中加 ,观察现象.
22.燃料和能源与社会发展息息相关。
(1)氢燃料具有广阔的应用前景。氢气燃烧的化学方程式为 。
(2)铜镁合金是一种潜在的贮氢材料,可用一定质量比的铜、镁单质在氢气环境下高温熔炼获得。铜镁合金的熔点比金属镁和铜 (填“高”或“低”);熔炼制备该合金时,氩气的作用是 。
(3)核能是全世界都在研究的重要能源,核能发电安全特别重要。核电站发生核泄漏所产生的碘-131原子(131I)与普通碘-127原子(127I)不同,具有能对人体造成损害的放射性。观察下图回答问题:
①碘属于 (填“金属”或“非金属”)元素:据1图,碘原子的核电荷数为 。
②“2图”表示的变化过程是有放射性的131I原子进入普通碘化合物的过程,该过程可用化学方程式表示为: +131I127I→ +127I2。
答案解析部分
1.【答案】D
2.【答案】A
3.【答案】A
4.【答案】B
5.【答案】C
6.【答案】A
7.【答案】D
8.【答案】B
9.【答案】B
10.【答案】B
11.【答案】A
12.【答案】B
13.【答案】红;中和;降低;盐酸和NaOH恰好完全反应(合理答案也给分);=;NaCl和HCl;8%
14.【答案】(1)bca
(2)cba
(3)cab
(4)bca
15.【答案】能量巨大,但分散、间断、不稳定,清洁等;2H2+O22H2O;天然气;二氧化碳;B
16.【答案】小于7
17.【答案】红;>;溶液由红色变为无色;减小;氯化钠和氯化氢
18.【答案】②;③;④;①;⑦;⑧;⑥;⑤;①②⑤
19.【答案】(1)60℃时10%的碳酸钠溶液
(2)碳酸钠溶液的碱性受温度和浓度影响
20.【答案】(1)Ca(OH)2+2HCl=CaCl2+2H2O
(2)CaCl2HCl
(3)小于
21.【答案】(1)固体部分溶解,有气泡冒出;减小
(2)碳酸钠、硫酸钠、硝酸钡;氯化钾
(3)硝酸钠、硝酸钡、硝酸
(4)足量的稀硝酸和硝酸钡溶液;硝酸银
22.【答案】(1)
(2)低;隔绝空气(或答“防止金属被氧化”、“保护气”等)
(3)非金属;53;K127I;K131I
一、单选题
1.向下列物质的水溶液中滴加酚酞,溶液变红的是( )
A.二氧化碳的水溶液 B.食盐的水溶液
C.氢氧化钙的水溶液 D.氯化氢气体的水溶液
2.在柠檬汁中滴入酚酞试液不变色,滴入石蕊试液变成红色,由此可知,柠檬汁( )
A.显酸性 B.显碱性 C.显中性 D.酸碱性不定
3.20g溶质质量分数为20%的氢氧化钠溶液和20g溶质质量分数为20%的稀硫酸充分反应后,滴入紫色石蕊溶液显( )。
A.蓝色 B.红色 C.无色 D.紫色
4.分析推理是化学学习中常用的思维方法,下列分析推理正确的是( )
A.氢氧化镁可治疗胃酸过多,故氢氧化钠也可治疗胃酸过多
B.O2和O3的分子构成不同,所以它们的化学性质不同
C.烧碱属于碱,故纯碱也属于碱
D.酸雨的pH小于7,所以pH小于7的雨水一定是酸雨
5.铜能与硝酸反应,但不产生H2.根据反应方程式:3Cu+8HNO3(稀)=3Cu(NO3)2+2X↑+4H2O,推测 X 的化学式是( )
A.N2O3 B.NO2 C.NO D.N2O
6.不同品牌的洗手液pH一般不同,25℃时四种洗手液的pH如图所示。下列说法不正确的是( )
A.洗手液a用蒸馏水稀释后pH减小
B.洗手液b的酸性比a弱
C.洗手液c能使石蕊试液变蓝色
D.洗手液d和a混合液的pH可能等于7
7.阅读下列84消毒液和洁厕灵等消毒液内容,判断下列说法错误的是( )
产品品名 84消毒液
主要原料 有效成分次氯酸钠(NaClO)
主要性能 无色或淡黄色液体,有刺激性味道,pH=11,具有漂白性、挥发性等
主要功能 高效消毒剂
注意事项 不能与洁厕灵混合[产生有毒物质氯气(Cl2 )]
产品品名 洁厕灵
主要原料 有效成分为盐酸(HCl)
主要性能 无色液体、有刺激性气味
主要功能 有效清除污垢、除异味
注意事项 密封、置于阴凉处
A.①次氯酸钠、②盐酸、③氯气三种物质按氯元素化合价由高到低顺序是:①>③>②
B.石蕊试液遇84消毒液变蓝,遇洁厕灵变红
C.洁厕灵不能用来清洗以大理石为原料做成的物品
D.将酚酞试液染成的小花放入84消毒液中,小花最终呈红色
8.分别向甲、乙、丙三种无色溶液中滴加紫色石蕊试液、观察到甲溶液变红色,乙溶液变蓝色,丙溶液变紫色。则它们的pH由小到大的排列是( )
A.甲、乙、丙 B.甲、丙、乙 C.乙、甲、丙 D.丙、甲、乙
9.下列对宏微观现象的观察、思考、推理的说法错误的是( )
A.水蒸发变成水蒸气体积变大,说明水分子间隔变大
B.过氧化氢分解生成水和氧气,说明过氧化氢是由水分子和氧分子构成的
C.将紫色石蕊溶液滴入某稀溶液中,溶液显红色,说明该稀溶液显酸性
D.氢氧化钠、氢氧化钙具有相似的化学性质,说明它们的溶液中都含有氢氧根离子
10.归纳法是学习化学的重要方法之一,下列归納正确的是( )
A. pH和溶液的酸碱性
B. 氟离子的结构示意图
C. 金属的一些物理性质
D. 置换反应与复分解反应
11.下列图像与对应的实验操作相符合的是( )
A.一定量NaOH固体投入到蒸馏水中
B.一定量NaOH溶液加水稀释
C.一定量NaOH溶液中滴加稀盐酸
D.一定量NaOH溶液中滴加硫酸铜溶液
12.为了维持人体的健康生命活动,人体不同器官内的体液保持不同的酸碱性( )
体液 尿液 胃液 血液
pH 4.7﹣8.4 0.9﹣1.5 7.35﹣7.45
A.人体的尿液一定呈酸性
B.人体的血液一定呈碱性
C.人体的胃液能使紫色石蕊试液变蓝色
D.pH试纸可精确测得以上体液的pH
二、填空题
13.将7.3%的稀盐酸逐滴加入50g滴有少量酚酞的NaOH溶液中,溶液的pH和加入稀盐酸的质量关系如图。
a点处溶液呈 色,滴加稀盐酸后,酸与碱发生 反应,溶液的pH不断 ,b点表示 ,此处溶液的pH 7,至c点处时,溶液中的溶质为 ,原NaOH溶液的质量分数为 。
14.请将下列物质按一定的要求从大到小(由高到低或由多到少)排列(填序号)
(1)氮元素的化合价:a.NH3 b.NaNO3 c.NO2 。
(2)溶解性:a.CuO b.Ca(OH)2 c.NaNO3 。
(3)溶液的pH:a.KCl b.CH3COOH c.NaHCO3 。
(4)含铁质量分数:a.Fe2O3 b.FeO c.Fe3O4
15.“低碳经济”的理想形态是充分发展“阳光经济”、“风能经济”、“氢能经济”、“生物质能经济”.请根据所学知识回答下列问题:
(1)太阳能的特点是 .
(2)氢能指氢气燃烧释放的能量,试写出氢气在空气中燃烧的化学方程式: .
(3)“低碳经济”、“低碳生活”的重要含义之一,就是节约化石能源的消耗,为新能源的普及利用提供时间保障.化石能源主要指煤、石油、 .它们燃烧后的产物之一 ,是温室效应气体,它“让地球发烧”
(4)随着“低碳”意识的不断深入,低碳生活已经成为我们初中生积极提倡并去实践的生活方式.作为初中生的我们应从点滴做起,以下做法不符合科学的低碳生活方式的是:
A、家里的白炽灯将其更换为节能灯.
B、为了节约洗涤餐具时用的水,我们应尽量使用一次性筷子和餐盒.
C、家中的水进行二次利用,比如洗脸水可以冲洗厕所.
D、家中的用电器不使用时应断开电源,以避免待机时消耗的电能.
16.中和一定质量的稀硫酸,需用20克氢氧化钠,若改用20克氢氧化钾时,反应后溶液的pH应当是 .(填大于7 或等于7 或小于7 )
17.向盛有氢氧化钠溶液的锥形瓶里滴入几滴酚酞溶液,溶液变成 色,pH (填“>”、“<”或“=”),逐滴向锥形瓶中滴入盐酸并振荡,观察到的现象是 ,溶液的pH (填“增大”或“减小”).盐酸过量后此时溶液中的溶质有 .
18.现有下列八种物质:①NaHCO3;②Na2CO3;③Ca(OH)2;④CaO;⑤KNO3;⑥甲醛;⑦SO2⑧CO.请用上述物质的序号填空.
(1)俗名叫纯碱的是 ,可用于改良酸性土壤的碱是 ,可做食品干燥剂的是 .
(2)可用于治疗胃酸过多的是 ,在空气中会导致酸雨形成的是 ,能与血液中的血红蛋白结合导致生物体中毒的是 ,其水溶液可用于浸泡动物标本的是 .某作物叶片发黄且易倒伏需使用 (3)属于盐类的是 .
三、综合题
19.碳酸钠溶液具有碱性,可以清洗餐具上的油污,碱性越强,效果越好。用2%、6%和10%的碳酸钠溶液进行实验,研究碳酸钠溶液碱性的影响因素。
浓度 2% 2% 2% 6% 6% 6% 10% 10% 10%
温度 20 40 60 20 40 60 20 40 60
pH 10.09 11.13 11.18 11.10 11.19 11.30 11.15 11.23 11.35
(1)溶液碱性最强的是 。
(2)分析表中数据得出的结论是 。
20.用氢氧化钙中和一定量的盐酸时,溶液的pH与加入的氢氧化钙质量的关系如图所示。
(1)氢氧化钙与盐酸反应的化学方程式为
(2)当加入氢氧化钙mg时,溶液中的溶质为
(3)若改用ng氢氧化钠与相同量盐酸反应,所得溶液的 7(填“>”“<”或“=”)。
21.有一包白色固体可能含碳酸钠、硫酸钠、氯化钾、硝酸钡、氢氧化钠中的一种或几种.某化学兴趣小组为探究其成分做了以下实验:
Ⅰ.取少量固体于烧杯中,逐渐加水并不断搅拌,烧杯内固体的质量随加入水的质量的变化如图1所示;
Ⅱ.取少量B点时的清液于试管中,滴加酚酞溶液,酚酞溶液不变色;
Ⅲ.继续向烧杯中滴加稀硝酸并不断搅拌,烧杯内固体的质量随加入稀硝酸的质量的变化如图2所示.
请回答下列问题:
(1)BC段可观察到的现象是 ,从C到D液体的pH (填“增大”、“减小”或“不变”);
(2)原白色固体中一定含有 ,可能含有 ;
(3)D点时,溶液中一定含有的溶质是 ;
(4)为进一步探究该白色固体的成分,该组同学取少量原固体样品于试管中,加足量水溶解,加 ,过滤;再向滤液中加 ,观察现象.
22.燃料和能源与社会发展息息相关。
(1)氢燃料具有广阔的应用前景。氢气燃烧的化学方程式为 。
(2)铜镁合金是一种潜在的贮氢材料,可用一定质量比的铜、镁单质在氢气环境下高温熔炼获得。铜镁合金的熔点比金属镁和铜 (填“高”或“低”);熔炼制备该合金时,氩气的作用是 。
(3)核能是全世界都在研究的重要能源,核能发电安全特别重要。核电站发生核泄漏所产生的碘-131原子(131I)与普通碘-127原子(127I)不同,具有能对人体造成损害的放射性。观察下图回答问题:
①碘属于 (填“金属”或“非金属”)元素:据1图,碘原子的核电荷数为 。
②“2图”表示的变化过程是有放射性的131I原子进入普通碘化合物的过程,该过程可用化学方程式表示为: +131I127I→ +127I2。
答案解析部分
1.【答案】D
2.【答案】A
3.【答案】A
4.【答案】B
5.【答案】C
6.【答案】A
7.【答案】D
8.【答案】B
9.【答案】B
10.【答案】B
11.【答案】A
12.【答案】B
13.【答案】红;中和;降低;盐酸和NaOH恰好完全反应(合理答案也给分);=;NaCl和HCl;8%
14.【答案】(1)bca
(2)cba
(3)cab
(4)bca
15.【答案】能量巨大,但分散、间断、不稳定,清洁等;2H2+O22H2O;天然气;二氧化碳;B
16.【答案】小于7
17.【答案】红;>;溶液由红色变为无色;减小;氯化钠和氯化氢
18.【答案】②;③;④;①;⑦;⑧;⑥;⑤;①②⑤
19.【答案】(1)60℃时10%的碳酸钠溶液
(2)碳酸钠溶液的碱性受温度和浓度影响
20.【答案】(1)Ca(OH)2+2HCl=CaCl2+2H2O
(2)CaCl2HCl
(3)小于
21.【答案】(1)固体部分溶解,有气泡冒出;减小
(2)碳酸钠、硫酸钠、硝酸钡;氯化钾
(3)硝酸钠、硝酸钡、硝酸
(4)足量的稀硝酸和硝酸钡溶液;硝酸银
22.【答案】(1)
(2)低;隔绝空气(或答“防止金属被氧化”、“保护气”等)
(3)非金属;53;K127I;K131I
