第7节 元素符号表示的量 同步练习(31张ppt)
文档属性
| 名称 | 第7节 元素符号表示的量 同步练习(31张ppt) |

|
|
| 格式 | pptx | ||
| 文件大小 | 2.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2023-03-03 00:00:00 | ||
图片预览









文档简介
(共31张PPT)
第2章 微粒的模型与符号
第7节 元素符号表示的量
学习目标
1.知道相对原子质量和相对分子质量的含义。
2.了解近似相对原子质量与质子数、中子数之间的关系。
3.能根据化学式计算物质的相对分子质量和化合物中各元素的质量比以及元素的质
量分数。
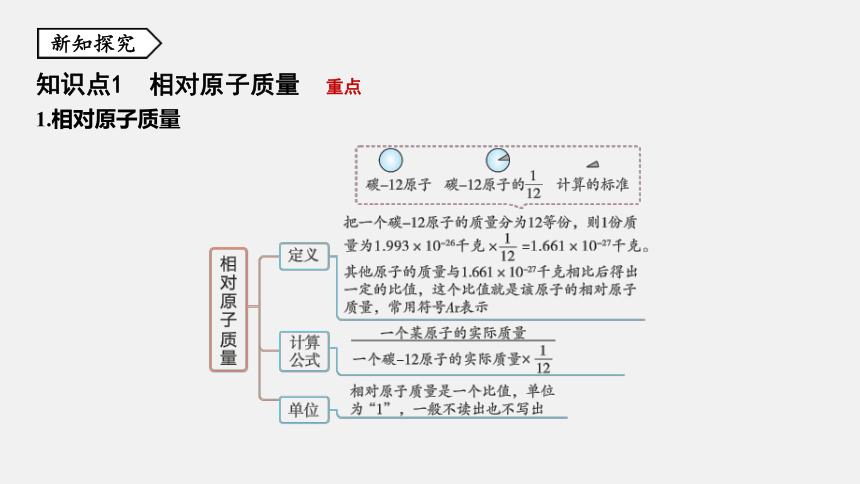
知识点1 相对原子质量 重点
1.相对原子质量
特别提醒
相对原子质量不是实际质量
相对原子质量是
相对原子质量只是一个比值,不是原子的实际质量,但能反映出原子实际质量的相
对大小,原子质量越大,相对原子质量越大,两者成正比。如氢的相对原子质量为1,
碳的相对原子质量为12,则一个碳原子的实际质量也是一个氢原子实际质量的12倍。
辨析比较
原子的质量 相对原子质量
性质 实验测出的一个 原子的实际质量 比较得出的相对质量
数值与单位 数值非常小,单 位为“
质量相同的不同原子构成的纯净物,相对原子质
量越小的物质所含的原子个数越多。如1克铁和1
克铝,由于铝的相对原子质量小于铁的相对原子
质量,所以1克铝中所含铝原子的个数比1克铁中
所含铁原子的个数多
联系 某原子的相对原子质量
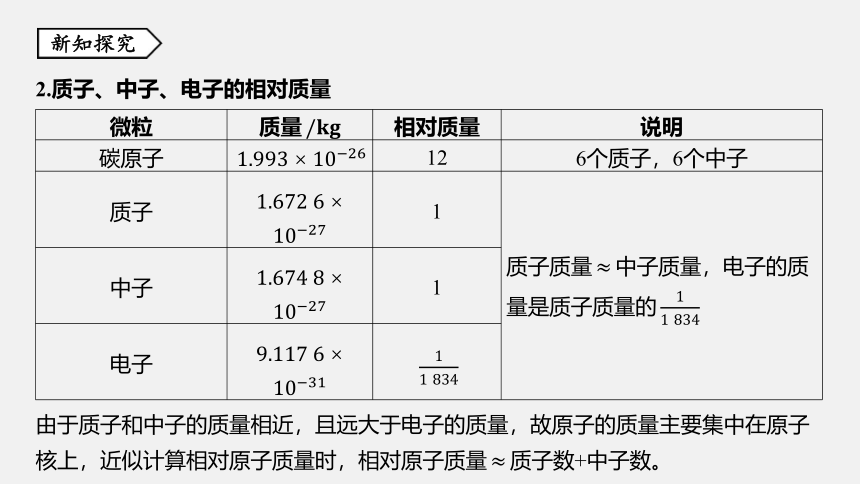
微粒 质量
碳原子
质子 1 质子质量
量是质子质量的
中子 1 电子
核上,近似计算相对原子质量时,相对原子质量
拓展
一个碳
量
典例1 下列关于相对原子质量的说法正确的是( )
A.相对原子质量就是原子的实际质量
B.相对原子质量是原子质量与一种碳原子质量的比值
C.原子的实际质量越大,相对原子质量就越大
D.相对原子质量是一个比值,单位为“
C
[解析] 相对原子质量是一个原子的质量与一个碳
常省略不写,它不是原子的实际质量,但能反应出一个原子的实际质量的相对大小。
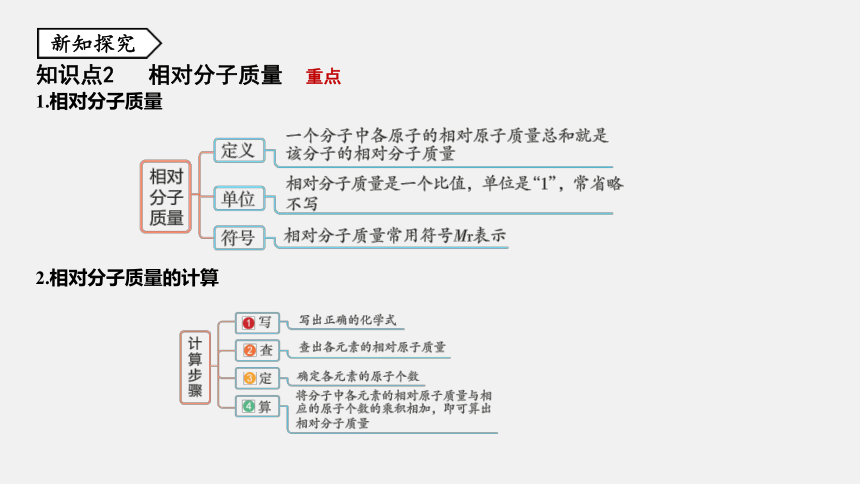
知识点2 相对分子质量 重点
1.相对分子质量
2.相对分子质量的计算
特别提醒
计算相对分子质量的注意事项
(1)元素符号与数字之间在计算相对分子质量时需用“×”号,元素符号之间在计算
相对分子质量时需用“+”号。
如
(2)化学式中原子团右下角的数字表示其个数,计算时可先求出一个原子团的相对
质量,再乘其个数。如
(3)结晶水合物中的“·”表示结合的含义,在计算相对分子质量时应将“·”前后两部
分的相对质量相加而不是相乘。如
拓展
空气的平均相对分子质量为29,可以通过比较某种气体的相对分子质量与29的大小
关系,判断该气体的密度与空气密度的大小关系。
若
若
典例2 [2022·杭州拱墅区期中] 甲烷是天然气的主要成分,可用作燃料,用“&1& ”表示
碳原子,“&2& ”表示氢原子,甲烷分子可表示为“&3& ”,则甲烷的化学式为
_____,每个甲烷分子由___个原子构成,甲烷分子中碳原子与氢原子的个数比是___,甲烷中碳元素的化合价为____,甲烷的相对分子质量为____。
5
1:4
-4
16
[解析] 由题意知,1个甲烷分子由1个碳原子和4个氢原子构成,则化学式为
所以每个甲烷分子中的原子个数为
甲烷中,氢元素的化合价为
合价的代数和为零得,
知识点3 元素质量分数和质量比的确定 重点
1.计算组成物质的各种元素的质量比
化合物中各元素的质量比等于化合物中各元素的相对原子质量与相应原子个数的乘
积之比。
示例1 水
特别提醒
计算化合物中元素的质量比的注意事项
(1)元素只讲种类,不讲个数。如在计算硝酸铵
不能写成
(2)不要把各元素的原子个数比误认为元素的质量比,如
2.计算化合物中某元素的质量分数
化合物中某元素的质量分数
示例2 硝酸铵
(2)有关化学式计算的其他公式
①物质中某元素的质量=物质的质量×物质中该元素的质量分数;
②物质的质量=物质中某元素的质量
示例3
已知
氧元素的质量
典例3 葡萄糖
(1)
[解析]
(2)
[解析]
(3)
[解析]
(4)葡萄糖中碳元素的质量分数___(选填“>”“<”或“=”)乳酸中碳元素的质量分数。
=
[解析] 葡萄糖分子与乳酸分子中,碳、氢、氧三种原子的个数比相等,故葡萄糖中
碳元素的质量分数=乳酸中碳元素的质量分数。
(5)
48
[解析]
例题点拨
根据、
题型1 相对原子质量的计算
典例4 [2022·杭州期中] 假设1个甲原子的实际质量为
质量为
A.
D
[解析] 甲原子的相对原子质量
方法点拨
相对原子质量的计算方法
1.公式法:相对原子质量
2.比值法:相对原子质量之比=原子实际质量之比。
3.微粒法:相对原子质量
题型2 元素质量分数和质量比的有关计算
角度1 根据模型或化学式进行计算
典例5 模型可以反映客观现象,简单明了地表示事物,根据下图回答问题。
读图指导
方法点拨
有关化学式的计算
(1)乙炔是一种简单的有机物,其分子结构模型如图甲所示,则乙炔中碳、氢两种
元素的质量比为______。
[解析] 由图甲知,乙炔的化学式为
(2)尿素
则图中的B表示的是____________元素。
氢(或
[解析] 由化学式
则图中B表示氢(H)元素。
(3)若乙炔分子和尿素分子的个数相同,则它们所含碳原子的个数比为_____。
[解析] 由化学式
个尿素分子含有1个碳原子,则相同数目的两种分子所含的碳原子的个数比为
角度2 巧用定值计算
典例6 已知
分数为( )
A.
B
[解析] 由混合物各组成成分的化学式可知,无论
与氧原子的个数比恒为
硫元素与氧元素的质量分数之和为
方法点拨
巧用定值计算混合物中某元素的质量分数
找出混合物中具有特定原子个数比的元素组合,根据混合物中已知的某元素的质量分数确定该组合在混合物中的质量分数,运用该特定元素组合中各元素的质量比,计算所求元素的质量分数。
角度3 结合实际生活进行计算
典例7 [2022·金华期末] 钙是维持人体正常功能所必需的元素,有时需要服用钙片来
满足人体需求,下图分别为两种补钙剂说明书的一部分。
葡萄糖酸钙片 【主要成分】葡萄糖酸钙 【含量】每片含葡萄糖酸钙
【主要成分】碳酸钙
氧化铜、维生素等
【含量】每片含钙
【用量】每日2次,一次1片
(1)葡萄糖酸钙
[答案]
[解析] 由
(2)碳酸钙
[答案]
[解析] 碳酸钙
(3)每片金钙尔奇中含有碳酸钙的质量为多少?
[答案]
[解析] 每片金钙尔奇中含有碳酸钙的质量为
(4)按照金钙尔奇说明书中每日的补钙量,若改服用葡萄糖酸钙片,一日3次,一次应服多少片?
[答案]
[解析] 每日的补钙量为
含量为
思路点拨
求解第(4)问需抓住“每次服用葡萄糖酸钙的片数×每日服用次数×每片葡萄糖酸钙的钙含量=每日补钙量”。
第2章 微粒的模型与符号
第7节 元素符号表示的量
学习目标
1.知道相对原子质量和相对分子质量的含义。
2.了解近似相对原子质量与质子数、中子数之间的关系。
3.能根据化学式计算物质的相对分子质量和化合物中各元素的质量比以及元素的质
量分数。
知识点1 相对原子质量 重点
1.相对原子质量
特别提醒
相对原子质量不是实际质量
相对原子质量是
相对原子质量只是一个比值,不是原子的实际质量,但能反映出原子实际质量的相
对大小,原子质量越大,相对原子质量越大,两者成正比。如氢的相对原子质量为1,
碳的相对原子质量为12,则一个碳原子的实际质量也是一个氢原子实际质量的12倍。
辨析比较
原子的质量 相对原子质量
性质 实验测出的一个 原子的实际质量 比较得出的相对质量
数值与单位 数值非常小,单 位为“
质量相同的不同原子构成的纯净物,相对原子质
量越小的物质所含的原子个数越多。如1克铁和1
克铝,由于铝的相对原子质量小于铁的相对原子
质量,所以1克铝中所含铝原子的个数比1克铁中
所含铁原子的个数多
联系 某原子的相对原子质量
微粒 质量
碳原子
质子
量是质子质量的
中子
核上,近似计算相对原子质量时,相对原子质量
拓展
一个碳
量
典例1 下列关于相对原子质量的说法正确的是( )
A.相对原子质量就是原子的实际质量
B.相对原子质量是原子质量与一种碳原子质量的比值
C.原子的实际质量越大,相对原子质量就越大
D.相对原子质量是一个比值,单位为“
C
[解析] 相对原子质量是一个原子的质量与一个碳
常省略不写,它不是原子的实际质量,但能反应出一个原子的实际质量的相对大小。
知识点2 相对分子质量 重点
1.相对分子质量
2.相对分子质量的计算
特别提醒
计算相对分子质量的注意事项
(1)元素符号与数字之间在计算相对分子质量时需用“×”号,元素符号之间在计算
相对分子质量时需用“+”号。
如
(2)化学式中原子团右下角的数字表示其个数,计算时可先求出一个原子团的相对
质量,再乘其个数。如
(3)结晶水合物中的“·”表示结合的含义,在计算相对分子质量时应将“·”前后两部
分的相对质量相加而不是相乘。如
拓展
空气的平均相对分子质量为29,可以通过比较某种气体的相对分子质量与29的大小
关系,判断该气体的密度与空气密度的大小关系。
若
若
典例2 [2022·杭州拱墅区期中] 甲烷是天然气的主要成分,可用作燃料,用“&1& ”表示
碳原子,“&2& ”表示氢原子,甲烷分子可表示为“&3& ”,则甲烷的化学式为
_____,每个甲烷分子由___个原子构成,甲烷分子中碳原子与氢原子的个数比是___,甲烷中碳元素的化合价为____,甲烷的相对分子质量为____。
5
1:4
-4
16
[解析] 由题意知,1个甲烷分子由1个碳原子和4个氢原子构成,则化学式为
所以每个甲烷分子中的原子个数为
甲烷中,氢元素的化合价为
合价的代数和为零得,
知识点3 元素质量分数和质量比的确定 重点
1.计算组成物质的各种元素的质量比
化合物中各元素的质量比等于化合物中各元素的相对原子质量与相应原子个数的乘
积之比。
示例1 水
特别提醒
计算化合物中元素的质量比的注意事项
(1)元素只讲种类,不讲个数。如在计算硝酸铵
不能写成
(2)不要把各元素的原子个数比误认为元素的质量比,如
2.计算化合物中某元素的质量分数
化合物中某元素的质量分数
示例2 硝酸铵
(2)有关化学式计算的其他公式
①物质中某元素的质量=物质的质量×物质中该元素的质量分数;
②物质的质量=物质中某元素的质量
示例3
已知
氧元素的质量
典例3 葡萄糖
(1)
[解析]
(2)
[解析]
(3)
[解析]
(4)葡萄糖中碳元素的质量分数___(选填“>”“<”或“=”)乳酸中碳元素的质量分数。
=
[解析] 葡萄糖分子与乳酸分子中,碳、氢、氧三种原子的个数比相等,故葡萄糖中
碳元素的质量分数=乳酸中碳元素的质量分数。
(5)
48
[解析]
例题点拨
根据
题型1 相对原子质量的计算
典例4 [2022·杭州期中] 假设1个甲原子的实际质量为
质量为
A.
D
[解析] 甲原子的相对原子质量
方法点拨
相对原子质量的计算方法
1.公式法:相对原子质量
2.比值法:相对原子质量之比=原子实际质量之比。
3.微粒法:相对原子质量
题型2 元素质量分数和质量比的有关计算
角度1 根据模型或化学式进行计算
典例5 模型可以反映客观现象,简单明了地表示事物,根据下图回答问题。
读图指导
方法点拨
有关化学式的计算
(1)乙炔是一种简单的有机物,其分子结构模型如图甲所示,则乙炔中碳、氢两种
元素的质量比为______。
[解析] 由图甲知,乙炔的化学式为
(2)尿素
则图中的B表示的是____________元素。
氢(或
[解析] 由化学式
则图中B表示氢(H)元素。
(3)若乙炔分子和尿素分子的个数相同,则它们所含碳原子的个数比为_____。
[解析] 由化学式
个尿素分子含有1个碳原子,则相同数目的两种分子所含的碳原子的个数比为
角度2 巧用定值计算
典例6 已知
分数为( )
A.
B
[解析] 由混合物各组成成分的化学式可知,无论
与氧原子的个数比恒为
硫元素与氧元素的质量分数之和为
方法点拨
巧用定值计算混合物中某元素的质量分数
找出混合物中具有特定原子个数比的元素组合,根据混合物中已知的某元素的质量分数确定该组合在混合物中的质量分数,运用该特定元素组合中各元素的质量比,计算所求元素的质量分数。
角度3 结合实际生活进行计算
典例7 [2022·金华期末] 钙是维持人体正常功能所必需的元素,有时需要服用钙片来
满足人体需求,下图分别为两种补钙剂说明书的一部分。
葡萄糖酸钙片 【主要成分】葡萄糖酸钙 【含量】每片含葡萄糖酸钙
【主要成分】碳酸钙
氧化铜、维生素等
【含量】每片含钙
【用量】每日2次,一次1片
(1)葡萄糖酸钙
[答案]
[解析] 由
(2)碳酸钙
[答案]
[解析] 碳酸钙
(3)每片金钙尔奇中含有碳酸钙的质量为多少?
[答案]
[解析] 每片金钙尔奇中含有碳酸钙的质量为
(4)按照金钙尔奇说明书中每日的补钙量,若改服用葡萄糖酸钙片,一日3次,一次应服多少片?
[答案]
[解析] 每日的补钙量为
含量为
思路点拨
求解第(4)问需抓住“每次服用葡萄糖酸钙的片数×每日服用次数×每片葡萄糖酸钙的钙含量=每日补钙量”。
同课章节目录
- 第1章 电与磁
- 第1节 指南针为什么能指方向
- 第2节 电生磁
- 第3节 电磁铁的应用
- 第4节 电动机
- 第5节 磁生电
- 第6节 家庭用电
- 第7节 电的安全使用
- 第2章 微粒的模型与符号
- 第1节 模型、符号的建立与作用
- 第2节 物质的微观粒子模型
- 第3节 原子结构的模型
- 第4节 组成物质的元素
- 第5节 表示元素的符号
- 第6节 表示物质的符号
- 第7节 元素符号表示的量
- 第3章 空气与生命
- 第1节 空气与氧气
- 第2节 氧化和燃烧
- 第3节 化学方程式
- 第4节 二氧化碳
- 第5节 生物的呼吸和呼吸作用
- 第6节 光合作用
- 第7节 自然界中的氧循环和碳循环
- 第8节 空气污染与保护
- 第4章 植物与土壤
- 第1节 土壤的成分
- 第2节 各种各样的土壤
- 第3节 植物的根与物质吸收
- 第4节 植物的茎与物质运输
- 第5节 植物的叶与蒸腾作用
- 第6节 保护土壤
- 研究性学习课题
- 一 设计简单的电磁控制电路
- 二 化学反应中质量守恒的研究
- 三 研究植物的呼吸
- 四 当地水土状况调查
