6.3 物质的溶解性 同步练习(含答案) 2022-2023学年沪教版(全国)九年级下册化学
文档属性
| 名称 | 6.3 物质的溶解性 同步练习(含答案) 2022-2023学年沪教版(全国)九年级下册化学 |

|
|
| 格式 | zip | ||
| 文件大小 | 100.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-03-03 00:00:00 | ||
图片预览




文档简介
6.3 物质的溶解性 同步练习
一、单选题
1.KNO3和KCl两种固体的溶解度曲线如图所示。下列说法错误的是( )
A.在t℃时,KNO3和KCl的溶解度相等
B.常温下(20℃),KNO3和KCl都是易溶物质
C.60℃时50gKNO3溶于50g水中恰好形成100gKNO3饱和溶液
D.分离混有少量氯化钾的硝酸钾时可采用冷却热饱和溶液的方法
2.甲、乙两种物质的溶解度曲线如图所示。下列说法不正确的是( )
A.在t1℃、t3℃时甲、乙两物质的溶解度相等
B.在t1℃至t3℃之间,乙的溶解度大于甲的溶解度
C.将甲、乙的饱和溶液从t3℃降到t1℃,析出甲、乙的质量相等
D.将t2℃时接近饱和的乙溶液变为饱和溶液可采取升温或降温的方法
3.下表是氯化铵在不同温度时的溶解度
温度/℃ 20 40 60 80
溶解度/g 40 50 58 68
据此数据,判断下列说法正确的是( )
A.20℃时,氯化铵饱和溶液中氯化铵的质量分数是25%
B.20℃时,70g氯化铵的饱和溶液升温至40℃得到不饱和溶液
C.40℃时,75g氯化铵的饱和溶液中加入25g水后氯化铵的质量分数为30%
D.80℃时,84g的氯化铵饱和溶液降温至60℃时有10g氯化铵析出
4.已知:20℃时,NaCl和NaNO3的溶解度分别为36 g和88 g。
序号 ① ② ③ ④ ⑤
固体种类 NaCl NaCl NaNO3 NaNO3 NaNO3
固体的质量/g 30 60 30 60 90
水的质量/g 100 100 100 100 100
上表是20℃时实验得出的数据,根据该数据,则下列关于①~⑤所得溶液的说法错误的是()
A.溶质质量:②=④
B.溶液质量: ①<②
C.溶质质量
5.甲、乙两种固体的溶解度曲线如图所示,下列说法正确的是( )
A.甲的溶解度大于乙的溶解度
B.t1°时,配制等质量甲、乙的饱和溶液,乙需要的水多
C.t2°时,乙的饱和溶液中溶质和溶剂的质量比为1∶1
D.t3°时,将90g甲的饱和溶液与110g水混合,所得溶液的溶质质量分数为20%
6.下列有关溶液的叙述中正确的是
A.任何溶液都具有导电性
B.溶液中的溶质可以是一种或多种
C.升高温度均能使饱和溶液变为不饱和溶液
D.析出晶体后的溶液一定是稀溶液
7.下列关于溶液的说法正确的是( )
A.溶液可以是固体,也可以是液体或气体
B.饱和溶液一定比不饱和溶液所含溶质多
C.长期放置不会分层的液体一定是溶液
D.溶液中只有一种溶质的溶液为纯净物
8.下图是KNO3和NaCl 的溶解度曲线。下列说法中正确的是
A.NaCl 的溶解度不受温度的影响
B.t1℃时,100g KNO3饱和溶液中含有20g KNO3
C.t2℃时,KNO3的饱和溶液和NaCl 的饱和溶液中溶质的质量分数不一定相等
D.温度高于t2℃时,KNO3的溶解度大于NaCl 的溶解度
9.据《说文解字》记载,我们的祖先在神农氏时代就开始利用海水晒盐.下列关于海水晒盐原理的说法正确的是( )
A.日晒风吹使海水中的氯化钠蒸发
B.日晒风吹使溶液由饱和变为不饱和
C.日晒风吹使水分蒸发、晶体析出
D.日晒风吹使氯化钠的溶解度变小
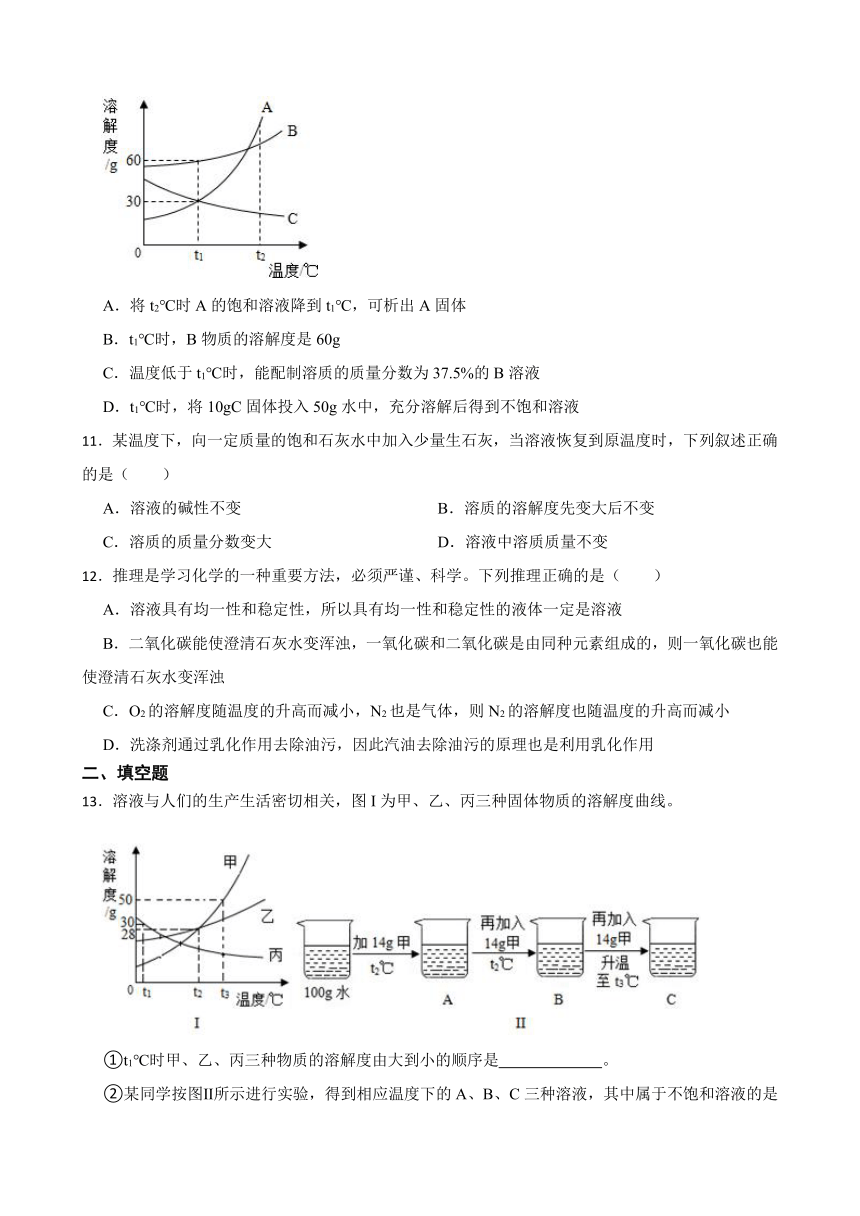
10.如图是A、B、C三种固体物质的溶解度曲线,下列叙述错误的是( )
A.将t2℃时A的饱和溶液降到t1℃,可析出A固体
B.t1℃时,B物质的溶解度是60g
C.温度低于t1℃时,能配制溶质的质量分数为37.5%的B溶液
D.t1℃时,将10gC固体投入50g水中,充分溶解后得到不饱和溶液
11.某温度下,向一定质量的饱和石灰水中加入少量生石灰,当溶液恢复到原温度时,下列叙述正确的是( )
A.溶液的碱性不变 B.溶质的溶解度先变大后不变
C.溶质的质量分数变大 D.溶液中溶质质量不变
12.推理是学习化学的一种重要方法,必须严谨、科学。下列推理正确的是( )
A.溶液具有均一性和稳定性,所以具有均一性和稳定性的液体一定是溶液
B.二氧化碳能使澄清石灰水变浑浊,一氧化碳和二氧化碳是由同种元素组成的,则一氧化碳也能使澄清石灰水变浑浊
C.O2的溶解度随温度的升高而减小,N2也是气体,则N2的溶解度也随温度的升高而减小
D.洗涤剂通过乳化作用去除油污,因此汽油去除油污的原理也是利用乳化作用
二、填空题
13.溶液与人们的生产生活密切相关,图I为甲、乙、丙三种固体物质的溶解度曲线。
①t1℃时甲、乙、丙三种物质的溶解度由大到小的顺序是 。
②某同学按图Ⅱ所示进行实验,得到相应温度下的A、B、C三种溶液,其中属于不饱和溶液的是 ( 填字母 ) 。
③t1℃时向盛有20g丙物质的烧杯中加入50g水充分溶解后,所得溶液溶质的质量分数为 。 ( 结果保留整数)
④将t3℃时三种物质的饱和溶液分别降温至t2℃,三种溶液的溶质质量分数由大到小的顺序是 。
14.许多气体、固体均能溶于水,下表为氯化钠、碳酸钠的溶解度数据:
温度(℃) 0 10 20 30 40
溶解 (g/100g水) 氯化钠 35.7 35.8 36 36.3 36.6
碳酸钠 7 12.5 22 40 48.8
①0℃~40℃,随温度升高碳酸钠的溶解度 (选填“变大” “变小”);20℃时碳酸钠溶解度为 g/100
g水。
②20℃时,取3.6
g氯化钠投入20g水中,充分搅拌后,形成的溶液质量分数为 (列式即可,无需计算);温度不变,若要将该溶液恰好变为饱和溶液,可以蒸发 g水,还可以采取的方法是 。
③23℃,一个标准大气压下,二氧化碳的溶解度为“0.8 L/1 L水”,该数值含义是 。若利用针筒(100
mL)测量15℃,一个标准大气压下的二氧化碳的溶解度,先在针简内吸入20
mL水,再吸入“16 mL”或“40
mL”的二氧化碳充分振荡,实验中你认为气体体积最好是 ,理由是 。
15.如图是a、b、c三种物质的溶解度曲线。
(1)b溶液在点P时处于 (填“饱和”或“不饱和”)状态。
(2)不改变溶液的溶质质量分数,可使C的不饱和溶液变成饱和溶液的方法是 。
(3)除去a固体中混有的少量b,提纯的步骤是:加水溶解、蒸发浓缩、 ,然后过滤、洗涤、干燥。
(4)t2℃时,将a、b、c三种物质的饱和溶液降温至t1℃,下列说法正确的是____。
A.溶质质量分数:b>a>c
B.析出固体的质量a>b,c无固体析出
C.溶剂的质量:aD.a、b是饱和溶液,c是不饱和溶液
16.将 60 g 某固体物质放入盛有 50 g 水的烧杯中充分溶解,测得溶液质量随温度变化的曲线如图。则 t1 ℃时该物质的溶解度为 g;A、B、C 三点所对应的溶液中,一定属于饱和溶液的是 点处的溶液;将 t3 ℃时的 110 g 溶液稀释成20%,需加水的质量为 g。
17.如图是A、B两种物质的溶解度曲线
(1)当温度低于t℃时,溶解度A B(填“>”,“<”或“=”.下同)
(2)t℃,将A,B两物质的饱和溶液均加热到40℃,两种溶液中溶质的质量分数A B(注:水分不蒸发)
18.甲、乙、丙三种固体物质的溶解度曲线如下图所示,请根据图示同答下列问题。
(1)丙物质的溶解度随温度的升高而 。(填“增大”或“减小”)。
(2)t1℃时,将甲物质的饱和溶液升温到t3℃,所得溶液中溶质的质量分数 。(填“变大”、“变小”或“不变”)。
(3)t2℃时,将100g水加入到盛有30g甲物质的烧杯中,充分溶解后得到不饱和溶液,若想使溶液恰好饱和,可采用的方法是: 。
(4)t3℃时,甲、乙、丙三种物质的溶解度的由大到小的顺序是 。
三、综合题
19.如图是X、Y、Z三种物质的溶解度曲线图,请仔细阅读,回答下列问题:
(1)P点表示的意义是 。
(2)t1℃时,三种物质的溶解度从大到小的顺序是 。
(3)t2℃时,将20gZ装入放有50g水的烧杯中,充分搅拌可得到 gZ的饱和溶液,其溶质质量分数是 (精确到0.1%)。
(4)将t3℃时的X、Y、Z三物质饱和溶液同时降温至t1℃后,所得溶液溶质质量分数从大到小的顺序是 。
(5)当Y中混有少量的X物质时,可用的 方法提纯Y(填蒸发结晶或降温结晶)。
20.请根据图中A,B,C三种物质的溶解度曲线,回答下列问题:
(1)温度越高,溶解度越小的物质是(填写代号) ;
(2)现有A,B,C三种物质的浓溶液,适用海水晒盐原理进行结晶提纯的是(填写代号) ;
(3)当溶液的浓度都用溶质的质量分数(m)表示时,下列说法中不正确的是 .
①t1℃时,A,C两种物质的溶解度相等,两种溶液的浓度也相等
②t1℃时,A,B,C三种溶液的浓度可能相等
③将t2℃的A,B,C三种饱和溶液的温度分别降至t1℃时,A溶液中析出的晶体最多
④将t2℃的A,B,C三种饱和溶液的温度分别降至t1℃时,所得溶液浓度的大小顺序为m(B)>m(A)=m(C)
⑤将t1℃的A,B,C三种溶液分别升温,其浓度都不可能发生变化
⑥将t2℃的A,B,C三种溶液分别降温,其浓度都可能发生变化.
21.溶液对于自然界中的生命活动和人类生产活动具有重要意义,如图是甲、乙、丙三种固体物质的溶解度曲线(固体均不含结晶水)。
(1)t1℃时,三种固体物质的溶解度大小关系是 。
(2)甲中混有少量乙,可采用 的方法提纯甲。
(3)t2℃时,将35克甲物质加入到盛有50克水的烧杯中,充分溶解再降温到t1℃,析出的固体质量为 。
(4)t2℃时,将等质量的三种固体物质加水配制成该温度下的饱和溶液,再降温至t1℃。下列说法正确的是____。
A.t1℃时,甲、乙形成的溶液为饱和溶液,丙为不饱和溶液
B.t1℃时,甲和丙形成的溶液溶质质量分数相等
C.t1℃时,三种溶液的质量关系是乙>甲=丙
22.在一定温度下,将30g、40g、50g、60g、70g的硝酸钾固体分别加入到50g水中,其五次实验数据记录如下表:(KNO3的溶解度随温度升高而增大)
实验次数 1 2 3 4 5
加入KNO3的质量(g) 30 40 50 60 70
所得KNO3溶液的质量(g) 80 90 100 105
根据表中数据分析回答下列问题:
(1)第 次起得到的KNO3溶液为饱和溶液。
(2)该温度下,KNO3的溶解度为 g。
(3)请你推测第5次实验所得溶液质量是 g。
(4)要使接近饱和的KNO3溶液,在不改变溶液质量的前提下变为饱和溶液可以采用的方法是 。
答案解析部分
1.【答案】C
2.【答案】C
3.【答案】B
4.【答案】A
5.【答案】D
6.【答案】B
7.【答案】A
8.【答案】D
9.【答案】C
10.【答案】C
11.【答案】A
12.【答案】C
13.【答案】丙>乙>甲;AC;23%;甲=乙>丙
14.【答案】变大;22;;10;加入溶质氯化钠3.6 g;23℃,1个标准大气压下,1 L水中溶解0.8LCO2时刚好达到饱和;40mL;相同压强下,温度越低,气体溶解度越大,15摄氏度时,20 mL水中溶解二氧化碳量大于16 mL
15.【答案】(1)不饱和
(2)升高温度
(3)降温结晶
(4)A;D
16.【答案】40;A;190
17.【答案】(1)<
(2)=
18.【答案】(1)减小
(2)不变
(3)加入甲物质30g或蒸发50g水或降低温度
(4)甲>乙>丙
19.【答案】(1)t2℃时,Y和Z的溶解度相等,均为30g
(2)Z>Y>X
(3)65;23.1%
(4)Y>Z>X
(5)蒸发结晶
20.【答案】(1)C
(2)B
(3)①③④⑤
21.【答案】(1)乙>丙>甲
(2)降温结晶
(3)20g
(4)A;B
22.【答案】(1)4
(2)110
(3)105
(4)降温
一、单选题
1.KNO3和KCl两种固体的溶解度曲线如图所示。下列说法错误的是( )
A.在t℃时,KNO3和KCl的溶解度相等
B.常温下(20℃),KNO3和KCl都是易溶物质
C.60℃时50gKNO3溶于50g水中恰好形成100gKNO3饱和溶液
D.分离混有少量氯化钾的硝酸钾时可采用冷却热饱和溶液的方法
2.甲、乙两种物质的溶解度曲线如图所示。下列说法不正确的是( )
A.在t1℃、t3℃时甲、乙两物质的溶解度相等
B.在t1℃至t3℃之间,乙的溶解度大于甲的溶解度
C.将甲、乙的饱和溶液从t3℃降到t1℃,析出甲、乙的质量相等
D.将t2℃时接近饱和的乙溶液变为饱和溶液可采取升温或降温的方法
3.下表是氯化铵在不同温度时的溶解度
温度/℃ 20 40 60 80
溶解度/g 40 50 58 68
据此数据,判断下列说法正确的是( )
A.20℃时,氯化铵饱和溶液中氯化铵的质量分数是25%
B.20℃时,70g氯化铵的饱和溶液升温至40℃得到不饱和溶液
C.40℃时,75g氯化铵的饱和溶液中加入25g水后氯化铵的质量分数为30%
D.80℃时,84g的氯化铵饱和溶液降温至60℃时有10g氯化铵析出
4.已知:20℃时,NaCl和NaNO3的溶解度分别为36 g和88 g。
序号 ① ② ③ ④ ⑤
固体种类 NaCl NaCl NaNO3 NaNO3 NaNO3
固体的质量/g 30 60 30 60 90
水的质量/g 100 100 100 100 100
上表是20℃时实验得出的数据,根据该数据,则下列关于①~⑤所得溶液的说法错误的是()
A.溶质质量:②=④
B.溶液质量: ①<②
C.溶质质量
5.甲、乙两种固体的溶解度曲线如图所示,下列说法正确的是( )
A.甲的溶解度大于乙的溶解度
B.t1°时,配制等质量甲、乙的饱和溶液,乙需要的水多
C.t2°时,乙的饱和溶液中溶质和溶剂的质量比为1∶1
D.t3°时,将90g甲的饱和溶液与110g水混合,所得溶液的溶质质量分数为20%
6.下列有关溶液的叙述中正确的是
A.任何溶液都具有导电性
B.溶液中的溶质可以是一种或多种
C.升高温度均能使饱和溶液变为不饱和溶液
D.析出晶体后的溶液一定是稀溶液
7.下列关于溶液的说法正确的是( )
A.溶液可以是固体,也可以是液体或气体
B.饱和溶液一定比不饱和溶液所含溶质多
C.长期放置不会分层的液体一定是溶液
D.溶液中只有一种溶质的溶液为纯净物
8.下图是KNO3和NaCl 的溶解度曲线。下列说法中正确的是
A.NaCl 的溶解度不受温度的影响
B.t1℃时,100g KNO3饱和溶液中含有20g KNO3
C.t2℃时,KNO3的饱和溶液和NaCl 的饱和溶液中溶质的质量分数不一定相等
D.温度高于t2℃时,KNO3的溶解度大于NaCl 的溶解度
9.据《说文解字》记载,我们的祖先在神农氏时代就开始利用海水晒盐.下列关于海水晒盐原理的说法正确的是( )
A.日晒风吹使海水中的氯化钠蒸发
B.日晒风吹使溶液由饱和变为不饱和
C.日晒风吹使水分蒸发、晶体析出
D.日晒风吹使氯化钠的溶解度变小
10.如图是A、B、C三种固体物质的溶解度曲线,下列叙述错误的是( )
A.将t2℃时A的饱和溶液降到t1℃,可析出A固体
B.t1℃时,B物质的溶解度是60g
C.温度低于t1℃时,能配制溶质的质量分数为37.5%的B溶液
D.t1℃时,将10gC固体投入50g水中,充分溶解后得到不饱和溶液
11.某温度下,向一定质量的饱和石灰水中加入少量生石灰,当溶液恢复到原温度时,下列叙述正确的是( )
A.溶液的碱性不变 B.溶质的溶解度先变大后不变
C.溶质的质量分数变大 D.溶液中溶质质量不变
12.推理是学习化学的一种重要方法,必须严谨、科学。下列推理正确的是( )
A.溶液具有均一性和稳定性,所以具有均一性和稳定性的液体一定是溶液
B.二氧化碳能使澄清石灰水变浑浊,一氧化碳和二氧化碳是由同种元素组成的,则一氧化碳也能使澄清石灰水变浑浊
C.O2的溶解度随温度的升高而减小,N2也是气体,则N2的溶解度也随温度的升高而减小
D.洗涤剂通过乳化作用去除油污,因此汽油去除油污的原理也是利用乳化作用
二、填空题
13.溶液与人们的生产生活密切相关,图I为甲、乙、丙三种固体物质的溶解度曲线。
①t1℃时甲、乙、丙三种物质的溶解度由大到小的顺序是 。
②某同学按图Ⅱ所示进行实验,得到相应温度下的A、B、C三种溶液,其中属于不饱和溶液的是 ( 填字母 ) 。
③t1℃时向盛有20g丙物质的烧杯中加入50g水充分溶解后,所得溶液溶质的质量分数为 。 ( 结果保留整数)
④将t3℃时三种物质的饱和溶液分别降温至t2℃,三种溶液的溶质质量分数由大到小的顺序是 。
14.许多气体、固体均能溶于水,下表为氯化钠、碳酸钠的溶解度数据:
温度(℃) 0 10 20 30 40
溶解 (g/100g水) 氯化钠 35.7 35.8 36 36.3 36.6
碳酸钠 7 12.5 22 40 48.8
①0℃~40℃,随温度升高碳酸钠的溶解度 (选填“变大” “变小”);20℃时碳酸钠溶解度为 g/100
g水。
②20℃时,取3.6
g氯化钠投入20g水中,充分搅拌后,形成的溶液质量分数为 (列式即可,无需计算);温度不变,若要将该溶液恰好变为饱和溶液,可以蒸发 g水,还可以采取的方法是 。
③23℃,一个标准大气压下,二氧化碳的溶解度为“0.8 L/1 L水”,该数值含义是 。若利用针筒(100
mL)测量15℃,一个标准大气压下的二氧化碳的溶解度,先在针简内吸入20
mL水,再吸入“16 mL”或“40
mL”的二氧化碳充分振荡,实验中你认为气体体积最好是 ,理由是 。
15.如图是a、b、c三种物质的溶解度曲线。
(1)b溶液在点P时处于 (填“饱和”或“不饱和”)状态。
(2)不改变溶液的溶质质量分数,可使C的不饱和溶液变成饱和溶液的方法是 。
(3)除去a固体中混有的少量b,提纯的步骤是:加水溶解、蒸发浓缩、 ,然后过滤、洗涤、干燥。
(4)t2℃时,将a、b、c三种物质的饱和溶液降温至t1℃,下列说法正确的是____。
A.溶质质量分数:b>a>c
B.析出固体的质量a>b,c无固体析出
C.溶剂的质量:a
16.将 60 g 某固体物质放入盛有 50 g 水的烧杯中充分溶解,测得溶液质量随温度变化的曲线如图。则 t1 ℃时该物质的溶解度为 g;A、B、C 三点所对应的溶液中,一定属于饱和溶液的是 点处的溶液;将 t3 ℃时的 110 g 溶液稀释成20%,需加水的质量为 g。
17.如图是A、B两种物质的溶解度曲线
(1)当温度低于t℃时,溶解度A B(填“>”,“<”或“=”.下同)
(2)t℃,将A,B两物质的饱和溶液均加热到40℃,两种溶液中溶质的质量分数A B(注:水分不蒸发)
18.甲、乙、丙三种固体物质的溶解度曲线如下图所示,请根据图示同答下列问题。
(1)丙物质的溶解度随温度的升高而 。(填“增大”或“减小”)。
(2)t1℃时,将甲物质的饱和溶液升温到t3℃,所得溶液中溶质的质量分数 。(填“变大”、“变小”或“不变”)。
(3)t2℃时,将100g水加入到盛有30g甲物质的烧杯中,充分溶解后得到不饱和溶液,若想使溶液恰好饱和,可采用的方法是: 。
(4)t3℃时,甲、乙、丙三种物质的溶解度的由大到小的顺序是 。
三、综合题
19.如图是X、Y、Z三种物质的溶解度曲线图,请仔细阅读,回答下列问题:
(1)P点表示的意义是 。
(2)t1℃时,三种物质的溶解度从大到小的顺序是 。
(3)t2℃时,将20gZ装入放有50g水的烧杯中,充分搅拌可得到 gZ的饱和溶液,其溶质质量分数是 (精确到0.1%)。
(4)将t3℃时的X、Y、Z三物质饱和溶液同时降温至t1℃后,所得溶液溶质质量分数从大到小的顺序是 。
(5)当Y中混有少量的X物质时,可用的 方法提纯Y(填蒸发结晶或降温结晶)。
20.请根据图中A,B,C三种物质的溶解度曲线,回答下列问题:
(1)温度越高,溶解度越小的物质是(填写代号) ;
(2)现有A,B,C三种物质的浓溶液,适用海水晒盐原理进行结晶提纯的是(填写代号) ;
(3)当溶液的浓度都用溶质的质量分数(m)表示时,下列说法中不正确的是 .
①t1℃时,A,C两种物质的溶解度相等,两种溶液的浓度也相等
②t1℃时,A,B,C三种溶液的浓度可能相等
③将t2℃的A,B,C三种饱和溶液的温度分别降至t1℃时,A溶液中析出的晶体最多
④将t2℃的A,B,C三种饱和溶液的温度分别降至t1℃时,所得溶液浓度的大小顺序为m(B)>m(A)=m(C)
⑤将t1℃的A,B,C三种溶液分别升温,其浓度都不可能发生变化
⑥将t2℃的A,B,C三种溶液分别降温,其浓度都可能发生变化.
21.溶液对于自然界中的生命活动和人类生产活动具有重要意义,如图是甲、乙、丙三种固体物质的溶解度曲线(固体均不含结晶水)。
(1)t1℃时,三种固体物质的溶解度大小关系是 。
(2)甲中混有少量乙,可采用 的方法提纯甲。
(3)t2℃时,将35克甲物质加入到盛有50克水的烧杯中,充分溶解再降温到t1℃,析出的固体质量为 。
(4)t2℃时,将等质量的三种固体物质加水配制成该温度下的饱和溶液,再降温至t1℃。下列说法正确的是____。
A.t1℃时,甲、乙形成的溶液为饱和溶液,丙为不饱和溶液
B.t1℃时,甲和丙形成的溶液溶质质量分数相等
C.t1℃时,三种溶液的质量关系是乙>甲=丙
22.在一定温度下,将30g、40g、50g、60g、70g的硝酸钾固体分别加入到50g水中,其五次实验数据记录如下表:(KNO3的溶解度随温度升高而增大)
实验次数 1 2 3 4 5
加入KNO3的质量(g) 30 40 50 60 70
所得KNO3溶液的质量(g) 80 90 100 105
根据表中数据分析回答下列问题:
(1)第 次起得到的KNO3溶液为饱和溶液。
(2)该温度下,KNO3的溶解度为 g。
(3)请你推测第5次实验所得溶液质量是 g。
(4)要使接近饱和的KNO3溶液,在不改变溶液质量的前提下变为饱和溶液可以采用的方法是 。
答案解析部分
1.【答案】C
2.【答案】C
3.【答案】B
4.【答案】A
5.【答案】D
6.【答案】B
7.【答案】A
8.【答案】D
9.【答案】C
10.【答案】C
11.【答案】A
12.【答案】C
13.【答案】丙>乙>甲;AC;23%;甲=乙>丙
14.【答案】变大;22;;10;加入溶质氯化钠3.6 g;23℃,1个标准大气压下,1 L水中溶解0.8LCO2时刚好达到饱和;40mL;相同压强下,温度越低,气体溶解度越大,15摄氏度时,20 mL水中溶解二氧化碳量大于16 mL
15.【答案】(1)不饱和
(2)升高温度
(3)降温结晶
(4)A;D
16.【答案】40;A;190
17.【答案】(1)<
(2)=
18.【答案】(1)减小
(2)不变
(3)加入甲物质30g或蒸发50g水或降低温度
(4)甲>乙>丙
19.【答案】(1)t2℃时,Y和Z的溶解度相等,均为30g
(2)Z>Y>X
(3)65;23.1%
(4)Y>Z>X
(5)蒸发结晶
20.【答案】(1)C
(2)B
(3)①③④⑤
21.【答案】(1)乙>丙>甲
(2)降温结晶
(3)20g
(4)A;B
22.【答案】(1)4
(2)110
(3)105
(4)降温
