6.2 溶液组成的表示 同步练习(含答案) 2022-2023学年沪教版(全国)九年级下册化学
文档属性
| 名称 | 6.2 溶液组成的表示 同步练习(含答案) 2022-2023学年沪教版(全国)九年级下册化学 |
|
|
| 格式 | zip | ||
| 文件大小 | 48.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-03-08 00:00:00 | ||
图片预览



文档简介
6.2 溶液组成的表示 同步练习
一、单选题
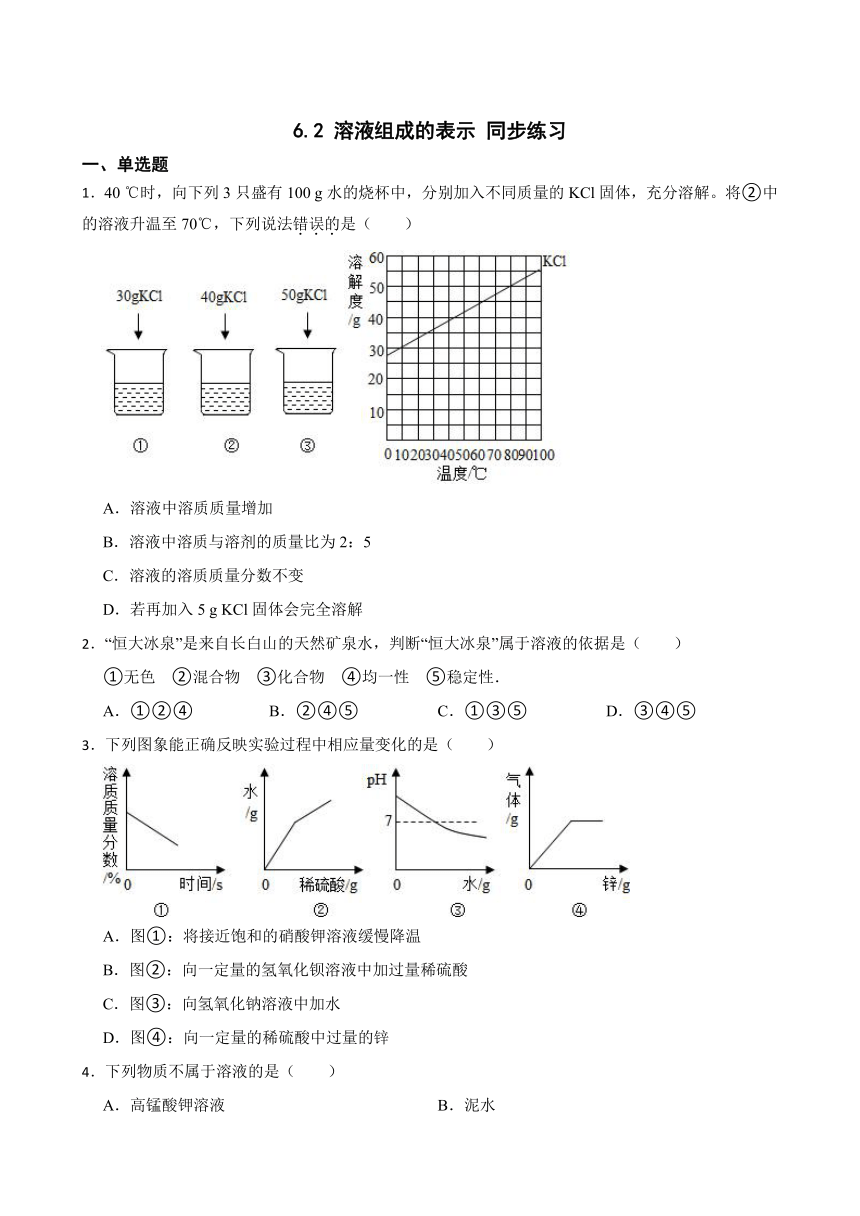
1.40 ℃时,向下列3只盛有100 g水的烧杯中,分别加入不同质量的KCl固体,充分溶解。将②中的溶液升温至70℃,下列说法错误的是( )
A.溶液中溶质质量增加
B.溶液中溶质与溶剂的质量比为2:5
C.溶液的溶质质量分数不变
D.若再加入5 g KCl固体会完全溶解
2.“恒大冰泉”是来自长白山的天然矿泉水,判断“恒大冰泉”属于溶液的依据是( )
①无色 ②混合物 ③化合物 ④均一性 ⑤稳定性.
A.①②④ B.②④⑤ C.①③⑤ D.③④⑤
3.下列图象能正确反映实验过程中相应量变化的是( )
A.图①:将接近饱和的硝酸钾溶液缓慢降温
B.图②:向一定量的氢氧化钡溶液中加过量稀硫酸
C.图③:向氢氧化钠溶液中加水
D.图④:向一定量的稀硫酸中过量的锌
4.下列物质不属于溶液的是( )
A.高锰酸钾溶液 B.泥水
C.医用酒精 D.食盐水
5.下列关于溶液的说法正确的是( )
A.溶液中溶质只能有一种,溶剂可以有多种
B.溶液中的溶质只能是固体物质
C.凡是无色透明的液体都是溶液
D.溶液的质量为溶质和溶剂质量之和
6.下列物质中,属于溶液的是( )
A.蔗糖水 B.鲜牛奶 C.果粒橙 D.芝麻糊
7.下列有关获取物质的说法正确的是( )
A.从海中获取了蒸馏水,发生了化学变化
B.海水制镁时,直接电解海水得到金属镁
C.侯氏制碱中所需的钠、碳、氧元素
D.获取物质时,先考虑化学方法,再考虑物理方法
8.电解水时常在水中加少量的硫酸以增加水的导电性。若用含水92%的稀硫酸25g,通电进行电解,一段时间后稀硫酸中含水为90%,则发生电解的水的质量为()
A.2g B.4g C.5g D.2.5g
9.下列物质分别加入适量水中,充分搅拌,能够得到溶液的是( )
A.牛奶 B.苏打 C.花生油 D.面粉
10.放入水中不能形成溶液的物质是( )
A.白酒 B.食盐 C.白糖 D.植物油
11.将下列各组物质混合,不能形成溶液的是( )
A.蔗糖+水 B.二氧化碳+水
C.植物油+水 D.碘+汽油
12.欲用KNO3和水配制100kg溶质质量分数为7.1%的KNO3溶液作无土栽培的营养液,需水的质量为( )
A.7.1kg B.92.9kg
C.71kg D.14.2kg
二、填空题
13.为了增强水的导电性,现采用4%的硫酸溶液135g进行电解水实验,一段时间后,测得硫酸溶液中溶质的质量分数为5%,计算电解水的质量是 。
14.用4g酚酞与酒精配制溶质质量分数为4%的酚酞溶液,需要酒精的质量是 g,这些酒精的体积为 mL(酒精的密度为0.8g/mL)。
15.通电分解水时,常在水中加少量的氢氧化钠或硫酸,目的是: ,小明同学用150克溶质质量分数8%的稀氢氧化钠溶液通电一段时间后发现溶质质量分数变为12%,则被分解的水的质量是 .
16.如图是“×××钙片商品标签图”
×××儿童咀嚼片 (60片装)
[主要成分]碳酸钙,维生素D [规格]2.5g/片,每片中含碳酸钙≥1.24g,维生素D 100l.U. [食用方法]嚼食,每天一片 [功效]补钙
根据标签内容信息,计算回答下列问题:(结果精确到0.1)
(1)主要成分碳酸钙中钙元素的质量分数为 ,每片中至少含钙元素的质量为 g.
(2)小红同学为测定其碳酸钙的含量标注是否属实,她取出4片钙片,研碎后放入烧杯中,逐滴加入稀盐酸,至不再放出气体为止,共用去稀盐酸40.0g.称量烧杯中剩余物为47.8g(不含烧杯质量,假定钙片其他成分不与稀盐酸反应).
试计算:①生成二氧化碳的质量 ;
②稀盐酸中溶质的质量分数 ;
③通过计算判断钙片中碳酸钙的含量标注是否属实 .
17.若把溶质质量分数为49%的H2SO4溶液100g稀释为20%的H2SO4溶液,需要水的质量为 .
18.如图所示为a、b、c三种物质的溶解度曲线。
(1)t1℃时,将30ga物质加入到50g水中,而后升温到t2℃,此时该溶液的溶质和溶剂的质量比为 。
(2)t1℃时,24ga的饱和溶液稀释为10%,需要加入水 g。
(3)将t2℃时等质量的a、c的饱和溶液降温至t1℃此时两种溶液中溶质的质量分数大小关系为 。
三、综合题
19.某同学用锌和稀硫酸制取氢气.向气体发生装置中加入一定量锌粒,将30g稀硫酸分三次加入,每次生产气体的质量如下表.
次数 第一次 第二次 第三次
加入稀硫酸质量/g 10 10 10
生成氢气质量/g 0.04 0.04 0.02
(1)共制得氢气 g.
(2)所用稀硫酸的溶质质量分数.
20.实验室用100g含杂质10%的石灰石与948.6g一定质量分数的稀盐酸恰好完全反应.石灰石中杂质不溶于水也不与稀盐酸反应.求:
(1)产生二氧化碳的质量.
(2)反应后所得溶液的溶质的质量分数.
21.实验室用大理石制取二氧化碳,同学们进行了如下实验,过程如图所示(杂质不溶于水也不与盐酸反应):求:
(1)反应中生成二氧化碳的质量为 .
(2)所用稀盐酸的溶质的质量分数是多少?
22.请你各举出一个实例,说明下列有关溶液的叙述是错误的。
(1)溶液一定是无色的。实例: 溶液不是无色的。
(2)均一、稳定的液体都是溶液。实例: 是液体,但不是溶液。
(3)溶液中的溶质一定是固体。实例: 可做溶质,但不是固体。
(4)升高温度,物质的溶解度一定增大。实例: 升高温度,溶解度减小。
答案解析部分
1.【答案】A
2.【答案】B
3.【答案】D
4.【答案】B
5.【答案】D
6.【答案】A
7.【答案】C
8.【答案】C
9.【答案】B
10.【答案】D
11.【答案】C
12.【答案】B
13.【答案】27g
14.【答案】96;120
15.【答案】增强导电性;50g
16.【答案】40%;0.5;2.2g;9.1%;属实
17.【答案】145g
18.【答案】(1)1:2
(2)16
(3)a>c
19.【答案】(1)0.1
(2)解:设10g硫酸中含有溶质的质量为x
Zn+ H2SO4=ZnSO4+ H2↑
98 2
x 0.04g
x=1.96g
答:故硫酸的质量分数为: =19.6%.
20.【答案】(1)解:设生成氯化钙质量为x,生成二氧化碳质量为y,
CaCO3+ 2HCl ═ CaCl2 +H2O+ CO2↑
100 111 44
100g×(1﹣10%) x y
= = ,
x=99.9g,y=39.6g,
答:生成了39.6g二氧化碳.
(2)解:反应后所得溶液的溶质的质量分数为: ×100%=10%,
答:反应后所得溶液的溶质的质量分数为10%.
21.【答案】(1)4.4g
(2)解:设参加反应的HCl的质量为x
CaCO3+ 2HCl = CaCl2+ H2O+ CO2↑
73 44
x 4.4g
x=7.3g
所用稀盐酸的溶质的质量分数为 ×100%=14.6%
22.【答案】(1)硫酸铜(或填氯化铁等)
(2)水
(3)氯化氢气体(或硫酸等)
(4)氢氧化钙或
一、单选题
1.40 ℃时,向下列3只盛有100 g水的烧杯中,分别加入不同质量的KCl固体,充分溶解。将②中的溶液升温至70℃,下列说法错误的是( )
A.溶液中溶质质量增加
B.溶液中溶质与溶剂的质量比为2:5
C.溶液的溶质质量分数不变
D.若再加入5 g KCl固体会完全溶解
2.“恒大冰泉”是来自长白山的天然矿泉水,判断“恒大冰泉”属于溶液的依据是( )
①无色 ②混合物 ③化合物 ④均一性 ⑤稳定性.
A.①②④ B.②④⑤ C.①③⑤ D.③④⑤
3.下列图象能正确反映实验过程中相应量变化的是( )
A.图①:将接近饱和的硝酸钾溶液缓慢降温
B.图②:向一定量的氢氧化钡溶液中加过量稀硫酸
C.图③:向氢氧化钠溶液中加水
D.图④:向一定量的稀硫酸中过量的锌
4.下列物质不属于溶液的是( )
A.高锰酸钾溶液 B.泥水
C.医用酒精 D.食盐水
5.下列关于溶液的说法正确的是( )
A.溶液中溶质只能有一种,溶剂可以有多种
B.溶液中的溶质只能是固体物质
C.凡是无色透明的液体都是溶液
D.溶液的质量为溶质和溶剂质量之和
6.下列物质中,属于溶液的是( )
A.蔗糖水 B.鲜牛奶 C.果粒橙 D.芝麻糊
7.下列有关获取物质的说法正确的是( )
A.从海中获取了蒸馏水,发生了化学变化
B.海水制镁时,直接电解海水得到金属镁
C.侯氏制碱中所需的钠、碳、氧元素
D.获取物质时,先考虑化学方法,再考虑物理方法
8.电解水时常在水中加少量的硫酸以增加水的导电性。若用含水92%的稀硫酸25g,通电进行电解,一段时间后稀硫酸中含水为90%,则发生电解的水的质量为()
A.2g B.4g C.5g D.2.5g
9.下列物质分别加入适量水中,充分搅拌,能够得到溶液的是( )
A.牛奶 B.苏打 C.花生油 D.面粉
10.放入水中不能形成溶液的物质是( )
A.白酒 B.食盐 C.白糖 D.植物油
11.将下列各组物质混合,不能形成溶液的是( )
A.蔗糖+水 B.二氧化碳+水
C.植物油+水 D.碘+汽油
12.欲用KNO3和水配制100kg溶质质量分数为7.1%的KNO3溶液作无土栽培的营养液,需水的质量为( )
A.7.1kg B.92.9kg
C.71kg D.14.2kg
二、填空题
13.为了增强水的导电性,现采用4%的硫酸溶液135g进行电解水实验,一段时间后,测得硫酸溶液中溶质的质量分数为5%,计算电解水的质量是 。
14.用4g酚酞与酒精配制溶质质量分数为4%的酚酞溶液,需要酒精的质量是 g,这些酒精的体积为 mL(酒精的密度为0.8g/mL)。
15.通电分解水时,常在水中加少量的氢氧化钠或硫酸,目的是: ,小明同学用150克溶质质量分数8%的稀氢氧化钠溶液通电一段时间后发现溶质质量分数变为12%,则被分解的水的质量是 .
16.如图是“×××钙片商品标签图”
×××儿童咀嚼片 (60片装)
[主要成分]碳酸钙,维生素D [规格]2.5g/片,每片中含碳酸钙≥1.24g,维生素D 100l.U. [食用方法]嚼食,每天一片 [功效]补钙
根据标签内容信息,计算回答下列问题:(结果精确到0.1)
(1)主要成分碳酸钙中钙元素的质量分数为 ,每片中至少含钙元素的质量为 g.
(2)小红同学为测定其碳酸钙的含量标注是否属实,她取出4片钙片,研碎后放入烧杯中,逐滴加入稀盐酸,至不再放出气体为止,共用去稀盐酸40.0g.称量烧杯中剩余物为47.8g(不含烧杯质量,假定钙片其他成分不与稀盐酸反应).
试计算:①生成二氧化碳的质量 ;
②稀盐酸中溶质的质量分数 ;
③通过计算判断钙片中碳酸钙的含量标注是否属实 .
17.若把溶质质量分数为49%的H2SO4溶液100g稀释为20%的H2SO4溶液,需要水的质量为 .
18.如图所示为a、b、c三种物质的溶解度曲线。
(1)t1℃时,将30ga物质加入到50g水中,而后升温到t2℃,此时该溶液的溶质和溶剂的质量比为 。
(2)t1℃时,24ga的饱和溶液稀释为10%,需要加入水 g。
(3)将t2℃时等质量的a、c的饱和溶液降温至t1℃此时两种溶液中溶质的质量分数大小关系为 。
三、综合题
19.某同学用锌和稀硫酸制取氢气.向气体发生装置中加入一定量锌粒,将30g稀硫酸分三次加入,每次生产气体的质量如下表.
次数 第一次 第二次 第三次
加入稀硫酸质量/g 10 10 10
生成氢气质量/g 0.04 0.04 0.02
(1)共制得氢气 g.
(2)所用稀硫酸的溶质质量分数.
20.实验室用100g含杂质10%的石灰石与948.6g一定质量分数的稀盐酸恰好完全反应.石灰石中杂质不溶于水也不与稀盐酸反应.求:
(1)产生二氧化碳的质量.
(2)反应后所得溶液的溶质的质量分数.
21.实验室用大理石制取二氧化碳,同学们进行了如下实验,过程如图所示(杂质不溶于水也不与盐酸反应):求:
(1)反应中生成二氧化碳的质量为 .
(2)所用稀盐酸的溶质的质量分数是多少?
22.请你各举出一个实例,说明下列有关溶液的叙述是错误的。
(1)溶液一定是无色的。实例: 溶液不是无色的。
(2)均一、稳定的液体都是溶液。实例: 是液体,但不是溶液。
(3)溶液中的溶质一定是固体。实例: 可做溶质,但不是固体。
(4)升高温度,物质的溶解度一定增大。实例: 升高温度,溶解度减小。
答案解析部分
1.【答案】A
2.【答案】B
3.【答案】D
4.【答案】B
5.【答案】D
6.【答案】A
7.【答案】C
8.【答案】C
9.【答案】B
10.【答案】D
11.【答案】C
12.【答案】B
13.【答案】27g
14.【答案】96;120
15.【答案】增强导电性;50g
16.【答案】40%;0.5;2.2g;9.1%;属实
17.【答案】145g
18.【答案】(1)1:2
(2)16
(3)a>c
19.【答案】(1)0.1
(2)解:设10g硫酸中含有溶质的质量为x
Zn+ H2SO4=ZnSO4+ H2↑
98 2
x 0.04g
x=1.96g
答:故硫酸的质量分数为: =19.6%.
20.【答案】(1)解:设生成氯化钙质量为x,生成二氧化碳质量为y,
CaCO3+ 2HCl ═ CaCl2 +H2O+ CO2↑
100 111 44
100g×(1﹣10%) x y
= = ,
x=99.9g,y=39.6g,
答:生成了39.6g二氧化碳.
(2)解:反应后所得溶液的溶质的质量分数为: ×100%=10%,
答:反应后所得溶液的溶质的质量分数为10%.
21.【答案】(1)4.4g
(2)解:设参加反应的HCl的质量为x
CaCO3+ 2HCl = CaCl2+ H2O+ CO2↑
73 44
x 4.4g
x=7.3g
所用稀盐酸的溶质的质量分数为 ×100%=14.6%
22.【答案】(1)硫酸铜(或填氯化铁等)
(2)水
(3)氯化氢气体(或硫酸等)
(4)氢氧化钙或
