基础实验 6 粗盐的初步提纯 同步练习(含答案) 2022-2023学年沪教版(全国)九年级下册化学
文档属性
| 名称 | 基础实验 6 粗盐的初步提纯 同步练习(含答案) 2022-2023学年沪教版(全国)九年级下册化学 |
|
|
| 格式 | zip | ||
| 文件大小 | 97.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-03-08 00:00:00 | ||
图片预览




文档简介
基础实验 6 粗盐的初步提纯 同步练习
一、单选题
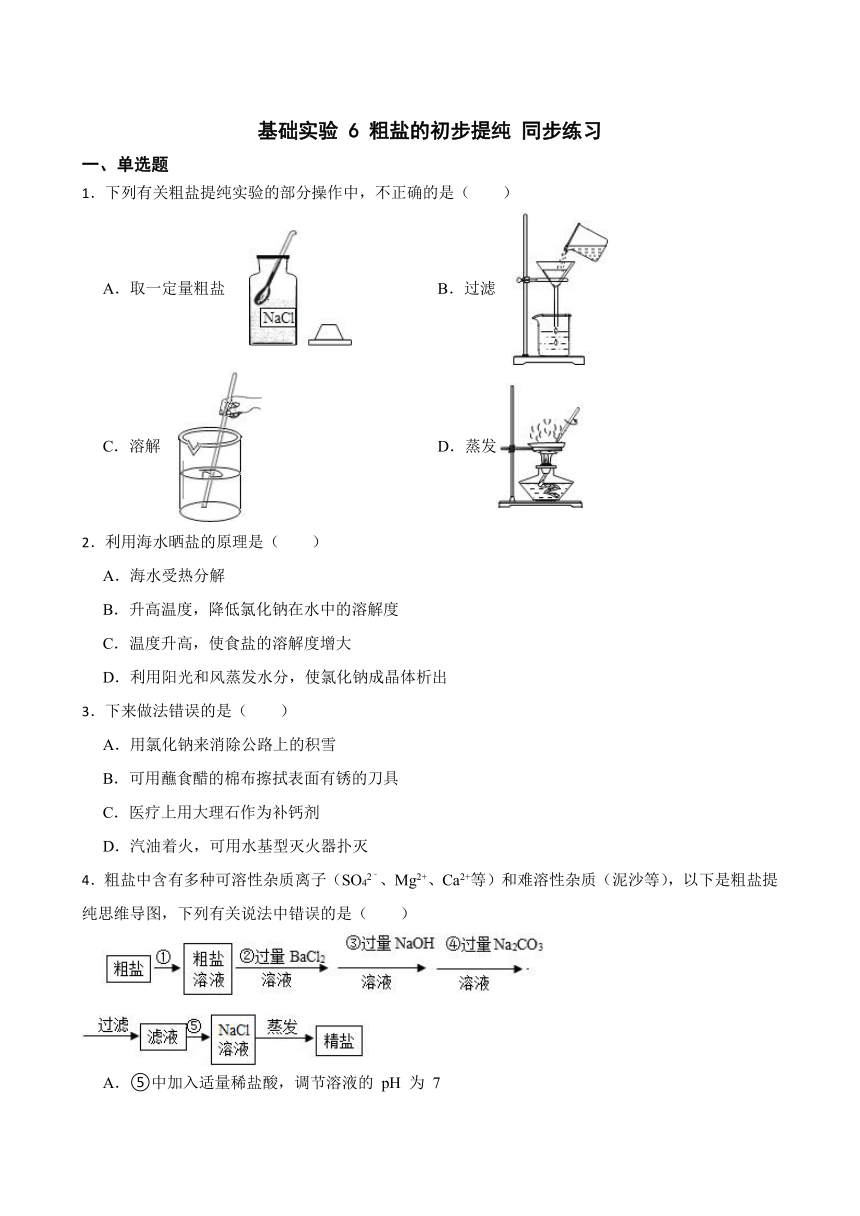
1.下列有关粗盐提纯实验的部分操作中,不正确的是( )
A.取一定量粗盐 B.过滤
C.溶解 D.蒸发
2.利用海水晒盐的原理是( )
A.海水受热分解
B.升高温度,降低氯化钠在水中的溶解度
C.温度升高,使食盐的溶解度增大
D.利用阳光和风蒸发水分,使氯化钠成晶体析出
3.下来做法错误的是( )
A.用氯化钠来消除公路上的积雪
B.可用蘸食醋的棉布擦拭表面有锈的刀具
C.医疗上用大理石作为补钙剂
D.汽油着火,可用水基型灭火器扑灭
4.粗盐中含有多种可溶性杂质离子(SO42﹣、Mg2+、Ca2+等)和难溶性杂质(泥沙等),以下是粗盐提纯思维导图,下列有关说法中错误的是( )
A.⑤中加入适量稀盐酸,调节溶液的 pH 为 7
B.①中通过溶解、过滤操作,可除去粗盐中难溶性杂质
C.任意交换②、③、④中加入试剂的顺序并不影响可溶性杂质的除去
D.②、③、④中通过加入相应试剂沉淀杂质离子,是因为相应离子在溶液中不能大量共存
5.以下是初中化学的一些基本实验操作,下列说法正确的是( )
A.粗盐中难溶性杂质去除的主要操作是②④⑤,其中去除杂质的关键操作是⑤
B.②④⑤各步操作中,玻璃棒的作用都是相同的
C.按①③②的步骤进行实验,可以配制一定溶质质量分数的溶液,但步骤③产生误差
D.按①③②实验时,若②所用的烧杯内壁沾有水,不影响实验结果
6.下图是粗盐提纯的部分实验操作。有关叙述错误的是( )
A.①中水的质量可以由食盐的溶解度计算得出
B.当②中蒸发皿内出现较多固体时应停止加热
C.④中缺少玻璃棒引流溶液
D.上述操作顺序为③①②④
7.在《一定质量分数的氯化钠溶液的配制 和 粗盐中难溶性杂质的去除》两个实验中都能使用到的( )
A.烧杯、玻璃棒、托盘天平、量筒
B.烧杯、玻璃棒、托盘天平、试管
C.托盘天平、量筒、烧杯、漏斗
D.蒸发皿、酒精灯、烧杯、铁架台
8.水是宝贵的自然资源,下列有关水的说法错误的是( )
A.水是最常用的溶剂 B.煮沸的汤比煮沸的水温度要高
C.蒸发海水得到粗盐 D.用明矾溶液来区别硬水和软水
9.用“海水晒盐”的方法得到的粗盐中,往往含有多种可溶性杂质(Na2SO4、MgCl2、CaCl2等)和难溶性杂质(泥沙等),需进行分离和提纯后才能用于人们的日常生活。以下是粗盐提纯的流程图,有关说法正确的是( )
A.①通过溶解、过滤操作,除去粗盐中可溶性杂质
B.只调换②与③的顺序,也能达到实验目的
C.⑤加入适量稀盐酸的目的是除去过量的Na2CO3和NaOH
D.若称得精盐的质量是8.5g,则该粗盐样品中氯化钠的纯度是85%
10.在粗盐提纯实验中,下列说法正确的是( )
A.过滤时,漏斗里的液体液面要低于滤纸的边缘
B.溶解和过滤操作中,玻璃棒的作用相同
C.蒸发时,将蒸发皿内液体蒸干后停止加热
D.溶解时,在量筒中边加粗盐边搅拌
11.实验室欲进行粗盐提纯,然后用提纯的精盐配制 50g 溶质质量分数为 15%的氯化钠溶液,说法正确的是( )
A.实验的步骤为:溶解、过滤、蒸发、转移、计算、称取、量取、溶解
B.蒸发实验结束后用手拿着蒸发皿小心的放在石棉网上,不可直接放在实验台上
C.把配制好的氯化钠溶液倒入刚用蒸馏水润洗过的试剂瓶中,结果会偏大
D.量取水时,用规格为 50mL 的量筒量取 42mL 蒸馏水
12.将粗盐溶解、过滤,除去泥沙后,溶液中仍含有少量的CaCl2、MgCl2、Na2SO4,为除去这些杂质,需用到①BaCl2溶液 ②Na2CO3溶液 ③NaOH溶液三种试剂(为将杂质除尽所加试剂均稍过量,且过量物质须在后续操作中被除去),充分反应后,过滤,再向滤液中加入适量的稀盐酸,加热蒸发,即可获得较为纯净的NaCl固体。以上三种试剂的加入顺序错误的是( )
A.①②③ B.①③② C.②③① D.③①②
二、填空题
13.某同学进行粗盐提纯的实验,粗盐中含有泥沙、氯化钠、氯化镁等物质。按下图流程进行实验。
操作1、2、3都用到的一种玻璃仪器是 ,操作2的名称为 。对上述实验过程,分析正确的是 。
A、粗盐和精盐都是混合物
B、粗盐变成精盐属于化学变化
C、溶解粗盐时,加入的水不宜过多,以免影响精盐的产率
D、为得到全部晶体,应把水分全部蒸干后,才停止加热
14.化学与生活、生产密切相关,请用所学知识回答问题:
(1)如图是超市销售的一种食盐标签的部分文字说明,请按要求回答:
①从成分上看,食盐中除含有NaCl外还有KIO3,KIO3的作用是 ;
②家庭生活中,食盐除了可以调味,还可用于 .
(2)炒菜时油锅中的油不慎着火,可用锅盖盖灭或放入较多的蔬菜,其目的是 .
15.结合下列实验,回答有关问题:
(1)去除粗盐中的不溶性杂质。
①溶解:将粗盐放入烧杯中,加入足量的蒸馏水溶解,用玻璃棒搅拌的目的是 ;
②过滤:向过滤器内倾倒滤液进行过滤,要控制液面的高度不超过 ;
③蒸发:当蒸发皿内出现 时,停止加热,利用余热蒸干剩余滤液。
(2)用氯化钠配制60g20%的食盐水。
①经计算,需要称量氯化钠的质量为 g;
②若量取所需蒸馏水时仰视读数,而其他操作均正确,则配制出的食盐水的浓度比20% (选填“偏高”、“偏低”或“无影响”)。
16.实验室要除去粗盐中难溶性杂质CaCl2、MgCl2、Na2SO4,可依次加入过量BaCl2、 、Na2CO3溶液,分离出沉淀后,再加入适量 。写出加入氯化钡后反应的化学反应方程式 。
17.粗盐提纯的步骤是 、 、 .在实验过程中可能使用到的仪器:
①铁架台②烧杯③量筒④试管夹⑤石棉网⑥集气瓶⑦药匙⑧胶头滴管⑨托盘天平⑩砝码.在这10种仪器中,实验中一定不需要是(填编号) ;需要增加的仪器是 .
18.实验室欲配制350g质量分数为16%的氯化钠溶液用于农业上的选种实验.实验室中只有粗盐,为了使结果更准确,实验员决定先将粗盐提纯后再配制.
(1)粗盐提纯的过程为:溶解→操作A→蒸发.操作A的名称为 ;该步骤中,玻璃棒的作用是 .
(2)需要精盐的质量为56g,水的质量为294g.配完溶液后发现,在用托盘天平称量精盐时,砝码和药品位置放颠倒了,(5g以下用游码).若其它操作均正确,则该实验员实际配制得到的氯化钠溶液的质量分数为 ,为了使溶液合乎要求,应该采取的补救措施是 .
三、综合题
19.食盐是我们生活中的重要物资
(1)食盐中含量最多的阳离子的符号为 。
(2)在提纯粗盐的过程中,需将粗盐溶解、 、蒸发、结晶。
(3)写出食盐的一种用途: 。
20.某同学欲在实验室测定含有泥沙的粗盐中氯化钠的纯度 ,实验的流程如图:
(1)称取粗盐样品时,粗盐样品应放在托盘天平的 (填写:左盘或右盘)。
(2)实验提纯中涉及的主要实验步骤是溶解、 、蒸发,氯化钠溶液是在 中进行蒸发(填仪器名称)。
(3)在此粗盐提纯的实验中,要多次用到玻璃棒,写出其中的两个作用 、 。
(4)操作②所获得的溶液仍浑浊,其原因可能是 。
(5)计算所获氯化钠的产率结果偏低,导致产率偏低的可能原因是 (写出一种原因)。
21.如图所示是利用海水提取粗盐的过程:
(1)根据海水晒盐的原理,下列说法中正确的是 (填字母序号)。
a.海水进入贮水池,海水的成分基本不变
b.在蒸发池中,海水中氯化钠的质量逐渐增加
c.在蒸发池中,海水中水的质量逐渐增加
d.析出晶体后的母液是氯化钠的饱和溶液
(2)在农业生产上,常用质量分数为16%的NaCl溶液选种,现要配制150kg这种溶液,需要氯化钠的质量是 kg,水的质量是 kg。
(3)若利用化学方法除去粗盐中CaCl2、MgSO4两种杂质,可在粗盐溶液中依次加入稍过量的三种溶液:氢氧化钠溶液、 (填化学式)溶液、 (填化学式)溶液。充分反应后过滤,加入稍过量的稀盐酸,搅拌、煮沸。
22.氯化钠具有广泛的用途。
(1)氯化钠是重要的调味品。组成氯化钠的钠元素和氯元素均是人体的 (选填“常量元素”或“微量元素”)。
(2)氯化钠是重要的化工原料。工业上电解饱和食盐水可制得氢氧化钠、氢气和氯气,请写出该反应的化学方程式 。
(3)粗盐中含有杂质,利用下图操作可除去难溶性杂质。请回答下列问题。
①操作C的不正确是 。
②海水晒盐采用操作D的原理,一般不采用降低氯化钠浓溶液温度的方法,原因是 。
(4)已知20℃时,氯化钠的溶解度为36.0g。20℃时,将20g氯化钠放入盛有50g水的烧杯中,充分搅拌后所得溶液的溶质质量分数为 (结果精确到0.1%)。若要配制溶质质量分数为5%的氯化钠溶液,还需向烧杯中加入水的质量为 g。
答案解析部分
1.【答案】B
2.【答案】D
3.【答案】C
4.【答案】C
5.【答案】C
6.【答案】D
7.【答案】A
8.【答案】D
9.【答案】C
10.【答案】A
11.【答案】A
12.【答案】C
13.【答案】玻璃棒;过滤;A
14.【答案】补充人体所需的碘元素,防止甲状腺肿大;腌制蔬菜、鱼、肉等;隔绝氧气或降低温度
15.【答案】(1)加快溶解速率;滤纸;较多晶体
(2)12.0;偏低
16.【答案】NaOH;稀盐酸(或HCl);BaCl2+Na2SO4=BaSO4↓+2NaCl
17.【答案】溶解;过滤;蒸发;③④⑥⑧⑨⑩;玻璃棒、漏斗、蒸发皿
18.【答案】过滤;引流;15.5%;再向该溶液中加入2g氯化钠,用玻璃棒进行搅拌
19.【答案】(1)Na+
(2)过滤
(3)作调味品
20.【答案】(1)左盘
(2)过滤;蒸发皿
(3)溶解时:搅拌,加快溶解;过滤时:引流(或蒸发时:玻璃棒的作用是搅拌,防止局部温度过高,造成液滴飞溅)
(4)滤纸破损(答案合理即可)
(5)蒸发溶液时液体外溅了一部分
21.【答案】(1)ad
(2)24;126
(3)BaCl2;Na2CO3
22.【答案】(1)常量元素
(2)
(3)没有用玻璃棒引流;氯化钠的溶解度随温度的升高变化不大
(4)26.5%;330
一、单选题
1.下列有关粗盐提纯实验的部分操作中,不正确的是( )
A.取一定量粗盐 B.过滤
C.溶解 D.蒸发
2.利用海水晒盐的原理是( )
A.海水受热分解
B.升高温度,降低氯化钠在水中的溶解度
C.温度升高,使食盐的溶解度增大
D.利用阳光和风蒸发水分,使氯化钠成晶体析出
3.下来做法错误的是( )
A.用氯化钠来消除公路上的积雪
B.可用蘸食醋的棉布擦拭表面有锈的刀具
C.医疗上用大理石作为补钙剂
D.汽油着火,可用水基型灭火器扑灭
4.粗盐中含有多种可溶性杂质离子(SO42﹣、Mg2+、Ca2+等)和难溶性杂质(泥沙等),以下是粗盐提纯思维导图,下列有关说法中错误的是( )
A.⑤中加入适量稀盐酸,调节溶液的 pH 为 7
B.①中通过溶解、过滤操作,可除去粗盐中难溶性杂质
C.任意交换②、③、④中加入试剂的顺序并不影响可溶性杂质的除去
D.②、③、④中通过加入相应试剂沉淀杂质离子,是因为相应离子在溶液中不能大量共存
5.以下是初中化学的一些基本实验操作,下列说法正确的是( )
A.粗盐中难溶性杂质去除的主要操作是②④⑤,其中去除杂质的关键操作是⑤
B.②④⑤各步操作中,玻璃棒的作用都是相同的
C.按①③②的步骤进行实验,可以配制一定溶质质量分数的溶液,但步骤③产生误差
D.按①③②实验时,若②所用的烧杯内壁沾有水,不影响实验结果
6.下图是粗盐提纯的部分实验操作。有关叙述错误的是( )
A.①中水的质量可以由食盐的溶解度计算得出
B.当②中蒸发皿内出现较多固体时应停止加热
C.④中缺少玻璃棒引流溶液
D.上述操作顺序为③①②④
7.在《一定质量分数的氯化钠溶液的配制 和 粗盐中难溶性杂质的去除》两个实验中都能使用到的( )
A.烧杯、玻璃棒、托盘天平、量筒
B.烧杯、玻璃棒、托盘天平、试管
C.托盘天平、量筒、烧杯、漏斗
D.蒸发皿、酒精灯、烧杯、铁架台
8.水是宝贵的自然资源,下列有关水的说法错误的是( )
A.水是最常用的溶剂 B.煮沸的汤比煮沸的水温度要高
C.蒸发海水得到粗盐 D.用明矾溶液来区别硬水和软水
9.用“海水晒盐”的方法得到的粗盐中,往往含有多种可溶性杂质(Na2SO4、MgCl2、CaCl2等)和难溶性杂质(泥沙等),需进行分离和提纯后才能用于人们的日常生活。以下是粗盐提纯的流程图,有关说法正确的是( )
A.①通过溶解、过滤操作,除去粗盐中可溶性杂质
B.只调换②与③的顺序,也能达到实验目的
C.⑤加入适量稀盐酸的目的是除去过量的Na2CO3和NaOH
D.若称得精盐的质量是8.5g,则该粗盐样品中氯化钠的纯度是85%
10.在粗盐提纯实验中,下列说法正确的是( )
A.过滤时,漏斗里的液体液面要低于滤纸的边缘
B.溶解和过滤操作中,玻璃棒的作用相同
C.蒸发时,将蒸发皿内液体蒸干后停止加热
D.溶解时,在量筒中边加粗盐边搅拌
11.实验室欲进行粗盐提纯,然后用提纯的精盐配制 50g 溶质质量分数为 15%的氯化钠溶液,说法正确的是( )
A.实验的步骤为:溶解、过滤、蒸发、转移、计算、称取、量取、溶解
B.蒸发实验结束后用手拿着蒸发皿小心的放在石棉网上,不可直接放在实验台上
C.把配制好的氯化钠溶液倒入刚用蒸馏水润洗过的试剂瓶中,结果会偏大
D.量取水时,用规格为 50mL 的量筒量取 42mL 蒸馏水
12.将粗盐溶解、过滤,除去泥沙后,溶液中仍含有少量的CaCl2、MgCl2、Na2SO4,为除去这些杂质,需用到①BaCl2溶液 ②Na2CO3溶液 ③NaOH溶液三种试剂(为将杂质除尽所加试剂均稍过量,且过量物质须在后续操作中被除去),充分反应后,过滤,再向滤液中加入适量的稀盐酸,加热蒸发,即可获得较为纯净的NaCl固体。以上三种试剂的加入顺序错误的是( )
A.①②③ B.①③② C.②③① D.③①②
二、填空题
13.某同学进行粗盐提纯的实验,粗盐中含有泥沙、氯化钠、氯化镁等物质。按下图流程进行实验。
操作1、2、3都用到的一种玻璃仪器是 ,操作2的名称为 。对上述实验过程,分析正确的是 。
A、粗盐和精盐都是混合物
B、粗盐变成精盐属于化学变化
C、溶解粗盐时,加入的水不宜过多,以免影响精盐的产率
D、为得到全部晶体,应把水分全部蒸干后,才停止加热
14.化学与生活、生产密切相关,请用所学知识回答问题:
(1)如图是超市销售的一种食盐标签的部分文字说明,请按要求回答:
①从成分上看,食盐中除含有NaCl外还有KIO3,KIO3的作用是 ;
②家庭生活中,食盐除了可以调味,还可用于 .
(2)炒菜时油锅中的油不慎着火,可用锅盖盖灭或放入较多的蔬菜,其目的是 .
15.结合下列实验,回答有关问题:
(1)去除粗盐中的不溶性杂质。
①溶解:将粗盐放入烧杯中,加入足量的蒸馏水溶解,用玻璃棒搅拌的目的是 ;
②过滤:向过滤器内倾倒滤液进行过滤,要控制液面的高度不超过 ;
③蒸发:当蒸发皿内出现 时,停止加热,利用余热蒸干剩余滤液。
(2)用氯化钠配制60g20%的食盐水。
①经计算,需要称量氯化钠的质量为 g;
②若量取所需蒸馏水时仰视读数,而其他操作均正确,则配制出的食盐水的浓度比20% (选填“偏高”、“偏低”或“无影响”)。
16.实验室要除去粗盐中难溶性杂质CaCl2、MgCl2、Na2SO4,可依次加入过量BaCl2、 、Na2CO3溶液,分离出沉淀后,再加入适量 。写出加入氯化钡后反应的化学反应方程式 。
17.粗盐提纯的步骤是 、 、 .在实验过程中可能使用到的仪器:
①铁架台②烧杯③量筒④试管夹⑤石棉网⑥集气瓶⑦药匙⑧胶头滴管⑨托盘天平⑩砝码.在这10种仪器中,实验中一定不需要是(填编号) ;需要增加的仪器是 .
18.实验室欲配制350g质量分数为16%的氯化钠溶液用于农业上的选种实验.实验室中只有粗盐,为了使结果更准确,实验员决定先将粗盐提纯后再配制.
(1)粗盐提纯的过程为:溶解→操作A→蒸发.操作A的名称为 ;该步骤中,玻璃棒的作用是 .
(2)需要精盐的质量为56g,水的质量为294g.配完溶液后发现,在用托盘天平称量精盐时,砝码和药品位置放颠倒了,(5g以下用游码).若其它操作均正确,则该实验员实际配制得到的氯化钠溶液的质量分数为 ,为了使溶液合乎要求,应该采取的补救措施是 .
三、综合题
19.食盐是我们生活中的重要物资
(1)食盐中含量最多的阳离子的符号为 。
(2)在提纯粗盐的过程中,需将粗盐溶解、 、蒸发、结晶。
(3)写出食盐的一种用途: 。
20.某同学欲在实验室测定含有泥沙的粗盐中氯化钠的纯度 ,实验的流程如图:
(1)称取粗盐样品时,粗盐样品应放在托盘天平的 (填写:左盘或右盘)。
(2)实验提纯中涉及的主要实验步骤是溶解、 、蒸发,氯化钠溶液是在 中进行蒸发(填仪器名称)。
(3)在此粗盐提纯的实验中,要多次用到玻璃棒,写出其中的两个作用 、 。
(4)操作②所获得的溶液仍浑浊,其原因可能是 。
(5)计算所获氯化钠的产率结果偏低,导致产率偏低的可能原因是 (写出一种原因)。
21.如图所示是利用海水提取粗盐的过程:
(1)根据海水晒盐的原理,下列说法中正确的是 (填字母序号)。
a.海水进入贮水池,海水的成分基本不变
b.在蒸发池中,海水中氯化钠的质量逐渐增加
c.在蒸发池中,海水中水的质量逐渐增加
d.析出晶体后的母液是氯化钠的饱和溶液
(2)在农业生产上,常用质量分数为16%的NaCl溶液选种,现要配制150kg这种溶液,需要氯化钠的质量是 kg,水的质量是 kg。
(3)若利用化学方法除去粗盐中CaCl2、MgSO4两种杂质,可在粗盐溶液中依次加入稍过量的三种溶液:氢氧化钠溶液、 (填化学式)溶液、 (填化学式)溶液。充分反应后过滤,加入稍过量的稀盐酸,搅拌、煮沸。
22.氯化钠具有广泛的用途。
(1)氯化钠是重要的调味品。组成氯化钠的钠元素和氯元素均是人体的 (选填“常量元素”或“微量元素”)。
(2)氯化钠是重要的化工原料。工业上电解饱和食盐水可制得氢氧化钠、氢气和氯气,请写出该反应的化学方程式 。
(3)粗盐中含有杂质,利用下图操作可除去难溶性杂质。请回答下列问题。
①操作C的不正确是 。
②海水晒盐采用操作D的原理,一般不采用降低氯化钠浓溶液温度的方法,原因是 。
(4)已知20℃时,氯化钠的溶解度为36.0g。20℃时,将20g氯化钠放入盛有50g水的烧杯中,充分搅拌后所得溶液的溶质质量分数为 (结果精确到0.1%)。若要配制溶质质量分数为5%的氯化钠溶液,还需向烧杯中加入水的质量为 g。
答案解析部分
1.【答案】B
2.【答案】D
3.【答案】C
4.【答案】C
5.【答案】C
6.【答案】D
7.【答案】A
8.【答案】D
9.【答案】C
10.【答案】A
11.【答案】A
12.【答案】C
13.【答案】玻璃棒;过滤;A
14.【答案】补充人体所需的碘元素,防止甲状腺肿大;腌制蔬菜、鱼、肉等;隔绝氧气或降低温度
15.【答案】(1)加快溶解速率;滤纸;较多晶体
(2)12.0;偏低
16.【答案】NaOH;稀盐酸(或HCl);BaCl2+Na2SO4=BaSO4↓+2NaCl
17.【答案】溶解;过滤;蒸发;③④⑥⑧⑨⑩;玻璃棒、漏斗、蒸发皿
18.【答案】过滤;引流;15.5%;再向该溶液中加入2g氯化钠,用玻璃棒进行搅拌
19.【答案】(1)Na+
(2)过滤
(3)作调味品
20.【答案】(1)左盘
(2)过滤;蒸发皿
(3)溶解时:搅拌,加快溶解;过滤时:引流(或蒸发时:玻璃棒的作用是搅拌,防止局部温度过高,造成液滴飞溅)
(4)滤纸破损(答案合理即可)
(5)蒸发溶液时液体外溅了一部分
21.【答案】(1)ad
(2)24;126
(3)BaCl2;Na2CO3
22.【答案】(1)常量元素
(2)
(3)没有用玻璃棒引流;氯化钠的溶解度随温度的升高变化不大
(4)26.5%;330
