2022—2023学年化学沪教版(全国)九年级下册第七章 应用广泛的酸、碱、盐 分层优选题(含答案)
文档属性
| 名称 | 2022—2023学年化学沪教版(全国)九年级下册第七章 应用广泛的酸、碱、盐 分层优选题(含答案) |

|
|
| 格式 | zip | ||
| 文件大小 | 506.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-03-09 00:00:00 | ||
图片预览



文档简介
2022—2023学年化学沪教版(全国)九年级下册第七章 应用广泛的酸、碱、盐 分层优选题含答案
沪教版(全国)第七章 应用广泛的酸、碱、盐
一、选择题。
1、20gKOH加入100g水中,配制成溶液。下列说法错误的是( )
A.KOH在水中解离出K+和OH-
B.一个K+带一个单位正电荷
C.该溶液的溶质质量分数为20%
D.向该溶液中滴入酚酞指示剂,溶液变红
2、下列物质与水充分相混后,能使紫色石蕊试液变蓝色的是( )
A.H2SO4 B.NH3 C.NaCl D.Cu(OH)2
3、现有甲、乙、丙三种金属,先将三者分别加入到硫酸亚铁溶液中,只有甲可使溶液中析出铁单质。再将三者加入到硝酸银溶液中,只有乙不能使溶液中析出银单质,则三者的金属活动性从强到弱的顺序是( )
A.甲>乙>丙 B.乙>甲>丙 C.甲>丙>乙 D.无法判断
4、下列有关化肥或农药的叙述错误的是( )
A.硫酸铵属于复合肥料,所含的营养元素是氮和硫
B.氯化铵和磷矿粉从外观即可区分
C.农药施用后,会通过农作物、农产品等发生转移
D.化肥和农药施用不当,会对环境造成污染
5、劳动创造美好生活。下列劳动项目所涉及的化学知识正确的是( )
选项 劳动项目 化学知识
A 用含洗涤剂的水洗管具上的油污 发生了乳化
B 清理家中鱼缸并通入空气 空气中的氧气易溶于水
C 给校园中的花草施用草木灰(含K2CO3) K2CO3属于复合肥料
D 用食醋去除热水瓶内壁的水垢 食醋的pH>7
A.A B.B C.C D.D
6、下列物质能与NaOH反应的是( )
A.Fe B.CO2 C.Fe2O3 D.NaCl
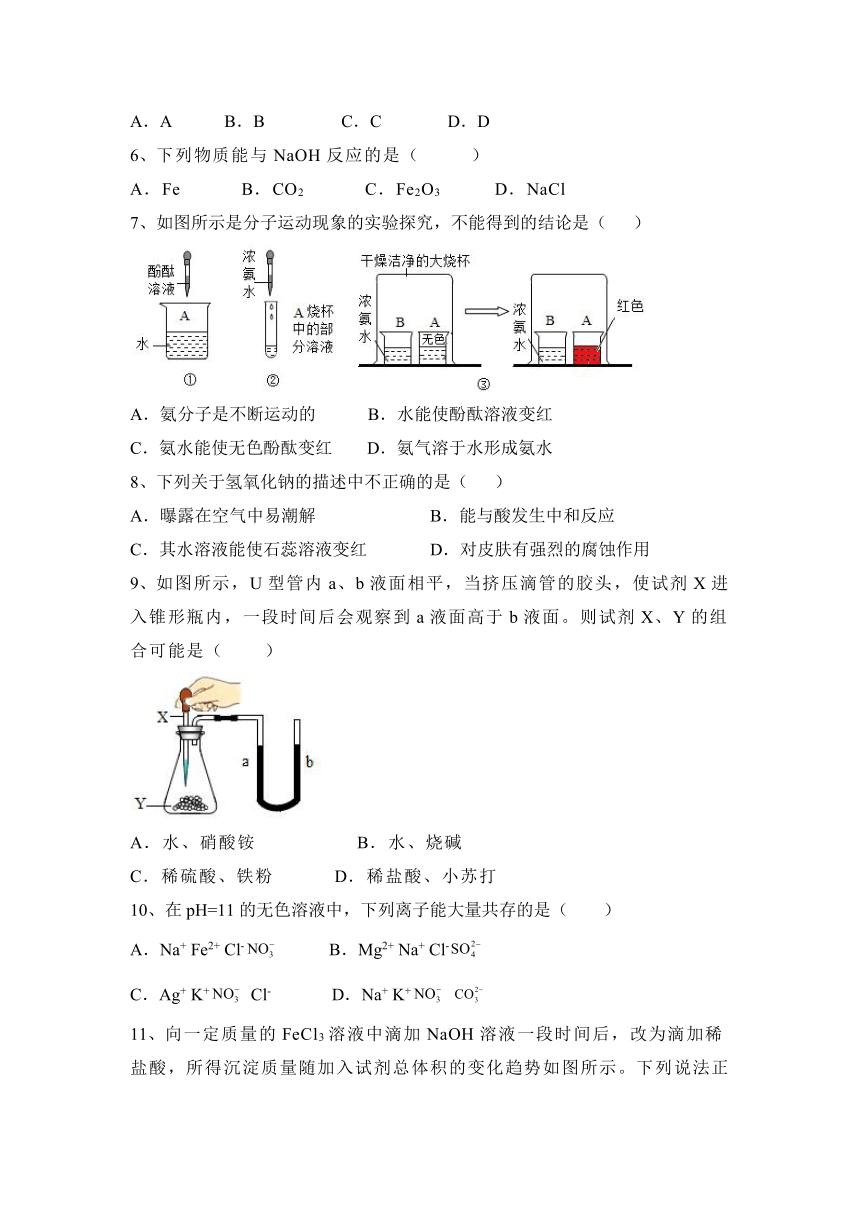
7、如图所示是分子运动现象的实验探究,不能得到的结论是( )
A.氨分子是不断运动的 B.水能使酚酞溶液变红
C.氨水能使无色酚酞变红 D.氨气溶于水形成氨水
8、下列关于氢氧化钠的描述中不正确的是( )
A.曝露在空气中易潮解 B.能与酸发生中和反应
C.其水溶液能使石蕊溶液变红 D.对皮肤有强烈的腐蚀作用
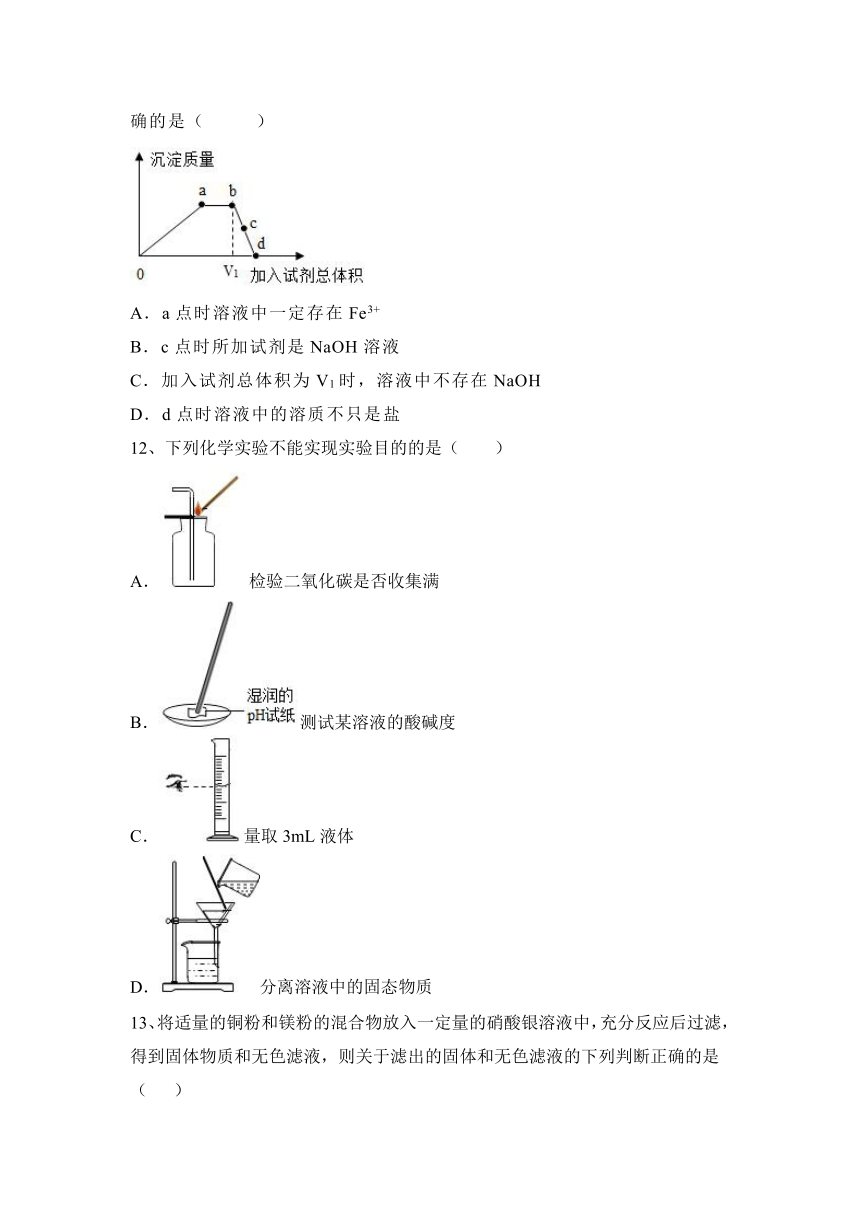
9、如图所示,U型管内a、b液面相平,当挤压滴管的胶头,使试剂X进入锥形瓶内,一段时间后会观察到a液面高于b液面。则试剂X、Y的组合可能是( )
A.水、硝酸铵 B.水、烧碱
C.稀硫酸、铁粉 D.稀盐酸、小苏打
10、在pH=11的无色溶液中,下列离子能大量共存的是( )
A.Na+ Fe2+ Cl- B.Mg2+ Na+ Cl-
C.Ag+ K+ Cl- D.Na+ K+
11、向一定质量的FeCl3溶液中滴加NaOH溶液一段时间后,改为滴加稀盐酸,所得沉淀质量随加入试剂总体积的变化趋势如图所示。下列说法正确的是( )
A.a点时溶液中一定存在Fe3+
B.c点时所加试剂是NaOH溶液
C.加入试剂总体积为V1时,溶液中不存在NaOH
D.d点时溶液中的溶质不只是盐
12、下列化学实验不能实现实验目的的是( )
A.检验二氧化碳是否收集满
B.测试某溶液的酸碱度
C.量取3mL液体
D.分离溶液中的固态物质
13、将适量的铜粉和镁粉的混合物放入一定量的硝酸银溶液中,充分反应后过滤,得到固体物质和无色滤液,则关于滤出的固体和无色滤液的下列判断正确的是( )
A.滤出的固体中一定含有银和铜,一定不含镁
B.滤出的固体中一定含有银,可能含有铜和镁
C.滤液中一定含有硝酸银和硝酸镁,一定没有硝酸铜
D.滤液中一定含有硝酸镁,一定没有硝酸银和硝酸铜
*14、钯(Pd)是一种稀有的贵金属,钯镍合金在电子工业等有广泛应用。已知钯、镍、铜三种金属的活动性强弱顺序是Ni>Cu>Pd,下列实验可以验证三者金属活动性强弱的实验组合是( )
①Cu+硝酸镍溶液 ②Pd+稀盐酸 ③Pd+硫酸铜溶液 ④Ni+稀盐酸
A.①② B.①③ C.②③ D.②④
15、下列4个图像分别对应4个变化过程,其中正确的是( )
A.电解水
B.将一定量的60℃硝酸钾饱和溶液冷却至室温
C.等质量的镁、铝分别与相同浓度的足量稀硫酸反应
D.向一定量CuSO4和K2SO4混合溶液中,不断加入KOH溶液
二、填空题。
16、现有白纸,溶质质量分数分别为:A、10%的NaOH溶液;B、5%的硫酸溶液;C、5%的紫色石蕊试液。试设计出《“雨”落叶出红花开》的趣味实验:先在白纸上用玻璃棒蘸取__________(填编号,下同)画上花,再蘸__________画上叶,将白纸挂上墙,用_________向纸上喷洒即可,实验的化学原理是_________________________________________。
17、回答下列下列生活、生产中的一些问题:
(1)如图是家庭中一些常见物质的pH.要减轻被蚂蚁叮咬后(向人体注入了甲酸)出现的皮肤搔痒、红肿症状,最适宜涂抹上表中的物质________(写名称)。
(2)工业用盐酸除铁锈,向盛有生锈的铁制零件的容器内加入足量的稀盐酸,首先观察到的现象是________,________,反应的化学方程式为________;放置一段时间,观察到的现象是________,反应的化学方程式为________。
(3)农药“波尔多液”可以杀灭柑橘上的害虫,它是将熟石灰加入硫酸铜溶液中搅拌而成,其混合时反应的化学方程式为________。
(4)烧碱固体如果暴露在空气中或密封不严,容易________潮解,还能与________反应,所以必须密封保存。写出烧碱变质的化学方程式________。
18、厨房里有两瓶白色固体,分别为食盐(NaCl) 和纯碱(Na2CO3)。
(1)可用于腌制肉类和蔬菜,使食物不易腐败的是 。
(2)为鉴别这两种物质,某同学取少量白色固体,进行如下实验。
方案一:分别滴加少量食醋,有气泡产生的是 。
方案二:加水溶解,分别滴加 溶液,有沉淀产生的是纯碱。
19、根据下列两组实验回答问题:
(1)图中仪器a的名称是 ,两组实验都用到的仪器是 。
(2)指出甲实验中的不正确操作 。
(3)乙实验中,正确的操作顺序为(填序号)②→ → → 。
20、判断题:
(1)氢氧化铝可治疗胃酸过多,故氢氧化钠也可治疗胃酸过多( )
(2)生锈的铁钉加入适量的稀盐酸后溶液也会变成浅绿色( )
(3)用稀盐酸除去水垢( )
(4)铁能与氢氧化钠溶液反应放出氢气( )
(5)“要留清白在人间”实现了从Ca(OH)2到CaCO3的转化( )
21、张老师上课时做了趣味实验:他选择了一种指示剂(无色酚酞试液或紫色石蕊试液)、稀盐酸、稀NaOH溶液。他先用玻璃棒蘸取某种指示剂在白纸上写上“化学”,可是学生什么也看不见。然后用某种物质喷洒在白纸上,出现了红色的“化学”二字。接着,又向纸上喷洒另一种物质,红字消失。则他选用的指示剂是 ,先喷洒的物质是 ,后喷洒的物质为 。如果选用另一种指示剂。情况会怎样?
22、把相同体积、相同质量分数的稀盐酸,分别滴到等质量、颗粒大小相同的X、Y、Z三种较活泼金属中,生成H2的质量与反应时间的关系如下图所示。这三种金属的活动性顺序为 ;假如X、Y、Z都是+2价金属,则相对原子质量由大到小的顺序为 。
23、无土栽培是利用营养液栽培作物的一种方法。
(1)下列化学肥料中属于复合肥的是 (填序号);
①硝酸铵 ②磷酸二氢铵 ③硝酸钾 ④硫酸钾
(2)某同学要在实验室配制150g溶质质量分数为2%的硝酸钾溶液,需要硝酸钾的质量为 g。
三、实验和综合应用题。
24、随着世界人口的增长,人类对农产品需求量增大,增施化肥逐渐成为农作物增产的最有力措施。NH4HCO3、NH4Cl、K2SO4、KCl都是常见的化肥。
(1)化肥能为农作物补充的营养元素主要有三种,上述化肥不能提供的营养元素是___________。
(2)有一包用剩的肥料,可能含有上述四种化肥中的一种或几种,为确定其成分,进行了如下实验:
a、取少量肥料样品于研钵中,加入少量熟石灰混合研磨,有刺激性气味。
b、取少量肥料样品于烧杯中,加水溶解,得到无色溶液A。
c、取少量溶液A于试管中,滴加AgNO3溶液,有白色沉淀产生。
d、取少量溶液A于试管中,滴加BaCl2溶液,无明显现象。
e、取少量溶液A于试管中,滴加稀盐酸,无明显现象。
①分析上述实验过程,可得该肥料一定有___________,一定没有___________,可能有___________。
②实验a~e中,不必要进行的一项是___________(填标号)。
③设计实验方案进一步确定该肥料的成分,完成下表。(已知:)
实验操作 预期现象与结论
取少量样品于试管中,并加热至无刺激性气味的气体产生为止,待冷却后,加入足量的水溶解后,往试管里加入少量___________溶液,振荡后观察现象。 若___________,则该肥料的成分是NH4Cl、KCl。
25、金属材料在生活中随处可见。某学习小组围绕金属材料展开项目式学习。
【项目一】金属的物理性质
(1)316不锈钢与组成它的纯金属相比,有良好的___________ 。
【项目二】金属的化学性质
(2)组员小王将打磨后的镁条放入硫酸铜溶液中,发生反应的化学方程式为__________ 。
组员小李意外发现镁条表面还有气泡产生,于是学习小组对此展开探究。
(3)小王用拇指堵住试管,收集一会气体之后伸入燃着的木条,发出尖锐的爆鸣声,说明该气体是__________。
【提出问题】为什么会产生该气体呢?
【作出猜想】硫酸铜溶液显酸性,所以放入镁条后会产生该气体。
【实验验证】
(4)用pH试纸测量硫酸铜溶液的pH,实验操作是__________ 。经测定,溶液pH<7,证实猜想正确。
【项目三】冶炼金属
(5)冶炼金属铁的原料有铁矿石、焦炭、__________、热空气。
铁的氧化物有FeO、Fe2O3、Fe3O4。组员小卫称取6.0g铁的氧化物混合样品,采用如图装置模拟炼铁过程(夹持装置省略),完全反应后,测得实验前后装置B增重4.4g。
(6)实验开始时先打开__________,关闭另一止水夹,让CO通一段时间。
(7)根据实验数据进行计算,该固体样品成分可能是 (填字母序号)。
A.FeO、Fe2O3 B.Fe2O3、Fe3O4
C.FeO、Fe3O4 D.FeO、Fe2O3、Fe3O4
三、计算题。
26、某氧化钠样品中含有氯化镁。为测定其中氧化钠的质量分数,称量5.00g样品于烧杯中,加适量水完全溶解,然后逐滴加入氢氧化钠溶液至恰好完全反应,生成0.58g沉淀。请回答下列问题:
(1)氢氧化钠溶液可使紫色石蕊溶液变成___________色。
(2)计算该样品中氧化钠的质量分数为____________。
2022—2023学年化学沪教版(全国)九年级下册第七章 应用广泛的酸、碱、盐 分层优选题含答案
沪教版(全国)第七章 应用广泛的酸、碱、盐
一、选择题。
1、20gKOH加入100g水中,配制成溶液。下列说法错误的是( )
A.KOH在水中解离出K+和OH-
B.一个K+带一个单位正电荷
C.该溶液的溶质质量分数为20%
D.向该溶液中滴入酚酞指示剂,溶液变红
【答案】C
2、下列物质与水充分相混后,能使紫色石蕊试液变蓝色的是( )
A.H2SO4 B.NH3 C.NaCl D.Cu(OH)2
【答案】B
3、现有甲、乙、丙三种金属,先将三者分别加入到硫酸亚铁溶液中,只有甲可使溶液中析出铁单质。再将三者加入到硝酸银溶液中,只有乙不能使溶液中析出银单质,则三者的金属活动性从强到弱的顺序是( )
A.甲>乙>丙 B.乙>甲>丙 C.甲>丙>乙 D.无法判断
【答案】C
4、下列有关化肥或农药的叙述错误的是( )
A.硫酸铵属于复合肥料,所含的营养元素是氮和硫
B.氯化铵和磷矿粉从外观即可区分
C.农药施用后,会通过农作物、农产品等发生转移
D.化肥和农药施用不当,会对环境造成污染
【答案】A
5、劳动创造美好生活。下列劳动项目所涉及的化学知识正确的是( )
选项 劳动项目 化学知识
A 用含洗涤剂的水洗管具上的油污 发生了乳化
B 清理家中鱼缸并通入空气 空气中的氧气易溶于水
C 给校园中的花草施用草木灰(含K2CO3) K2CO3属于复合肥料
D 用食醋去除热水瓶内壁的水垢 食醋的pH>7
A.A B.B C.C D.D
【答案】A
6、下列物质能与NaOH反应的是( )
A.Fe B.CO2 C.Fe2O3 D.NaCl
【答案】B
7、如图所示是分子运动现象的实验探究,不能得到的结论是( )
A.氨分子是不断运动的 B.水能使酚酞溶液变红
C.氨水能使无色酚酞变红 D.氨气溶于水形成氨水
【答案】B
8、下列关于氢氧化钠的描述中不正确的是( )
A.曝露在空气中易潮解 B.能与酸发生中和反应
C.其水溶液能使石蕊溶液变红 D.对皮肤有强烈的腐蚀作用
【答案】C
9、如图所示,U型管内a、b液面相平,当挤压滴管的胶头,使试剂X进入锥形瓶内,一段时间后会观察到a液面高于b液面。则试剂X、Y的组合可能是( )
A.水、硝酸铵 B.水、烧碱
C.稀硫酸、铁粉 D.稀盐酸、小苏打
【答案】A
10、在pH=11的无色溶液中,下列离子能大量共存的是( )
A.Na+ Fe2+ Cl- B.Mg2+ Na+ Cl-
C.Ag+ K+ Cl- D.Na+ K+
【答案】D
11、向一定质量的FeCl3溶液中滴加NaOH溶液一段时间后,改为滴加稀盐酸,所得沉淀质量随加入试剂总体积的变化趋势如图所示。下列说法正确的是( )
A.a点时溶液中一定存在Fe3+
B.c点时所加试剂是NaOH溶液
C.加入试剂总体积为V1时,溶液中不存在NaOH
D.d点时溶液中的溶质不只是盐
【答案】C
12、下列化学实验不能实现实验目的的是( )
A.检验二氧化碳是否收集满
B.测试某溶液的酸碱度
C.量取3mL液体
D.分离溶液中的固态物质
【答案】B
13、将适量的铜粉和镁粉的混合物放入一定量的硝酸银溶液中,充分反应后过滤,得到固体物质和无色滤液,则关于滤出的固体和无色滤液的下列判断正确的是( )
A.滤出的固体中一定含有银和铜,一定不含镁
B.滤出的固体中一定含有银,可能含有铜和镁
C.滤液中一定含有硝酸银和硝酸镁,一定没有硝酸铜
D.滤液中一定含有硝酸镁,一定没有硝酸银和硝酸铜
【答案】B
*14、钯(Pd)是一种稀有的贵金属,钯镍合金在电子工业等有广泛应用。已知钯、镍、铜三种金属的活动性强弱顺序是Ni>Cu>Pd,下列实验可以验证三者金属活动性强弱的实验组合是( )
①Cu+硝酸镍溶液 ②Pd+稀盐酸 ③Pd+硫酸铜溶液 ④Ni+稀盐酸
A.①② B.①③ C.②③ D.②④
【答案】B
15、下列4个图像分别对应4个变化过程,其中正确的是( )
A.电解水
B.将一定量的60℃硝酸钾饱和溶液冷却至室温
C.等质量的镁、铝分别与相同浓度的足量稀硫酸反应
D.向一定量CuSO4和K2SO4混合溶液中,不断加入KOH溶液
【答案】B
二、填空题。
16、现有白纸,溶质质量分数分别为:A、10%的NaOH溶液;B、5%的硫酸溶液;C、5%的紫色石蕊试液。试设计出《“雨”落叶出红花开》的趣味实验:先在白纸上用玻璃棒蘸取__________(填编号,下同)画上花,再蘸__________画上叶,将白纸挂上墙,用_________向纸上喷洒即可,实验的化学原理是_________________________________________。
【答案】B A C 紫色石蕊试液遇酸变红、遇碱变蓝
17、回答下列下列生活、生产中的一些问题:
(1)如图是家庭中一些常见物质的pH.要减轻被蚂蚁叮咬后(向人体注入了甲酸)出现的皮肤搔痒、红肿症状,最适宜涂抹上表中的物质________(写名称)。
(2)工业用盐酸除铁锈,向盛有生锈的铁制零件的容器内加入足量的稀盐酸,首先观察到的现象是________,________,反应的化学方程式为________;放置一段时间,观察到的现象是________,反应的化学方程式为________。
(3)农药“波尔多液”可以杀灭柑橘上的害虫,它是将熟石灰加入硫酸铜溶液中搅拌而成,其混合时反应的化学方程式为________。
(4)烧碱固体如果暴露在空气中或密封不严,容易________潮解,还能与________反应,所以必须密封保存。写出烧碱变质的化学方程式________。
【答案】(1)牙膏
(2) 红棕色逐渐消失 溶液由无色变成黄色
Fe2O3+6HCl=2FeCl3+3H2O 有气泡产生,溶液变为浅绿色
Fe+2HCl=FeCl2+H2↑
(3)CuSO4+Ca(OH)2=Cu(OH)2↓+CaSO4
(4) 吸收水分 二氧化碳或CO2 CO2+2NaOH=Na2CO3+H2O
18、厨房里有两瓶白色固体,分别为食盐(NaCl) 和纯碱(Na2CO3)。
(1)可用于腌制肉类和蔬菜,使食物不易腐败的是 。
(2)为鉴别这两种物质,某同学取少量白色固体,进行如下实验。
方案一:分别滴加少量食醋,有气泡产生的是 。
方案二:加水溶解,分别滴加 溶液,有沉淀产生的是纯碱。
【答案】食盐; 碳酸钠; 氯化钙(合理即可)
19、根据下列两组实验回答问题:
(1)图中仪器a的名称是 ,两组实验都用到的仪器是 。
(2)指出甲实验中的不正确操作 。
(3)乙实验中,正确的操作顺序为(填序号)②→ → → 。
【答案】(1)漏斗 玻璃棒
(2)用镊子夹取pH试纸放入待测液中 (3)① ④ ③
20、判断题:
(1)氢氧化铝可治疗胃酸过多,故氢氧化钠也可治疗胃酸过多( )
(2)生锈的铁钉加入适量的稀盐酸后溶液也会变成浅绿色( )
(3)用稀盐酸除去水垢( )
(4)铁能与氢氧化钠溶液反应放出氢气( )
(5)“要留清白在人间”实现了从Ca(OH)2到CaCO3的转化( )
【答案】(1)错误 (2)错误 (3)正确 (4)错误 (5)正确
21、张老师上课时做了趣味实验:他选择了一种指示剂(无色酚酞试液或紫色石蕊试液)、稀盐酸、稀NaOH溶液。他先用玻璃棒蘸取某种指示剂在白纸上写上“化学”,可是学生什么也看不见。然后用某种物质喷洒在白纸上,出现了红色的“化学”二字。接着,又向纸上喷洒另一种物质,红字消失。则他选用的指示剂是 ,先喷洒的物质是 ,后喷洒的物质为 。如果选用另一种指示剂。情况会怎样?
【答案】无色酚酞试液 氢氧化钠溶液 稀盐酸 字先变紫色,喷氢氧化钠后变成蓝色,再喷盐酸字色变化为“蓝→紫→红”
22、把相同体积、相同质量分数的稀盐酸,分别滴到等质量、颗粒大小相同的X、Y、Z三种较活泼金属中,生成H2的质量与反应时间的关系如下图所示。这三种金属的活动性顺序为 ;假如X、Y、Z都是+2价金属,则相对原子质量由大到小的顺序为 。
【答案】Y>X>Z,Z>Y>X.
23、无土栽培是利用营养液栽培作物的一种方法。
(1)下列化学肥料中属于复合肥的是 (填序号);
①硝酸铵 ②磷酸二氢铵 ③硝酸钾 ④硫酸钾
(2)某同学要在实验室配制150g溶质质量分数为2%的硝酸钾溶液,需要硝酸钾的质量为 g。
【答案】 ②③;3
三、实验和综合应用题。
24、随着世界人口的增长,人类对农产品需求量增大,增施化肥逐渐成为农作物增产的最有力措施。NH4HCO3、NH4Cl、K2SO4、KCl都是常见的化肥。
(1)化肥能为农作物补充的营养元素主要有三种,上述化肥不能提供的营养元素是___________。
(2)有一包用剩的肥料,可能含有上述四种化肥中的一种或几种,为确定其成分,进行了如下实验:
a、取少量肥料样品于研钵中,加入少量熟石灰混合研磨,有刺激性气味。
b、取少量肥料样品于烧杯中,加水溶解,得到无色溶液A。
c、取少量溶液A于试管中,滴加AgNO3溶液,有白色沉淀产生。
d、取少量溶液A于试管中,滴加BaCl2溶液,无明显现象。
e、取少量溶液A于试管中,滴加稀盐酸,无明显现象。
①分析上述实验过程,可得该肥料一定有___________,一定没有___________,可能有___________。
②实验a~e中,不必要进行的一项是___________(填标号)。
③设计实验方案进一步确定该肥料的成分,完成下表。(已知:)
实验操作 预期现象与结论
取少量样品于试管中,并加热至无刺激性气味的气体产生为止,待冷却后,加入足量的水溶解后,往试管里加入少量___________溶液,振荡后观察现象。 若___________,则该肥料的成分是NH4Cl、KCl。
【答案】(1)P(磷)
(2) 氯化铵() 碳酸氢铵和硫酸钾() 氯化钾()C 硝酸银() 产生白色沉淀
25、金属材料在生活中随处可见。某学习小组围绕金属材料展开项目式学习。
【项目一】金属的物理性质
(1)316不锈钢与组成它的纯金属相比,有良好的___________ 。
【项目二】金属的化学性质
(2)组员小王将打磨后的镁条放入硫酸铜溶液中,发生反应的化学方程式为__________ 。
组员小李意外发现镁条表面还有气泡产生,于是学习小组对此展开探究。
(3)小王用拇指堵住试管,收集一会气体之后伸入燃着的木条,发出尖锐的爆鸣声,说明该气体是__________。
【提出问题】为什么会产生该气体呢?
【作出猜想】硫酸铜溶液显酸性,所以放入镁条后会产生该气体。
【实验验证】
(4)用pH试纸测量硫酸铜溶液的pH,实验操作是__________ 。经测定,溶液pH<7,证实猜想正确。
【项目三】冶炼金属
(5)冶炼金属铁的原料有铁矿石、焦炭、__________、热空气。
铁的氧化物有FeO、Fe2O3、Fe3O4。组员小卫称取6.0g铁的氧化物混合样品,采用如图装置模拟炼铁过程(夹持装置省略),完全反应后,测得实验前后装置B增重4.4g。
(6)实验开始时先打开__________,关闭另一止水夹,让CO通一段时间。
(7)根据实验数据进行计算,该固体样品成分可能是 (填字母序号)。
A.FeO、Fe2O3 B.Fe2O3、Fe3O4
C.FeO、Fe3O4 D.FeO、Fe2O3、Fe3O4
【答案】(1)硬度大、熔点低 (2) (3)氢气##
(4)在白瓷板或玻璃片上放一小片pH试纸,用玻璃棒蘸取溶液滴到pH试纸上,把试纸显示的颜色与标准比色卡比较,读出pH。
(5)石灰石 (6)K2 (7)ACD
三、计算题。
26、某氧化钠样品中含有氯化镁。为测定其中氧化钠的质量分数,称量5.00g样品于烧杯中,加适量水完全溶解,然后逐滴加入氢氧化钠溶液至恰好完全反应,生成0.58g沉淀。请回答下列问题:
(1)氢氧化钠溶液可使紫色石蕊溶液变成___________色。
(2)计算该样品中氧化钠的质量分数为____________。
【答案】(1)蓝 (2)81%
沪教版(全国)第七章 应用广泛的酸、碱、盐
一、选择题。
1、20gKOH加入100g水中,配制成溶液。下列说法错误的是( )
A.KOH在水中解离出K+和OH-
B.一个K+带一个单位正电荷
C.该溶液的溶质质量分数为20%
D.向该溶液中滴入酚酞指示剂,溶液变红
2、下列物质与水充分相混后,能使紫色石蕊试液变蓝色的是( )
A.H2SO4 B.NH3 C.NaCl D.Cu(OH)2
3、现有甲、乙、丙三种金属,先将三者分别加入到硫酸亚铁溶液中,只有甲可使溶液中析出铁单质。再将三者加入到硝酸银溶液中,只有乙不能使溶液中析出银单质,则三者的金属活动性从强到弱的顺序是( )
A.甲>乙>丙 B.乙>甲>丙 C.甲>丙>乙 D.无法判断
4、下列有关化肥或农药的叙述错误的是( )
A.硫酸铵属于复合肥料,所含的营养元素是氮和硫
B.氯化铵和磷矿粉从外观即可区分
C.农药施用后,会通过农作物、农产品等发生转移
D.化肥和农药施用不当,会对环境造成污染
5、劳动创造美好生活。下列劳动项目所涉及的化学知识正确的是( )
选项 劳动项目 化学知识
A 用含洗涤剂的水洗管具上的油污 发生了乳化
B 清理家中鱼缸并通入空气 空气中的氧气易溶于水
C 给校园中的花草施用草木灰(含K2CO3) K2CO3属于复合肥料
D 用食醋去除热水瓶内壁的水垢 食醋的pH>7
A.A B.B C.C D.D
6、下列物质能与NaOH反应的是( )
A.Fe B.CO2 C.Fe2O3 D.NaCl
7、如图所示是分子运动现象的实验探究,不能得到的结论是( )
A.氨分子是不断运动的 B.水能使酚酞溶液变红
C.氨水能使无色酚酞变红 D.氨气溶于水形成氨水
8、下列关于氢氧化钠的描述中不正确的是( )
A.曝露在空气中易潮解 B.能与酸发生中和反应
C.其水溶液能使石蕊溶液变红 D.对皮肤有强烈的腐蚀作用
9、如图所示,U型管内a、b液面相平,当挤压滴管的胶头,使试剂X进入锥形瓶内,一段时间后会观察到a液面高于b液面。则试剂X、Y的组合可能是( )
A.水、硝酸铵 B.水、烧碱
C.稀硫酸、铁粉 D.稀盐酸、小苏打
10、在pH=11的无色溶液中,下列离子能大量共存的是( )
A.Na+ Fe2+ Cl- B.Mg2+ Na+ Cl-
C.Ag+ K+ Cl- D.Na+ K+
11、向一定质量的FeCl3溶液中滴加NaOH溶液一段时间后,改为滴加稀盐酸,所得沉淀质量随加入试剂总体积的变化趋势如图所示。下列说法正确的是( )
A.a点时溶液中一定存在Fe3+
B.c点时所加试剂是NaOH溶液
C.加入试剂总体积为V1时,溶液中不存在NaOH
D.d点时溶液中的溶质不只是盐
12、下列化学实验不能实现实验目的的是( )
A.检验二氧化碳是否收集满
B.测试某溶液的酸碱度
C.量取3mL液体
D.分离溶液中的固态物质
13、将适量的铜粉和镁粉的混合物放入一定量的硝酸银溶液中,充分反应后过滤,得到固体物质和无色滤液,则关于滤出的固体和无色滤液的下列判断正确的是( )
A.滤出的固体中一定含有银和铜,一定不含镁
B.滤出的固体中一定含有银,可能含有铜和镁
C.滤液中一定含有硝酸银和硝酸镁,一定没有硝酸铜
D.滤液中一定含有硝酸镁,一定没有硝酸银和硝酸铜
*14、钯(Pd)是一种稀有的贵金属,钯镍合金在电子工业等有广泛应用。已知钯、镍、铜三种金属的活动性强弱顺序是Ni>Cu>Pd,下列实验可以验证三者金属活动性强弱的实验组合是( )
①Cu+硝酸镍溶液 ②Pd+稀盐酸 ③Pd+硫酸铜溶液 ④Ni+稀盐酸
A.①② B.①③ C.②③ D.②④
15、下列4个图像分别对应4个变化过程,其中正确的是( )
A.电解水
B.将一定量的60℃硝酸钾饱和溶液冷却至室温
C.等质量的镁、铝分别与相同浓度的足量稀硫酸反应
D.向一定量CuSO4和K2SO4混合溶液中,不断加入KOH溶液
二、填空题。
16、现有白纸,溶质质量分数分别为:A、10%的NaOH溶液;B、5%的硫酸溶液;C、5%的紫色石蕊试液。试设计出《“雨”落叶出红花开》的趣味实验:先在白纸上用玻璃棒蘸取__________(填编号,下同)画上花,再蘸__________画上叶,将白纸挂上墙,用_________向纸上喷洒即可,实验的化学原理是_________________________________________。
17、回答下列下列生活、生产中的一些问题:
(1)如图是家庭中一些常见物质的pH.要减轻被蚂蚁叮咬后(向人体注入了甲酸)出现的皮肤搔痒、红肿症状,最适宜涂抹上表中的物质________(写名称)。
(2)工业用盐酸除铁锈,向盛有生锈的铁制零件的容器内加入足量的稀盐酸,首先观察到的现象是________,________,反应的化学方程式为________;放置一段时间,观察到的现象是________,反应的化学方程式为________。
(3)农药“波尔多液”可以杀灭柑橘上的害虫,它是将熟石灰加入硫酸铜溶液中搅拌而成,其混合时反应的化学方程式为________。
(4)烧碱固体如果暴露在空气中或密封不严,容易________潮解,还能与________反应,所以必须密封保存。写出烧碱变质的化学方程式________。
18、厨房里有两瓶白色固体,分别为食盐(NaCl) 和纯碱(Na2CO3)。
(1)可用于腌制肉类和蔬菜,使食物不易腐败的是 。
(2)为鉴别这两种物质,某同学取少量白色固体,进行如下实验。
方案一:分别滴加少量食醋,有气泡产生的是 。
方案二:加水溶解,分别滴加 溶液,有沉淀产生的是纯碱。
19、根据下列两组实验回答问题:
(1)图中仪器a的名称是 ,两组实验都用到的仪器是 。
(2)指出甲实验中的不正确操作 。
(3)乙实验中,正确的操作顺序为(填序号)②→ → → 。
20、判断题:
(1)氢氧化铝可治疗胃酸过多,故氢氧化钠也可治疗胃酸过多( )
(2)生锈的铁钉加入适量的稀盐酸后溶液也会变成浅绿色( )
(3)用稀盐酸除去水垢( )
(4)铁能与氢氧化钠溶液反应放出氢气( )
(5)“要留清白在人间”实现了从Ca(OH)2到CaCO3的转化( )
21、张老师上课时做了趣味实验:他选择了一种指示剂(无色酚酞试液或紫色石蕊试液)、稀盐酸、稀NaOH溶液。他先用玻璃棒蘸取某种指示剂在白纸上写上“化学”,可是学生什么也看不见。然后用某种物质喷洒在白纸上,出现了红色的“化学”二字。接着,又向纸上喷洒另一种物质,红字消失。则他选用的指示剂是 ,先喷洒的物质是 ,后喷洒的物质为 。如果选用另一种指示剂。情况会怎样?
22、把相同体积、相同质量分数的稀盐酸,分别滴到等质量、颗粒大小相同的X、Y、Z三种较活泼金属中,生成H2的质量与反应时间的关系如下图所示。这三种金属的活动性顺序为 ;假如X、Y、Z都是+2价金属,则相对原子质量由大到小的顺序为 。
23、无土栽培是利用营养液栽培作物的一种方法。
(1)下列化学肥料中属于复合肥的是 (填序号);
①硝酸铵 ②磷酸二氢铵 ③硝酸钾 ④硫酸钾
(2)某同学要在实验室配制150g溶质质量分数为2%的硝酸钾溶液,需要硝酸钾的质量为 g。
三、实验和综合应用题。
24、随着世界人口的增长,人类对农产品需求量增大,增施化肥逐渐成为农作物增产的最有力措施。NH4HCO3、NH4Cl、K2SO4、KCl都是常见的化肥。
(1)化肥能为农作物补充的营养元素主要有三种,上述化肥不能提供的营养元素是___________。
(2)有一包用剩的肥料,可能含有上述四种化肥中的一种或几种,为确定其成分,进行了如下实验:
a、取少量肥料样品于研钵中,加入少量熟石灰混合研磨,有刺激性气味。
b、取少量肥料样品于烧杯中,加水溶解,得到无色溶液A。
c、取少量溶液A于试管中,滴加AgNO3溶液,有白色沉淀产生。
d、取少量溶液A于试管中,滴加BaCl2溶液,无明显现象。
e、取少量溶液A于试管中,滴加稀盐酸,无明显现象。
①分析上述实验过程,可得该肥料一定有___________,一定没有___________,可能有___________。
②实验a~e中,不必要进行的一项是___________(填标号)。
③设计实验方案进一步确定该肥料的成分,完成下表。(已知:)
实验操作 预期现象与结论
取少量样品于试管中,并加热至无刺激性气味的气体产生为止,待冷却后,加入足量的水溶解后,往试管里加入少量___________溶液,振荡后观察现象。 若___________,则该肥料的成分是NH4Cl、KCl。
25、金属材料在生活中随处可见。某学习小组围绕金属材料展开项目式学习。
【项目一】金属的物理性质
(1)316不锈钢与组成它的纯金属相比,有良好的___________ 。
【项目二】金属的化学性质
(2)组员小王将打磨后的镁条放入硫酸铜溶液中,发生反应的化学方程式为__________ 。
组员小李意外发现镁条表面还有气泡产生,于是学习小组对此展开探究。
(3)小王用拇指堵住试管,收集一会气体之后伸入燃着的木条,发出尖锐的爆鸣声,说明该气体是__________。
【提出问题】为什么会产生该气体呢?
【作出猜想】硫酸铜溶液显酸性,所以放入镁条后会产生该气体。
【实验验证】
(4)用pH试纸测量硫酸铜溶液的pH,实验操作是__________ 。经测定,溶液pH<7,证实猜想正确。
【项目三】冶炼金属
(5)冶炼金属铁的原料有铁矿石、焦炭、__________、热空气。
铁的氧化物有FeO、Fe2O3、Fe3O4。组员小卫称取6.0g铁的氧化物混合样品,采用如图装置模拟炼铁过程(夹持装置省略),完全反应后,测得实验前后装置B增重4.4g。
(6)实验开始时先打开__________,关闭另一止水夹,让CO通一段时间。
(7)根据实验数据进行计算,该固体样品成分可能是 (填字母序号)。
A.FeO、Fe2O3 B.Fe2O3、Fe3O4
C.FeO、Fe3O4 D.FeO、Fe2O3、Fe3O4
三、计算题。
26、某氧化钠样品中含有氯化镁。为测定其中氧化钠的质量分数,称量5.00g样品于烧杯中,加适量水完全溶解,然后逐滴加入氢氧化钠溶液至恰好完全反应,生成0.58g沉淀。请回答下列问题:
(1)氢氧化钠溶液可使紫色石蕊溶液变成___________色。
(2)计算该样品中氧化钠的质量分数为____________。
2022—2023学年化学沪教版(全国)九年级下册第七章 应用广泛的酸、碱、盐 分层优选题含答案
沪教版(全国)第七章 应用广泛的酸、碱、盐
一、选择题。
1、20gKOH加入100g水中,配制成溶液。下列说法错误的是( )
A.KOH在水中解离出K+和OH-
B.一个K+带一个单位正电荷
C.该溶液的溶质质量分数为20%
D.向该溶液中滴入酚酞指示剂,溶液变红
【答案】C
2、下列物质与水充分相混后,能使紫色石蕊试液变蓝色的是( )
A.H2SO4 B.NH3 C.NaCl D.Cu(OH)2
【答案】B
3、现有甲、乙、丙三种金属,先将三者分别加入到硫酸亚铁溶液中,只有甲可使溶液中析出铁单质。再将三者加入到硝酸银溶液中,只有乙不能使溶液中析出银单质,则三者的金属活动性从强到弱的顺序是( )
A.甲>乙>丙 B.乙>甲>丙 C.甲>丙>乙 D.无法判断
【答案】C
4、下列有关化肥或农药的叙述错误的是( )
A.硫酸铵属于复合肥料,所含的营养元素是氮和硫
B.氯化铵和磷矿粉从外观即可区分
C.农药施用后,会通过农作物、农产品等发生转移
D.化肥和农药施用不当,会对环境造成污染
【答案】A
5、劳动创造美好生活。下列劳动项目所涉及的化学知识正确的是( )
选项 劳动项目 化学知识
A 用含洗涤剂的水洗管具上的油污 发生了乳化
B 清理家中鱼缸并通入空气 空气中的氧气易溶于水
C 给校园中的花草施用草木灰(含K2CO3) K2CO3属于复合肥料
D 用食醋去除热水瓶内壁的水垢 食醋的pH>7
A.A B.B C.C D.D
【答案】A
6、下列物质能与NaOH反应的是( )
A.Fe B.CO2 C.Fe2O3 D.NaCl
【答案】B
7、如图所示是分子运动现象的实验探究,不能得到的结论是( )
A.氨分子是不断运动的 B.水能使酚酞溶液变红
C.氨水能使无色酚酞变红 D.氨气溶于水形成氨水
【答案】B
8、下列关于氢氧化钠的描述中不正确的是( )
A.曝露在空气中易潮解 B.能与酸发生中和反应
C.其水溶液能使石蕊溶液变红 D.对皮肤有强烈的腐蚀作用
【答案】C
9、如图所示,U型管内a、b液面相平,当挤压滴管的胶头,使试剂X进入锥形瓶内,一段时间后会观察到a液面高于b液面。则试剂X、Y的组合可能是( )
A.水、硝酸铵 B.水、烧碱
C.稀硫酸、铁粉 D.稀盐酸、小苏打
【答案】A
10、在pH=11的无色溶液中,下列离子能大量共存的是( )
A.Na+ Fe2+ Cl- B.Mg2+ Na+ Cl-
C.Ag+ K+ Cl- D.Na+ K+
【答案】D
11、向一定质量的FeCl3溶液中滴加NaOH溶液一段时间后,改为滴加稀盐酸,所得沉淀质量随加入试剂总体积的变化趋势如图所示。下列说法正确的是( )
A.a点时溶液中一定存在Fe3+
B.c点时所加试剂是NaOH溶液
C.加入试剂总体积为V1时,溶液中不存在NaOH
D.d点时溶液中的溶质不只是盐
【答案】C
12、下列化学实验不能实现实验目的的是( )
A.检验二氧化碳是否收集满
B.测试某溶液的酸碱度
C.量取3mL液体
D.分离溶液中的固态物质
【答案】B
13、将适量的铜粉和镁粉的混合物放入一定量的硝酸银溶液中,充分反应后过滤,得到固体物质和无色滤液,则关于滤出的固体和无色滤液的下列判断正确的是( )
A.滤出的固体中一定含有银和铜,一定不含镁
B.滤出的固体中一定含有银,可能含有铜和镁
C.滤液中一定含有硝酸银和硝酸镁,一定没有硝酸铜
D.滤液中一定含有硝酸镁,一定没有硝酸银和硝酸铜
【答案】B
*14、钯(Pd)是一种稀有的贵金属,钯镍合金在电子工业等有广泛应用。已知钯、镍、铜三种金属的活动性强弱顺序是Ni>Cu>Pd,下列实验可以验证三者金属活动性强弱的实验组合是( )
①Cu+硝酸镍溶液 ②Pd+稀盐酸 ③Pd+硫酸铜溶液 ④Ni+稀盐酸
A.①② B.①③ C.②③ D.②④
【答案】B
15、下列4个图像分别对应4个变化过程,其中正确的是( )
A.电解水
B.将一定量的60℃硝酸钾饱和溶液冷却至室温
C.等质量的镁、铝分别与相同浓度的足量稀硫酸反应
D.向一定量CuSO4和K2SO4混合溶液中,不断加入KOH溶液
【答案】B
二、填空题。
16、现有白纸,溶质质量分数分别为:A、10%的NaOH溶液;B、5%的硫酸溶液;C、5%的紫色石蕊试液。试设计出《“雨”落叶出红花开》的趣味实验:先在白纸上用玻璃棒蘸取__________(填编号,下同)画上花,再蘸__________画上叶,将白纸挂上墙,用_________向纸上喷洒即可,实验的化学原理是_________________________________________。
【答案】B A C 紫色石蕊试液遇酸变红、遇碱变蓝
17、回答下列下列生活、生产中的一些问题:
(1)如图是家庭中一些常见物质的pH.要减轻被蚂蚁叮咬后(向人体注入了甲酸)出现的皮肤搔痒、红肿症状,最适宜涂抹上表中的物质________(写名称)。
(2)工业用盐酸除铁锈,向盛有生锈的铁制零件的容器内加入足量的稀盐酸,首先观察到的现象是________,________,反应的化学方程式为________;放置一段时间,观察到的现象是________,反应的化学方程式为________。
(3)农药“波尔多液”可以杀灭柑橘上的害虫,它是将熟石灰加入硫酸铜溶液中搅拌而成,其混合时反应的化学方程式为________。
(4)烧碱固体如果暴露在空气中或密封不严,容易________潮解,还能与________反应,所以必须密封保存。写出烧碱变质的化学方程式________。
【答案】(1)牙膏
(2) 红棕色逐渐消失 溶液由无色变成黄色
Fe2O3+6HCl=2FeCl3+3H2O 有气泡产生,溶液变为浅绿色
Fe+2HCl=FeCl2+H2↑
(3)CuSO4+Ca(OH)2=Cu(OH)2↓+CaSO4
(4) 吸收水分 二氧化碳或CO2 CO2+2NaOH=Na2CO3+H2O
18、厨房里有两瓶白色固体,分别为食盐(NaCl) 和纯碱(Na2CO3)。
(1)可用于腌制肉类和蔬菜,使食物不易腐败的是 。
(2)为鉴别这两种物质,某同学取少量白色固体,进行如下实验。
方案一:分别滴加少量食醋,有气泡产生的是 。
方案二:加水溶解,分别滴加 溶液,有沉淀产生的是纯碱。
【答案】食盐; 碳酸钠; 氯化钙(合理即可)
19、根据下列两组实验回答问题:
(1)图中仪器a的名称是 ,两组实验都用到的仪器是 。
(2)指出甲实验中的不正确操作 。
(3)乙实验中,正确的操作顺序为(填序号)②→ → → 。
【答案】(1)漏斗 玻璃棒
(2)用镊子夹取pH试纸放入待测液中 (3)① ④ ③
20、判断题:
(1)氢氧化铝可治疗胃酸过多,故氢氧化钠也可治疗胃酸过多( )
(2)生锈的铁钉加入适量的稀盐酸后溶液也会变成浅绿色( )
(3)用稀盐酸除去水垢( )
(4)铁能与氢氧化钠溶液反应放出氢气( )
(5)“要留清白在人间”实现了从Ca(OH)2到CaCO3的转化( )
【答案】(1)错误 (2)错误 (3)正确 (4)错误 (5)正确
21、张老师上课时做了趣味实验:他选择了一种指示剂(无色酚酞试液或紫色石蕊试液)、稀盐酸、稀NaOH溶液。他先用玻璃棒蘸取某种指示剂在白纸上写上“化学”,可是学生什么也看不见。然后用某种物质喷洒在白纸上,出现了红色的“化学”二字。接着,又向纸上喷洒另一种物质,红字消失。则他选用的指示剂是 ,先喷洒的物质是 ,后喷洒的物质为 。如果选用另一种指示剂。情况会怎样?
【答案】无色酚酞试液 氢氧化钠溶液 稀盐酸 字先变紫色,喷氢氧化钠后变成蓝色,再喷盐酸字色变化为“蓝→紫→红”
22、把相同体积、相同质量分数的稀盐酸,分别滴到等质量、颗粒大小相同的X、Y、Z三种较活泼金属中,生成H2的质量与反应时间的关系如下图所示。这三种金属的活动性顺序为 ;假如X、Y、Z都是+2价金属,则相对原子质量由大到小的顺序为 。
【答案】Y>X>Z,Z>Y>X.
23、无土栽培是利用营养液栽培作物的一种方法。
(1)下列化学肥料中属于复合肥的是 (填序号);
①硝酸铵 ②磷酸二氢铵 ③硝酸钾 ④硫酸钾
(2)某同学要在实验室配制150g溶质质量分数为2%的硝酸钾溶液,需要硝酸钾的质量为 g。
【答案】 ②③;3
三、实验和综合应用题。
24、随着世界人口的增长,人类对农产品需求量增大,增施化肥逐渐成为农作物增产的最有力措施。NH4HCO3、NH4Cl、K2SO4、KCl都是常见的化肥。
(1)化肥能为农作物补充的营养元素主要有三种,上述化肥不能提供的营养元素是___________。
(2)有一包用剩的肥料,可能含有上述四种化肥中的一种或几种,为确定其成分,进行了如下实验:
a、取少量肥料样品于研钵中,加入少量熟石灰混合研磨,有刺激性气味。
b、取少量肥料样品于烧杯中,加水溶解,得到无色溶液A。
c、取少量溶液A于试管中,滴加AgNO3溶液,有白色沉淀产生。
d、取少量溶液A于试管中,滴加BaCl2溶液,无明显现象。
e、取少量溶液A于试管中,滴加稀盐酸,无明显现象。
①分析上述实验过程,可得该肥料一定有___________,一定没有___________,可能有___________。
②实验a~e中,不必要进行的一项是___________(填标号)。
③设计实验方案进一步确定该肥料的成分,完成下表。(已知:)
实验操作 预期现象与结论
取少量样品于试管中,并加热至无刺激性气味的气体产生为止,待冷却后,加入足量的水溶解后,往试管里加入少量___________溶液,振荡后观察现象。 若___________,则该肥料的成分是NH4Cl、KCl。
【答案】(1)P(磷)
(2) 氯化铵() 碳酸氢铵和硫酸钾() 氯化钾()C 硝酸银() 产生白色沉淀
25、金属材料在生活中随处可见。某学习小组围绕金属材料展开项目式学习。
【项目一】金属的物理性质
(1)316不锈钢与组成它的纯金属相比,有良好的___________ 。
【项目二】金属的化学性质
(2)组员小王将打磨后的镁条放入硫酸铜溶液中,发生反应的化学方程式为__________ 。
组员小李意外发现镁条表面还有气泡产生,于是学习小组对此展开探究。
(3)小王用拇指堵住试管,收集一会气体之后伸入燃着的木条,发出尖锐的爆鸣声,说明该气体是__________。
【提出问题】为什么会产生该气体呢?
【作出猜想】硫酸铜溶液显酸性,所以放入镁条后会产生该气体。
【实验验证】
(4)用pH试纸测量硫酸铜溶液的pH,实验操作是__________ 。经测定,溶液pH<7,证实猜想正确。
【项目三】冶炼金属
(5)冶炼金属铁的原料有铁矿石、焦炭、__________、热空气。
铁的氧化物有FeO、Fe2O3、Fe3O4。组员小卫称取6.0g铁的氧化物混合样品,采用如图装置模拟炼铁过程(夹持装置省略),完全反应后,测得实验前后装置B增重4.4g。
(6)实验开始时先打开__________,关闭另一止水夹,让CO通一段时间。
(7)根据实验数据进行计算,该固体样品成分可能是 (填字母序号)。
A.FeO、Fe2O3 B.Fe2O3、Fe3O4
C.FeO、Fe3O4 D.FeO、Fe2O3、Fe3O4
【答案】(1)硬度大、熔点低 (2) (3)氢气##
(4)在白瓷板或玻璃片上放一小片pH试纸,用玻璃棒蘸取溶液滴到pH试纸上,把试纸显示的颜色与标准比色卡比较,读出pH。
(5)石灰石 (6)K2 (7)ACD
三、计算题。
26、某氧化钠样品中含有氯化镁。为测定其中氧化钠的质量分数,称量5.00g样品于烧杯中,加适量水完全溶解,然后逐滴加入氢氧化钠溶液至恰好完全反应,生成0.58g沉淀。请回答下列问题:
(1)氢氧化钠溶液可使紫色石蕊溶液变成___________色。
(2)计算该样品中氧化钠的质量分数为____________。
【答案】(1)蓝 (2)81%
