第1节空气与氧气(第3课时氧气的实验室制法)
文档属性
| 名称 | 第1节空气与氧气(第3课时氧气的实验室制法) |
|
|
| 格式 | zip | ||
| 文件大小 | 230.3KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2014-05-08 00:00:00 | ||
图片预览



文档简介
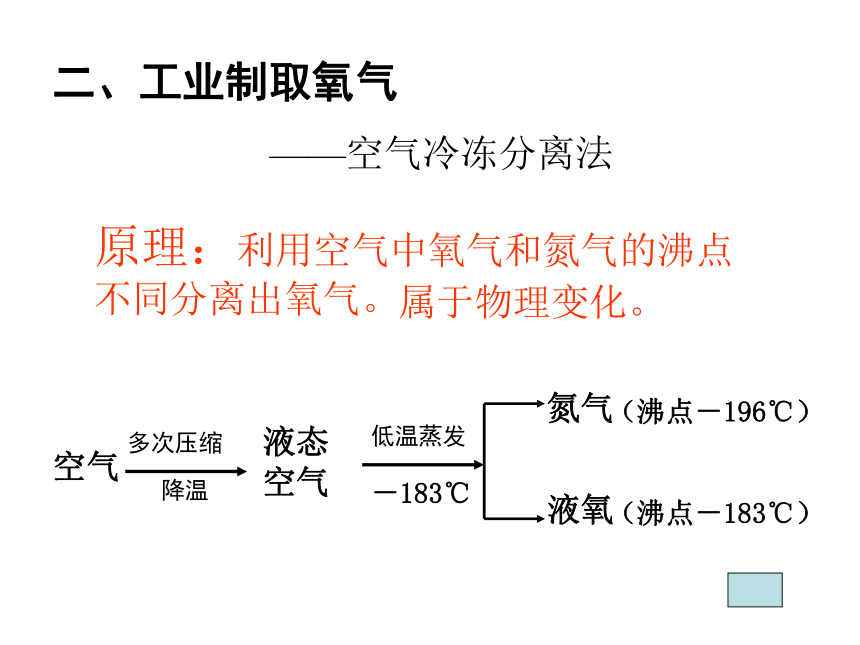
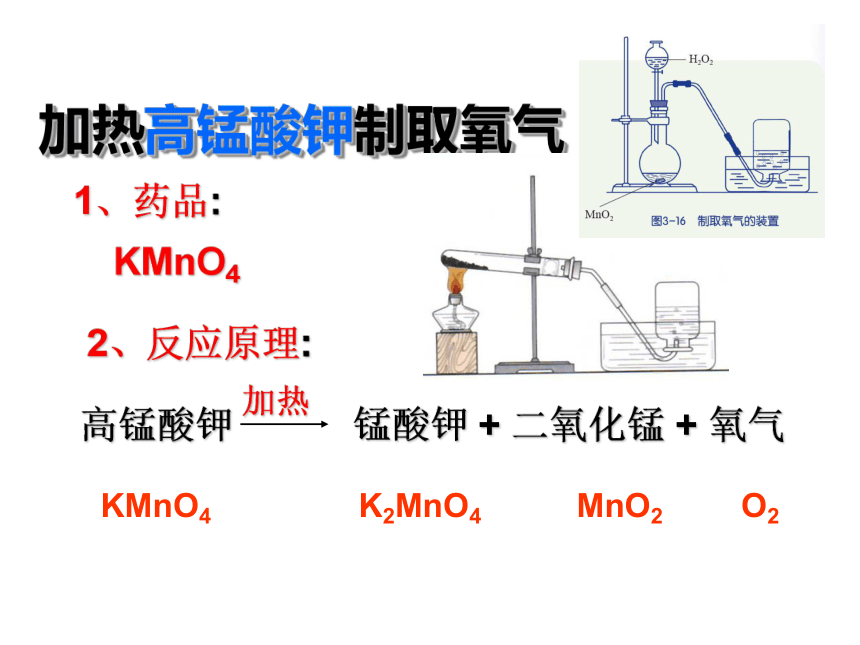
课件15张PPT。过氧化氢 氧气水+高锰酸钾加热锰酸钾 +二氧化锰 +氧气H2O2H2OO2KMnO4K2MnO4MnO2O2氯酸钾二氧化锰( MnO2 )加热氯化钾 +氧气KClO3KClO2二氧化锰( MnO2 )——空气冷冻分离法空气 液态空气液氧(沸点-183℃)原理:利用空气中氧气和氮气的沸点不同分离出氧气。二、工业制取氧气多次压缩低温蒸发降温氮气(沸点-196℃)-183℃属于物理变化。加热高锰酸钾制取氧气2、反应原理:1、药品:KMnO4KMnO4K2MnO4MnO2O2发生装置收集装置试 管带铁夹铁架台酒精灯带导管的橡皮塞集气瓶水槽
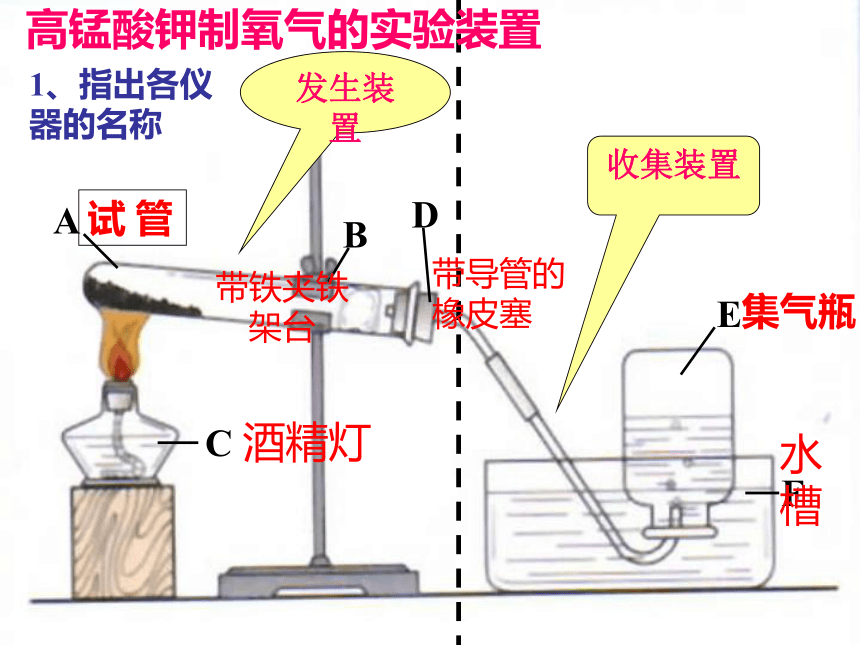
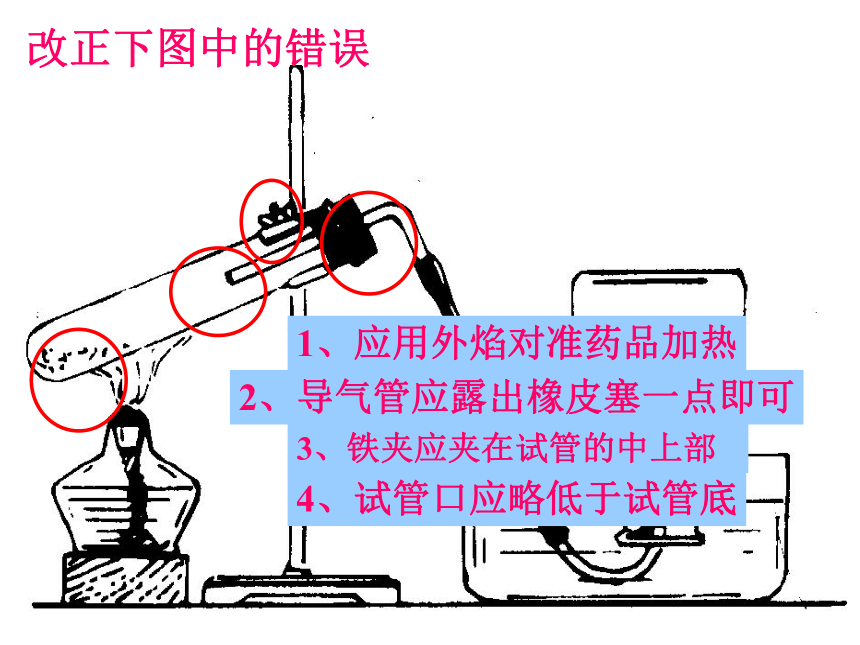
高锰酸钾制氧气的实验装置1、指出各仪器的名称(1)试管口为什么要略向下倾斜? 防止冷凝的水回流到热的试管底部,使试管炸裂。讨论(2)为什么要在试管口放一团棉花? 为了防止加热时高锰酸钾粉末进入导管到水槽中,甚至堵塞导管。(3)实验结束时为什么要先从水槽中取出导管,后熄灭酒精灯?防止水倒吸回热的试管,使试管炸裂。改正下图中的错误3、铁夹应夹在试管的中上部4、试管口应略低于试管底1、应用外焰对准药品加热2、导气管应露出橡皮塞一点即可小结:实验室制取气体的装置实验装置发
生
装
置收
集
装
置向上排空气法向下排空气法排水集气法过氧化氢 氧气水+高锰酸钾加热锰酸钾 +二氧化锰 +氧气H2O2H2OO2KMnO4K2MnO4MnO2O2二氧化锰( MnO2 )FeO2Fe3O4+点燃硫氧气二氧化硫SO2SO2过氧化氢 氧气水+高锰酸钾加热锰酸钾 +二氧化锰 +氧气H2O2H2OO2KMnO4K2MnO4MnO2O2二氧化锰( MnO2 ) 由一种反应物生成两种或两种以上其他物质的反应。分解反应:FeO2Fe3O4+点燃硫氧气二氧化硫SO2SO2 由两种或两种以上的物质生成一种物质的反应叫化合反应。化合反应:2.以下有四种制取氧气的方法,其中有一种方法与其他三种方法有本质的不同,该方法是( ) A.分离液态空气 B.加热氯酸钾 C.加热高锰酸钾 D.电解水
3、实验室用过氧化氢和二氧化锰代替高锰酸钾加热制取氧气的优点是 。
①生成物无污染 ②不需加热 ③需加热
④操作简便基础巩固A ① ② ④ ⑶利用改进后的装置进行实验,有如下操作步骤:①将药品装入锥形瓶,塞上带导管的橡皮塞
②检查装置的气密性
③将收集好的氧气正放在桌面上
④用排水法收集氧气
⑤组装仪器
正确的操作步骤是
。
⑤ ② ① ④ ③反应物都是固体,反应需要加热反应物是固体和液体的混合物,
反应不需要加热固液不加热型固固加热型怎样检查装置的气密性?【原理】升高温度,使试管内空气受热膨胀。【方法】将导管伸入烧杯中,双手紧握试管,一段时间后若导管口有气泡冒出,说明装置气密性良好。
高锰酸钾制氧气的实验装置1、指出各仪器的名称(1)试管口为什么要略向下倾斜? 防止冷凝的水回流到热的试管底部,使试管炸裂。讨论(2)为什么要在试管口放一团棉花? 为了防止加热时高锰酸钾粉末进入导管到水槽中,甚至堵塞导管。(3)实验结束时为什么要先从水槽中取出导管,后熄灭酒精灯?防止水倒吸回热的试管,使试管炸裂。改正下图中的错误3、铁夹应夹在试管的中上部4、试管口应略低于试管底1、应用外焰对准药品加热2、导气管应露出橡皮塞一点即可小结:实验室制取气体的装置实验装置发
生
装
置收
集
装
置向上排空气法向下排空气法排水集气法过氧化氢 氧气水+高锰酸钾加热锰酸钾 +二氧化锰 +氧气H2O2H2OO2KMnO4K2MnO4MnO2O2二氧化锰( MnO2 )FeO2Fe3O4+点燃硫氧气二氧化硫SO2SO2过氧化氢 氧气水+高锰酸钾加热锰酸钾 +二氧化锰 +氧气H2O2H2OO2KMnO4K2MnO4MnO2O2二氧化锰( MnO2 ) 由一种反应物生成两种或两种以上其他物质的反应。分解反应:FeO2Fe3O4+点燃硫氧气二氧化硫SO2SO2 由两种或两种以上的物质生成一种物质的反应叫化合反应。化合反应:2.以下有四种制取氧气的方法,其中有一种方法与其他三种方法有本质的不同,该方法是( ) A.分离液态空气 B.加热氯酸钾 C.加热高锰酸钾 D.电解水
3、实验室用过氧化氢和二氧化锰代替高锰酸钾加热制取氧气的优点是 。
①生成物无污染 ②不需加热 ③需加热
④操作简便基础巩固A ① ② ④ ⑶利用改进后的装置进行实验,有如下操作步骤:①将药品装入锥形瓶,塞上带导管的橡皮塞
②检查装置的气密性
③将收集好的氧气正放在桌面上
④用排水法收集氧气
⑤组装仪器
正确的操作步骤是
。
⑤ ② ① ④ ③反应物都是固体,反应需要加热反应物是固体和液体的混合物,
反应不需要加热固液不加热型固固加热型怎样检查装置的气密性?【原理】升高温度,使试管内空气受热膨胀。【方法】将导管伸入烧杯中,双手紧握试管,一段时间后若导管口有气泡冒出,说明装置气密性良好。
同课章节目录
- 第1章 电与磁
- 第1节 指南针为什么能指方向
- 第2节 电生磁
- 第3节 电磁铁的应用
- 第4节 电动机
- 第5节 磁生电
- 第6节 家庭用电
- 第7节 电的安全使用
- 第2章 微粒的模型与符号
- 第1节 模型、符号的建立与作用
- 第2节 物质的微观粒子模型
- 第3节 原子结构的模型
- 第4节 组成物质的元素
- 第5节 表示元素的符号
- 第6节 表示物质的符号
- 第7节 元素符号表示的量
- 第3章 空气与生命
- 第1节 空气与氧气
- 第2节 氧化和燃烧
- 第3节 化学方程式
- 第4节 二氧化碳
- 第5节 生物的呼吸和呼吸作用
- 第6节 光合作用
- 第7节 自然界中的氧循环和碳循环
- 第8节 空气污染与保护
- 第4章 植物与土壤
- 第1节 土壤的成分
- 第2节 各种各样的土壤
- 第3节 植物的根与物质吸收
- 第4节 植物的茎与物质运输
- 第5节 植物的叶与蒸腾作用
- 第6节 保护土壤
- 研究性学习课题
- 一 设计简单的电磁控制电路
- 二 化学反应中质量守恒的研究
- 三 研究植物的呼吸
- 四 当地水土状况调查
