第3节 化学方程式(3)——化学方程式复习
文档属性
| 名称 | 第3节 化学方程式(3)——化学方程式复习 |

|
|
| 格式 | zip | ||
| 文件大小 | 503.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2014-05-25 00:00:00 | ||
图片预览




文档简介
课件18张PPT。——化学方程式复习第3节 化学方程式 用化学式来表示化学反应的式子叫化学方程式.一、化学方程式1、定义:2、书写原则:A.以客观事实为依据;
(反应物生成物要符合实际)B.符合质量守恒定律。
(反应前后两边的
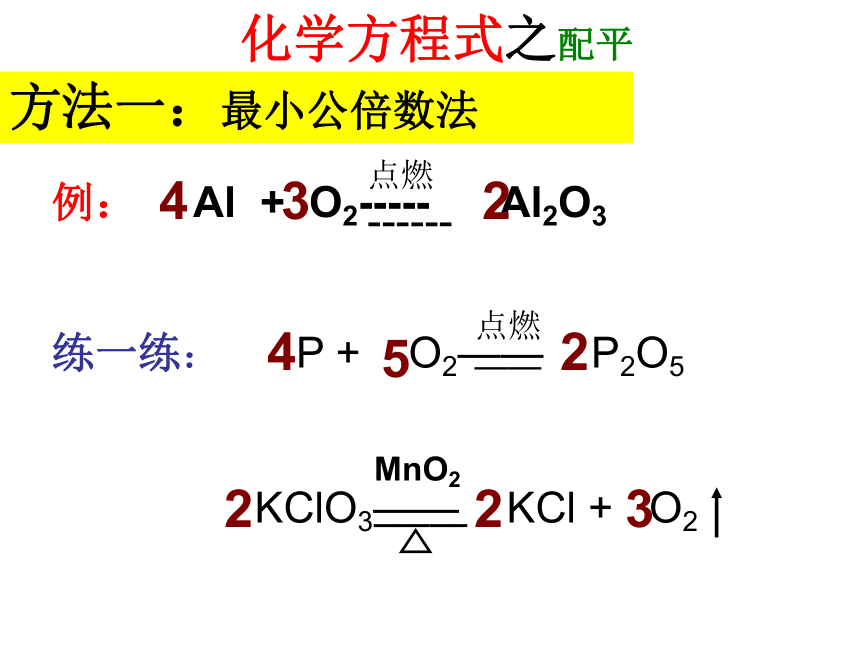
原子个数必须相等)化学式要书写正确配平 左 (短线连接) 右 反应物分子式 生成物分子式O2P+P2O5红磷燃烧的化学反应方程式45点燃1.写2.配3.注2二、化学方程式书写步骤化学方程式之正确书写化学式按要求书写化学式:例:(1)磷在氧气中燃烧的产物P2O5练:(1)硫在氧气中燃烧的产物 (2)高锰酸钾 (3)碳酸钙KMnO4CaCO3 (2)铁在氧气中燃烧的产物(3)锰酸钾 (4)氯酸钾 (5)氯化钾 (6)碳酸钠 (7)过氧化氢(8)碳酸 (9)氢氧化钙(10)葡萄糖 方法一:最小公倍数法练一练: P + O2—— P2O5
KClO3—— KCl + O24522点燃
——化学方程式之配平例: Al + O2----- Al2O3 324点燃
------MnO2
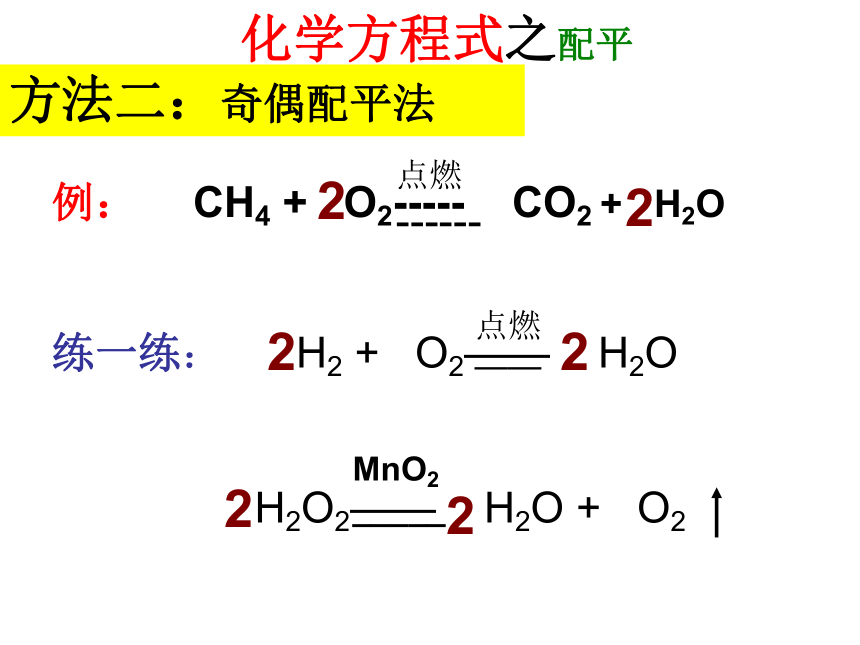
_____23练一练: H2 + O2—— H2O
H2O2—— H2O + O2222点燃
——化学方程式之配平例: CH4 + O2----- CO2 + H2O22点燃
------MnO2
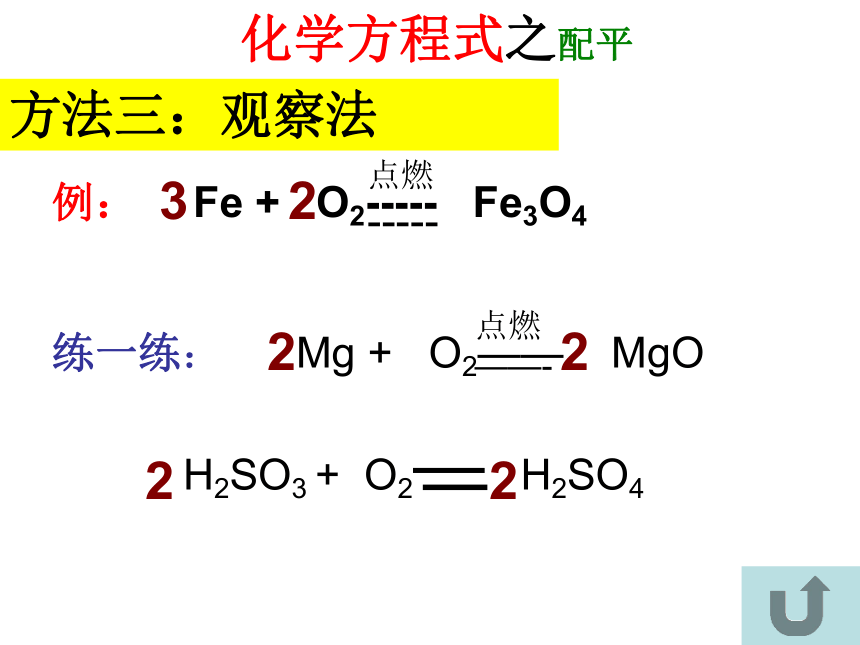
_____2方法二:奇偶配平法练一练: Mg + O2—— MgO
H2SO3 + O2— H2SO4222点燃
——-化学方程式之配平例: Fe + O2----- Fe3O42点燃
-----23方法三:观察法化学方程式之注明反应条件 注明反应发生的外加条件:加热“ ” 、点燃、催化剂(如MnO2)、高温、通电等,用等号把反应物与生成物连接起来;生成物中的气体和沉淀要用“↑”和“↓”标明。2KMnO4 K2MnO4+MnO2+O22H2O2—— 2H2O + O2CO2 + Ca(OH)2 = CaCO3↓+ H2OMnO2教你一招 没有学过的化学方程式更简单,
因为题目中有提示!把题目的提示
拿来用就是!没有学过的化学方程式怎么写?下面是自来水消毒过程中发生反应的微观图,产物之一是次氯酸(HClO),具有杀菌消毒作用。
请写出该反应的化学方程式为 。Cl2H2OHClHClO试一试再试试 我国陈亁旺等科学家的最新研究表明,在高温高压下,二氧化碳和金属钠反应产生金刚石和碳酸钠,合成的金刚石最大直径达1.2毫米,完全可以满足工业用途。二氧化碳和反应生成金刚石和碳酸钠的化学方程式为 CO2+ Na C+ Na2CO3342高温高压1、铁、镁、铝分别在氧气中燃烧;
2、碳、硫、磷分别在空气中燃烧;
3、分别用过氧化氢、氯酸钾、高锰酸钾制氧气
4、二氧化碳分别与水、石灰水反应;
5、实验室和工业上分别制取二氧化碳;
6、酸碱灭火器原理。写出下列各反应的化学方程式:1、质的方面:
表示参加反应是什么物质,结果生成什么物质;
表示反应物在什么条件下进行反应。2、量的方面:
表示反应物、生成物各物质之间的分子数比;
表示反应物、生成物各物质之间的质量比。三、化学方程式的涵义12+(1×4)2×(16 × 2)1664算一算相对原子质量:H-1 C-12 O-16 S-32 Cl-35.5 K-39 Ca-40试计算下列化学式的相对质量2H2O2 CaCO3 2KClO3 3O26824510096完全燃烧多少克镁,可生成10克氧化镁?(Mg:24 O:16)解:设需完全燃烧镁X 。488010gx = 6 g答:完全燃烧6克镁,可生成10克氧化镁。【解题步骤】(1)设未知量(2)写出反应的化学方程式(3)找:计算相关物质的相对分子质量及质量比 标出已知量、未知量(4)列比例式求解(5)简明地写出答案【书写格式】x四、依据化学方程式计算练习1:实验室里用加热氯酸钾和二氧化锰的混合物制取氧气,现将氯酸钾和二氧化锰混合物25克加热至气体不再产生,称得剩余固体的质量为15.4克, 问:(1)产生氧气多少克?(2)原混合物中含氯酸钾多少克?解:氧气的质量为:25克-15.4克=9.6克设:原混合物中含氯酸钾X。245969.6克X答:产生氧气9.6克,原混合物中含氯酸钾24.5克。X=24.5克练习2:实验室里用50克含6.8%的过氧化氢的双氧水溶液在二氧化锰作催化剂条件下制取氧气。问:(1)可制得氧气多少克? (2)若氧气的密度是1.43克/升,求制得的氧气体积是多少升?(H:1 O:16)解:过氧化氢的质量为:50克×6.8%=3.4克设:可制得氧气X。68323.4克X答:产生氧气1.6克,合体积1.12升。X=1.6克∴ V = m/ρ =1.6g÷1.43g/L = 1.12L同学们,再见!
(反应前后两边的
原子个数必须相等)化学式要书写正确配平 左 (短线连接) 右 反应物分子式 生成物分子式O2P+P2O5红磷燃烧的化学反应方程式45点燃1.写2.配3.注2二、化学方程式书写步骤化学方程式之正确书写化学式按要求书写化学式:例:(1)磷在氧气中燃烧的产物P2O5练:(1)硫在氧气中燃烧的产物 (2)高锰酸钾 (3)碳酸钙KMnO4CaCO3 (2)铁在氧气中燃烧的产物(3)锰酸钾 (4)氯酸钾 (5)氯化钾 (6)碳酸钠 (7)过氧化氢(8)碳酸 (9)氢氧化钙(10)葡萄糖 方法一:最小公倍数法练一练: P + O2—— P2O5
KClO3—— KCl + O24522点燃
——化学方程式之配平例: Al + O2----- Al2O3 324点燃
------MnO2
_____23练一练: H2 + O2—— H2O
H2O2—— H2O + O2222点燃
——化学方程式之配平例: CH4 + O2----- CO2 + H2O22点燃
------MnO2
_____2方法二:奇偶配平法练一练: Mg + O2—— MgO
H2SO3 + O2— H2SO4222点燃
——-化学方程式之配平例: Fe + O2----- Fe3O42点燃
-----23方法三:观察法化学方程式之注明反应条件 注明反应发生的外加条件:加热“ ” 、点燃、催化剂(如MnO2)、高温、通电等,用等号把反应物与生成物连接起来;生成物中的气体和沉淀要用“↑”和“↓”标明。2KMnO4 K2MnO4+MnO2+O22H2O2—— 2H2O + O2CO2 + Ca(OH)2 = CaCO3↓+ H2OMnO2教你一招 没有学过的化学方程式更简单,
因为题目中有提示!把题目的提示
拿来用就是!没有学过的化学方程式怎么写?下面是自来水消毒过程中发生反应的微观图,产物之一是次氯酸(HClO),具有杀菌消毒作用。
请写出该反应的化学方程式为 。Cl2H2OHClHClO试一试再试试 我国陈亁旺等科学家的最新研究表明,在高温高压下,二氧化碳和金属钠反应产生金刚石和碳酸钠,合成的金刚石最大直径达1.2毫米,完全可以满足工业用途。二氧化碳和反应生成金刚石和碳酸钠的化学方程式为 CO2+ Na C+ Na2CO3342高温高压1、铁、镁、铝分别在氧气中燃烧;
2、碳、硫、磷分别在空气中燃烧;
3、分别用过氧化氢、氯酸钾、高锰酸钾制氧气
4、二氧化碳分别与水、石灰水反应;
5、实验室和工业上分别制取二氧化碳;
6、酸碱灭火器原理。写出下列各反应的化学方程式:1、质的方面:
表示参加反应是什么物质,结果生成什么物质;
表示反应物在什么条件下进行反应。2、量的方面:
表示反应物、生成物各物质之间的分子数比;
表示反应物、生成物各物质之间的质量比。三、化学方程式的涵义12+(1×4)2×(16 × 2)1664算一算相对原子质量:H-1 C-12 O-16 S-32 Cl-35.5 K-39 Ca-40试计算下列化学式的相对质量2H2O2 CaCO3 2KClO3 3O26824510096完全燃烧多少克镁,可生成10克氧化镁?(Mg:24 O:16)解:设需完全燃烧镁X 。488010gx = 6 g答:完全燃烧6克镁,可生成10克氧化镁。【解题步骤】(1)设未知量(2)写出反应的化学方程式(3)找:计算相关物质的相对分子质量及质量比 标出已知量、未知量(4)列比例式求解(5)简明地写出答案【书写格式】x四、依据化学方程式计算练习1:实验室里用加热氯酸钾和二氧化锰的混合物制取氧气,现将氯酸钾和二氧化锰混合物25克加热至气体不再产生,称得剩余固体的质量为15.4克, 问:(1)产生氧气多少克?(2)原混合物中含氯酸钾多少克?解:氧气的质量为:25克-15.4克=9.6克设:原混合物中含氯酸钾X。245969.6克X答:产生氧气9.6克,原混合物中含氯酸钾24.5克。X=24.5克练习2:实验室里用50克含6.8%的过氧化氢的双氧水溶液在二氧化锰作催化剂条件下制取氧气。问:(1)可制得氧气多少克? (2)若氧气的密度是1.43克/升,求制得的氧气体积是多少升?(H:1 O:16)解:过氧化氢的质量为:50克×6.8%=3.4克设:可制得氧气X。68323.4克X答:产生氧气1.6克,合体积1.12升。X=1.6克∴ V = m/ρ =1.6g÷1.43g/L = 1.12L同学们,再见!
同课章节目录
- 第1章 电与磁
- 第1节 指南针为什么能指方向
- 第2节 电生磁
- 第3节 电磁铁的应用
- 第4节 电动机
- 第5节 磁生电
- 第6节 家庭用电
- 第7节 电的安全使用
- 第2章 微粒的模型与符号
- 第1节 模型、符号的建立与作用
- 第2节 物质的微观粒子模型
- 第3节 原子结构的模型
- 第4节 组成物质的元素
- 第5节 表示元素的符号
- 第6节 表示物质的符号
- 第7节 元素符号表示的量
- 第3章 空气与生命
- 第1节 空气与氧气
- 第2节 氧化和燃烧
- 第3节 化学方程式
- 第4节 二氧化碳
- 第5节 生物的呼吸和呼吸作用
- 第6节 光合作用
- 第7节 自然界中的氧循环和碳循环
- 第8节 空气污染与保护
- 第4章 植物与土壤
- 第1节 土壤的成分
- 第2节 各种各样的土壤
- 第3节 植物的根与物质吸收
- 第4节 植物的茎与物质运输
- 第5节 植物的叶与蒸腾作用
- 第6节 保护土壤
- 研究性学习课题
- 一 设计简单的电磁控制电路
- 二 化学反应中质量守恒的研究
- 三 研究植物的呼吸
- 四 当地水土状况调查
