2022—2023学年沪教版(全国)化学九年级下册第七章 应用广泛的酸、碱、盐 培优与检测(含答案)
文档属性
| 名称 | 2022—2023学年沪教版(全国)化学九年级下册第七章 应用广泛的酸、碱、盐 培优与检测(含答案) |  | |
| 格式 | zip | ||
| 文件大小 | 594.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-04-13 10:52:26 | ||
图片预览


文档简介
2022—2023学年沪教版(全国)化学九年级下册第七章 应用广泛的酸、碱、盐 培优与检测含答案
沪教版(全国)第七章 应用广泛的酸、碱、盐 培优与检测
一、选择题。
1、“雪碧”是一种无色的碳酸饮料,将少量“雪碧”滴入紫色石蕊试液中,然后再加热,溶液颜色的变化是( )
A.先变蓝后变紫 B.变红后颜色不再改变
C.先变无色后变红 D.先变红后变紫
2、如图所示的实验中,小烧杯①盛的是紫色石蕊试液,②盛的是浓盐酸。片刻后,可以观察到烧杯①中液体的颜色是( )
A.紫色 B.红色 C.无色 D.蓝色
3、下列物质中,易溶于水其水溶液显碱性的物质是( )
A.氢氧化钾 B.石灰石 C.氢氧化铁 D.消石灰
4、下列各组物质中按酸、碱、盐顺序排列的是( )
A.碳酸钠、硝酸、硫酸锌 B.硫酸亚铁、氢氧化钙、硫酸
C.盐酸、氢氧化镁、硫酸铜 D.氯化钙、碳酸钙、氧化钙
5、下列物质既可以做治疗胃酸的胃药,又可以做面点发酵剂的是( )
A.NaCl B.NaOH C.NaHCO3 D.Na2SO4
6、下列是实验室中常见的几项化学实验基本操作,其中正确的是( )
A.测溶液pH B.检查装置气密性 C.稀释浓硫酸 D.过滤
7、下列物质能与NaOH反应的是( )
A.Fe B.CO2 C.Fe2O3 D.NaCl
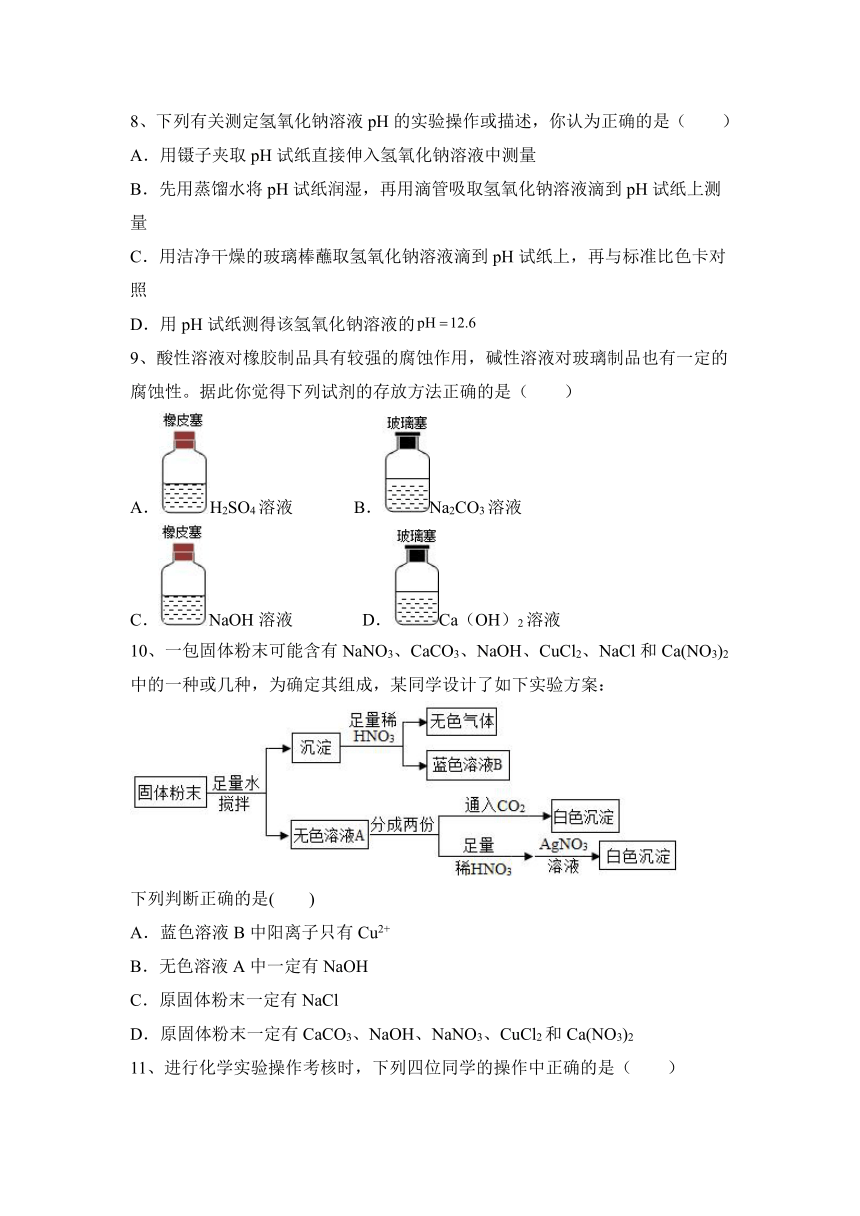
8、下列有关测定氢氧化钠溶液pH的实验操作或描述,你认为正确的是( )
A.用镊子夹取pH试纸直接伸入氢氧化钠溶液中测量
B.先用蒸馏水将pH试纸润湿,再用滴管吸取氢氧化钠溶液滴到pH试纸上测量
C.用洁净干燥的玻璃棒蘸取氢氧化钠溶液滴到pH试纸上,再与标准比色卡对照
D.用pH试纸测得该氢氧化钠溶液的
9、酸性溶液对橡胶制品具有较强的腐蚀作用,碱性溶液对玻璃制品也有一定的腐蚀性。据此你觉得下列试剂的存放方法正确的是( )
A.H2SO4溶液 B.Na2CO3溶液
C.NaOH溶液 D.Ca(OH)2溶液
10、一包固体粉末可能含有NaNO3、CaCO3、NaOH、CuCl2、NaCl和Ca(NO3)2中的一种或几种,为确定其组成,某同学设计了如下实验方案:
下列判断正确的是( )
A.蓝色溶液B中阳离子只有Cu2+
B.无色溶液A中一定有NaOH
C.原固体粉末一定有NaCl
D.原固体粉末一定有CaCO3、NaOH、NaNO3、CuCl2和Ca(NO3)2
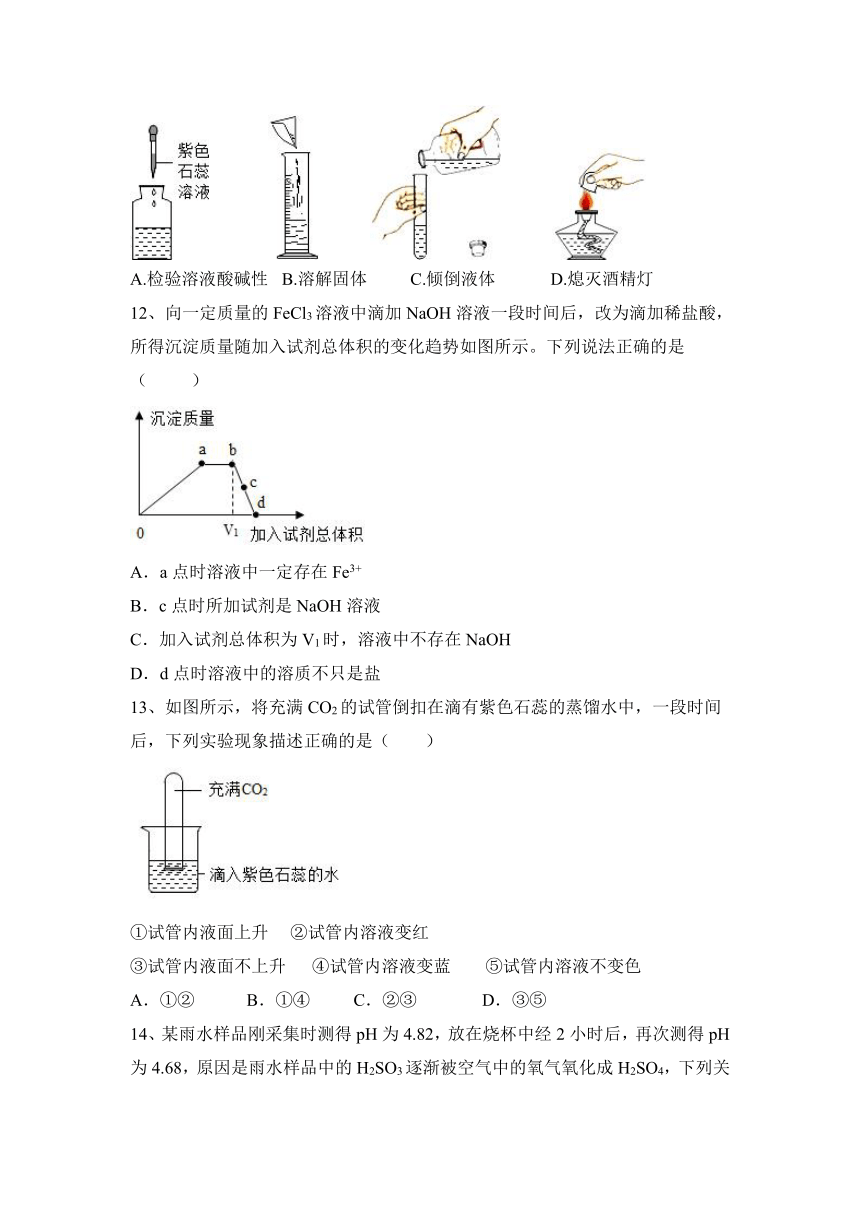
11、进行化学实验操作考核时,下列四位同学的操作中正确的是( )
A.检验溶液酸碱性 B.溶解固体 C.倾倒液体 D.熄灭酒精灯
12、向一定质量的FeCl3溶液中滴加NaOH溶液一段时间后,改为滴加稀盐酸,所得沉淀质量随加入试剂总体积的变化趋势如图所示。下列说法正确的是( )
A.a点时溶液中一定存在Fe3+
B.c点时所加试剂是NaOH溶液
C.加入试剂总体积为V1时,溶液中不存在NaOH
D.d点时溶液中的溶质不只是盐
13、如图所示,将充满CO2的试管倒扣在滴有紫色石蕊的蒸馏水中,一段时间后,下列实验现象描述正确的是( )
①试管内液面上升 ②试管内溶液变红
③试管内液面不上升 ④试管内溶液变蓝 ⑤试管内溶液不变色
A.①② B.①④ C.②③ D.③⑤
14、某雨水样品刚采集时测得pH为4.82,放在烧杯中经2小时后,再次测得pH为4.68,原因是雨水样品中的H2SO3逐渐被空气中的氧气氧化成H2SO4,下列关于雨水样品的说法正确的是( )
A.雨水样品酸性逐渐减弱 B.雨水样品酸性强弱未变
C.雨水样品酸性逐渐增强 D.无法判断
15、若利用碱的性质进行下列实验,不能达到相应目的的是( )
A.分别加入少量Mg(OH)2固体,根据是否溶解,可鉴别稀盐酸和Na2CO3溶液
B.分别加入适量水溶解,根据温度是否明显升高,可鉴别NaOH固体和NaCl固体
C.分别加入Ba(OH)2溶液,根据是否产生沉淀,可鉴别MgCl2溶液和Na2SO4溶液
D.分别加入熟石灰粉末研磨,根据是否产生氨味,可鉴别(NH4)2SO4固体和K2SO4固体
二、填空题。
16、现有白纸,溶质质量分数分别为:A、10%的NaOH溶液;B、5%的硫酸溶液;C、5%的紫色石蕊试液。试设计出《“雨”落叶出红花开》的趣味实验:先在白纸上用玻璃棒蘸取__________(填编号,下同)画上花,再蘸__________画上叶,将白纸挂上墙,用_________向纸上喷洒即可,实验的化学原理是_________________________________________。
17、请根据酸、碱、盐的相关知识,回答下列问题:
(1)亚硝酸钠(NaNO2)外观极像食盐,误食易引起中毒。其中氮元素的化合价为 。
(2)水壶中水垢的主要成分碳酸钙是一种不溶于水的物质。生活中清除水垢时,可往水壶中加入一种适量的厨房中常用的调味品,该调味品是 。
(3)胃液中含有适量的盐酸。由于胃酸过多而引起的胃痛,可服用含有Mg(OH)2的药物来中和过多的胃酸。反应的化学方程式为 。
18、请根据课本的“酸、碱、盐的溶解性表”,指出下列盐的溶解性:
(1)硝酸钾(KNO3) ,硫酸钾(K2SO4) ,碳酸钾(K2CO3) 。
(2)碳酸钙(CaCO3) ,碳酸钡(BaCO3) ,碳酸铜(CuCO3) 。
(3)氯化铵(NH4Cl) ,硝酸铵(NH4NO3) ,
碳酸铵〔(NH4)2CO3〕 。
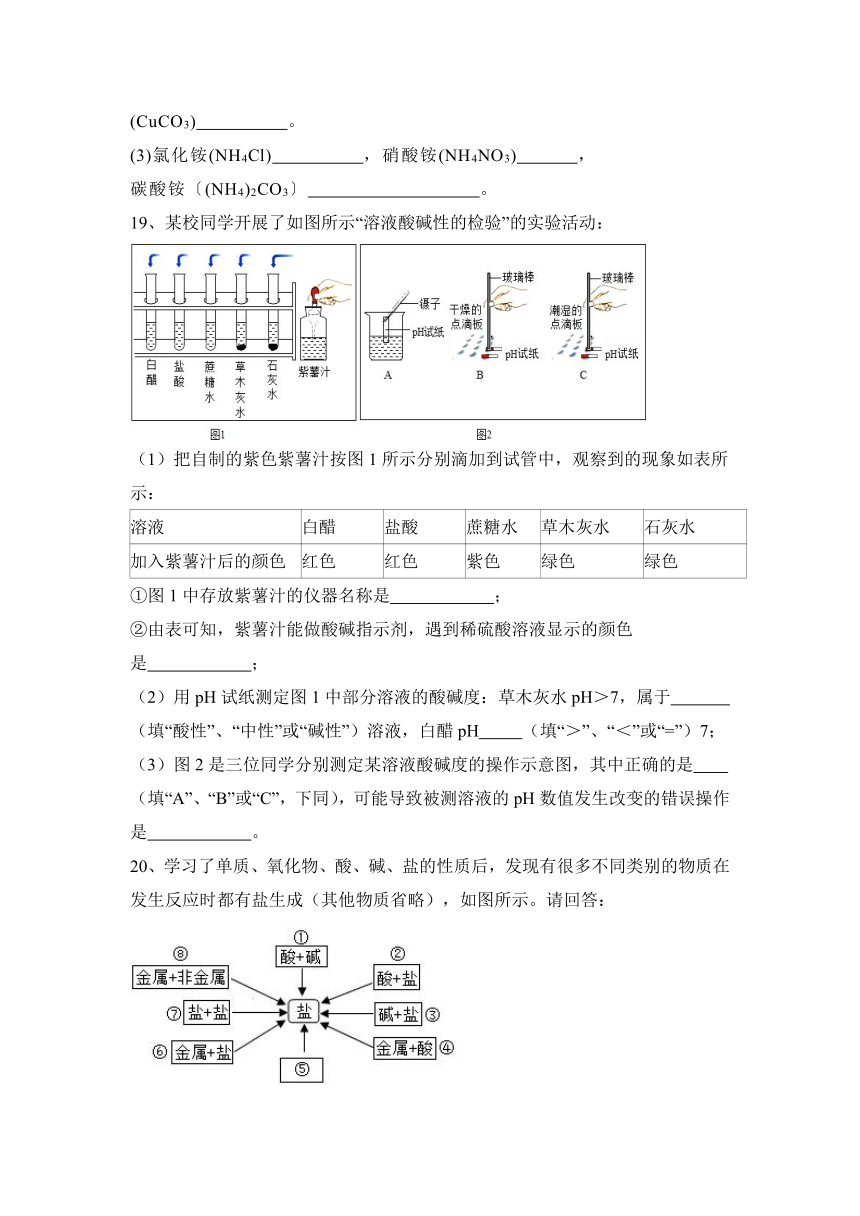
19、某校同学开展了如图所示“溶液酸碱性的检验”的实验活动:
(1)把自制的紫色紫薯汁按图1所示分别滴加到试管中,观察到的现象如表所示:
溶液 白醋 盐酸 蔗糖水 草木灰水 石灰水
加入紫薯汁后的颜色 红色 红色 紫色 绿色 绿色
①图1中存放紫薯汁的仪器名称是 ;
②由表可知,紫薯汁能做酸碱指示剂,遇到稀硫酸溶液显示的颜色是 ;
(2)用pH试纸测定图1中部分溶液的酸碱度:草木灰水pH>7,属于 (填“酸性”、“中性”或“碱性”)溶液,白醋pH (填“>”、“<”或“=”)7;
(3)图2是三位同学分别测定某溶液酸碱度的操作示意图,其中正确的是
(填“A”、“B”或“C”,下同),可能导致被测溶液的pH数值发生改变的错误操作是 。
20、学习了单质、氧化物、酸、碱、盐的性质后,发现有很多不同类别的物质在发生反应时都有盐生成(其他物质省略),如图所示。请回答:
(1)若盐是硫酸钾,则①中发生反应的化学方程式为:
。
(2)若盐是氯化亚铁,则在已显示的变化中可以通过置换反应来实现的有:
(填序号)。
(3)若盐是硝酸铜,则由⑦来实现的化学方程式为:
,属于 (填基本反应类型)反应。
(4)图中⑤处应补充的文字是 (写一种,不能与图中已有信息重复)。
21、张老师上课时做了趣味实验:他选择了一种指示剂(无色酚酞试液或紫色石蕊试液)、稀盐酸、稀NaOH溶液。他先用玻璃棒蘸取某种指示剂在白纸上写上“化学”,可是学生什么也看不见。然后用某种物质喷洒在白纸上,出现了红色的“化学”二字。接着,又向纸上喷洒另一种物质,红字消失。则他选用的指示剂是 ,先喷洒的物质是 ,后喷洒的物质为 。如果选用另一种指示剂。情况会怎样?
22、实验室检验二氧化碳的物质是 ,反应方程式为:
;实验室吸收二氧化碳的物质是 ,反应的方程式为 。
实验室为何用不同的物质检验和吸收二氧化碳?原因是:
。
23、用科学方法认识物质
获取知识、形成认识需要借助一定的科学方法。“观察”“抽象”“演绎”“归纳”“比较”“推理”等是常用的科学方法。下列描述分别运用了以上哪种科学方法
(1)打开盛放浓盐酸的试剂瓶,“瓶口有白雾出现”,运用的是__ 法;
“白雾是浓盐酸挥发出来的氯化氢气体与空气里的水蒸气接触,形成的盐酸小液滴”,运用的
是 法。
(2)“Na2CO3、K2CO3、CaCO3都能与盐酸反应生成二氧化碳气体,所以碳酸盐能与盐酸反应生成二氧化碳气体”,运用的___ 法;
“BaCO3属于碳酸盐,因此BaCO3也能与盐酸反应生成二氧化碳气体”,运用的是 法。
三、综合应用题。
24、在实验室里,可用如图装置进行CO还原Fe2O3的实验,并检验该反应的气体生成物。已知由一氧化碳发生装置得到的CO中混有CO2和H2O。
(1)写出装置C处尾气处理的方法______ (写一种即可);A装置中有关反应的化学方程式______ 。(写出一个即可)
(2)检验CO还原Fe2O3反应的气体生成物的现象是什么?
______ 。
(3)实验后取A中固体溶于水,滴加酚酞溶液,溶液变红色,请分析可能的原因:______ 。
(4)某钢铁厂用赤铁矿石炼铁。若该厂每天需消耗6000t含氧化铁80%的赤铁矿石,则理论上可日产含铁96%的生铁的质量是多少?(写出计算过程)
四、计算题。
25、钢是铁的合金。为测定某钢样中铁的质量分数,取11.4g钢样,向其中加入稀硫酸,产生氢气的质量与加入稀硫酸的质量关系如图所示(不考虑钢样中其它成分与稀硫酸的反应)。
(1)钢_____(填“是”或“不是”)金属材料。
(2)计算此钢样中铁的质量分数。
2022—2023学年沪教版(全国)化学九年级下册第七章 应用广泛的酸、碱、盐 培优与检测含答案
沪教版(全国)第七章 应用广泛的酸、碱、盐 培优与检测
一、选择题。
1、“雪碧”是一种无色的碳酸饮料,将少量“雪碧”滴入紫色石蕊试液中,然后再加热,溶液颜色的变化是( )
A.先变蓝后变紫 B.变红后颜色不再改变
C.先变无色后变红 D.先变红后变紫
【答案】D
2、如图所示的实验中,小烧杯①盛的是紫色石蕊试液,②盛的是浓盐酸。片刻后,可以观察到烧杯①中液体的颜色是( )
A.紫色 B.红色 C.无色 D.蓝色
【答案】B
3、下列物质中,易溶于水其水溶液显碱性的物质是( )
A.氢氧化钾 B.石灰石 C.氢氧化铁 D.消石灰
【答案】A
4、下列各组物质中按酸、碱、盐顺序排列的是( )
A.碳酸钠、硝酸、硫酸锌 B.硫酸亚铁、氢氧化钙、硫酸
C.盐酸、氢氧化镁、硫酸铜 D.氯化钙、碳酸钙、氧化钙
【答案】C
5、下列物质既可以做治疗胃酸的胃药,又可以做面点发酵剂的是( )
A.NaCl B.NaOH C.NaHCO3 D.Na2SO4
【答案】C
6、下列是实验室中常见的几项化学实验基本操作,其中正确的是( )
A.测溶液pH B.检查装置气密性 C.稀释浓硫酸 D.过滤
【答案】B
7、下列物质能与NaOH反应的是( )
A.Fe B.CO2 C.Fe2O3 D.NaCl
【答案】B
8、下列有关测定氢氧化钠溶液pH的实验操作或描述,你认为正确的是( )
A.用镊子夹取pH试纸直接伸入氢氧化钠溶液中测量
B.先用蒸馏水将pH试纸润湿,再用滴管吸取氢氧化钠溶液滴到pH试纸上测量
C.用洁净干燥的玻璃棒蘸取氢氧化钠溶液滴到pH试纸上,再与标准比色卡对照
D.用pH试纸测得该氢氧化钠溶液的
【答案】C
9、酸性溶液对橡胶制品具有较强的腐蚀作用,碱性溶液对玻璃制品也有一定的腐蚀性。据此你觉得下列试剂的存放方法正确的是( )
A.H2SO4溶液 B.Na2CO3溶液
C.NaOH溶液 D.Ca(OH)2溶液
【答案】C
10、一包固体粉末可能含有NaNO3、CaCO3、NaOH、CuCl2、NaCl和Ca(NO3)2中的一种或几种,为确定其组成,某同学设计了如下实验方案:
下列判断正确的是( )
A.蓝色溶液B中阳离子只有Cu2+
B.无色溶液A中一定有NaOH
C.原固体粉末一定有NaCl
D.原固体粉末一定有CaCO3、NaOH、NaNO3、CuCl2和Ca(NO3)2
【答案】B
11、进行化学实验操作考核时,下列四位同学的操作中正确的是( )
A.检验溶液酸碱性 B.溶解固体 C.倾倒液体 D.熄灭酒精灯
【答案】D
12、向一定质量的FeCl3溶液中滴加NaOH溶液一段时间后,改为滴加稀盐酸,所得沉淀质量随加入试剂总体积的变化趋势如图所示。下列说法正确的是( )
A.a点时溶液中一定存在Fe3+
B.c点时所加试剂是NaOH溶液
C.加入试剂总体积为V1时,溶液中不存在NaOH
D.d点时溶液中的溶质不只是盐
【答案】C
13、如图所示,将充满CO2的试管倒扣在滴有紫色石蕊的蒸馏水中,一段时间后,下列实验现象描述正确的是( )
①试管内液面上升 ②试管内溶液变红
③试管内液面不上升 ④试管内溶液变蓝 ⑤试管内溶液不变色
A.①② B.①④ C.②③ D.③⑤
【答案】A
14、某雨水样品刚采集时测得pH为4.82,放在烧杯中经2小时后,再次测得pH为4.68,原因是雨水样品中的H2SO3逐渐被空气中的氧气氧化成H2SO4,下列关于雨水样品的说法正确的是( )
A.雨水样品酸性逐渐减弱 B.雨水样品酸性强弱未变
C.雨水样品酸性逐渐增强 D.无法判断
【答案】C
15、若利用碱的性质进行下列实验,不能达到相应目的的是( )
A.分别加入少量Mg(OH)2固体,根据是否溶解,可鉴别稀盐酸和Na2CO3溶液
B.分别加入适量水溶解,根据温度是否明显升高,可鉴别NaOH固体和NaCl固体
C.分别加入Ba(OH)2溶液,根据是否产生沉淀,可鉴别MgCl2溶液和Na2SO4溶液
D.分别加入熟石灰粉末研磨,根据是否产生氨味,可鉴别(NH4)2SO4固体和K2SO4固体
【答案】C
二、填空题。
16、现有白纸,溶质质量分数分别为:A、10%的NaOH溶液;B、5%的硫酸溶液;C、5%的紫色石蕊试液。试设计出《“雨”落叶出红花开》的趣味实验:先在白纸上用玻璃棒蘸取__________(填编号,下同)画上花,再蘸__________画上叶,将白纸挂上墙,用_________向纸上喷洒即可,实验的化学原理是_________________________________________。
【答案】B A C 紫色石蕊试液遇酸变红、遇碱变蓝
17、请根据酸、碱、盐的相关知识,回答下列问题:
(1)亚硝酸钠(NaNO2)外观极像食盐,误食易引起中毒。其中氮元素的化合价为 。
(2)水壶中水垢的主要成分碳酸钙是一种不溶于水的物质。生活中清除水垢时,可往水壶中加入一种适量的厨房中常用的调味品,该调味品是 。
(3)胃液中含有适量的盐酸。由于胃酸过多而引起的胃痛,可服用含有Mg(OH)2的药物来中和过多的胃酸。反应的化学方程式为 。
【答案】(1)+3; (2)食醋; (3)Mg(OH)2+2HCl=MgCl2+2H2O。
18、请根据课本的“酸、碱、盐的溶解性表”,指出下列盐的溶解性:
(1)硝酸钾(KNO3) ,硫酸钾(K2SO4) ,碳酸钾(K2CO3) 。
(2)碳酸钙(CaCO3) ,碳酸钡(BaCO3) ,碳酸铜(CuCO3) 。
(3)氯化铵(NH4Cl) ,硝酸铵(NH4NO3) ,
碳酸铵〔(NH4)2CO3〕 。
【答案】溶; 溶; 溶; 不溶; 不溶; 不溶; 溶; 溶; 溶
19、某校同学开展了如图所示“溶液酸碱性的检验”的实验活动:
(1)把自制的紫色紫薯汁按图1所示分别滴加到试管中,观察到的现象如表所示:
溶液 白醋 盐酸 蔗糖水 草木灰水 石灰水
加入紫薯汁后的颜色 红色 红色 紫色 绿色 绿色
①图1中存放紫薯汁的仪器名称是 ;
②由表可知,紫薯汁能做酸碱指示剂,遇到稀硫酸溶液显示的颜色是 ;
(2)用pH试纸测定图1中部分溶液的酸碱度:草木灰水pH>7,属于 (填“酸性”、“中性”或“碱性”)溶液,白醋pH (填“>”、“<”或“=”)7;
(3)图2是三位同学分别测定某溶液酸碱度的操作示意图,其中正确的是
(填“A”、“B”或“C”,下同),可能导致被测溶液的pH数值发生改变的错误操作是 。
【答案】(1)①滴瓶 ②红色 (2)碱性 < (3)B C
20、学习了单质、氧化物、酸、碱、盐的性质后,发现有很多不同类别的物质在发生反应时都有盐生成(其他物质省略),如图所示。请回答:
(1)若盐是硫酸钾,则①中发生反应的化学方程式为:
。
(2)若盐是氯化亚铁,则在已显示的变化中可以通过置换反应来实现的有:
(填序号)。
(3)若盐是硝酸铜,则由⑦来实现的化学方程式为:
,属于 (填基本反应类型)反应。
(4)图中⑤处应补充的文字是 (写一种,不能与图中已有信息重复)。
【答案】(1); (2) ④⑥;
(3); 复分解;
金属氧化物+酸(或非金属氧化物+碱)
21、张老师上课时做了趣味实验:他选择了一种指示剂(无色酚酞试液或紫色石蕊试液)、稀盐酸、稀NaOH溶液。他先用玻璃棒蘸取某种指示剂在白纸上写上“化学”,可是学生什么也看不见。然后用某种物质喷洒在白纸上,出现了红色的“化学”二字。接着,又向纸上喷洒另一种物质,红字消失。则他选用的指示剂是 ,先喷洒的物质是 ,后喷洒的物质为 。如果选用另一种指示剂。情况会怎样?
【答案】无色酚酞试液 氢氧化钠溶液 稀盐酸 字先变紫色,喷氢氧化钠后变成蓝色,再喷盐酸字色变化为“蓝→紫→红”
22、实验室检验二氧化碳的物质是 ,反应方程式为:
;实验室吸收二氧化碳的物质是 ,反应的方程式为 。
实验室为何用不同的物质检验和吸收二氧化碳?原因是:
。
【答案】澄清石灰水,CO2+Ca(OH)2═CaCO3↓+H2O;
氢氧化钠溶液,2NaOH+CO2═Na2CO3+H2O;
氢氧化钙在水中的溶解度比氢氧化钠的溶解度小,吸收效果没有氢氧化钠好。
23、用科学方法认识物质
获取知识、形成认识需要借助一定的科学方法。“观察”“抽象”“演绎”“归纳”“比较”“推理”等是常用的科学方法。下列描述分别运用了以上哪种科学方法
(1)打开盛放浓盐酸的试剂瓶,“瓶口有白雾出现”,运用的是__ 法;
“白雾是浓盐酸挥发出来的氯化氢气体与空气里的水蒸气接触,形成的盐酸小液滴”,运用的
是 法。
(2)“Na2CO3、K2CO3、CaCO3都能与盐酸反应生成二氧化碳气体,所以碳酸盐能与盐酸反应生成二氧化碳气体”,运用的___ 法;
“BaCO3属于碳酸盐,因此BaCO3也能与盐酸反应生成二氧化碳气体”,运用的是 法。
【答案】观察; 推理; 归纳; 演绎
三、综合应用题。
24、在实验室里,可用如图装置进行CO还原Fe2O3的实验,并检验该反应的气体生成物。已知由一氧化碳发生装置得到的CO中混有CO2和H2O。
(1)写出装置C处尾气处理的方法______ (写一种即可);A装置中有关反应的化学方程式______ 。(写出一个即可)
(2)检验CO还原Fe2O3反应的气体生成物的现象是什么?
______ 。
(3)实验后取A中固体溶于水,滴加酚酞溶液,溶液变红色,请分析可能的原因:______ 。
(4)某钢铁厂用赤铁矿石炼铁。若该厂每天需消耗6000t含氧化铁80%的赤铁矿石,则理论上可日产含铁96%的生铁的质量是多少?(写出计算过程)
【答案】(1) 加一个燃着的酒精灯或绑一个气球
或 或
(2)C处澄清石灰水变浑浊
(3)氢氧化钠、氢氧化钙、碳酸钠溶液均显碱性,均能使无色酚酞试液变色
(4)解:设理论上可日产含铁96%的生铁的质量是x
x=3500t
答:理论上可日产含铁96%的生铁的质量是3500t。
四、计算题。
25、钢是铁的合金。为测定某钢样中铁的质量分数,取11.4g钢样,向其中加入稀硫酸,产生氢气的质量与加入稀硫酸的质量关系如图所示(不考虑钢样中其它成分与稀硫酸的反应)。
(1)钢_____(填“是”或“不是”)金属材料。
(2)计算此钢样中铁的质量分数。
【答案】(1)是 (2)98%
沪教版(全国)第七章 应用广泛的酸、碱、盐 培优与检测
一、选择题。
1、“雪碧”是一种无色的碳酸饮料,将少量“雪碧”滴入紫色石蕊试液中,然后再加热,溶液颜色的变化是( )
A.先变蓝后变紫 B.变红后颜色不再改变
C.先变无色后变红 D.先变红后变紫
2、如图所示的实验中,小烧杯①盛的是紫色石蕊试液,②盛的是浓盐酸。片刻后,可以观察到烧杯①中液体的颜色是( )
A.紫色 B.红色 C.无色 D.蓝色
3、下列物质中,易溶于水其水溶液显碱性的物质是( )
A.氢氧化钾 B.石灰石 C.氢氧化铁 D.消石灰
4、下列各组物质中按酸、碱、盐顺序排列的是( )
A.碳酸钠、硝酸、硫酸锌 B.硫酸亚铁、氢氧化钙、硫酸
C.盐酸、氢氧化镁、硫酸铜 D.氯化钙、碳酸钙、氧化钙
5、下列物质既可以做治疗胃酸的胃药,又可以做面点发酵剂的是( )
A.NaCl B.NaOH C.NaHCO3 D.Na2SO4
6、下列是实验室中常见的几项化学实验基本操作,其中正确的是( )
A.测溶液pH B.检查装置气密性 C.稀释浓硫酸 D.过滤
7、下列物质能与NaOH反应的是( )
A.Fe B.CO2 C.Fe2O3 D.NaCl
8、下列有关测定氢氧化钠溶液pH的实验操作或描述,你认为正确的是( )
A.用镊子夹取pH试纸直接伸入氢氧化钠溶液中测量
B.先用蒸馏水将pH试纸润湿,再用滴管吸取氢氧化钠溶液滴到pH试纸上测量
C.用洁净干燥的玻璃棒蘸取氢氧化钠溶液滴到pH试纸上,再与标准比色卡对照
D.用pH试纸测得该氢氧化钠溶液的
9、酸性溶液对橡胶制品具有较强的腐蚀作用,碱性溶液对玻璃制品也有一定的腐蚀性。据此你觉得下列试剂的存放方法正确的是( )
A.H2SO4溶液 B.Na2CO3溶液
C.NaOH溶液 D.Ca(OH)2溶液
10、一包固体粉末可能含有NaNO3、CaCO3、NaOH、CuCl2、NaCl和Ca(NO3)2中的一种或几种,为确定其组成,某同学设计了如下实验方案:
下列判断正确的是( )
A.蓝色溶液B中阳离子只有Cu2+
B.无色溶液A中一定有NaOH
C.原固体粉末一定有NaCl
D.原固体粉末一定有CaCO3、NaOH、NaNO3、CuCl2和Ca(NO3)2
11、进行化学实验操作考核时,下列四位同学的操作中正确的是( )
A.检验溶液酸碱性 B.溶解固体 C.倾倒液体 D.熄灭酒精灯
12、向一定质量的FeCl3溶液中滴加NaOH溶液一段时间后,改为滴加稀盐酸,所得沉淀质量随加入试剂总体积的变化趋势如图所示。下列说法正确的是( )
A.a点时溶液中一定存在Fe3+
B.c点时所加试剂是NaOH溶液
C.加入试剂总体积为V1时,溶液中不存在NaOH
D.d点时溶液中的溶质不只是盐
13、如图所示,将充满CO2的试管倒扣在滴有紫色石蕊的蒸馏水中,一段时间后,下列实验现象描述正确的是( )
①试管内液面上升 ②试管内溶液变红
③试管内液面不上升 ④试管内溶液变蓝 ⑤试管内溶液不变色
A.①② B.①④ C.②③ D.③⑤
14、某雨水样品刚采集时测得pH为4.82,放在烧杯中经2小时后,再次测得pH为4.68,原因是雨水样品中的H2SO3逐渐被空气中的氧气氧化成H2SO4,下列关于雨水样品的说法正确的是( )
A.雨水样品酸性逐渐减弱 B.雨水样品酸性强弱未变
C.雨水样品酸性逐渐增强 D.无法判断
15、若利用碱的性质进行下列实验,不能达到相应目的的是( )
A.分别加入少量Mg(OH)2固体,根据是否溶解,可鉴别稀盐酸和Na2CO3溶液
B.分别加入适量水溶解,根据温度是否明显升高,可鉴别NaOH固体和NaCl固体
C.分别加入Ba(OH)2溶液,根据是否产生沉淀,可鉴别MgCl2溶液和Na2SO4溶液
D.分别加入熟石灰粉末研磨,根据是否产生氨味,可鉴别(NH4)2SO4固体和K2SO4固体
二、填空题。
16、现有白纸,溶质质量分数分别为:A、10%的NaOH溶液;B、5%的硫酸溶液;C、5%的紫色石蕊试液。试设计出《“雨”落叶出红花开》的趣味实验:先在白纸上用玻璃棒蘸取__________(填编号,下同)画上花,再蘸__________画上叶,将白纸挂上墙,用_________向纸上喷洒即可,实验的化学原理是_________________________________________。
17、请根据酸、碱、盐的相关知识,回答下列问题:
(1)亚硝酸钠(NaNO2)外观极像食盐,误食易引起中毒。其中氮元素的化合价为 。
(2)水壶中水垢的主要成分碳酸钙是一种不溶于水的物质。生活中清除水垢时,可往水壶中加入一种适量的厨房中常用的调味品,该调味品是 。
(3)胃液中含有适量的盐酸。由于胃酸过多而引起的胃痛,可服用含有Mg(OH)2的药物来中和过多的胃酸。反应的化学方程式为 。
18、请根据课本的“酸、碱、盐的溶解性表”,指出下列盐的溶解性:
(1)硝酸钾(KNO3) ,硫酸钾(K2SO4) ,碳酸钾(K2CO3) 。
(2)碳酸钙(CaCO3) ,碳酸钡(BaCO3) ,碳酸铜(CuCO3) 。
(3)氯化铵(NH4Cl) ,硝酸铵(NH4NO3) ,
碳酸铵〔(NH4)2CO3〕 。
19、某校同学开展了如图所示“溶液酸碱性的检验”的实验活动:
(1)把自制的紫色紫薯汁按图1所示分别滴加到试管中,观察到的现象如表所示:
溶液 白醋 盐酸 蔗糖水 草木灰水 石灰水
加入紫薯汁后的颜色 红色 红色 紫色 绿色 绿色
①图1中存放紫薯汁的仪器名称是 ;
②由表可知,紫薯汁能做酸碱指示剂,遇到稀硫酸溶液显示的颜色是 ;
(2)用pH试纸测定图1中部分溶液的酸碱度:草木灰水pH>7,属于 (填“酸性”、“中性”或“碱性”)溶液,白醋pH (填“>”、“<”或“=”)7;
(3)图2是三位同学分别测定某溶液酸碱度的操作示意图,其中正确的是
(填“A”、“B”或“C”,下同),可能导致被测溶液的pH数值发生改变的错误操作是 。
20、学习了单质、氧化物、酸、碱、盐的性质后,发现有很多不同类别的物质在发生反应时都有盐生成(其他物质省略),如图所示。请回答:
(1)若盐是硫酸钾,则①中发生反应的化学方程式为:
。
(2)若盐是氯化亚铁,则在已显示的变化中可以通过置换反应来实现的有:
(填序号)。
(3)若盐是硝酸铜,则由⑦来实现的化学方程式为:
,属于 (填基本反应类型)反应。
(4)图中⑤处应补充的文字是 (写一种,不能与图中已有信息重复)。
21、张老师上课时做了趣味实验:他选择了一种指示剂(无色酚酞试液或紫色石蕊试液)、稀盐酸、稀NaOH溶液。他先用玻璃棒蘸取某种指示剂在白纸上写上“化学”,可是学生什么也看不见。然后用某种物质喷洒在白纸上,出现了红色的“化学”二字。接着,又向纸上喷洒另一种物质,红字消失。则他选用的指示剂是 ,先喷洒的物质是 ,后喷洒的物质为 。如果选用另一种指示剂。情况会怎样?
22、实验室检验二氧化碳的物质是 ,反应方程式为:
;实验室吸收二氧化碳的物质是 ,反应的方程式为 。
实验室为何用不同的物质检验和吸收二氧化碳?原因是:
。
23、用科学方法认识物质
获取知识、形成认识需要借助一定的科学方法。“观察”“抽象”“演绎”“归纳”“比较”“推理”等是常用的科学方法。下列描述分别运用了以上哪种科学方法
(1)打开盛放浓盐酸的试剂瓶,“瓶口有白雾出现”,运用的是__ 法;
“白雾是浓盐酸挥发出来的氯化氢气体与空气里的水蒸气接触,形成的盐酸小液滴”,运用的
是 法。
(2)“Na2CO3、K2CO3、CaCO3都能与盐酸反应生成二氧化碳气体,所以碳酸盐能与盐酸反应生成二氧化碳气体”,运用的___ 法;
“BaCO3属于碳酸盐,因此BaCO3也能与盐酸反应生成二氧化碳气体”,运用的是 法。
三、综合应用题。
24、在实验室里,可用如图装置进行CO还原Fe2O3的实验,并检验该反应的气体生成物。已知由一氧化碳发生装置得到的CO中混有CO2和H2O。
(1)写出装置C处尾气处理的方法______ (写一种即可);A装置中有关反应的化学方程式______ 。(写出一个即可)
(2)检验CO还原Fe2O3反应的气体生成物的现象是什么?
______ 。
(3)实验后取A中固体溶于水,滴加酚酞溶液,溶液变红色,请分析可能的原因:______ 。
(4)某钢铁厂用赤铁矿石炼铁。若该厂每天需消耗6000t含氧化铁80%的赤铁矿石,则理论上可日产含铁96%的生铁的质量是多少?(写出计算过程)
四、计算题。
25、钢是铁的合金。为测定某钢样中铁的质量分数,取11.4g钢样,向其中加入稀硫酸,产生氢气的质量与加入稀硫酸的质量关系如图所示(不考虑钢样中其它成分与稀硫酸的反应)。
(1)钢_____(填“是”或“不是”)金属材料。
(2)计算此钢样中铁的质量分数。
2022—2023学年沪教版(全国)化学九年级下册第七章 应用广泛的酸、碱、盐 培优与检测含答案
沪教版(全国)第七章 应用广泛的酸、碱、盐 培优与检测
一、选择题。
1、“雪碧”是一种无色的碳酸饮料,将少量“雪碧”滴入紫色石蕊试液中,然后再加热,溶液颜色的变化是( )
A.先变蓝后变紫 B.变红后颜色不再改变
C.先变无色后变红 D.先变红后变紫
【答案】D
2、如图所示的实验中,小烧杯①盛的是紫色石蕊试液,②盛的是浓盐酸。片刻后,可以观察到烧杯①中液体的颜色是( )
A.紫色 B.红色 C.无色 D.蓝色
【答案】B
3、下列物质中,易溶于水其水溶液显碱性的物质是( )
A.氢氧化钾 B.石灰石 C.氢氧化铁 D.消石灰
【答案】A
4、下列各组物质中按酸、碱、盐顺序排列的是( )
A.碳酸钠、硝酸、硫酸锌 B.硫酸亚铁、氢氧化钙、硫酸
C.盐酸、氢氧化镁、硫酸铜 D.氯化钙、碳酸钙、氧化钙
【答案】C
5、下列物质既可以做治疗胃酸的胃药,又可以做面点发酵剂的是( )
A.NaCl B.NaOH C.NaHCO3 D.Na2SO4
【答案】C
6、下列是实验室中常见的几项化学实验基本操作,其中正确的是( )
A.测溶液pH B.检查装置气密性 C.稀释浓硫酸 D.过滤
【答案】B
7、下列物质能与NaOH反应的是( )
A.Fe B.CO2 C.Fe2O3 D.NaCl
【答案】B
8、下列有关测定氢氧化钠溶液pH的实验操作或描述,你认为正确的是( )
A.用镊子夹取pH试纸直接伸入氢氧化钠溶液中测量
B.先用蒸馏水将pH试纸润湿,再用滴管吸取氢氧化钠溶液滴到pH试纸上测量
C.用洁净干燥的玻璃棒蘸取氢氧化钠溶液滴到pH试纸上,再与标准比色卡对照
D.用pH试纸测得该氢氧化钠溶液的
【答案】C
9、酸性溶液对橡胶制品具有较强的腐蚀作用,碱性溶液对玻璃制品也有一定的腐蚀性。据此你觉得下列试剂的存放方法正确的是( )
A.H2SO4溶液 B.Na2CO3溶液
C.NaOH溶液 D.Ca(OH)2溶液
【答案】C
10、一包固体粉末可能含有NaNO3、CaCO3、NaOH、CuCl2、NaCl和Ca(NO3)2中的一种或几种,为确定其组成,某同学设计了如下实验方案:
下列判断正确的是( )
A.蓝色溶液B中阳离子只有Cu2+
B.无色溶液A中一定有NaOH
C.原固体粉末一定有NaCl
D.原固体粉末一定有CaCO3、NaOH、NaNO3、CuCl2和Ca(NO3)2
【答案】B
11、进行化学实验操作考核时,下列四位同学的操作中正确的是( )
A.检验溶液酸碱性 B.溶解固体 C.倾倒液体 D.熄灭酒精灯
【答案】D
12、向一定质量的FeCl3溶液中滴加NaOH溶液一段时间后,改为滴加稀盐酸,所得沉淀质量随加入试剂总体积的变化趋势如图所示。下列说法正确的是( )
A.a点时溶液中一定存在Fe3+
B.c点时所加试剂是NaOH溶液
C.加入试剂总体积为V1时,溶液中不存在NaOH
D.d点时溶液中的溶质不只是盐
【答案】C
13、如图所示,将充满CO2的试管倒扣在滴有紫色石蕊的蒸馏水中,一段时间后,下列实验现象描述正确的是( )
①试管内液面上升 ②试管内溶液变红
③试管内液面不上升 ④试管内溶液变蓝 ⑤试管内溶液不变色
A.①② B.①④ C.②③ D.③⑤
【答案】A
14、某雨水样品刚采集时测得pH为4.82,放在烧杯中经2小时后,再次测得pH为4.68,原因是雨水样品中的H2SO3逐渐被空气中的氧气氧化成H2SO4,下列关于雨水样品的说法正确的是( )
A.雨水样品酸性逐渐减弱 B.雨水样品酸性强弱未变
C.雨水样品酸性逐渐增强 D.无法判断
【答案】C
15、若利用碱的性质进行下列实验,不能达到相应目的的是( )
A.分别加入少量Mg(OH)2固体,根据是否溶解,可鉴别稀盐酸和Na2CO3溶液
B.分别加入适量水溶解,根据温度是否明显升高,可鉴别NaOH固体和NaCl固体
C.分别加入Ba(OH)2溶液,根据是否产生沉淀,可鉴别MgCl2溶液和Na2SO4溶液
D.分别加入熟石灰粉末研磨,根据是否产生氨味,可鉴别(NH4)2SO4固体和K2SO4固体
【答案】C
二、填空题。
16、现有白纸,溶质质量分数分别为:A、10%的NaOH溶液;B、5%的硫酸溶液;C、5%的紫色石蕊试液。试设计出《“雨”落叶出红花开》的趣味实验:先在白纸上用玻璃棒蘸取__________(填编号,下同)画上花,再蘸__________画上叶,将白纸挂上墙,用_________向纸上喷洒即可,实验的化学原理是_________________________________________。
【答案】B A C 紫色石蕊试液遇酸变红、遇碱变蓝
17、请根据酸、碱、盐的相关知识,回答下列问题:
(1)亚硝酸钠(NaNO2)外观极像食盐,误食易引起中毒。其中氮元素的化合价为 。
(2)水壶中水垢的主要成分碳酸钙是一种不溶于水的物质。生活中清除水垢时,可往水壶中加入一种适量的厨房中常用的调味品,该调味品是 。
(3)胃液中含有适量的盐酸。由于胃酸过多而引起的胃痛,可服用含有Mg(OH)2的药物来中和过多的胃酸。反应的化学方程式为 。
【答案】(1)+3; (2)食醋; (3)Mg(OH)2+2HCl=MgCl2+2H2O。
18、请根据课本的“酸、碱、盐的溶解性表”,指出下列盐的溶解性:
(1)硝酸钾(KNO3) ,硫酸钾(K2SO4) ,碳酸钾(K2CO3) 。
(2)碳酸钙(CaCO3) ,碳酸钡(BaCO3) ,碳酸铜(CuCO3) 。
(3)氯化铵(NH4Cl) ,硝酸铵(NH4NO3) ,
碳酸铵〔(NH4)2CO3〕 。
【答案】溶; 溶; 溶; 不溶; 不溶; 不溶; 溶; 溶; 溶
19、某校同学开展了如图所示“溶液酸碱性的检验”的实验活动:
(1)把自制的紫色紫薯汁按图1所示分别滴加到试管中,观察到的现象如表所示:
溶液 白醋 盐酸 蔗糖水 草木灰水 石灰水
加入紫薯汁后的颜色 红色 红色 紫色 绿色 绿色
①图1中存放紫薯汁的仪器名称是 ;
②由表可知,紫薯汁能做酸碱指示剂,遇到稀硫酸溶液显示的颜色是 ;
(2)用pH试纸测定图1中部分溶液的酸碱度:草木灰水pH>7,属于 (填“酸性”、“中性”或“碱性”)溶液,白醋pH (填“>”、“<”或“=”)7;
(3)图2是三位同学分别测定某溶液酸碱度的操作示意图,其中正确的是
(填“A”、“B”或“C”,下同),可能导致被测溶液的pH数值发生改变的错误操作是 。
【答案】(1)①滴瓶 ②红色 (2)碱性 < (3)B C
20、学习了单质、氧化物、酸、碱、盐的性质后,发现有很多不同类别的物质在发生反应时都有盐生成(其他物质省略),如图所示。请回答:
(1)若盐是硫酸钾,则①中发生反应的化学方程式为:
。
(2)若盐是氯化亚铁,则在已显示的变化中可以通过置换反应来实现的有:
(填序号)。
(3)若盐是硝酸铜,则由⑦来实现的化学方程式为:
,属于 (填基本反应类型)反应。
(4)图中⑤处应补充的文字是 (写一种,不能与图中已有信息重复)。
【答案】(1); (2) ④⑥;
(3); 复分解;
金属氧化物+酸(或非金属氧化物+碱)
21、张老师上课时做了趣味实验:他选择了一种指示剂(无色酚酞试液或紫色石蕊试液)、稀盐酸、稀NaOH溶液。他先用玻璃棒蘸取某种指示剂在白纸上写上“化学”,可是学生什么也看不见。然后用某种物质喷洒在白纸上,出现了红色的“化学”二字。接着,又向纸上喷洒另一种物质,红字消失。则他选用的指示剂是 ,先喷洒的物质是 ,后喷洒的物质为 。如果选用另一种指示剂。情况会怎样?
【答案】无色酚酞试液 氢氧化钠溶液 稀盐酸 字先变紫色,喷氢氧化钠后变成蓝色,再喷盐酸字色变化为“蓝→紫→红”
22、实验室检验二氧化碳的物质是 ,反应方程式为:
;实验室吸收二氧化碳的物质是 ,反应的方程式为 。
实验室为何用不同的物质检验和吸收二氧化碳?原因是:
。
【答案】澄清石灰水,CO2+Ca(OH)2═CaCO3↓+H2O;
氢氧化钠溶液,2NaOH+CO2═Na2CO3+H2O;
氢氧化钙在水中的溶解度比氢氧化钠的溶解度小,吸收效果没有氢氧化钠好。
23、用科学方法认识物质
获取知识、形成认识需要借助一定的科学方法。“观察”“抽象”“演绎”“归纳”“比较”“推理”等是常用的科学方法。下列描述分别运用了以上哪种科学方法
(1)打开盛放浓盐酸的试剂瓶,“瓶口有白雾出现”,运用的是__ 法;
“白雾是浓盐酸挥发出来的氯化氢气体与空气里的水蒸气接触,形成的盐酸小液滴”,运用的
是 法。
(2)“Na2CO3、K2CO3、CaCO3都能与盐酸反应生成二氧化碳气体,所以碳酸盐能与盐酸反应生成二氧化碳气体”,运用的___ 法;
“BaCO3属于碳酸盐,因此BaCO3也能与盐酸反应生成二氧化碳气体”,运用的是 法。
【答案】观察; 推理; 归纳; 演绎
三、综合应用题。
24、在实验室里,可用如图装置进行CO还原Fe2O3的实验,并检验该反应的气体生成物。已知由一氧化碳发生装置得到的CO中混有CO2和H2O。
(1)写出装置C处尾气处理的方法______ (写一种即可);A装置中有关反应的化学方程式______ 。(写出一个即可)
(2)检验CO还原Fe2O3反应的气体生成物的现象是什么?
______ 。
(3)实验后取A中固体溶于水,滴加酚酞溶液,溶液变红色,请分析可能的原因:______ 。
(4)某钢铁厂用赤铁矿石炼铁。若该厂每天需消耗6000t含氧化铁80%的赤铁矿石,则理论上可日产含铁96%的生铁的质量是多少?(写出计算过程)
【答案】(1) 加一个燃着的酒精灯或绑一个气球
或 或
(2)C处澄清石灰水变浑浊
(3)氢氧化钠、氢氧化钙、碳酸钠溶液均显碱性,均能使无色酚酞试液变色
(4)解:设理论上可日产含铁96%的生铁的质量是x
x=3500t
答:理论上可日产含铁96%的生铁的质量是3500t。
四、计算题。
25、钢是铁的合金。为测定某钢样中铁的质量分数,取11.4g钢样,向其中加入稀硫酸,产生氢气的质量与加入稀硫酸的质量关系如图所示(不考虑钢样中其它成分与稀硫酸的反应)。
(1)钢_____(填“是”或“不是”)金属材料。
(2)计算此钢样中铁的质量分数。
【答案】(1)是 (2)98%
