化学键与化学反应_学案(无答案)
图片预览

文档简介
化学键与化学反应学案
【学习目标】 1.认识化学键的含义,知道离子键和共价键的形成。
2.知道化学键的断裂和形成是化学反应中物质变化的主要原因。
【重点、难点】化学键与化学反应中的物质变化
【学习过程】
一、化学键与物质变化
【思考】水在通电条件下能够发生分解,为什么要通电?
1、化学键的定义 。
【几点说明】:①首先必须相邻,不相邻一般就 ( http: / / www.21cnjy.com )不强烈; ②只相邻但不强烈,也不叫化学键; ③“相互作用”不能说成“相互吸引”(实际既包括吸引又包括排斥)。
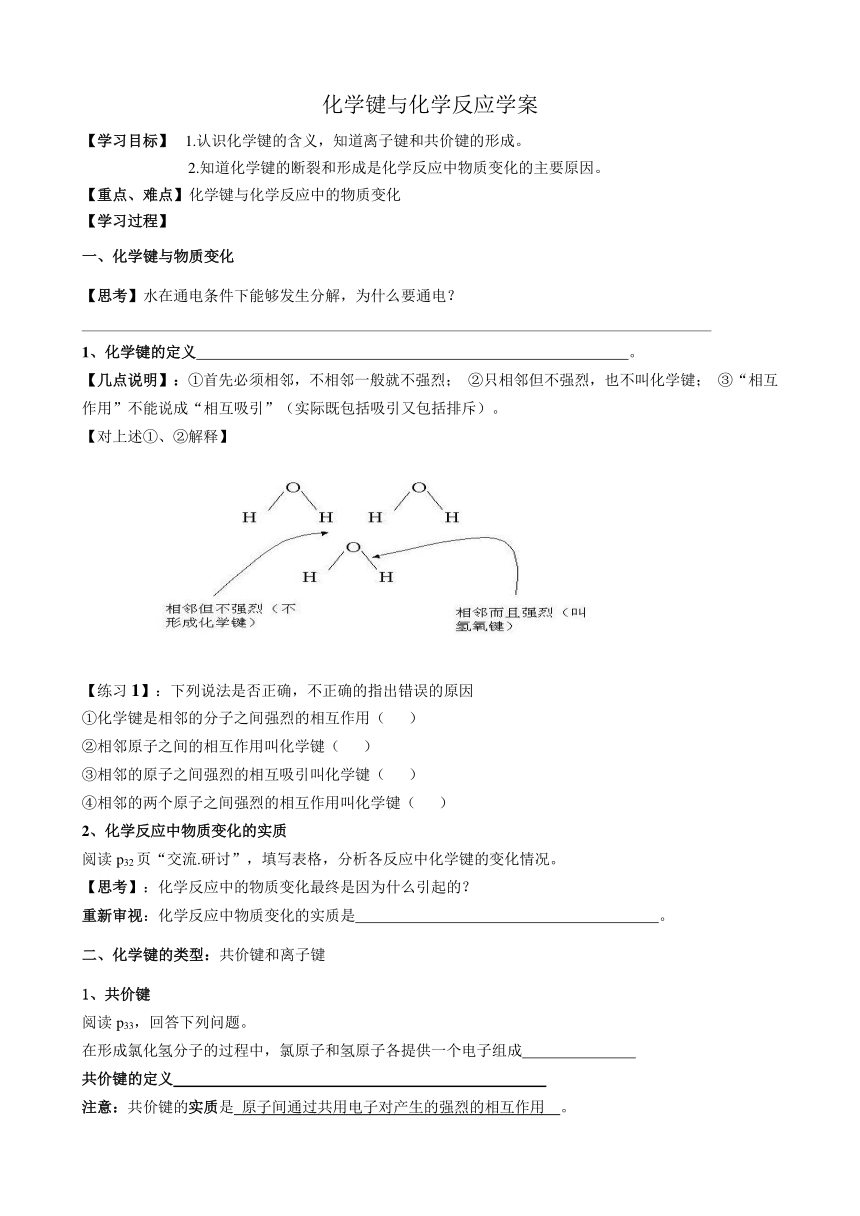
【对上述①、②解释】
【练习1】:下列说法是否正确,不正确的指出错误的原因
①化学键是相邻的分子之间强烈的相互作用( )
②相邻原子之间的相互作用叫化学键( )
③相邻的原子之间强烈的相互吸引叫化学键( )
④相邻的两个原子之间强烈的相互作用叫化学键( )
2、化学反应中物质变化的实质
阅读p32页“交流.研讨”,填写表格,分析各反应中化学键的变化情况。
【思考】:化学反应中的物质变化最终是因为什么引起的?
重新审视:化学反应中物质变化的实质是 。
二、化学键的类型:共价键和离子键
1、共价键
阅读p33,回答下列问题。
在形成氯化氢分子的过程中,氯原子和氢原子各提供一个电子组成
共价键的定义
注意:共价键的实质是 原子间通过共用电子对产生的强烈的相互作用 。
【交流研讨】
1.形成共价键的两原子为什么会发生这样的变化?
2.形成共价键的微粒是什么?
3.共价键的成键方式是什么 (即靠什么结合到一起?)
4.哪些元素的原子之间可能形成共价键(成键条件)?
【练习2】请运用你所学的知识判断下列哪些物质中存在共价键?
NaF CH4 H2O CaO H2 MgCl2 O2 CO 2
2、离子键
阅读P34,并回答下列问题。
离子键的定义
注意:离子键的实质是 阴离子与阳离子之间的静电作用 。
【思考】怎样理解这种静电作用? ( http: / / www.21cnjy.com )
【交流研讨】
1.氯原子、钠原子为什么要形成阴阳离子进而形成离子键呢?
2.形成离子键的微粒是什么?
3.离子键的成键方式是什么 (靠什么作用到一起?)
4.从钠原子、氯原子所属的元素种类看,哪些类元素能形成离子键(成键条件)?
【练习3】请运用你所学的知识判断下列物质中分别存在哪些类型的化学键?
KBr HF BaC ( http: / / www.21cnjy.com )l2 NaF CH4 H2O CaO H2 MgCl2 O2 CO 2
离子键: 共价键
【小结】:比较离子键和共价键特点,完成以下表格。
键的类型 离子键 共价键
定 义
成键原因
成键微粒
成键方式
成键元素
【当堂检测】:
1.下列关于化学键的叙述正确的是( )
A.化学键既存在于相邻原子间,又存在于相邻分子之间
B.两个原子间的相互作用叫化学键
C.化学键通常指的是相邻原子之间的强相互作用
D.化学键是相邻的分子之间强烈的相互作用
2.下列物质中含有离子键的是
A.H2O B CaCl2 C. HCl D. Cl2
3.下列各组化合物中化学键类型不同的是
A. NaCl和KF B. H2O和NH3 C. CaF2和CsCl D. CCl4和Na2O
4.下列数值表示有关元素的 ( http: / / www.21cnjy.com )原子序数,各原子能以离子键相互结合成稳定的化合物的是( ) A.10 与19 B. 6与 16 C. 11 与17 D. 14 与8
【课后练习】:
1、下列关于化学键的叙述正确的是
A.化学键既存在于相邻原子间,又存在于相邻分子之间
B.两个原子间的相互作用叫化学键
C.化学键通常指的是相邻原子之间的强相互作用
D.阴阳离子之间有强烈的吸引作用而没有排斥作用,所以离子键的核间距相当小
E.构成单质分子的微粒中一定含有共价键
F.只有非金属元素组成的化合物不一定是共价化合物
G.共价键只存在共价化合物中,离子键只存在于离子化合物中
2、关于离子键的描述正确的是
A.离子键是阴、阳离子通过静电吸引而形成的
B.离子键只能在金属元素和非金属元素的原子之间形成
C.离子键的作用仅局限在阴、阳离子之间
D.离子键是阴、阳离子通过静电作用而形成的
3.下列各物质中,化学键类型完全相同的是( )
A.KOH和CO2 B.H2S和K2S C.HCl和HClO D.MgF2和MgO
4. 下列各数值表示元素的原子序数,其表示的各组原子能以离子键相结合的是
A.13和17 B.1和17 C.6和8 D.3和9
5.下列各组物质中,原子间的化学键形式不同的是( )
A.CH4和Na2O B.H2O和NH3 C.Cl2和HCl D.NaCl和CaF2
6. 下列分子中,所有成键原子最外层均为8个电子的是
A.CS2 B.BF3 C.XeF2 D.SF6
7、下列各组化合物中化学键的类型不同的是
A.KBr和 HNO3 B.Cl2 和NH3 C.CaF2 和CsCl D.CCl4 和Na2O
8、下列物质: (要求填写序号)
①O2 ② NaCl ③ Na2S ④ H2SO4 ⑤NH4Cl ⑥Na2CO3 ⑦CO2 ⑧ NaOH
⑨CaCl2 ⑩CH4
这些物质中,只含共价键的是
只含离子键的是
既含共价键又含离子键的是
【学习目标】 1.认识化学键的含义,知道离子键和共价键的形成。
2.知道化学键的断裂和形成是化学反应中物质变化的主要原因。
【重点、难点】化学键与化学反应中的物质变化
【学习过程】
一、化学键与物质变化
【思考】水在通电条件下能够发生分解,为什么要通电?
1、化学键的定义 。
【几点说明】:①首先必须相邻,不相邻一般就 ( http: / / www.21cnjy.com )不强烈; ②只相邻但不强烈,也不叫化学键; ③“相互作用”不能说成“相互吸引”(实际既包括吸引又包括排斥)。
【对上述①、②解释】
【练习1】:下列说法是否正确,不正确的指出错误的原因
①化学键是相邻的分子之间强烈的相互作用( )
②相邻原子之间的相互作用叫化学键( )
③相邻的原子之间强烈的相互吸引叫化学键( )
④相邻的两个原子之间强烈的相互作用叫化学键( )
2、化学反应中物质变化的实质
阅读p32页“交流.研讨”,填写表格,分析各反应中化学键的变化情况。
【思考】:化学反应中的物质变化最终是因为什么引起的?
重新审视:化学反应中物质变化的实质是 。
二、化学键的类型:共价键和离子键
1、共价键
阅读p33,回答下列问题。
在形成氯化氢分子的过程中,氯原子和氢原子各提供一个电子组成
共价键的定义
注意:共价键的实质是 原子间通过共用电子对产生的强烈的相互作用 。
【交流研讨】
1.形成共价键的两原子为什么会发生这样的变化?
2.形成共价键的微粒是什么?
3.共价键的成键方式是什么 (即靠什么结合到一起?)
4.哪些元素的原子之间可能形成共价键(成键条件)?
【练习2】请运用你所学的知识判断下列哪些物质中存在共价键?
NaF CH4 H2O CaO H2 MgCl2 O2 CO 2
2、离子键
阅读P34,并回答下列问题。
离子键的定义
注意:离子键的实质是 阴离子与阳离子之间的静电作用 。
【思考】怎样理解这种静电作用? ( http: / / www.21cnjy.com )
【交流研讨】
1.氯原子、钠原子为什么要形成阴阳离子进而形成离子键呢?
2.形成离子键的微粒是什么?
3.离子键的成键方式是什么 (靠什么作用到一起?)
4.从钠原子、氯原子所属的元素种类看,哪些类元素能形成离子键(成键条件)?
【练习3】请运用你所学的知识判断下列物质中分别存在哪些类型的化学键?
KBr HF BaC ( http: / / www.21cnjy.com )l2 NaF CH4 H2O CaO H2 MgCl2 O2 CO 2
离子键: 共价键
【小结】:比较离子键和共价键特点,完成以下表格。
键的类型 离子键 共价键
定 义
成键原因
成键微粒
成键方式
成键元素
【当堂检测】:
1.下列关于化学键的叙述正确的是( )
A.化学键既存在于相邻原子间,又存在于相邻分子之间
B.两个原子间的相互作用叫化学键
C.化学键通常指的是相邻原子之间的强相互作用
D.化学键是相邻的分子之间强烈的相互作用
2.下列物质中含有离子键的是
A.H2O B CaCl2 C. HCl D. Cl2
3.下列各组化合物中化学键类型不同的是
A. NaCl和KF B. H2O和NH3 C. CaF2和CsCl D. CCl4和Na2O
4.下列数值表示有关元素的 ( http: / / www.21cnjy.com )原子序数,各原子能以离子键相互结合成稳定的化合物的是( ) A.10 与19 B. 6与 16 C. 11 与17 D. 14 与8
【课后练习】:
1、下列关于化学键的叙述正确的是
A.化学键既存在于相邻原子间,又存在于相邻分子之间
B.两个原子间的相互作用叫化学键
C.化学键通常指的是相邻原子之间的强相互作用
D.阴阳离子之间有强烈的吸引作用而没有排斥作用,所以离子键的核间距相当小
E.构成单质分子的微粒中一定含有共价键
F.只有非金属元素组成的化合物不一定是共价化合物
G.共价键只存在共价化合物中,离子键只存在于离子化合物中
2、关于离子键的描述正确的是
A.离子键是阴、阳离子通过静电吸引而形成的
B.离子键只能在金属元素和非金属元素的原子之间形成
C.离子键的作用仅局限在阴、阳离子之间
D.离子键是阴、阳离子通过静电作用而形成的
3.下列各物质中,化学键类型完全相同的是( )
A.KOH和CO2 B.H2S和K2S C.HCl和HClO D.MgF2和MgO
4. 下列各数值表示元素的原子序数,其表示的各组原子能以离子键相结合的是
A.13和17 B.1和17 C.6和8 D.3和9
5.下列各组物质中,原子间的化学键形式不同的是( )
A.CH4和Na2O B.H2O和NH3 C.Cl2和HCl D.NaCl和CaF2
6. 下列分子中,所有成键原子最外层均为8个电子的是
A.CS2 B.BF3 C.XeF2 D.SF6
7、下列各组化合物中化学键的类型不同的是
A.KBr和 HNO3 B.Cl2 和NH3 C.CaF2 和CsCl D.CCl4 和Na2O
8、下列物质: (要求填写序号)
①O2 ② NaCl ③ Na2S ④ H2SO4 ⑤NH4Cl ⑥Na2CO3 ⑦CO2 ⑧ NaOH
⑨CaCl2 ⑩CH4
这些物质中,只含共价键的是
只含离子键的是
既含共价键又含离子键的是
