化学键与化学反应_教案(两个课时)
图片预览


文档简介
第一节 化学键与化学反应
第1课时
第一部分:化学键与化学反应中的物质变化
知识点1:化学键的定义
【引入】前边通过元素周期律、周期表的学习,知道目前已知的元素种类只有一百多种,可这些元素却构成了已发现或合成的一千多万种物质,元素的原子能够相互结合形成多种多样的物质,说明形成这些物质的原子间一定存在着相互作用。
【演示实验】水在直流电的作用下分解
2H2O 2H2 + O2
【思考·质疑】水在通电条件下能够发生分解,为什么要通电?
【归纳】水分子是由两个氢原子和一个氧原子构成的,氢原子和氧原子之间存在着很强的相互作用,要破坏这种相互作用就需要消耗能量,通电正是为了提供使水分解所需要的能量。
【媒体展示——板书】 第1节 化学键与化学反应
化学键:相邻的(两个或多个)原子间的强相互作用
【对定义的强调】(1)首先必须相邻。不相邻一般就不强烈 (2)只相邻但不强烈,也不叫化学键 (3)“相互作用”不能说成“相互吸引”(实际既包括吸引又包括排斥)
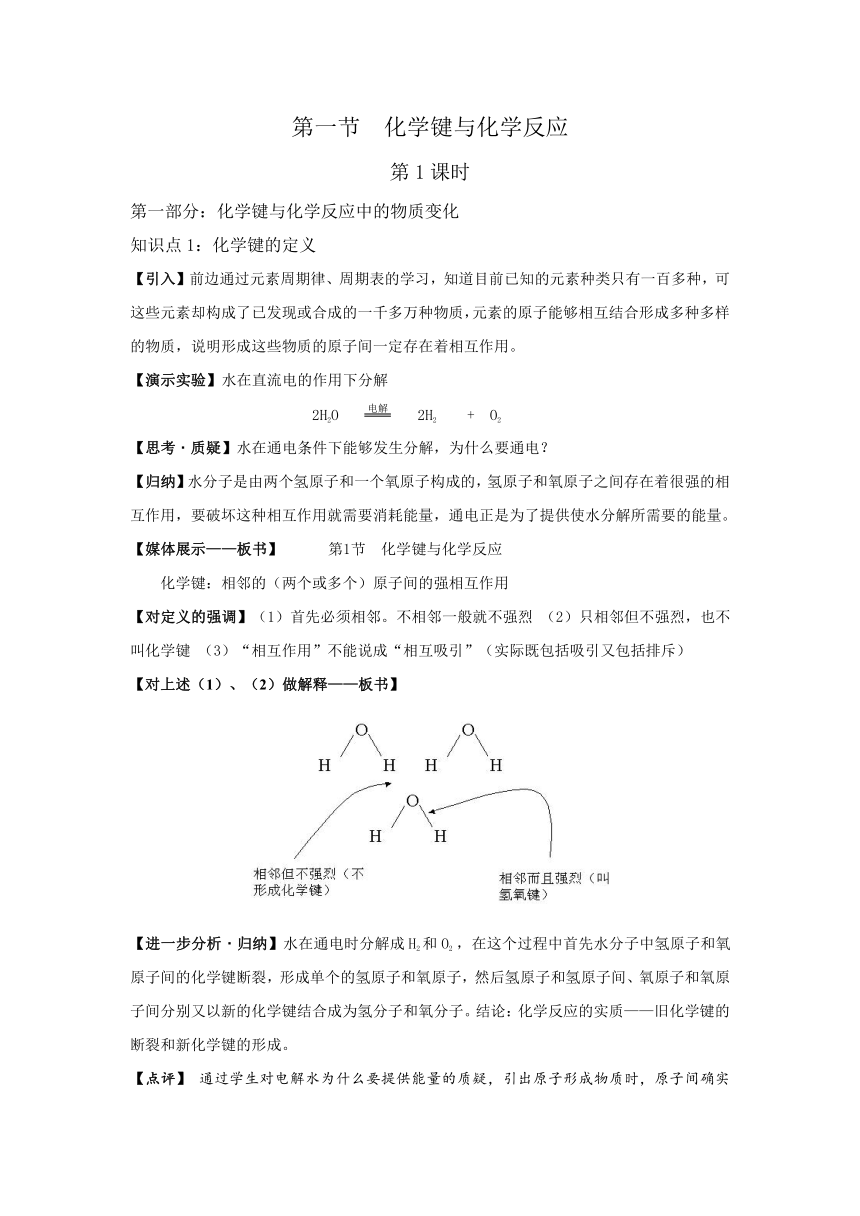
【对上述(1)、(2)做解释——板书】
【进一步分析·归纳】水在通电时分解成H2和O2 ,在这个过程中首先水分子中氢原子和氧原子间的化学键断裂,形成单个的氢原子和氧原子,然后氢原子和氢原子间、氧原子和氧原子间分别又以新的化学键结合成为氢分子和氧分子。结论:化学反应的实质——旧化学键的断裂和新化学键的形成。
【点评】 通过学生对电解水为什么要提供能量的质疑,引出原子形成物质时,原子间确实存在着相互作用,教师及时引导给出化学键的定义。通过学生对化学键定义的阅读理解,教师进一步通过板书解释(水分子间的化学键的存在情况),强调理解化学键定义的几个关键点:(1)首先必须相邻。不相邻一般就不强烈 (2)只相邻但不强烈,也不叫化学键 (3)“相互作用”不能说成“相互吸引”(实际既包括吸引又包括排斥)。通过解释定义使学生对化学键作到了较深刻的理解。
知识点2:化学键的类型
【引入】元素有一百多种,这些元素从大的角度分两类:金属元素、非金属元素。金属元素一般容易失电子,非金属元素一般容易得电子。我们发现非金属和非金属元素之间,非金属元素和金属元素之间、金属元素和金属元素之间都可以通过化学键构成物质,他们之间的化学键是否一样呢?
【实验录象】钠在氯气中的燃烧实验录象
2Na + Cl2 ==== 2NaCl
氢气在氯气中的燃烧实验录象
H2 + Cl2 ==== 2HCl
【点评】“氢气在氯气中的燃烧”和“金属钠在氯气中的燃烧”是《化学1(必修)》中的演示实验,且实验过程中用到了有毒的气体——氯气。此时借助于实验录象不仅快捷省事,而且也不会因氯气的毒性或气体扩散而搞得满屋刺激性气味而影响教学。
【联想·质疑】氢气在氯气中的燃烧形成氯化氢和钠在氯气中的燃烧形成氯化钠,在形成化学键方面是否相同?
【归纳】氢气在氯气中燃烧时,氢分子和氯分子获得能量,化学键分别断裂,从而形成氢原子和氯原子。由于氢和氯都是非金属元素,都有得电子的趋势,最终谁也不能把对方的电子完全得到,而是氯原子和氢原子各提供一个电子组成共用电子对,从而使两者的最外层都达到稳定结构并产生强烈的相互作用——形成化学键。这样的化学键叫共价键。由于氯和氢都没有完全得失电子,因此,都不形成离子,HCl中的氢和氯不能叫氢离子氯离子,只能叫氢原子氯原子。
而在氯化钠的形成过程中,由于钠是金属元素很容易失电子,氯是非金属元素很容易得电子,当钠原子和氯原子靠近时,钠原子就失去最外层的一个电子形成钠阳离子,氯原子最外层得到钠的一个电子形成氯阴离子(两者最外层均达到稳定结构),阴、阳离子靠静电作用形成化学键——离子键,构成氯化钠。由于钠和氯原子之间是完全的得失电子,他们已形成了离子,因此NaCl中的微粒不能再叫原子,而应该叫离子。
【媒体展示——板书】
共价键:原子间通过共用电子对形成的化学键。一般非金属元素之间形成共价键。
离子键:阴阳离子之间通过静电作用形成的化学键。一般存在于金属和非金属之间。
【对定义的强调】(1)共价键的成键微粒是原子,而离子键的成键微粒是阴阳离子 (2)一般典型的非金属和非金属之间都形成共价键,典型的金属和非金属之间都形成离子键 (3)共价键和离子键的实质相同,都属于电性作用。成键原因都是原子都有使自己的最外层达到稳定结构状态的趋势。(稀有气体原子的最外层都已达到稳定结构,因此稀有气体分子都是单原子分子,分子内不形成化学键)
【迁移·应用——课堂练习】
指出构成下列物质的微粒和键型:NaCl、CaO、MgCl2 、H2O、CH4、NH3 、CO2
物质
形成化学键的微粒
化学键类型
H2O
CH4
NH3
NaCl
MgCl2
CaO
CO2
【知识拓展】非极性共价键:在单质分子中同种原子形成的共价键,两个原子对共用电子对共用电子对的吸引能力相同;共用电子对不偏向于任何一个原子,成键原子不显电性。这样的共价键叫非极性共价键。
极性共价键:在共价键形成的化合物分子中,由于不同原子对共用电子对的吸引能力不同,共用电子对会偏向于吸引电子能力强的一方,因此吸引电子能力强的原子带部分负电荷,吸引电子能力较弱的一方带部分正电荷,这样的共价键叫极性共价键。如氯化氢中的共价键就是极性共价键,共用电子对会偏向于氯原子一方偏离于氢原子一方。H2 、Cl2中的化学键。
【点评】 通过氯化氢和氯化钠两种物质的形成过程的剖析,分别给出共价键、离子键的定义;又通过他们化学键的形成特点,从成键微粒、成键原因、成键本质等方面,找出他们之间的异同点。然后把从具体事例得出的结论推广开来,重点强调在什么情况下会形成共价键,在什么情况下会形成离子键,再通过当堂举例判断、练习,使学生对概念的掌握比较清晰。
对于程度好的同学,通过“知识拓展”补充介绍“非极性共价键”和“极性共价键”的概念,以及化合价与共价键的关系,但不要进一步拓展,这样可以达到开拓学生思路的目的。
第2课时
知识点3:化学键与物质构成
【引入】我们已经学习过物质的分类,知道物质分纯净物、混合物;纯净物又分单质和化合物。通过化学键的学习,我们知道构成物的离子(或原子)之间的化学键也是有区别的——又分为离子键、共价键等。于是,人们根据化合物中所含化学键类型的不同,把化合物分为离子化合物和共价化合物。
【媒体展示——板书】
离子化合物:含有离子键的化合物。如:NaCl、CaCl2、KOH、CaO等
共价化合物:只含有共价键的化合物。如:HCl、H2O、CH4、NH3 、CO2
【联想·质疑】分析KOH中所含有的键型,该化合物属于哪类化合物?
【归纳·强调】(1)当一个化合物中只存在离子键时,该化合物是离子化合物(2)当一个化合中同时存在离子键和共价键时,以离子键为主,该化合物也称为离子化合物(3)只有当化合物中只存在共价键时,该化合物才称为共价化合物。(4)在离子化合物中一般既含有金属元素又含有非金属元素;共价化合物一般只含有非金属元素(NH4+例外)
【迁移·应用——课堂练习】
指出下列化合物内部的键型和化合物的分类(离子化合物、共价化合物)
化合物
内部的键型
分类(离子化合物、共价化合物)
H2O
NaCl
NaOH
CaCl2
KNO3
H2SO4
【点评】 通过“联想质疑”、“归纳强调”、“迁移应用”,三个阶段,使学生对离子化合物和共价化合物的分类有一个清晰的认识。使学生认识到只要化合物中含离子键(不管是否含有有共价键)都叫离子化合物;只有当化合物中完全是共价键时,该化合物才叫共价化合物。
【知识点击】化学键与物质的性质是紧密联系的,离子键和共价键都是比较强的化学键,要破坏这些化学键都需要较多的能量,例如,氯化钠、碳酸钙、氧化镁等物质是离子化合物,他们熔化时要破坏离子键,由于离子键很强,因此他们的熔点也很高。氮分子发生化学反应时要破坏分子内很强的的共价键,由于该共价键很难破坏,因此氮分子化学性质很稳定;再如金刚石完全是由共价键构成的,金刚石熔化时要破坏内部的共价键,因此金刚石的熔点、沸点、硬度等都非常高。
【点评】通过学生阅读“知识点击”,将化学键与物质的性质联系起来,知道化学键是影响物质性质的重要因素之一。通过一些具体物质的熔沸点分析,使学生认识到离子键、共价键都是比较强的化学键,但由于影响物质性质的因素较多和学生知识的有限,这个地方也不要拓展、延伸过多。
【媒体展示——板书】第二部分:化学键与化学反应中的能量变化
【引入】研究化学反应中的能量转化关系是很重要的。在工农业生产和生活中,要利用各种能源,而化学反应所释放的能量(如石油、煤的燃烧)是当今世界上的重要能源之一。研究反应热,对于化工生产条件的选择,设备的设计和使用,以及对热能的综合利用,都具有很大的实际意义。以研究反应热为主要内容的化学热力学,是化学科学的一个重要分支。化学反应可以热、电或光等形式与外界环境进行能量交换,但通常主要表现为热能变化。
【交流·研讨】氢气和氧气反应生成1mol水蒸汽时的能量变化过程
【归纳·总结】在化学反应中,从反应物分子转化为生成物分子的过程中,各原子的内部并没有发生什么变化,但原子的结合方式发生了改变。在这个过程中反应物分子的化学键部分或全部遭到破坏,在生成物分子中形成新的化学键。实验证明,破坏旧的化学键时,需要从环境吸收能量来破坏原子间的相互吸引;在形成新的化学键时,由于原子间的相互吸引而对外释放能量。化学反应热就来源于旧化学键的破坏和新化学键的形成所发生的能量变化。
【思考·质疑——板书】能量会不会在反应过程中损耗或消失?
【拓展·引导】能量有各种不同的形式,它能从一种形式转化为另一种形式,或者从一物体传递给另一物体,但在转化和传递过程中,能量的总值是保持不变的(这叫能量守衡或转化定律)。化学反应过程遵循能量守衡定律。
【讨论】是不是所有的化学反应都是放热的?
【活动·探索】
【媒体显示——板书】每一个化学反应都伴随有能量的改变,有的对外释放能量,有的从外界吸收能量。如果新化学键的形成所释放的能量大于破坏旧化学键所吸收的能量,该反应就是放热反应;如果新化学键的形成所释放的能量小于破坏旧化学键所吸收的能量,该反应就是吸热反应;
【媒体显示——概括整合】
【点评】通过氢气和氧气生成1mol水蒸气的能量变化过程的分析,然后推广开来,得出结论:破坏旧的化学键时,需要从环境吸收能量来破坏原子间的相互吸引;在形成新的化学键时,由于原子间的相互吸引而对外释放能量。化学反应热就来源于旧化学键的破坏和新化学键的形成所发生的能量变化;通过“思考质疑”,对程度好的学生进行“知识拓展”,引入“能量守衡或转化”定律;通过“活动探索”使同学们对吸热和放热反应,增强直观印象,同时明白化学反应不仅存在放热反应也存在吸热反应;再通过“概括整合”,使同学们对化学反应过程中的能量变化过程有一个清晰的认识,知道能量变化与旧化学键的断裂和新化学键的形成有着密切的联系。
【作业】1、课本38页2、3、4
2、拓展延伸习题(略)
第1课时
第一部分:化学键与化学反应中的物质变化
知识点1:化学键的定义
【引入】前边通过元素周期律、周期表的学习,知道目前已知的元素种类只有一百多种,可这些元素却构成了已发现或合成的一千多万种物质,元素的原子能够相互结合形成多种多样的物质,说明形成这些物质的原子间一定存在着相互作用。
【演示实验】水在直流电的作用下分解
2H2O 2H2 + O2
【思考·质疑】水在通电条件下能够发生分解,为什么要通电?
【归纳】水分子是由两个氢原子和一个氧原子构成的,氢原子和氧原子之间存在着很强的相互作用,要破坏这种相互作用就需要消耗能量,通电正是为了提供使水分解所需要的能量。
【媒体展示——板书】 第1节 化学键与化学反应
化学键:相邻的(两个或多个)原子间的强相互作用
【对定义的强调】(1)首先必须相邻。不相邻一般就不强烈 (2)只相邻但不强烈,也不叫化学键 (3)“相互作用”不能说成“相互吸引”(实际既包括吸引又包括排斥)
【对上述(1)、(2)做解释——板书】
【进一步分析·归纳】水在通电时分解成H2和O2 ,在这个过程中首先水分子中氢原子和氧原子间的化学键断裂,形成单个的氢原子和氧原子,然后氢原子和氢原子间、氧原子和氧原子间分别又以新的化学键结合成为氢分子和氧分子。结论:化学反应的实质——旧化学键的断裂和新化学键的形成。
【点评】 通过学生对电解水为什么要提供能量的质疑,引出原子形成物质时,原子间确实存在着相互作用,教师及时引导给出化学键的定义。通过学生对化学键定义的阅读理解,教师进一步通过板书解释(水分子间的化学键的存在情况),强调理解化学键定义的几个关键点:(1)首先必须相邻。不相邻一般就不强烈 (2)只相邻但不强烈,也不叫化学键 (3)“相互作用”不能说成“相互吸引”(实际既包括吸引又包括排斥)。通过解释定义使学生对化学键作到了较深刻的理解。
知识点2:化学键的类型
【引入】元素有一百多种,这些元素从大的角度分两类:金属元素、非金属元素。金属元素一般容易失电子,非金属元素一般容易得电子。我们发现非金属和非金属元素之间,非金属元素和金属元素之间、金属元素和金属元素之间都可以通过化学键构成物质,他们之间的化学键是否一样呢?
【实验录象】钠在氯气中的燃烧实验录象
2Na + Cl2 ==== 2NaCl
氢气在氯气中的燃烧实验录象
H2 + Cl2 ==== 2HCl
【点评】“氢气在氯气中的燃烧”和“金属钠在氯气中的燃烧”是《化学1(必修)》中的演示实验,且实验过程中用到了有毒的气体——氯气。此时借助于实验录象不仅快捷省事,而且也不会因氯气的毒性或气体扩散而搞得满屋刺激性气味而影响教学。
【联想·质疑】氢气在氯气中的燃烧形成氯化氢和钠在氯气中的燃烧形成氯化钠,在形成化学键方面是否相同?
【归纳】氢气在氯气中燃烧时,氢分子和氯分子获得能量,化学键分别断裂,从而形成氢原子和氯原子。由于氢和氯都是非金属元素,都有得电子的趋势,最终谁也不能把对方的电子完全得到,而是氯原子和氢原子各提供一个电子组成共用电子对,从而使两者的最外层都达到稳定结构并产生强烈的相互作用——形成化学键。这样的化学键叫共价键。由于氯和氢都没有完全得失电子,因此,都不形成离子,HCl中的氢和氯不能叫氢离子氯离子,只能叫氢原子氯原子。
而在氯化钠的形成过程中,由于钠是金属元素很容易失电子,氯是非金属元素很容易得电子,当钠原子和氯原子靠近时,钠原子就失去最外层的一个电子形成钠阳离子,氯原子最外层得到钠的一个电子形成氯阴离子(两者最外层均达到稳定结构),阴、阳离子靠静电作用形成化学键——离子键,构成氯化钠。由于钠和氯原子之间是完全的得失电子,他们已形成了离子,因此NaCl中的微粒不能再叫原子,而应该叫离子。
【媒体展示——板书】
共价键:原子间通过共用电子对形成的化学键。一般非金属元素之间形成共价键。
离子键:阴阳离子之间通过静电作用形成的化学键。一般存在于金属和非金属之间。
【对定义的强调】(1)共价键的成键微粒是原子,而离子键的成键微粒是阴阳离子 (2)一般典型的非金属和非金属之间都形成共价键,典型的金属和非金属之间都形成离子键 (3)共价键和离子键的实质相同,都属于电性作用。成键原因都是原子都有使自己的最外层达到稳定结构状态的趋势。(稀有气体原子的最外层都已达到稳定结构,因此稀有气体分子都是单原子分子,分子内不形成化学键)
【迁移·应用——课堂练习】
指出构成下列物质的微粒和键型:NaCl、CaO、MgCl2 、H2O、CH4、NH3 、CO2
物质
形成化学键的微粒
化学键类型
H2O
CH4
NH3
NaCl
MgCl2
CaO
CO2
【知识拓展】非极性共价键:在单质分子中同种原子形成的共价键,两个原子对共用电子对共用电子对的吸引能力相同;共用电子对不偏向于任何一个原子,成键原子不显电性。这样的共价键叫非极性共价键。
极性共价键:在共价键形成的化合物分子中,由于不同原子对共用电子对的吸引能力不同,共用电子对会偏向于吸引电子能力强的一方,因此吸引电子能力强的原子带部分负电荷,吸引电子能力较弱的一方带部分正电荷,这样的共价键叫极性共价键。如氯化氢中的共价键就是极性共价键,共用电子对会偏向于氯原子一方偏离于氢原子一方。H2 、Cl2中的化学键。
【点评】 通过氯化氢和氯化钠两种物质的形成过程的剖析,分别给出共价键、离子键的定义;又通过他们化学键的形成特点,从成键微粒、成键原因、成键本质等方面,找出他们之间的异同点。然后把从具体事例得出的结论推广开来,重点强调在什么情况下会形成共价键,在什么情况下会形成离子键,再通过当堂举例判断、练习,使学生对概念的掌握比较清晰。
对于程度好的同学,通过“知识拓展”补充介绍“非极性共价键”和“极性共价键”的概念,以及化合价与共价键的关系,但不要进一步拓展,这样可以达到开拓学生思路的目的。
第2课时
知识点3:化学键与物质构成
【引入】我们已经学习过物质的分类,知道物质分纯净物、混合物;纯净物又分单质和化合物。通过化学键的学习,我们知道构成物的离子(或原子)之间的化学键也是有区别的——又分为离子键、共价键等。于是,人们根据化合物中所含化学键类型的不同,把化合物分为离子化合物和共价化合物。
【媒体展示——板书】
离子化合物:含有离子键的化合物。如:NaCl、CaCl2、KOH、CaO等
共价化合物:只含有共价键的化合物。如:HCl、H2O、CH4、NH3 、CO2
【联想·质疑】分析KOH中所含有的键型,该化合物属于哪类化合物?
【归纳·强调】(1)当一个化合物中只存在离子键时,该化合物是离子化合物(2)当一个化合中同时存在离子键和共价键时,以离子键为主,该化合物也称为离子化合物(3)只有当化合物中只存在共价键时,该化合物才称为共价化合物。(4)在离子化合物中一般既含有金属元素又含有非金属元素;共价化合物一般只含有非金属元素(NH4+例外)
【迁移·应用——课堂练习】
指出下列化合物内部的键型和化合物的分类(离子化合物、共价化合物)
化合物
内部的键型
分类(离子化合物、共价化合物)
H2O
NaCl
NaOH
CaCl2
KNO3
H2SO4
【点评】 通过“联想质疑”、“归纳强调”、“迁移应用”,三个阶段,使学生对离子化合物和共价化合物的分类有一个清晰的认识。使学生认识到只要化合物中含离子键(不管是否含有有共价键)都叫离子化合物;只有当化合物中完全是共价键时,该化合物才叫共价化合物。
【知识点击】化学键与物质的性质是紧密联系的,离子键和共价键都是比较强的化学键,要破坏这些化学键都需要较多的能量,例如,氯化钠、碳酸钙、氧化镁等物质是离子化合物,他们熔化时要破坏离子键,由于离子键很强,因此他们的熔点也很高。氮分子发生化学反应时要破坏分子内很强的的共价键,由于该共价键很难破坏,因此氮分子化学性质很稳定;再如金刚石完全是由共价键构成的,金刚石熔化时要破坏内部的共价键,因此金刚石的熔点、沸点、硬度等都非常高。
【点评】通过学生阅读“知识点击”,将化学键与物质的性质联系起来,知道化学键是影响物质性质的重要因素之一。通过一些具体物质的熔沸点分析,使学生认识到离子键、共价键都是比较强的化学键,但由于影响物质性质的因素较多和学生知识的有限,这个地方也不要拓展、延伸过多。
【媒体展示——板书】第二部分:化学键与化学反应中的能量变化
【引入】研究化学反应中的能量转化关系是很重要的。在工农业生产和生活中,要利用各种能源,而化学反应所释放的能量(如石油、煤的燃烧)是当今世界上的重要能源之一。研究反应热,对于化工生产条件的选择,设备的设计和使用,以及对热能的综合利用,都具有很大的实际意义。以研究反应热为主要内容的化学热力学,是化学科学的一个重要分支。化学反应可以热、电或光等形式与外界环境进行能量交换,但通常主要表现为热能变化。
【交流·研讨】氢气和氧气反应生成1mol水蒸汽时的能量变化过程
【归纳·总结】在化学反应中,从反应物分子转化为生成物分子的过程中,各原子的内部并没有发生什么变化,但原子的结合方式发生了改变。在这个过程中反应物分子的化学键部分或全部遭到破坏,在生成物分子中形成新的化学键。实验证明,破坏旧的化学键时,需要从环境吸收能量来破坏原子间的相互吸引;在形成新的化学键时,由于原子间的相互吸引而对外释放能量。化学反应热就来源于旧化学键的破坏和新化学键的形成所发生的能量变化。
【思考·质疑——板书】能量会不会在反应过程中损耗或消失?
【拓展·引导】能量有各种不同的形式,它能从一种形式转化为另一种形式,或者从一物体传递给另一物体,但在转化和传递过程中,能量的总值是保持不变的(这叫能量守衡或转化定律)。化学反应过程遵循能量守衡定律。
【讨论】是不是所有的化学反应都是放热的?
【活动·探索】
【媒体显示——板书】每一个化学反应都伴随有能量的改变,有的对外释放能量,有的从外界吸收能量。如果新化学键的形成所释放的能量大于破坏旧化学键所吸收的能量,该反应就是放热反应;如果新化学键的形成所释放的能量小于破坏旧化学键所吸收的能量,该反应就是吸热反应;
【媒体显示——概括整合】
【点评】通过氢气和氧气生成1mol水蒸气的能量变化过程的分析,然后推广开来,得出结论:破坏旧的化学键时,需要从环境吸收能量来破坏原子间的相互吸引;在形成新的化学键时,由于原子间的相互吸引而对外释放能量。化学反应热就来源于旧化学键的破坏和新化学键的形成所发生的能量变化;通过“思考质疑”,对程度好的学生进行“知识拓展”,引入“能量守衡或转化”定律;通过“活动探索”使同学们对吸热和放热反应,增强直观印象,同时明白化学反应不仅存在放热反应也存在吸热反应;再通过“概括整合”,使同学们对化学反应过程中的能量变化过程有一个清晰的认识,知道能量变化与旧化学键的断裂和新化学键的形成有着密切的联系。
【作业】1、课本38页2、3、4
2、拓展延伸习题(略)
