6.3溶解度曲线同步练习题 沪教版 九年级下册
文档属性
| 名称 | 6.3溶解度曲线同步练习题 沪教版 九年级下册 |

|
|
| 格式 | docx | ||
| 文件大小 | 422.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-05-14 00:00:00 | ||
图片预览


文档简介
溶解度曲线
甲、乙、丙三种固体物质的溶解度曲线如图所示,下列叙述错误的是( )
A.丙物质的溶解度随温度的升高而减小
B.t1℃时,甲和丙的溶解度均为20g
C.t2℃时,甲物质的饱和溶液中溶质质量分数为50%
D.甲物质中含有少量的乙物质,可用降温结晶的方法提纯甲
甲、乙两种物质的溶解度曲线如图所示。下列叙述正确的是( )
A.甲的溶解度比乙大
B.t2 C 时,100 g 甲溶液中最多有 50 g 甲
C.t1 C 时,甲、乙溶液中溶质的质量分数相等
D.甲、乙两种物质的溶解度都随温度升高而增大
如图为硫酸锌的溶解度曲线,下列说法正确的是( )
A.20 C 时,向 100 g 水中加入 60 g 硫酸锌,得到 160 g 溶液
B.30 C 时,硫酸锌饱和溶液中溶质的质量分数为 60%
C.将 80 C 的硫酸锌饱和溶液降温至 60 C,溶液仍饱和
D.60 C 的硫酸锌饱和溶液,无论升温或降温,均会有固体析出
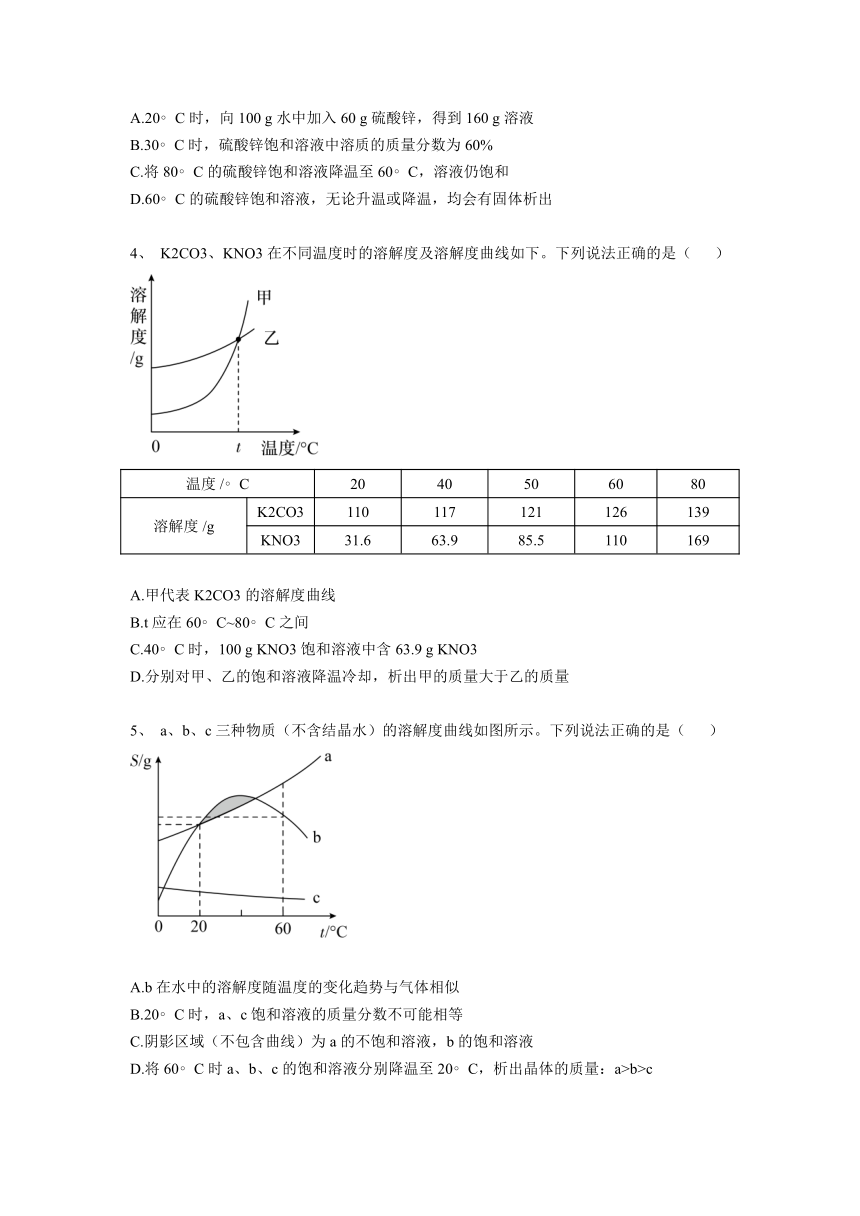
K2CO3、KNO3 在不同温度时的溶解度及溶解度曲线如下。下列说法正确的是( )
温度 / C 20 40 50 60 80
溶解度 /g K2CO3 110 117 121 126 139
KNO3 31.6 63.9 85.5 110 169
A.甲代表 K2CO3 的溶解度曲线
B.t 应在 60 C~80 C 之间
C.40 C 时,100 g KNO3 饱和溶液中含 63.9 g KNO3
D.分别对甲、乙的饱和溶液降温冷却,析出甲的质量大于乙的质量
a、b、c 三种物质(不含结晶水)的溶解度曲线如图所示。下列说法正确的是( )
A.b 在水中的溶解度随温度的变化趋势与气体相似
B.20 C 时,a、c 饱和溶液的质量分数不可能相等
C.阴影区域(不包含曲线)为 a 的不饱和溶液,b 的饱和溶液
D.将 60 C 时 a、b、c 的饱和溶液分别降温至 20 C,析出晶体的质量:a>b>c
小组同学们利用甲、乙物质进行了如图溶解实验,依据甲、乙物质的溶解度曲线分析,下列说法正确的是( )
A.a为乙物质
B.①和②中溶质的质量分数均为20%
C.甲中混有少量乙时,可用升温结晶的方法除去乙
D.t2℃时,等质量甲、乙分别配制成饱和溶液甲所需的水更少
固体物质 a、b、c 的溶解度曲线如图所示,下列相关说法正确的是( )
A.t1 C 时,将接近饱和的 c 溶液通过降温变为饱和溶液
B.要从 b 物质的饱和溶液中得到 b 物质的晶体,一般采用降温结晶法
C.t2 C 时,将 30 g 的 a 加入 50 g 水中充分溶解,可得 75 g 的 a 物质饱和溶液
D.分别将 a 和 c 的饱和溶液从 t1 C 升温至 t2 C,溶质质量分数 a 增大、c 减小
将一定质量的氢氧化钠固体加入一定质量蒸馏水中,不断搅拌,溶解过程中温度的变化如图所示。a、c 点溶液中有固体存在,b 点固体全部消失。下列说法不正确的是( )
A.a 点一定为饱和溶液,b 点不一定是饱和溶液
B.a 点溶液中氢氧化钠的溶质质量分数比 b 点小
C.c 点氢氧化钠溶解度比 d 点大
D.c 点析出固体的质量和 d 点一样多
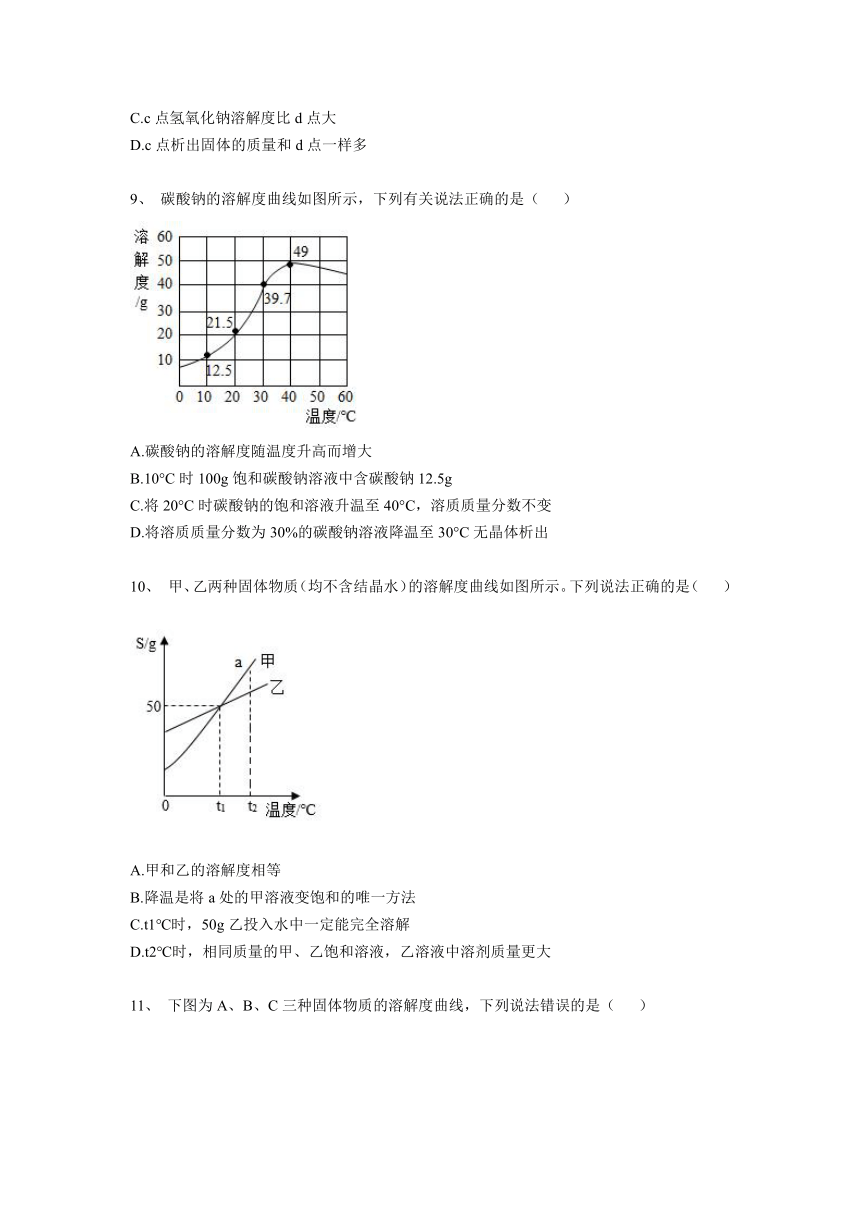
碳酸钠的溶解度曲线如图所示,下列有关说法正确的是( )
A.碳酸钠的溶解度随温度升高而增大
B.10°C时100g饱和碳酸钠溶液中含碳酸钠12.5g
C.将20°C时碳酸钠的饱和溶液升温至40°C,溶质质量分数不变
D.将溶质质量分数为30%的碳酸钠溶液降温至30°C无晶体析出
甲、乙两种固体物质(均不含结晶水)的溶解度曲线如图所示。下列说法正确的是( )
A.甲和乙的溶解度相等
B.降温是将a处的甲溶液变饱和的唯一方法
C.t1℃时,50g乙投入水中一定能完全溶解
D.t2℃时,相同质量的甲、乙饱和溶液,乙溶液中溶剂质量更大
下图为A、B、C三种固体物质的溶解度曲线,下列说法错误的是( )
A.A、B、C三种物质的溶解度都随着温度的升高而增大
B.在50℃时A物质的溶解度最大
C.在20℃时A物质和C物质的溶解度相等
D.根据溶解度曲线图,A物质适合采用降温结晶法得到晶体
我国航天员王亚平在太空演示“冰雪”实验时用到了过饱和醋酸钠溶液。如图是醋酸钠的溶解度曲线,下列说法正确的是( )
A.40℃时,醋酸钠的溶解度是65.6
B.图中P点所表示的醋酸钠溶液是饱和的
C.40℃时,饱和醋酸钠溶液的溶质质量分数是65.6%
D.将A点的饱和溶液降温至20℃,会有晶体析出
水和溶液在生产、生活中具有广泛的用途。
(1)明矾可用于净水,是因为明矾溶于水生成的胶状物可以__________悬浮于水中的杂质,使之从水中沉降出来。
(2)日常生活中软化硬水的方法是__________。
(3)KNO3 和 NaCl 两种固体的溶解度曲线如图。
①a 点对应的 KNO3 溶液与 a 点对应的 NaCl 溶液,前者与后者的溶质质量分数的关系是__________(填字母)。
A.大于 B.小于 C.等于 D.无法确定
②将 b 点对应的 KNO3 溶液升温至 t3 C,转变为__________(填“c”或“d”)点对应的 KNO3 溶液,前者与后者的溶质质量分数的关系是__________(填字母)。
A.大于 B.小于 C.等于 D.无法确定
③t3 C 时,将 50 g KNO3 加入到 50 g 水中,充分溶解,所得溶液的质量为 __________ 。(4)20 C 时,氯化钠的溶解度为 36 g.20 C 时,将 68 g 饱和氯化钠溶液稀释成质量分数为 18% 的氯化钠溶液,需要水的质量为__________。
甲、乙、丙三种固体物质的溶解度曲线如图所示,根据图示回答下列问题:
(1)t1℃时,甲的溶解度__________(填“>”、“<”或“=”)丙的溶解度。
(2)t2℃时,将100g水加入到盛有15g甲物质的烧杯中,充分溶解后所得溶液是甲物质的 __________(填“饱和”或“不饱和”)溶液。
(3)t3℃时,乙的饱和溶液中一定含40g乙物质,此说法是__________(填“正确”或“错误”)的。
(4)t3℃时,将甲、乙、丙三种物质的饱和溶液同时降温到t1℃,所得溶液中溶质的质量分数由小到大的顺序是__________。
(5)假设甲、丙均为白色固体,利用t3℃时的溶解度数据,__________(填“能”或“不能”)鉴别出甲、丙两种物质。
(6)若甲中含有少量乙,则提纯甲的方法是__________ 。
如图所示是甲、乙两种固体物质的溶解度曲线,请回答下列问题:
(1)t1℃时,甲物质的溶解度__________ (填“>”、“=”或“<”)乙物质的溶解度;
(2)溶解度受温度影响变化较大的是 __________ (填“甲”或“乙”)物质;
(3)t2℃时,把45g乙物质放入50g水中,充分搅拌,所得溶液是 __________(填“饱和”或“不饱和”)溶液;
(4)t2℃时,有一接近饱和的甲溶液,可采用__________的方法(写1种)使它变为该温度下的饱和溶液。
答案:
CDDBB DCDCD AD
吸附;煮沸;C;d;C;90g;32g
<
(2)不饱和
(3)错误
(4)甲< 丙< 乙
(5)能
(6)冷却热饱和溶液
(1)=
(2)甲
(3)饱和
(4)加入溶质(合理即可)
甲、乙、丙三种固体物质的溶解度曲线如图所示,下列叙述错误的是( )
A.丙物质的溶解度随温度的升高而减小
B.t1℃时,甲和丙的溶解度均为20g
C.t2℃时,甲物质的饱和溶液中溶质质量分数为50%
D.甲物质中含有少量的乙物质,可用降温结晶的方法提纯甲
甲、乙两种物质的溶解度曲线如图所示。下列叙述正确的是( )
A.甲的溶解度比乙大
B.t2 C 时,100 g 甲溶液中最多有 50 g 甲
C.t1 C 时,甲、乙溶液中溶质的质量分数相等
D.甲、乙两种物质的溶解度都随温度升高而增大
如图为硫酸锌的溶解度曲线,下列说法正确的是( )
A.20 C 时,向 100 g 水中加入 60 g 硫酸锌,得到 160 g 溶液
B.30 C 时,硫酸锌饱和溶液中溶质的质量分数为 60%
C.将 80 C 的硫酸锌饱和溶液降温至 60 C,溶液仍饱和
D.60 C 的硫酸锌饱和溶液,无论升温或降温,均会有固体析出
K2CO3、KNO3 在不同温度时的溶解度及溶解度曲线如下。下列说法正确的是( )
温度 / C 20 40 50 60 80
溶解度 /g K2CO3 110 117 121 126 139
KNO3 31.6 63.9 85.5 110 169
A.甲代表 K2CO3 的溶解度曲线
B.t 应在 60 C~80 C 之间
C.40 C 时,100 g KNO3 饱和溶液中含 63.9 g KNO3
D.分别对甲、乙的饱和溶液降温冷却,析出甲的质量大于乙的质量
a、b、c 三种物质(不含结晶水)的溶解度曲线如图所示。下列说法正确的是( )
A.b 在水中的溶解度随温度的变化趋势与气体相似
B.20 C 时,a、c 饱和溶液的质量分数不可能相等
C.阴影区域(不包含曲线)为 a 的不饱和溶液,b 的饱和溶液
D.将 60 C 时 a、b、c 的饱和溶液分别降温至 20 C,析出晶体的质量:a>b>c
小组同学们利用甲、乙物质进行了如图溶解实验,依据甲、乙物质的溶解度曲线分析,下列说法正确的是( )
A.a为乙物质
B.①和②中溶质的质量分数均为20%
C.甲中混有少量乙时,可用升温结晶的方法除去乙
D.t2℃时,等质量甲、乙分别配制成饱和溶液甲所需的水更少
固体物质 a、b、c 的溶解度曲线如图所示,下列相关说法正确的是( )
A.t1 C 时,将接近饱和的 c 溶液通过降温变为饱和溶液
B.要从 b 物质的饱和溶液中得到 b 物质的晶体,一般采用降温结晶法
C.t2 C 时,将 30 g 的 a 加入 50 g 水中充分溶解,可得 75 g 的 a 物质饱和溶液
D.分别将 a 和 c 的饱和溶液从 t1 C 升温至 t2 C,溶质质量分数 a 增大、c 减小
将一定质量的氢氧化钠固体加入一定质量蒸馏水中,不断搅拌,溶解过程中温度的变化如图所示。a、c 点溶液中有固体存在,b 点固体全部消失。下列说法不正确的是( )
A.a 点一定为饱和溶液,b 点不一定是饱和溶液
B.a 点溶液中氢氧化钠的溶质质量分数比 b 点小
C.c 点氢氧化钠溶解度比 d 点大
D.c 点析出固体的质量和 d 点一样多
碳酸钠的溶解度曲线如图所示,下列有关说法正确的是( )
A.碳酸钠的溶解度随温度升高而增大
B.10°C时100g饱和碳酸钠溶液中含碳酸钠12.5g
C.将20°C时碳酸钠的饱和溶液升温至40°C,溶质质量分数不变
D.将溶质质量分数为30%的碳酸钠溶液降温至30°C无晶体析出
甲、乙两种固体物质(均不含结晶水)的溶解度曲线如图所示。下列说法正确的是( )
A.甲和乙的溶解度相等
B.降温是将a处的甲溶液变饱和的唯一方法
C.t1℃时,50g乙投入水中一定能完全溶解
D.t2℃时,相同质量的甲、乙饱和溶液,乙溶液中溶剂质量更大
下图为A、B、C三种固体物质的溶解度曲线,下列说法错误的是( )
A.A、B、C三种物质的溶解度都随着温度的升高而增大
B.在50℃时A物质的溶解度最大
C.在20℃时A物质和C物质的溶解度相等
D.根据溶解度曲线图,A物质适合采用降温结晶法得到晶体
我国航天员王亚平在太空演示“冰雪”实验时用到了过饱和醋酸钠溶液。如图是醋酸钠的溶解度曲线,下列说法正确的是( )
A.40℃时,醋酸钠的溶解度是65.6
B.图中P点所表示的醋酸钠溶液是饱和的
C.40℃时,饱和醋酸钠溶液的溶质质量分数是65.6%
D.将A点的饱和溶液降温至20℃,会有晶体析出
水和溶液在生产、生活中具有广泛的用途。
(1)明矾可用于净水,是因为明矾溶于水生成的胶状物可以__________悬浮于水中的杂质,使之从水中沉降出来。
(2)日常生活中软化硬水的方法是__________。
(3)KNO3 和 NaCl 两种固体的溶解度曲线如图。
①a 点对应的 KNO3 溶液与 a 点对应的 NaCl 溶液,前者与后者的溶质质量分数的关系是__________(填字母)。
A.大于 B.小于 C.等于 D.无法确定
②将 b 点对应的 KNO3 溶液升温至 t3 C,转变为__________(填“c”或“d”)点对应的 KNO3 溶液,前者与后者的溶质质量分数的关系是__________(填字母)。
A.大于 B.小于 C.等于 D.无法确定
③t3 C 时,将 50 g KNO3 加入到 50 g 水中,充分溶解,所得溶液的质量为 __________ 。(4)20 C 时,氯化钠的溶解度为 36 g.20 C 时,将 68 g 饱和氯化钠溶液稀释成质量分数为 18% 的氯化钠溶液,需要水的质量为__________。
甲、乙、丙三种固体物质的溶解度曲线如图所示,根据图示回答下列问题:
(1)t1℃时,甲的溶解度__________(填“>”、“<”或“=”)丙的溶解度。
(2)t2℃时,将100g水加入到盛有15g甲物质的烧杯中,充分溶解后所得溶液是甲物质的 __________(填“饱和”或“不饱和”)溶液。
(3)t3℃时,乙的饱和溶液中一定含40g乙物质,此说法是__________(填“正确”或“错误”)的。
(4)t3℃时,将甲、乙、丙三种物质的饱和溶液同时降温到t1℃,所得溶液中溶质的质量分数由小到大的顺序是__________。
(5)假设甲、丙均为白色固体,利用t3℃时的溶解度数据,__________(填“能”或“不能”)鉴别出甲、丙两种物质。
(6)若甲中含有少量乙,则提纯甲的方法是__________ 。
如图所示是甲、乙两种固体物质的溶解度曲线,请回答下列问题:
(1)t1℃时,甲物质的溶解度__________ (填“>”、“=”或“<”)乙物质的溶解度;
(2)溶解度受温度影响变化较大的是 __________ (填“甲”或“乙”)物质;
(3)t2℃时,把45g乙物质放入50g水中,充分搅拌,所得溶液是 __________(填“饱和”或“不饱和”)溶液;
(4)t2℃时,有一接近饱和的甲溶液,可采用__________的方法(写1种)使它变为该温度下的饱和溶液。
答案:
CDDBB DCDCD AD
吸附;煮沸;C;d;C;90g;32g
<
(2)不饱和
(3)错误
(4)甲< 丙< 乙
(5)能
(6)冷却热饱和溶液
(1)=
(2)甲
(3)饱和
(4)加入溶质(合理即可)
