浙教版科学八年级下册期末专题复习:解答题三(含解析)
文档属性
| 名称 | 浙教版科学八年级下册期末专题复习:解答题三(含解析) |

|
|
| 格式 | docx | ||
| 文件大小 | 135.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2023-06-11 00:00:00 | ||
图片预览




文档简介
浙教版科学八年级下册期末专题复习:解答题三
一 、解答题
1.有一种电加热恒温箱,工作原理如图甲所示. 控制电路由电压为 U1=9V 的电源、电磁继电器(线圈 电阻不计)、滑动变阻器 R2 和热敏电阻 R1 组成, 图乙是热敏电阻 R1 阻值随温度变化的图象;工作 电路由电压为 U2=220V 的电源和电阻为 R0 的电热丝组成.通过实验测得当电磁继电器线圈的电流达
到 60mA 时,电磁继电器的衔铁被吸下来。求:
(1) 按照题意将图中的工作电路连接完整,C 点应与 相连。(选填 “A”或 “B” );
(2) 在升温的过程中, 通过电阻 R1 的电流会 (选填“变大”、“变小”或“不变”);
(3)要使恒温箱设定的温度值升高,应调节滑动变阻器 R2 的滑片,使其接入电路的阻值 (选 填“变大”或“变小”)。
(4) 当滑动变阻器 R2 接入电路中的电阻为 90Ω 时,恒温箱内的温度是多大?
2.电梯为了安全, 都设置超载自动报警系统,其工作原理如图甲所示。已知控制电路电源电压 U=6V,
保护电阻 R1 =100Ω,压敏电阻 R2 的阻值随压力 F 大小变化如图乙所示,电梯底架自重和电磁铁线圈的
阻值都忽略不计。
第 1 页(共 13 页)
(1) 电梯超载时, 衔铁被电磁铁吸住,触点 K 与触点 接触, 电铃发出警报声, 同时电动机 (选填“能”、“不能”)工作。
(2)当电磁铁线圈电流达到 20mA 时,衔铁刚好被吸住。若该电梯厢内站立总质量为 1000kg 的乘客时, 则通过电磁铁的电流 mA.此时电梯是否超载 ?请通过计算回答。 (g 取 10N/kg) 3.
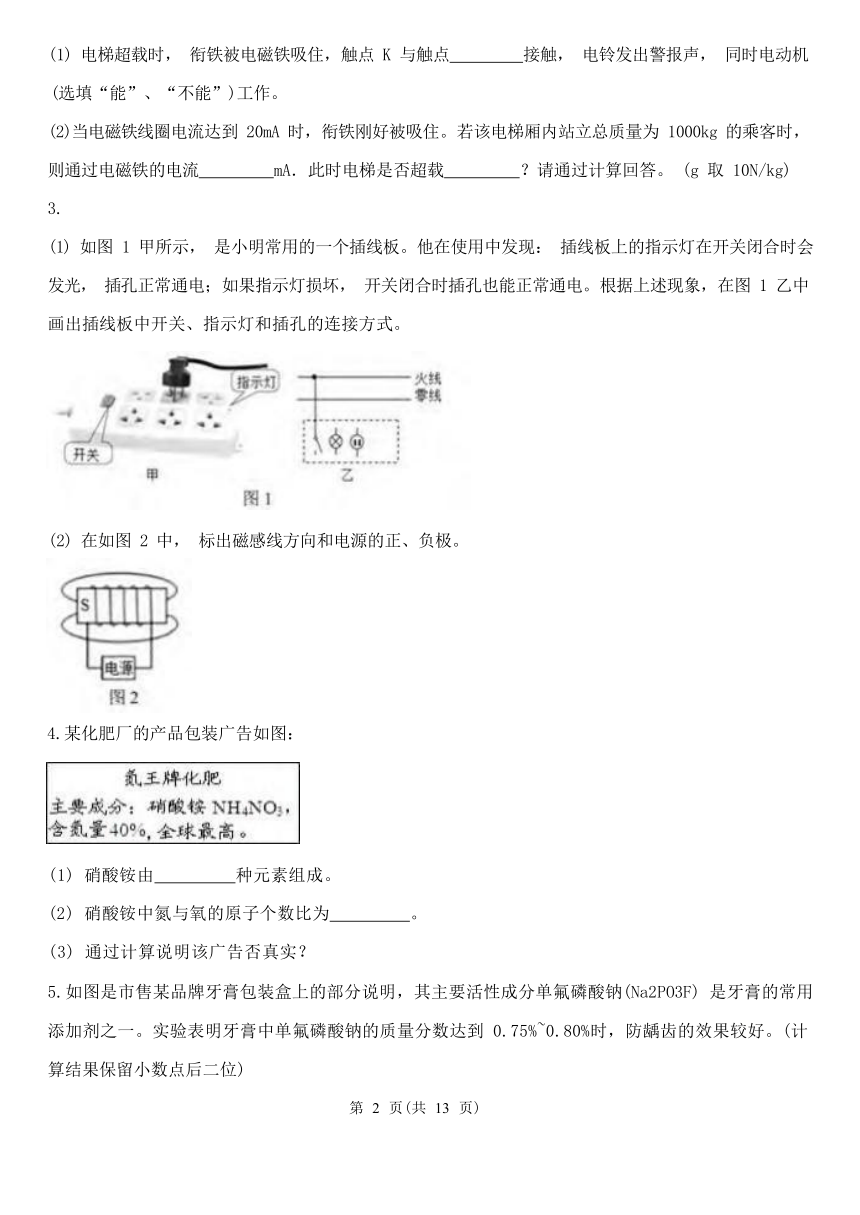
(1) 如图 1 甲所示, 是小明常用的一个插线板。他在使用中发现: 插线板上的指示灯在开关闭合时会 发光, 插孔正常通电;如果指示灯损坏, 开关闭合时插孔也能正常通电。根据上述现象,在图 1 乙中 画出插线板中开关、指示灯和插孔的连接方式。
(2) 在如图 2 中, 标出磁感线方向和电源的正、负极。
4.某化肥厂的产品包装广告如图:
(1) 硝酸铵由 种元素组成。
(2) 硝酸铵中氮与氧的原子个数比为 。
(3) 通过计算说明该广告否真实?
5.如图是市售某品牌牙膏包装盒上的部分说明,其主要活性成分单氟磷酸钠(Na2PO3F) 是牙膏的常用 添加剂之一。实验表明牙膏中单氟磷酸钠的质量分数达到 0.75%~0.80%时,防龋齿的效果较好。(计 算结果保留小数点后二位)
第 2 页(共 13 页)
(1) 根据单氟磷酸钠的化学式, 计算单氟磷酸钠的相对分子质量:
(2) 根据单氟磷酸钠的化学式, 计算单氟磷酸钠中氟元素的质量分数为
(3) 为了判断该牙膏的说明是否准确,需进行如下计算:
① 该牙膏中氟元素的质量分数为 ;
②该牙膏中单氟磷酸钠的质量分数为 ,该牙膏 (填“具有”或“没有”) 较好的 防龋齿效果。
6.蛋白质是机体生长及修补受损组织的主要原料,人体通过食物获得的蛋白质在胃肠中与水反应生成
氨基酸,蛋氨酸(分子式为 C5H11O2NS)就是其中的一种。请回答下列问题:
(1) 蛋氨酸中各元素的质量比: C∶H∶O∶N∶S= ;
(2) 蛋氨酸中氮元素的质量分数为多少? ;
(3) 合格奶粉每 100g 中含蛋白质约 18g,蛋白质中氮元素的平均质量分数为 16%,则每 100g 合格奶 粉中氮的质量为多少?现测定某奶粉每 100g 中含有氮元素的质量为 1.5g。则这种奶粉合格吗? 7.酸雨、温室效应、生物的多样性减少、土地荒漠化、化学污染、极地臭氧层空洞…世界环境问题已 经严重的威胁到人类的生存.1972 年 6 月 5 日《联合国人类环境会议》将每年的 6 月 5 日定为“世界环 境日 ”.“世界环境日”的作用在于唤起全世界人民都来注意保护人类赖以生存的环境,自觉采取行 动参与环境保护,同时要求各国政府和联合国系统为推进保护进程做出贡献.2010 年世界环境日的世界 主题为“多个物种, 一个星球, 一个未来”,点出了保护地球上生命多样性的紧迫性.中国主题为“低 碳减排 绿色生活”,意指二氧化碳直接威胁到人类的生存与生活,倡导人们过上”绿色、低碳生活. (1) 在世界环境问题中,全球性大气污染问题不容忽视. 其中引起温室效应的气体主要是 ; 造成酸雨的主要气体是
A.二氧化碳 B.二氧化硫 C.一氧化碳
(2) 有“空中死神”之称的是
A.臭氧层空洞 B.酸雨 C.温室效应
(3) “多个物种, 一个星球,一个未来”,其中“多个物种”具体是指 第 3 页(共 13 页)
A.生物种类的多样性
B.基因的多样性
C.生态系统的多样性.
8.将 9.5 克 KClO3 和 MnO2 的混合物装入大试管中,加热至质量不再发生变化, 冷却试管后称量,剩有 6.62 克固体物质。计算:
(1)写出上述涉及到的化学方程式________。
(2)6.62 克固体中含有哪些物质?各多少克?
9.学校八年级科学兴趣小组为了测定某矿山石灰石中碳酸钙的质量分数, 取石灰石样品与足量稀盐酸 在烧杯中反应(假设石灰石样品中杂质不与稀盐酸反应也不溶于水,杂质中不含钙元素)。有关实验数
据如下表:
反 应 前 反 应 后
实验数据 烧杯和稀盐酸的质量 石灰石样品的质量 烧杯和剩余物的总质量
150g 12.5g 158.1g
(1) 根据质量守恒定律可知,反应中生成二氧化碳的质量为 g。
(2) 该石灰石中碳酸钙的质量分数
为
。
(3) 反应中生成氯化钙的质量是多少克? (写出计算过程) 10.树叶叶片不仅可以吸收一些有害气体,还可以利用光能把二氧化碳转化为淀粉和氧气, 起到改善环 境的作用.通常晴天时, 每天每平方米叶片可吸收 5g 二氧化碳来进行光合作用,则:
(1) 某公园中叶片面积约为 100 万平方米,在一个月 (按 20 个晴天计)内可以吸收二氧化碳气
体 ;
(2) 空气中二氧化碳含量增加会引起“温室效应”,导致地球气候变暖,①空气中二氧化碳的主要来 源是 ,②为了防止温室效应的产生可以采取 的措施
是
.
第 4 页(共 13 页)
11.环境污染对植物的生长有不同程度的影响,在一定程度上,植物在被污染的环境中生活时,也有继 续保持正常生理活动的特性,这种特性称为抗性。研究植物的抗性对筛选具有净化环境作用的植物种 类和保护环境有积极的意义。一项研究表明, 植物对 SO2 的抗性与叶片上气孔的大小和多少有关。所得
数据如下表:
被测植物 平均受害面积/% 气孔
气孔密度/(个/厘米 2) 每个气孔面积/微米 2
甲植物 13.5 370 2.72
乙植物 33.5 250 4.16
丙植物 57.5 180 5.56
(1)该研究表明,植物对 SO2 的抗性与气孔密度的关系是 , 与每个气孔面积的关系是 。
(2)在 SO2 污染严重的地区, 最好选择表中 植物为主要绿化树种。大气中 SO2 的主要危害是 产生 现象,即 pH 小于 的酸性降水。除 SO2 外,常见的大气污染物还有 (写出一种)。
(3)对 SO2 污染物的处理,可用 NaOH 溶液吸收(化学方程式为 2NaOH+SO2===Na2SO3+H2O)。2005 年, 我国排放 SO2 总量约达 2549 万吨。若全部用 NaOH 处理,则需 NaOH 固体多少吨?
第 5 页(共 13 页)
12. “毒大米”事件让人们认识到了重金属污染的危害,重金属在土壤中的分散范围广、隐蔽性强、 难清理,现在科学家利用一类超强金属吸收能力的植物(又叫超富集植物)对土壤进行“排毒”。
(1)双子叶的超富集植物, 由根系从土壤中吸取重金属,可通过木质茎中的________ (填“韧皮 部”“木质部”或“形成层”),转移、贮存到枝叶等地上部分。
(2)一种叫做重雪球的植物,富集金属镍的能力很强。通过改良植株增强重雪球的吸镍性,每克干燥的 枝叶可含有 0.2 克镍。对 500 千克的重雪球的干燥枝叶进行提纯处理, 理论上可获得________千克的 镍。
(3)超富集植物能帮助人们更好地改善由于采矿等原因而恶化的土壤,使耕地重新焕发生机。植物“排
毒”具有的优势是________ (写出一点即可)。
13.下图是一副叶和根对话的漫画图,仔细分析漫画, 回答下列问题;
(1) 叶进行光合作用为茎和根提供 ,同时释放氧气。
(2) 如果茎中的 “罢工”,则根吸收的 和 无法运输到叶。
第 6 页(共 13 页)
0.浙教版科学八年级下册期末专题复习:解答题三答案解析
一 、解答题
1. 【答案】(1) A
(2) 变大
(3) 变大
(4) 当电流为 60mA 时, 总电阻R总 = I (U)总 (总) = = 150;
此时热敏电阻 R1=R 总-R2=150Ω-90Ω=60Ω。
根据乙图可知,此时恒温箱内的温度是 100℃。
【解析】(1)根据恒温箱的工作状态确定衔铁的位置,进而判断接线情况;
(2) 首先根据乙图确定温度升高后热敏电阻 R1 的阻值变化,再根据 R 总=R1+R2 判断总电阻的变化, 最 后根据“电流与电阻的反比关系”确定电流变化。
(3) 电磁铁吸合时的电流大小不变, 则总电阻不变,根据 R 总=R1+R2 分析变阻器的阻值变化即可;
(4) 首先根据公式R总 = I (U)总 (总)计算出总电阻,再根据 R1=R 总-R2 计算出热敏电阻的阻值,最后根据图乙确 定恒温箱内的温度。
【解答】(1)当温度升高时,热敏电阻的阻值减小,那么总电阻变小而总电流变大,那么电磁铁的磁 场增强,将衔铁吸下来切断发热电阻 R0 的工作, 则 C 应该与 A 相接。
(2) 在升温的过程中, 热敏电阻 R1 的阻值减小, 根据 R 总=R1+R2 可知, 总电阻减小, 而总电流增大。
(3) 电磁铁吸合时的电流大小不变, 则总电阻不变。当温度升高时,热敏电阻 R1 的阻值减小, 据 R 总
=R1+R2 可知, 此时变阻器接入的阻值应该变大。
(4) 当电流为 60mA 时, 总电阻R总 = I (U)总 (总) = = 150; 此时热敏电阻 R1=R 总-R2=150Ω-90Ω=60Ω。
根据乙图可知, 此时恒温箱内的温度是 100℃。
2. (1) B;不能
(2) 30;是超载
【解析】(1)根据衔铁的运动方向判断它与哪个触点接触,进而判断电动机所在的电路是否被接通即
可。
第 7 页(共 13 页)
(2) 首先根据 F=G=mg 计算出乘客对电梯的压力, 然后根据乙图确定此时压敏电阻 R2 的阻值, 接下来 根据串联电路 R 总=R1+R2 计算出总电阻,最后根据I总 = R (U)总 (总)计算出总电流,并与 20mA 进行比较即可。
(1) 根据甲图可知,电梯超载时,衔铁被电磁铁吸住, 衔铁向下运动,触点 K 与触点 B 接触,电铃所 在的电路被接通,电铃发出警报声, 电动机所在的电路断开, 因此电动机不能工作。
(2) 乘客对电梯的压力 F=G=mg=1000kg×10N/kg=10 N;4
根据乙图可知, 此时压敏电阻 R2=100Ω;
电路的总电阻 R 总=R1+R2=100Ω+100Ω=200Ω;
通过电磁铁的电流I总 = R (U)总 (总) = = 0.03A = 30mA > 20mA。
则此时电梯是超载的。
3. 【答案】(1)
(2)
【解析】(1) ①如果用电器相互影响,那么它们串联;否则, 它们并联;
②干路开关控制所有用电器,支路开关只能控制它所在支路上的开关。
(2) 根据安培定则确定线圈上的电流方向,进而确定电源的正负极;在磁体外部, 磁感线总是从磁体 的 N 极回到S 极。
【解答】(1)如果指示灯损坏, 插孔依然可以正常通电, 那么说明二者不相互影响,因此它们并联。 开关能够同时控制指示灯和插孔,说明它在干路上。从火线上引线,首先通过开关,然后灯泡与插座
并联, 再接在零线上即可,如下图所示:
(2) 根据图片可知, 螺线管的右端为 N 极,因此磁感线的方向都是向左的。右手握住螺线管,大拇指 第 8 页(共 13 页)
指向右端, 此时弯曲的四指指尖向下,那么线圈上电流方向向下, 即电流从左端流入, 那么电源的左
端为正极, 右端为负极, 如下图所示:
4. (1) 3
(2) 2∶3
(3) N%=14×2/(14×2+4+16×3)=35%<40% 所以 不真实
(1) 根据化学式确定该物质的元素组成分析;
(2) 根据元素质量比为相对原子质量×原子个数之比分析;
(3) 根据化学式确定氮元素的质量分数, 然后对比标签中所给数值确定是否真实。
【解答】(1)硝酸铵是由氮、氢、氧三种元素组成的;
(2) 硝酸铵中氮与氧的原子个数比为 2:3;
(3)硝酸铵中氮元素质量分数为 14×2/(14×2+4+16×3)=35% ,与所给 40%不相符,所以广告不真实;
故答案为: (1) 3;(2) 2:3;(3) 不真实。
5. (1) 144
(2) 13.19%
(3) 0.10%;0.79%;具有
(1) 根据相对分子质量为分子中各原子的相对原子质量之和分析;
(2) 根据元素质量分数=相对原子质量×原子个数/相对分子质量分析;
(3) 根据标签中所给信息利用牙膏中氟元素质量即为 单氟磷酸钠 中氟元素质量分析;
【解答】(1) 单氟磷酸钠的相对分子质量为 23×2+31+16×3+19=144;
(2) 单氟磷酸钠中氟元素的质量分数为 × 100%=13.19%;
(3) 该牙膏中氟元素的质量分数为 × 100% = 0.10%; 该牙膏中单氟磷酸钠的质量分数为 =0.79%,牙膏中氟的含量在 0.75%~0.80% 范围内, 有 较好的防龋齿效果。
第 9 页(共 13 页)
故答案为: (1) 144;(2) 13.19%;(3) 0.10%;0.79%;具有。 6. (1) 60:11:32:14:32 (2) 9.4% (3) 根据题意,合格奶粉每 100g 中含蛋白质 18g,蛋白质中氮元素的平均质量分数为 16%,则每 1000g
合格奶粉中氮元素的质量至少为:18g×16%=2.88g>1.5g. 故该奶粉不合格.故答案为: 2.88g;不合格. (1) 根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.(2)根据 元素的质量分数的计算方法来分析.(3) 根据物质的质量和元素的质量分数可以计算出元素的质量.本 题难度不大,考查同学们结合新信息、灵活运用化学式的有关计算进行分析问题、解决问题的能力. 【解答】解:(1) 根据化合物中各元素质量比=各元素的相对原子质量×原子个数之比,可得蛋氨酸(化 学式为 C5H11O2NS) 中碳、氢、氧、氮、硫五种元素的质量比为(12×5):(1×11):(16×2):(14×1): (32×1) =60:11:32:14:32.故答案为:60:11:32:14:32;(2) 蛋氨酸(化学式为 C5H11O2NS) 中氮元素的质量分数= ≈ 9.4% .故答案为: 9.4%; 7. 【答案】(1) A;B (2) B (3) A 【解析】此题主要考查的是温室效应、酸雨的危害以及低碳生活的相关内容,分析资料解答. 【解答】解:(1)、二氧化碳气体具有吸热和隔热的功能. 它在大气中增多的结果是形成一种无形的玻 璃罩, 使太阳辐射到地球上的热量无法向外层空间发散, 其结果是地球表面变热起来. 因此,二氧化 碳也被称为温室气体.温室效应加剧主要是由于现代化工业社会燃烧过多煤炭、石油和天然气, 这些 燃料燃烧后放出大量的二氧化碳气体进入大气造成的. 酸雨是由于人类大量使用含硫量高的煤、石油、天然气等化石燃料,燃烧后产生的含有二氧化硫等的 气体, 在大气中经过复杂的化学反应后, 形成硫酸或硝酸气溶胶, 或为云、雨、雪、雾捕捉吸收,降 到地面成为的.(2)、酸雨危害水生生物, 它使许多河、湖水质酸化,导致许多对酸敏感的水生生物种 群灭绝,湖泊失去生态机能,最后变成死湖. 酸雨还杀死水中的浮游生物, 破坏水生生态系统此外, 酸化的水源威胁人们的健康, 酸雨对生物有极大的危害, 因此被称为“空中死神”.(3)、生物的多样 性包括生物种类的多样性、基因的多样性、生态系统的多样性等三个方面的内容, “多个物种, 一个
第 10 页(共 13 页)
星球, 一个未来”,其中“多个物种”具体指的是生物种类的多样性.
故答案为: (1) A.B (2) B (3) A
8. (1)2KClO3 2KCl+3O2 ↑ (2)mO2=9.5g-6.62g=2.88g 设生成氯化钾质量为 X,则
2KClO3 MnO2 2KCl+ 3O2 ↑
第 11 页(共 13 页)
149
X
96
2.88
克
149∶96=X∶2.88 克 X=4.47 克
二氧化锰的质量=6.62 克-4.47 克=2.15 克
9. (1) 4.4
(2) 设该石灰石样品中碳酸钙的质量为 x. CaCO3+2HCl═CaCl2+H2O+CO2 ↑ 100 44 x 4.4g = 解 得: x=10.0g 此石灰石中碳酸钙的质量分数为: × 100% = 80%。
(3) 设生成的氯化钙的质量为 y
CaCO3+2HCl═CaCl2+H2O+CO2 ↑
111
y
=
解得:y=11.1g
44
4.4g
则生成的氯化钙的质量为 11.1g。
【解析】(1)根据质量守恒定律可知:反应后比反应前减少的质量是生成二氧化碳的质量;
(2) 根据化学方程式由二氧化碳的质量可以计算出石灰石中碳酸钙的质量, 进而计算出石灰石中碳酸 钙的质量分数;
(3) 根据化学方程式由二氧化碳的质量可以计算出氯化钙的质量。(1) 根据质量守恒定律, 二氧化碳 的质量为: 150g+12.5g-158.1g=4.4g;
10. 【答案】(1) 1.0×108g;
(2) 化石燃料的燃烧,动物的呼吸,动植物尸体的腐烂等;大量植树造林、禁止乱砍乱伐,更多的利
用核能、太阳能、风能、地热能、氢能等新能源等.
【解析】【解答】 (1)叶片面积约 100 万平方米,在一个月 (按 20 个晴天计)内可吸收 CO2 气体 1×106×5g×20=1.0×108g.
(2)①空气中二氧化碳的主要来源是化石燃料的燃烧,动物的呼吸, 动植物尸体的腐烂等; ②为了防止温室效应的产生可以采取的措施有大量植树造林、禁止乱砍乱伐,更多的利用核能、太阳 能、风能、地热能、氢能等新能源等.
(1)先根据植物每天每平方米需吸收 5g 二氧化碳,则 100 万平方米的叶片在一个月 (按 20 个晴天计)可 吸收二氧化碳.
(2)根据二氧化碳的来源和防止温室效应的措施回答.
11. (1) 气孔密度越大,植物对 SO2 的抗性越强;每个气孔面积越大,植物对 SO2 的抗性越弱
(2) 甲; 酸雨;5.6;一氧化碳(合理均可)
(3) 解: 设需要 NaOH x 万吨。
2NaOH┼SO2=Na2SO3┼H2O
第 12 页(共 13 页)
80
x
64
2549
80:64=x:2549
x=80*2549/64=3186.25 万吨
答:若全部用 NaOH 处理,则需 NaOH 固体 3186.25 万吨。
【解析】本题为分析和计算综合题,通过分析题中信息, 可以得出答案。(1) 若植物对 SO2 的抗性越强, 则植物的平均受害面积越小。(2)甲植物的平均受害面积最小。(3)大气中 SO2 的主要危害是产生硫酸, 可表示为 2SO2+2H2O+O2===2H2SO4 。常见的大气污染物还有 CO、NO2、可吸入颗粒物等。
(1) 依题意, 由表可知: 植物对二氧化硫的抗性随着叶片上气孔密度的增大而减小,随着叶片上每个 气孔的面积的增大而增大。(2)在 SO2 污染严重的地区, 最好选择表中甲植物为主要绿化树种。大气中 SO2 的主要危害是产生酸雨现象,即 pH 小于 5.6 的酸性降水。除 SO2 外,常见的大气污染物还有一氧化 碳。(3)设需要 NaOH x 万吨。根据物质守恒定律进行计算即可。
故答案为: (1) 气孔密度越大, 植物对 SO2 的抗性越强;每个气孔面积越大, 植物对 SO2 的抗性越弱;
(2) 酸雨;5.6;一氧化碳(合理均可);
(3) 解: 设需要 NaOH x 万吨。
2NaOH┼SO2=Na2SO3┼H2O
80 64
x 2549
80:64=x:2549
x=80*2549/64=3186.25 万吨
答:若全部用 NaOH 处理,则需 NaOH 固体 3186.25 万吨。
12. (1)木质部(2)100(3)简便(或高效、环保、资源回收、增加收入等, 合理均可) 13. (1) 有机物
(2) 导管;水;无机盐
【解析】(1)植物光合作用的过程是十分复杂的, 它包括许多化学反应。但主要包含了以下两方面的 变化: 一方面, 把简单的无机物制成了复杂的有机物,并放出氧气,发生了物质转化; 另一方面,把 光能变成储存在有机物里的化学能, 实现了能量的转化。
(2) 输导水分和无机盐的导管是多种多样的,它们位于木质部中,水分和无机盐在茎木质部的导管中 能自下而上地向枝端运输;而输导有机物的是筛管 ,位于韧皮部中,韧皮部在树皮靠近木质部的地方, 有机物在茎的树皮中由上而下地运输着。
(1) 绿色植物通过光合作用制造的有机物不仅满足了自身生长、发育、繁殖的需要, 还为其他生物 提供了基本的食物来源; 同时生成的氧气也供给其它生物呼吸所用。叶进行光合作用为茎和根提供有 机物, 同时释放氧气。
(2) 根吸收的水和无机盐是通过茎中的导管之下而上运送到叶的; 叶光合作用制造的有机物是通过茎 中的筛管自上而下运送到植物各部位的。所以如果茎中的导管“罢工”,则根是、吸收的水和无机盐 就无法运输到叶。
故答案为: (1) 有机物; (2)导管; 水; 无机盐
第 13 页(共 13 页)
一 、解答题
1.有一种电加热恒温箱,工作原理如图甲所示. 控制电路由电压为 U1=9V 的电源、电磁继电器(线圈 电阻不计)、滑动变阻器 R2 和热敏电阻 R1 组成, 图乙是热敏电阻 R1 阻值随温度变化的图象;工作 电路由电压为 U2=220V 的电源和电阻为 R0 的电热丝组成.通过实验测得当电磁继电器线圈的电流达
到 60mA 时,电磁继电器的衔铁被吸下来。求:
(1) 按照题意将图中的工作电路连接完整,C 点应与 相连。(选填 “A”或 “B” );
(2) 在升温的过程中, 通过电阻 R1 的电流会 (选填“变大”、“变小”或“不变”);
(3)要使恒温箱设定的温度值升高,应调节滑动变阻器 R2 的滑片,使其接入电路的阻值 (选 填“变大”或“变小”)。
(4) 当滑动变阻器 R2 接入电路中的电阻为 90Ω 时,恒温箱内的温度是多大?
2.电梯为了安全, 都设置超载自动报警系统,其工作原理如图甲所示。已知控制电路电源电压 U=6V,
保护电阻 R1 =100Ω,压敏电阻 R2 的阻值随压力 F 大小变化如图乙所示,电梯底架自重和电磁铁线圈的
阻值都忽略不计。
第 1 页(共 13 页)
(1) 电梯超载时, 衔铁被电磁铁吸住,触点 K 与触点 接触, 电铃发出警报声, 同时电动机 (选填“能”、“不能”)工作。
(2)当电磁铁线圈电流达到 20mA 时,衔铁刚好被吸住。若该电梯厢内站立总质量为 1000kg 的乘客时, 则通过电磁铁的电流 mA.此时电梯是否超载 ?请通过计算回答。 (g 取 10N/kg) 3.
(1) 如图 1 甲所示, 是小明常用的一个插线板。他在使用中发现: 插线板上的指示灯在开关闭合时会 发光, 插孔正常通电;如果指示灯损坏, 开关闭合时插孔也能正常通电。根据上述现象,在图 1 乙中 画出插线板中开关、指示灯和插孔的连接方式。
(2) 在如图 2 中, 标出磁感线方向和电源的正、负极。
4.某化肥厂的产品包装广告如图:
(1) 硝酸铵由 种元素组成。
(2) 硝酸铵中氮与氧的原子个数比为 。
(3) 通过计算说明该广告否真实?
5.如图是市售某品牌牙膏包装盒上的部分说明,其主要活性成分单氟磷酸钠(Na2PO3F) 是牙膏的常用 添加剂之一。实验表明牙膏中单氟磷酸钠的质量分数达到 0.75%~0.80%时,防龋齿的效果较好。(计 算结果保留小数点后二位)
第 2 页(共 13 页)
(1) 根据单氟磷酸钠的化学式, 计算单氟磷酸钠的相对分子质量:
(2) 根据单氟磷酸钠的化学式, 计算单氟磷酸钠中氟元素的质量分数为
(3) 为了判断该牙膏的说明是否准确,需进行如下计算:
① 该牙膏中氟元素的质量分数为 ;
②该牙膏中单氟磷酸钠的质量分数为 ,该牙膏 (填“具有”或“没有”) 较好的 防龋齿效果。
6.蛋白质是机体生长及修补受损组织的主要原料,人体通过食物获得的蛋白质在胃肠中与水反应生成
氨基酸,蛋氨酸(分子式为 C5H11O2NS)就是其中的一种。请回答下列问题:
(1) 蛋氨酸中各元素的质量比: C∶H∶O∶N∶S= ;
(2) 蛋氨酸中氮元素的质量分数为多少? ;
(3) 合格奶粉每 100g 中含蛋白质约 18g,蛋白质中氮元素的平均质量分数为 16%,则每 100g 合格奶 粉中氮的质量为多少?现测定某奶粉每 100g 中含有氮元素的质量为 1.5g。则这种奶粉合格吗? 7.酸雨、温室效应、生物的多样性减少、土地荒漠化、化学污染、极地臭氧层空洞…世界环境问题已 经严重的威胁到人类的生存.1972 年 6 月 5 日《联合国人类环境会议》将每年的 6 月 5 日定为“世界环 境日 ”.“世界环境日”的作用在于唤起全世界人民都来注意保护人类赖以生存的环境,自觉采取行 动参与环境保护,同时要求各国政府和联合国系统为推进保护进程做出贡献.2010 年世界环境日的世界 主题为“多个物种, 一个星球, 一个未来”,点出了保护地球上生命多样性的紧迫性.中国主题为“低 碳减排 绿色生活”,意指二氧化碳直接威胁到人类的生存与生活,倡导人们过上”绿色、低碳生活. (1) 在世界环境问题中,全球性大气污染问题不容忽视. 其中引起温室效应的气体主要是 ; 造成酸雨的主要气体是
A.二氧化碳 B.二氧化硫 C.一氧化碳
(2) 有“空中死神”之称的是
A.臭氧层空洞 B.酸雨 C.温室效应
(3) “多个物种, 一个星球,一个未来”,其中“多个物种”具体是指 第 3 页(共 13 页)
A.生物种类的多样性
B.基因的多样性
C.生态系统的多样性.
8.将 9.5 克 KClO3 和 MnO2 的混合物装入大试管中,加热至质量不再发生变化, 冷却试管后称量,剩有 6.62 克固体物质。计算:
(1)写出上述涉及到的化学方程式________。
(2)6.62 克固体中含有哪些物质?各多少克?
9.学校八年级科学兴趣小组为了测定某矿山石灰石中碳酸钙的质量分数, 取石灰石样品与足量稀盐酸 在烧杯中反应(假设石灰石样品中杂质不与稀盐酸反应也不溶于水,杂质中不含钙元素)。有关实验数
据如下表:
反 应 前 反 应 后
实验数据 烧杯和稀盐酸的质量 石灰石样品的质量 烧杯和剩余物的总质量
150g 12.5g 158.1g
(1) 根据质量守恒定律可知,反应中生成二氧化碳的质量为 g。
(2) 该石灰石中碳酸钙的质量分数
为
。
(3) 反应中生成氯化钙的质量是多少克? (写出计算过程) 10.树叶叶片不仅可以吸收一些有害气体,还可以利用光能把二氧化碳转化为淀粉和氧气, 起到改善环 境的作用.通常晴天时, 每天每平方米叶片可吸收 5g 二氧化碳来进行光合作用,则:
(1) 某公园中叶片面积约为 100 万平方米,在一个月 (按 20 个晴天计)内可以吸收二氧化碳气
体 ;
(2) 空气中二氧化碳含量增加会引起“温室效应”,导致地球气候变暖,①空气中二氧化碳的主要来 源是 ,②为了防止温室效应的产生可以采取 的措施
是
.
第 4 页(共 13 页)
11.环境污染对植物的生长有不同程度的影响,在一定程度上,植物在被污染的环境中生活时,也有继 续保持正常生理活动的特性,这种特性称为抗性。研究植物的抗性对筛选具有净化环境作用的植物种 类和保护环境有积极的意义。一项研究表明, 植物对 SO2 的抗性与叶片上气孔的大小和多少有关。所得
数据如下表:
被测植物 平均受害面积/% 气孔
气孔密度/(个/厘米 2) 每个气孔面积/微米 2
甲植物 13.5 370 2.72
乙植物 33.5 250 4.16
丙植物 57.5 180 5.56
(1)该研究表明,植物对 SO2 的抗性与气孔密度的关系是 , 与每个气孔面积的关系是 。
(2)在 SO2 污染严重的地区, 最好选择表中 植物为主要绿化树种。大气中 SO2 的主要危害是 产生 现象,即 pH 小于 的酸性降水。除 SO2 外,常见的大气污染物还有 (写出一种)。
(3)对 SO2 污染物的处理,可用 NaOH 溶液吸收(化学方程式为 2NaOH+SO2===Na2SO3+H2O)。2005 年, 我国排放 SO2 总量约达 2549 万吨。若全部用 NaOH 处理,则需 NaOH 固体多少吨?
第 5 页(共 13 页)
12. “毒大米”事件让人们认识到了重金属污染的危害,重金属在土壤中的分散范围广、隐蔽性强、 难清理,现在科学家利用一类超强金属吸收能力的植物(又叫超富集植物)对土壤进行“排毒”。
(1)双子叶的超富集植物, 由根系从土壤中吸取重金属,可通过木质茎中的________ (填“韧皮 部”“木质部”或“形成层”),转移、贮存到枝叶等地上部分。
(2)一种叫做重雪球的植物,富集金属镍的能力很强。通过改良植株增强重雪球的吸镍性,每克干燥的 枝叶可含有 0.2 克镍。对 500 千克的重雪球的干燥枝叶进行提纯处理, 理论上可获得________千克的 镍。
(3)超富集植物能帮助人们更好地改善由于采矿等原因而恶化的土壤,使耕地重新焕发生机。植物“排
毒”具有的优势是________ (写出一点即可)。
13.下图是一副叶和根对话的漫画图,仔细分析漫画, 回答下列问题;
(1) 叶进行光合作用为茎和根提供 ,同时释放氧气。
(2) 如果茎中的 “罢工”,则根吸收的 和 无法运输到叶。
第 6 页(共 13 页)
0.浙教版科学八年级下册期末专题复习:解答题三答案解析
一 、解答题
1. 【答案】(1) A
(2) 变大
(3) 变大
(4) 当电流为 60mA 时, 总电阻R总 = I (U)总 (总) = = 150;
此时热敏电阻 R1=R 总-R2=150Ω-90Ω=60Ω。
根据乙图可知,此时恒温箱内的温度是 100℃。
【解析】(1)根据恒温箱的工作状态确定衔铁的位置,进而判断接线情况;
(2) 首先根据乙图确定温度升高后热敏电阻 R1 的阻值变化,再根据 R 总=R1+R2 判断总电阻的变化, 最 后根据“电流与电阻的反比关系”确定电流变化。
(3) 电磁铁吸合时的电流大小不变, 则总电阻不变,根据 R 总=R1+R2 分析变阻器的阻值变化即可;
(4) 首先根据公式R总 = I (U)总 (总)计算出总电阻,再根据 R1=R 总-R2 计算出热敏电阻的阻值,最后根据图乙确 定恒温箱内的温度。
【解答】(1)当温度升高时,热敏电阻的阻值减小,那么总电阻变小而总电流变大,那么电磁铁的磁 场增强,将衔铁吸下来切断发热电阻 R0 的工作, 则 C 应该与 A 相接。
(2) 在升温的过程中, 热敏电阻 R1 的阻值减小, 根据 R 总=R1+R2 可知, 总电阻减小, 而总电流增大。
(3) 电磁铁吸合时的电流大小不变, 则总电阻不变。当温度升高时,热敏电阻 R1 的阻值减小, 据 R 总
=R1+R2 可知, 此时变阻器接入的阻值应该变大。
(4) 当电流为 60mA 时, 总电阻R总 = I (U)总 (总) = = 150; 此时热敏电阻 R1=R 总-R2=150Ω-90Ω=60Ω。
根据乙图可知, 此时恒温箱内的温度是 100℃。
2. (1) B;不能
(2) 30;是超载
【解析】(1)根据衔铁的运动方向判断它与哪个触点接触,进而判断电动机所在的电路是否被接通即
可。
第 7 页(共 13 页)
(2) 首先根据 F=G=mg 计算出乘客对电梯的压力, 然后根据乙图确定此时压敏电阻 R2 的阻值, 接下来 根据串联电路 R 总=R1+R2 计算出总电阻,最后根据I总 = R (U)总 (总)计算出总电流,并与 20mA 进行比较即可。
(1) 根据甲图可知,电梯超载时,衔铁被电磁铁吸住, 衔铁向下运动,触点 K 与触点 B 接触,电铃所 在的电路被接通,电铃发出警报声, 电动机所在的电路断开, 因此电动机不能工作。
(2) 乘客对电梯的压力 F=G=mg=1000kg×10N/kg=10 N;4
根据乙图可知, 此时压敏电阻 R2=100Ω;
电路的总电阻 R 总=R1+R2=100Ω+100Ω=200Ω;
通过电磁铁的电流I总 = R (U)总 (总) = = 0.03A = 30mA > 20mA。
则此时电梯是超载的。
3. 【答案】(1)
(2)
【解析】(1) ①如果用电器相互影响,那么它们串联;否则, 它们并联;
②干路开关控制所有用电器,支路开关只能控制它所在支路上的开关。
(2) 根据安培定则确定线圈上的电流方向,进而确定电源的正负极;在磁体外部, 磁感线总是从磁体 的 N 极回到S 极。
【解答】(1)如果指示灯损坏, 插孔依然可以正常通电, 那么说明二者不相互影响,因此它们并联。 开关能够同时控制指示灯和插孔,说明它在干路上。从火线上引线,首先通过开关,然后灯泡与插座
并联, 再接在零线上即可,如下图所示:
(2) 根据图片可知, 螺线管的右端为 N 极,因此磁感线的方向都是向左的。右手握住螺线管,大拇指 第 8 页(共 13 页)
指向右端, 此时弯曲的四指指尖向下,那么线圈上电流方向向下, 即电流从左端流入, 那么电源的左
端为正极, 右端为负极, 如下图所示:
4. (1) 3
(2) 2∶3
(3) N%=14×2/(14×2+4+16×3)=35%<40% 所以 不真实
(1) 根据化学式确定该物质的元素组成分析;
(2) 根据元素质量比为相对原子质量×原子个数之比分析;
(3) 根据化学式确定氮元素的质量分数, 然后对比标签中所给数值确定是否真实。
【解答】(1)硝酸铵是由氮、氢、氧三种元素组成的;
(2) 硝酸铵中氮与氧的原子个数比为 2:3;
(3)硝酸铵中氮元素质量分数为 14×2/(14×2+4+16×3)=35% ,与所给 40%不相符,所以广告不真实;
故答案为: (1) 3;(2) 2:3;(3) 不真实。
5. (1) 144
(2) 13.19%
(3) 0.10%;0.79%;具有
(1) 根据相对分子质量为分子中各原子的相对原子质量之和分析;
(2) 根据元素质量分数=相对原子质量×原子个数/相对分子质量分析;
(3) 根据标签中所给信息利用牙膏中氟元素质量即为 单氟磷酸钠 中氟元素质量分析;
【解答】(1) 单氟磷酸钠的相对分子质量为 23×2+31+16×3+19=144;
(2) 单氟磷酸钠中氟元素的质量分数为 × 100%=13.19%;
(3) 该牙膏中氟元素的质量分数为 × 100% = 0.10%; 该牙膏中单氟磷酸钠的质量分数为 =0.79%,牙膏中氟的含量在 0.75%~0.80% 范围内, 有 较好的防龋齿效果。
第 9 页(共 13 页)
故答案为: (1) 144;(2) 13.19%;(3) 0.10%;0.79%;具有。 6. (1) 60:11:32:14:32 (2) 9.4% (3) 根据题意,合格奶粉每 100g 中含蛋白质 18g,蛋白质中氮元素的平均质量分数为 16%,则每 1000g
合格奶粉中氮元素的质量至少为:18g×16%=2.88g>1.5g. 故该奶粉不合格.故答案为: 2.88g;不合格. (1) 根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.(2)根据 元素的质量分数的计算方法来分析.(3) 根据物质的质量和元素的质量分数可以计算出元素的质量.本 题难度不大,考查同学们结合新信息、灵活运用化学式的有关计算进行分析问题、解决问题的能力. 【解答】解:(1) 根据化合物中各元素质量比=各元素的相对原子质量×原子个数之比,可得蛋氨酸(化 学式为 C5H11O2NS) 中碳、氢、氧、氮、硫五种元素的质量比为(12×5):(1×11):(16×2):(14×1): (32×1) =60:11:32:14:32.故答案为:60:11:32:14:32;(2) 蛋氨酸(化学式为 C5H11O2NS) 中氮元素的质量分数= ≈ 9.4% .故答案为: 9.4%; 7. 【答案】(1) A;B (2) B (3) A 【解析】此题主要考查的是温室效应、酸雨的危害以及低碳生活的相关内容,分析资料解答. 【解答】解:(1)、二氧化碳气体具有吸热和隔热的功能. 它在大气中增多的结果是形成一种无形的玻 璃罩, 使太阳辐射到地球上的热量无法向外层空间发散, 其结果是地球表面变热起来. 因此,二氧化 碳也被称为温室气体.温室效应加剧主要是由于现代化工业社会燃烧过多煤炭、石油和天然气, 这些 燃料燃烧后放出大量的二氧化碳气体进入大气造成的. 酸雨是由于人类大量使用含硫量高的煤、石油、天然气等化石燃料,燃烧后产生的含有二氧化硫等的 气体, 在大气中经过复杂的化学反应后, 形成硫酸或硝酸气溶胶, 或为云、雨、雪、雾捕捉吸收,降 到地面成为的.(2)、酸雨危害水生生物, 它使许多河、湖水质酸化,导致许多对酸敏感的水生生物种 群灭绝,湖泊失去生态机能,最后变成死湖. 酸雨还杀死水中的浮游生物, 破坏水生生态系统此外, 酸化的水源威胁人们的健康, 酸雨对生物有极大的危害, 因此被称为“空中死神”.(3)、生物的多样 性包括生物种类的多样性、基因的多样性、生态系统的多样性等三个方面的内容, “多个物种, 一个
第 10 页(共 13 页)
星球, 一个未来”,其中“多个物种”具体指的是生物种类的多样性.
故答案为: (1) A.B (2) B (3) A
8. (1)2KClO3 2KCl+3O2 ↑ (2)mO2=9.5g-6.62g=2.88g 设生成氯化钾质量为 X,则
2KClO3 MnO2 2KCl+ 3O2 ↑
第 11 页(共 13 页)
149
X
96
2.88
克
149∶96=X∶2.88 克 X=4.47 克
二氧化锰的质量=6.62 克-4.47 克=2.15 克
9. (1) 4.4
(2) 设该石灰石样品中碳酸钙的质量为 x. CaCO3+2HCl═CaCl2+H2O+CO2 ↑ 100 44 x 4.4g = 解 得: x=10.0g 此石灰石中碳酸钙的质量分数为: × 100% = 80%。
(3) 设生成的氯化钙的质量为 y
CaCO3+2HCl═CaCl2+H2O+CO2 ↑
111
y
=
解得:y=11.1g
44
4.4g
则生成的氯化钙的质量为 11.1g。
【解析】(1)根据质量守恒定律可知:反应后比反应前减少的质量是生成二氧化碳的质量;
(2) 根据化学方程式由二氧化碳的质量可以计算出石灰石中碳酸钙的质量, 进而计算出石灰石中碳酸 钙的质量分数;
(3) 根据化学方程式由二氧化碳的质量可以计算出氯化钙的质量。(1) 根据质量守恒定律, 二氧化碳 的质量为: 150g+12.5g-158.1g=4.4g;
10. 【答案】(1) 1.0×108g;
(2) 化石燃料的燃烧,动物的呼吸,动植物尸体的腐烂等;大量植树造林、禁止乱砍乱伐,更多的利
用核能、太阳能、风能、地热能、氢能等新能源等.
【解析】【解答】 (1)叶片面积约 100 万平方米,在一个月 (按 20 个晴天计)内可吸收 CO2 气体 1×106×5g×20=1.0×108g.
(2)①空气中二氧化碳的主要来源是化石燃料的燃烧,动物的呼吸, 动植物尸体的腐烂等; ②为了防止温室效应的产生可以采取的措施有大量植树造林、禁止乱砍乱伐,更多的利用核能、太阳 能、风能、地热能、氢能等新能源等.
(1)先根据植物每天每平方米需吸收 5g 二氧化碳,则 100 万平方米的叶片在一个月 (按 20 个晴天计)可 吸收二氧化碳.
(2)根据二氧化碳的来源和防止温室效应的措施回答.
11. (1) 气孔密度越大,植物对 SO2 的抗性越强;每个气孔面积越大,植物对 SO2 的抗性越弱
(2) 甲; 酸雨;5.6;一氧化碳(合理均可)
(3) 解: 设需要 NaOH x 万吨。
2NaOH┼SO2=Na2SO3┼H2O
第 12 页(共 13 页)
80
x
64
2549
80:64=x:2549
x=80*2549/64=3186.25 万吨
答:若全部用 NaOH 处理,则需 NaOH 固体 3186.25 万吨。
【解析】本题为分析和计算综合题,通过分析题中信息, 可以得出答案。(1) 若植物对 SO2 的抗性越强, 则植物的平均受害面积越小。(2)甲植物的平均受害面积最小。(3)大气中 SO2 的主要危害是产生硫酸, 可表示为 2SO2+2H2O+O2===2H2SO4 。常见的大气污染物还有 CO、NO2、可吸入颗粒物等。
(1) 依题意, 由表可知: 植物对二氧化硫的抗性随着叶片上气孔密度的增大而减小,随着叶片上每个 气孔的面积的增大而增大。(2)在 SO2 污染严重的地区, 最好选择表中甲植物为主要绿化树种。大气中 SO2 的主要危害是产生酸雨现象,即 pH 小于 5.6 的酸性降水。除 SO2 外,常见的大气污染物还有一氧化 碳。(3)设需要 NaOH x 万吨。根据物质守恒定律进行计算即可。
故答案为: (1) 气孔密度越大, 植物对 SO2 的抗性越强;每个气孔面积越大, 植物对 SO2 的抗性越弱;
(2) 酸雨;5.6;一氧化碳(合理均可);
(3) 解: 设需要 NaOH x 万吨。
2NaOH┼SO2=Na2SO3┼H2O
80 64
x 2549
80:64=x:2549
x=80*2549/64=3186.25 万吨
答:若全部用 NaOH 处理,则需 NaOH 固体 3186.25 万吨。
12. (1)木质部(2)100(3)简便(或高效、环保、资源回收、增加收入等, 合理均可) 13. (1) 有机物
(2) 导管;水;无机盐
【解析】(1)植物光合作用的过程是十分复杂的, 它包括许多化学反应。但主要包含了以下两方面的 变化: 一方面, 把简单的无机物制成了复杂的有机物,并放出氧气,发生了物质转化; 另一方面,把 光能变成储存在有机物里的化学能, 实现了能量的转化。
(2) 输导水分和无机盐的导管是多种多样的,它们位于木质部中,水分和无机盐在茎木质部的导管中 能自下而上地向枝端运输;而输导有机物的是筛管 ,位于韧皮部中,韧皮部在树皮靠近木质部的地方, 有机物在茎的树皮中由上而下地运输着。
(1) 绿色植物通过光合作用制造的有机物不仅满足了自身生长、发育、繁殖的需要, 还为其他生物 提供了基本的食物来源; 同时生成的氧气也供给其它生物呼吸所用。叶进行光合作用为茎和根提供有 机物, 同时释放氧气。
(2) 根吸收的水和无机盐是通过茎中的导管之下而上运送到叶的; 叶光合作用制造的有机物是通过茎 中的筛管自上而下运送到植物各部位的。所以如果茎中的导管“罢工”,则根是、吸收的水和无机盐 就无法运输到叶。
故答案为: (1) 有机物; (2)导管; 水; 无机盐
第 13 页(共 13 页)
同课章节目录
- 第1章 电与磁
- 第1节 指南针为什么能指方向
- 第2节 电生磁
- 第3节 电磁铁的应用
- 第4节 电动机
- 第5节 磁生电
- 第6节 家庭用电
- 第7节 电的安全使用
- 第2章 微粒的模型与符号
- 第1节 模型、符号的建立与作用
- 第2节 物质的微观粒子模型
- 第3节 原子结构的模型
- 第4节 组成物质的元素
- 第5节 表示元素的符号
- 第6节 表示物质的符号
- 第7节 元素符号表示的量
- 第3章 空气与生命
- 第1节 空气与氧气
- 第2节 氧化和燃烧
- 第3节 化学方程式
- 第4节 二氧化碳
- 第5节 生物的呼吸和呼吸作用
- 第6节 光合作用
- 第7节 自然界中的氧循环和碳循环
- 第8节 空气污染与保护
- 第4章 植物与土壤
- 第1节 土壤的成分
- 第2节 各种各样的土壤
- 第3节 植物的根与物质吸收
- 第4节 植物的茎与物质运输
- 第5节 植物的叶与蒸腾作用
- 第6节 保护土壤
- 研究性学习课题
- 一 设计简单的电磁控制电路
- 二 化学反应中质量守恒的研究
- 三 研究植物的呼吸
- 四 当地水土状况调查
