1.2 生物大分子以碳链为骨架(第二课时)(共62张PPT)高一生物学(浙科版2019必修1)
文档属性
| 名称 | 1.2 生物大分子以碳链为骨架(第二课时)(共62张PPT)高一生物学(浙科版2019必修1) |

|
|
| 格式 | pptx | ||
| 文件大小 | 15.4MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 浙科版(2019) | ||
| 科目 | 生物学 | ||
| 更新时间 | 2023-06-25 00:00:00 | ||
图片预览









文档简介
(共62张PPT)
1.2 生物大分子以碳链为骨架(第2课时)
第一章 细胞的分子组成
课程导入
你知道哪些富含蛋白质的食物?
资料:专家建议每天吃1—2个鸡蛋
蛋白质与糖类和脂质不同,通常不是生物体内的能源物质,也不能贮存,而每天都要消耗一定的蛋白质,因此,有专家建议每天吃1—2个鸡蛋,有益健康 。
一旦摄入的蛋白质不足,就会出现易患病、面黄肌瘦 、发育不好等症状,若自身的蛋白质消耗超过20%,人的生命就会终止。
你知道这是什么原因吗?
一、蛋白质是生命活动的主要承载者
蚕和蜘蛛吐出的细而坚韧的丝、雄孔雀求偶季节展示的华丽的羽毛、羚羊浓密的毛和坚硬的角,这些看似完全不同的物质,却是由结构大同小异的同一类蛋白质,即角蛋白构成的。曾有人形象地称“一个蛋白一张脸”,反映了蛋白质分子空间结构的多样性。弗里德里希·恩格斯(Friedrich Engels,1820—1895)则从另一个角度指出“蛋白质是生命活动的体现者”,反映了蛋白质功能的多样性。
(一)蛋白质的功能
蛋白质与糖类及脂质不同。蛋白质不是能量供给的主要来源,却在其他方面发挥着不可替代的作用。
肌肉中的收缩蛋白
头发中的角蛋白
红细胞中的运输蛋白
种子中的储备蛋白
头发
蛛丝
肌肉纤维
1. 结构蛋白
许多蛋白质是构成细胞和生物体结构的重要物质,称为结构蛋白。
羽毛
2. 催化功能
胃蛋白酶结晶
细胞中的化学反应离不开酶的催化,绝大多数酶都是蛋白质。
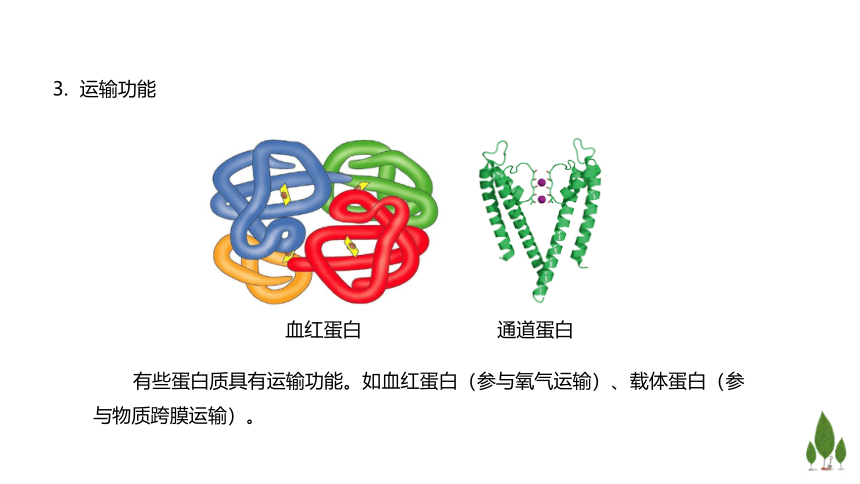
3. 运输功能
有些蛋白质具有运输功能。如血红蛋白(参与氧气运输)、载体蛋白(参与物质跨膜运输)。
血红蛋白
通道蛋白
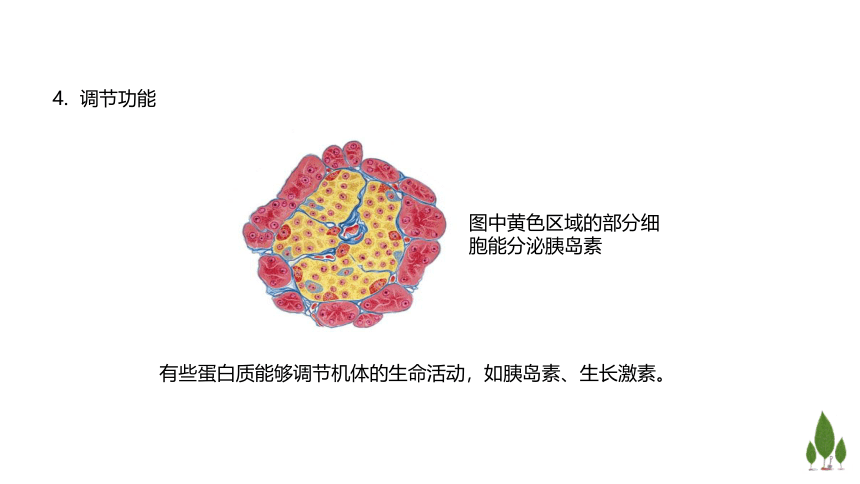
4. 调节功能
有些蛋白质能够调节机体的生命活动,如胰岛素、生长激素。
图中黄色区域的部分细胞能分泌胰岛素
5. 免疫功能
有些蛋白质有免疫功能。人体内的抗体是蛋白质,可以帮助人体抵御病菌和病毒等抗原的侵害。
抗体
抗原
①结构功能
②催化功能
③运输功能
④调节功能
⑤免疫功能
蛋白质每种特定的功能都取决于其特定的结构
(二)蛋白质的结构
食物中的蛋白质是怎样被人体吸收的?
蛋白质在人体内经过消化,分解为各种氨基酸,才可以被吸收、利用。
许多蛋白质已经获得结晶的纯品。在此基础上分析蛋白质的元素组成发现,蛋白质分子主要由C、H、O、N四种元素组成,有此蛋白质还含有S元素。
必需氨基酸:人体需要的,但不能在人体内合成,必须由食物供给的那些氨基酸,包括甲硫氨酸、缬氨酸、亮氨酸、异亮氨酸、赖氨酸、苏氨酸、色氨酸和苯丙氨酸。动物性食品一般含必需氨基酸较多,豆类食品也含有较多的必需氨基酸。(甲携来一本亮色书)
非必需氨基酸:可以在体内由其他化合物转化而来的,如甘氨酸、丙氨酸、丝氨酸、天冬氨酸、天冬酰胺、谷氨酸、谷氨酰胺、脯氨酸、酪氨酸和半胱氨酸等。
(1)分类
1. 基本单位——氨基酸
一个蛋白质分子可由数百至数千个氮基酸分子组成。绝大多数蛋白质是由约20种不同的氨基酸组成的。
C
H
C
H
H2N
OH
O
C
H
C
H2N
OH
O
CH3
CH3
CH
C
H
C
H2N
OH
O
CH3
C
H
C
H2N
OH
O
CH2
CH3
CH3
CH
甘氨酸
缬氨酸
丙氨酸
亮氨酸
几种氨基酸的结构式
2. 结构
C
H
H2N
R
氨基
羧基
侧链基团
C
OH
O
决定氨基酸的种类
一个中央碳原子上通过共价键连接着四个基团,即一个氨基(-NH2)、一个羧基(-COOH)、一个H和一个R基团。不同氨基酸的R基团不同,它可以较小,如丙氨酸中的R为-CH3、缬氨酸中的R为-CH(CH3)2。R基团也可以是较长的链,或是环状结构。R基团中也可能含有氨基(-NH2)或羧基(一COOH),有时还含有硫原子。
生物体内绝大多数氨基酸的生物通式如下图所示
哪些是组成蛋白质的氨基酸?C
H
R1
NH2
OH
C
O
H2O
C
H
COOH
R2
H
N
H
脱水缩合
3. 氨基酸形成蛋白质的方式
肽键
H H O
H N C C
R1
H H O
N C C OH
R2
H2O
H H O
H N C C OH
R1
H H O
H N C C OH
R2
二肽
两个氨基酸分子发生脱水缩合,形成二肽,其间的化学键称为肽键。许多个氨基酸以肽键连成一长串的肽链,称为多肽。
蛋白质是生命活动的主要承担者
人血红蛋白
胰岛素
蛋白质是生命活动的执行者和体现者。
C257H383O77N65S6
C3022H4816O872N780S8Fe4
氨基酸
肽链
脱水缩合
蛋白质
一条或多条
空间结构肽链
盘曲折叠
蛋白质的形成
4. 蛋白质的结构的多样性
脱水缩合 盘曲折叠
氨基酸 肽链(一条或多条) 蛋白质
人体组织蛋白酶
胰岛素空间结构
球状蛋白质
纤维状蛋白质
蛋白质分子可由一条或几条多肽链组成。每一种蛋白质都有其独特的空间结构,即三维立体结构。蛋白质分子的空间结构多种多样。例如,组成毛发和指甲的蛋白质是纤维状的,血液中的血红蛋白则是球形的。蛋白质正确的空间结构是蛋白质表现其特有的生物学活性所必需的。蛋白质的空间结构并不稳定,会随着温度的升高而发生改变。蛋白质的生物学活性会随着温度的升高而发生改变,在温度超过40~50℃时就可能丧失活性。
蛋白质的形成
许多蛋白质分子都含有两条或多条肽链,它们通过一定的化学键如二硫键相互结合在一起。
二硫键
两条肽链
—SH
—SH
+
—S—S—
+
2H
① 构成每种蛋白质的氨基酸的种类不同
② 每个蛋白质分子中氨基酸的数目不同
③ 氨基酸的排列顺序变化多端
(1)不同的多肽的差别在于其中氨基酸的种类、数目和排列顺序各不相同
假定20种氨基酸任意组成一个含100个氨基酸分子的蛋白质,将有多少种蛋白质?
20100
氨基酸
二肽
三肽
多肽
一条多肽链折叠形成蛋白质
几条多肽链折叠形成蛋白质
折叠盘曲成空间结构
(2)肽链的盘区、折叠方式及其空间结构千差万别
构成各种蛋白质的氨基酸的种类、氨基酸的数目、氨基酸的排列顺序以及多肽链盘曲、折叠的空间结构的不同是蛋白质多种多样的原因。
每一种蛋白质分子都有与它所承担功能相适应的独特结构,如果氨基酸序列改变或蛋白质的空间结构改变,就可能会影响其功能。
蛋白质功能多种多样的原因
蛋白质的结构决定功能
血红蛋白β链第6位氨基酸谷氨酸被缬氨酸代替,形成了异常的血红蛋白S,取代了正常血红蛋白,氧分压下降时血红蛋白S分子之间相互作用,聚合成为螺旋形多聚体,使红细胞扭曲成镰状细胞(即镰变现象),导致运输氧的能力大为削弱。
正常红细胞
镰状细胞
特定蛋白质的空间结构决定其具有的特定生理功能
下面是日常生活中的一些实例,你知道为什么吗
3. 含丰富蛋白质的食物最好煮熟后再食用。
2. 加酶的洗衣粉不宜用开水溶解。
1. 沾有血渍、牛奶的衣服不易用热水洗净。
血渍、牛奶的主要成分是蛋白质,一般温度下,蛋白质能以胶体的形态溶解于水中,一旦受热,它就会凝固起来,不易溶解于水。
绝大多数酶为蛋白质成分,蛋白质在高温时会变性,失去蛋白酶的功能。
加热以后,具备一定空间结构的螺旋形蛋白质分子链会松开,这是蛋白质的变性,蛋白质在变性后更加容易消化和吸收。
蛋白质的变性是指蛋白质在某些物理和化学因素作用下,其特定的空间构象被破坏,从而导致其理化性质的改变和生物活性丧失的现象。
致变因素:化学方法有加强酸、强碱、重金属盐、尿素、丙酮等;物理方法有加热(高温)、紫外线及X射线照射、超声波、剧烈振荡或搅拌等。
变性
5. 盐析与变性
(1)蛋白质变性
互动探究
?
鸡蛋是生吃还是熟吃更易消化吸收?
空间结构松散、伸展
肽键变了没?
①鸡蛋、肉类等经高温后蛋白质变性,更易消化。
②细菌、病毒经过加热、酸、重金属处理后因蛋白质变性而灭活。
③动物、昆虫标本固定保存、防腐。
④很多毒素是蛋白质,经甲醛固定,减毒、封闭毒性碱基团作类毒素抗原,制作抗毒素。
(2)蛋白质变性的应用
使蛋白质变性的因素:高温、酒精、紫外线、强酸、强碱、重金属盐。这也是消毒灭菌的原理。
生物世界
加5%卵清蛋白溶液5ml于试管中,再加等量的饱和硫酸铵溶液,混匀后静置数分钟析出球蛋白沉淀。倒出少量浑浊沉淀,加少量水,沉淀是否溶解,为什么
溶解,蛋白溶液加入浓无机盐溶液,导致蛋白质溶解度降低而析出,这是盐析过程,蛋白质只是沉淀,并未变性,加水后即恢复溶解。
【思考】
盐析是指在蛋白质水溶液中加入中性盐,随着盐浓度增大而使蛋白质沉淀出来的现象。得到的蛋白质一般不失活,一定条件下又可重新溶解。
盐析:
变化实质:物理变化(溶解度降低)
变化过程:可逆
用途:分离、提纯等
变性:
变化实质:化学变化(空间结构改变)
变化过程:不可逆
用途:杀菌、消毒等
(3)盐析与变性的区别
6. 蛋白质形成过程中的数量计算
肽键数=6-1
肽键数=8-1
肽链数为1时:肽键数 = 脱去水分子个数 = n-1
肽键数=14-2
肽链数为2时:肽键数 = 脱去水分子个数= n-2
肽键数 = 脱去水分子个数 = 氨基酸数-肽链条数= n-m
(n表示氨基酸数、m表示肽链数)
(1)肽键数和水分子数计算
—C
NH2
H
R1
—C—
O
N—
H
C
H
R2
—C—
O
N—
H
C—
COOH
H
R3
一条肽链至少含有____个羧基和_____个氨基。
一
一
m条肽链至少含有____个羧基和_____个氨基。
m
m
蛋白质中至少含有的游离的氨基或羧基数=肽链的条数。
(2)氨基数和羧基数的计算
蛋白质相对分子质量=氨基酸平均相对分子质量×氨基酸数量-失去水分子数×18
—C
NH2
H
R1
—C—
O
N—
H
C
H
R2
—C—
O
N—
H
C—
COOH
H
R3
(3)蛋白质相对分子量的计算
7. 检测生物组织中蛋白质的实验
(1)实验原理:蛋白质+双缩脲试剂→紫色反应
具有两个或两个以上肽键的化合物在碱性条件下与Cu2+反应生成紫色络合物
·本实验是显色反应,因此选用材料有两个要求:
·蛋白质的检测实验,我们使用的实验材料是稀蛋清,为什么用稀释了的鸡蛋清呢?
含有蛋白质、浅色系
浓度太大,反应不完全
A液 0.1 g/ml NaOH溶液
B液 0.01g/ml CuSO4溶液
使用方法:先滴加A液(制造碱性环境),再滴加B液,最后摇匀。
(2)实验试剂:双缩脲试剂
目的要求
1. 尝试用化学试剂检测生物组织中的糖类、蛋白质。
2. 分析实验现象,得出结论。
材料用具
供教师用的蛋白质溶液、淀粉溶液、葡萄糖溶液,供学生用的梨和白萝卜(或匀浆)、稀释的蛋清液、马铃薯块茎 (或匀浆),清水,双缩脲试剂A,双缩脲试剂B,本尼迪特试剂,碘-碘化钾溶液,试管若干支,10 mL的量筒,研钵,漏斗,滤纸,80~100汇的热水浴等。
方法步骤
1. 观察教师用指示剂分别检测蛋白质溶液、淀粉溶液和葡萄糖溶液的显色结果。
2.下表中的食物是否含有淀粉、蛋白质、还原糖?请将你对实验结果的预测填入表格中。
3. 将需要匀浆的生物组织材料剪碎,置于研钵中,加少量清水研磨,并将硏磨液过滤或静置使其中的固形物沉淀。各种材料单独进行操作。
4.检测。
( 1)检测淀粉:取2mL样本上清液,加入5滴碘一碘化钾溶液,与样本上清液比较,观察颜色变化并记录在下表的相应位置(“十”表示有,“一〞表示无)。
(2)检测蛋白质:取2mL样本上清液,加入2mL双缩脲试剂A,振荡试管,使样本与试剂A混合均匀,再加入5滴双缩服试剂B,与样本上清液比较,观察颜色变化并记录在下表的相应位置。
(3)检测还原糖:取2mL样本上清液,加入2mL本尼迪特试剂,振荡试管,使样本与本尼迪特试剂混合均匀,然后将试管置于热水浴中加热2~3 min,与样本上清液比较,观察颜色变化并记录在下表的相应位置。
选材:含蛋白质丰富的豆浆或鸡蛋清溶液。
黄豆浆滤液或蛋清稀释液
制备样液
呈色反应
组织样
液2 mL
双缩脲试剂A
双缩脲试剂B液5滴
摇匀后变成紫色
结论:组织样液中存在蛋白质。
(3)实验过程
巩固练习
1. 下列物质中,不是构成蛋白质的氨基酸( )
D
A.
B.
C.
D.
2.催产素、牛加压素、血管舒缓素等多肽化合物的氨基酸数量相同,但其生理功能却不同,原因有( )
①氨基酸种类不同 ②合成的场所不同
③氨基酸的排列顺序不同 ④肽链的折叠盘曲方式不同
A.①②③ B.①③④
C.②③④ D.①②③④
B
3. 胰岛素是含有51个氨基酸的蛋白质,相对分子质量为6000,胰岛素分子有A链(21个氨基酸)与B链(30个氨基酸)组成。问:胰岛素分子中总共含有多少个肽键?形成时脱去了多少个水分子?分子量减少了多少?
49
49
二硫键
二硫键
49×18+2×3 =888
脱氢缩合
4. 某五十肽中有丙氨酸(R基为-CH3)2个,现脱掉其中的丙氨酸(相应位置如右图)得到几种不同有机产物,其中脱下的氨基酸均以游离态正常存在。下列有关该过程产生的全部有机物中有关原子、基团或肽键数目的叙述,错误的是( )
A.肽键数目减少4个
B.氨基和羧基分别增加4个
C.氢原子数目增加8个
D.氧原子数目增加2个
D
丙氨酸
丙氨酸
新型冠状病毒(2019-nCoV)属于β属的冠状病毒,具有囊膜的单股正链RNA病毒。
目前正在通过核酸检测确定感染病例。新型冠状病毒是RNA病毒,不同的病毒核酸序列不同。标记新型冠状病毒的某个核酸片段,与核酸检测样本进行对比。
核酸的种类及其分布核酸脱氧核糖核酸核 糖 核 酸种类简称DNA简称RNA分布DNARNA真核生物原核生物主要分布在细胞核中;少量分布在线粒体、叶绿体中。主要分布在拟核中(环状DNA分子)主要分布在细胞质中。病毒只含一种核酸,DNA或者RNA。二、核酸储存与传递遗传信息
(一)核酸的基本单位——核苷酸
1. 组成元素:C、H、O、N、P
2. 组成单位:核苷酸
一个核苷酸 = 一分子(磷酸 + 五碳糖 + 含氮碱基)
五碳糖
含氮碱基
P
(二)核酸的分类
脱氧核苷酸
脱氧核苷酸连接成的长链
DNA分子
1. DNA(脱氧核糖核酸)
碱基
核糖核苷酸
核糖核苷酸连接成的长链
2. RNA(核糖核酸)
RNA分子
碱基
碱基:A、T、G、C
碱基:A、U、G、C
脱氧核苷酸
核糖核苷酸
碱基
碱基
①脱氧核糖核苷酸(4种)——DNA组成单位
p
T
p
G
腺嘌呤脱氧核苷酸
鸟嘌呤脱氧核苷酸
p
C
胞嘧啶脱氧核苷酸
胸腺嘧啶脱氧核苷酸
根据碱基种类不同,将核苷酸分为:
p
A
②核糖核苷酸(4种)——RNA组成单位
P
A
p
G
p
C
p
U
腺嘌呤核糖核苷酸
鸟嘌呤核糖核苷酸
胞嘧啶核糖核苷酸
尿嘧啶核糖核苷酸
RNA
DNA
核糖核苷酸
构成RNA
脱氧核糖核苷酸
构成DNA
脱氧核糖
胸腺嘧啶(T)
磷酸
腺嘌呤(A)
鸟嘌呤(G)
胞嘧啶(C)
核糖
尿嘧啶(U)
3. DNA与RNA的区别
(三)核酸的分布
DNA:真核细胞的DNA主要分布在细胞核中。线粒体、叶绿体中也有少量DNA。此外,原核细胞的拟核、质粒,DNA病毒中也有。
RNA:主要分布在细胞质中。RNA病毒中也有。
(四)核酸的功能
核酸是细胞中控制其生命活动的生物大分子。组成生物体的亿万个细胞中都有DNA和RNA。DNA中储藏的信息控制着细胞的所有活动,并且决定着细胞和整个生物体的遗传特性。RNA是合成蛋白质所必需的。
种类 真核生物及原核生物 病毒
五碳糖 2种(核糖和脱氧核糖) 1种(核糖或脱氧核糖)
碱基 5种(A、T、C、G、U) 4种(A、G、C、T
或A、G、C、U)
核苷酸 8种(4种脱氧核苷酸 和4种核糖核苷酸) 4种(4种脱氧核苷酸
或4种核糖核苷酸)
彻底水解产物 8种(1种磷酸+2种五碳糖+ 5种碱基) 6种(1种磷酸+1种五碳糖+
4种碱基)
小分子物质元素基本单位核苷酸链核酸相互连接脱水缩合磷酸五碳糖含氮碱基++C、H、O、N、P核苷酸RNADNA核苷酸之间也通过脱水缩合形成核苷酸链,核苷酸发生脱水缩合之后,通过磷酸二酯键结合。前一个核苷酸的羰基中的3碳上'—OH(羟基)和后一个核苷酸的5'—磷酸基形成酯键,此处的磷酸基同时与前后两个羟基形成酯键,故称磷酸二酯键。依次连下去,形成多核苷酸链,即核酸大分子链。核苷酸链之间通过氢键连接。两条链上的含氮碱基通过碱基互补以氢键相连。碱基互补配对原则中:A-T A-U G-C巩固练习
1. 噬菌体、烟草、HIV病毒的核酸中具有碱基和核苷酸的种类分别是( )
A.4种、8种、4种和4种、8种、4种
B.4种、5种、4种和4种、5种、4种
C.4种、5种、4种和4种、8种、4种
D.4种、8种、4种和4种、5种、4种
C
2. 有关DNA、RNA的说法,正确的是( )
A.均由C、H、O、N、P五种元素组成
B.DNA是大分子物质,RNA是小分子物质
C.DNA是主要的遗传物质,RNA不作为遗传物质
D.基本组成单位都是核糖核苷酸,但所含的碱基有所不同
A
3. 如下图所示,由1分子磷酸、1分子含氮碱基m和1分子化合物a构成了化合物b,下列叙述正确的是( )
A.若m为腺嘌呤,则b肯定为腺嘌呤脱氧核苷酸
B.若a为核糖,则b为DNA的基本组成单位
C.若m为尿嘧啶,则DNA中肯定不含b这种化合物
D.若由b构成的核酸为单链,则b一定为脱氧核苷酸
C
THANKS
1.2 生物大分子以碳链为骨架(第2课时)
第一章 细胞的分子组成
课程导入
你知道哪些富含蛋白质的食物?
资料:专家建议每天吃1—2个鸡蛋
蛋白质与糖类和脂质不同,通常不是生物体内的能源物质,也不能贮存,而每天都要消耗一定的蛋白质,因此,有专家建议每天吃1—2个鸡蛋,有益健康 。
一旦摄入的蛋白质不足,就会出现易患病、面黄肌瘦 、发育不好等症状,若自身的蛋白质消耗超过20%,人的生命就会终止。
你知道这是什么原因吗?
一、蛋白质是生命活动的主要承载者
蚕和蜘蛛吐出的细而坚韧的丝、雄孔雀求偶季节展示的华丽的羽毛、羚羊浓密的毛和坚硬的角,这些看似完全不同的物质,却是由结构大同小异的同一类蛋白质,即角蛋白构成的。曾有人形象地称“一个蛋白一张脸”,反映了蛋白质分子空间结构的多样性。弗里德里希·恩格斯(Friedrich Engels,1820—1895)则从另一个角度指出“蛋白质是生命活动的体现者”,反映了蛋白质功能的多样性。
(一)蛋白质的功能
蛋白质与糖类及脂质不同。蛋白质不是能量供给的主要来源,却在其他方面发挥着不可替代的作用。
肌肉中的收缩蛋白
头发中的角蛋白
红细胞中的运输蛋白
种子中的储备蛋白
头发
蛛丝
肌肉纤维
1. 结构蛋白
许多蛋白质是构成细胞和生物体结构的重要物质,称为结构蛋白。
羽毛
2. 催化功能
胃蛋白酶结晶
细胞中的化学反应离不开酶的催化,绝大多数酶都是蛋白质。
3. 运输功能
有些蛋白质具有运输功能。如血红蛋白(参与氧气运输)、载体蛋白(参与物质跨膜运输)。
血红蛋白
通道蛋白
4. 调节功能
有些蛋白质能够调节机体的生命活动,如胰岛素、生长激素。
图中黄色区域的部分细胞能分泌胰岛素
5. 免疫功能
有些蛋白质有免疫功能。人体内的抗体是蛋白质,可以帮助人体抵御病菌和病毒等抗原的侵害。
抗体
抗原
①结构功能
②催化功能
③运输功能
④调节功能
⑤免疫功能
蛋白质每种特定的功能都取决于其特定的结构
(二)蛋白质的结构
食物中的蛋白质是怎样被人体吸收的?
蛋白质在人体内经过消化,分解为各种氨基酸,才可以被吸收、利用。
许多蛋白质已经获得结晶的纯品。在此基础上分析蛋白质的元素组成发现,蛋白质分子主要由C、H、O、N四种元素组成,有此蛋白质还含有S元素。
必需氨基酸:人体需要的,但不能在人体内合成,必须由食物供给的那些氨基酸,包括甲硫氨酸、缬氨酸、亮氨酸、异亮氨酸、赖氨酸、苏氨酸、色氨酸和苯丙氨酸。动物性食品一般含必需氨基酸较多,豆类食品也含有较多的必需氨基酸。(甲携来一本亮色书)
非必需氨基酸:可以在体内由其他化合物转化而来的,如甘氨酸、丙氨酸、丝氨酸、天冬氨酸、天冬酰胺、谷氨酸、谷氨酰胺、脯氨酸、酪氨酸和半胱氨酸等。
(1)分类
1. 基本单位——氨基酸
一个蛋白质分子可由数百至数千个氮基酸分子组成。绝大多数蛋白质是由约20种不同的氨基酸组成的。
C
H
C
H
H2N
OH
O
C
H
C
H2N
OH
O
CH3
CH3
CH
C
H
C
H2N
OH
O
CH3
C
H
C
H2N
OH
O
CH2
CH3
CH3
CH
甘氨酸
缬氨酸
丙氨酸
亮氨酸
几种氨基酸的结构式
2. 结构
C
H
H2N
R
氨基
羧基
侧链基团
C
OH
O
决定氨基酸的种类
一个中央碳原子上通过共价键连接着四个基团,即一个氨基(-NH2)、一个羧基(-COOH)、一个H和一个R基团。不同氨基酸的R基团不同,它可以较小,如丙氨酸中的R为-CH3、缬氨酸中的R为-CH(CH3)2。R基团也可以是较长的链,或是环状结构。R基团中也可能含有氨基(-NH2)或羧基(一COOH),有时还含有硫原子。
生物体内绝大多数氨基酸的生物通式如下图所示
哪些是组成蛋白质的氨基酸?C
H
R1
NH2
OH
C
O
H2O
C
H
COOH
R2
H
N
H
脱水缩合
3. 氨基酸形成蛋白质的方式
肽键
H H O
H N C C
R1
H H O
N C C OH
R2
H2O
H H O
H N C C OH
R1
H H O
H N C C OH
R2
二肽
两个氨基酸分子发生脱水缩合,形成二肽,其间的化学键称为肽键。许多个氨基酸以肽键连成一长串的肽链,称为多肽。
蛋白质是生命活动的主要承担者
人血红蛋白
胰岛素
蛋白质是生命活动的执行者和体现者。
C257H383O77N65S6
C3022H4816O872N780S8Fe4
氨基酸
肽链
脱水缩合
蛋白质
一条或多条
空间结构肽链
盘曲折叠
蛋白质的形成
4. 蛋白质的结构的多样性
脱水缩合 盘曲折叠
氨基酸 肽链(一条或多条) 蛋白质
人体组织蛋白酶
胰岛素空间结构
球状蛋白质
纤维状蛋白质
蛋白质分子可由一条或几条多肽链组成。每一种蛋白质都有其独特的空间结构,即三维立体结构。蛋白质分子的空间结构多种多样。例如,组成毛发和指甲的蛋白质是纤维状的,血液中的血红蛋白则是球形的。蛋白质正确的空间结构是蛋白质表现其特有的生物学活性所必需的。蛋白质的空间结构并不稳定,会随着温度的升高而发生改变。蛋白质的生物学活性会随着温度的升高而发生改变,在温度超过40~50℃时就可能丧失活性。
蛋白质的形成
许多蛋白质分子都含有两条或多条肽链,它们通过一定的化学键如二硫键相互结合在一起。
二硫键
两条肽链
—SH
—SH
+
—S—S—
+
2H
① 构成每种蛋白质的氨基酸的种类不同
② 每个蛋白质分子中氨基酸的数目不同
③ 氨基酸的排列顺序变化多端
(1)不同的多肽的差别在于其中氨基酸的种类、数目和排列顺序各不相同
假定20种氨基酸任意组成一个含100个氨基酸分子的蛋白质,将有多少种蛋白质?
20100
氨基酸
二肽
三肽
多肽
一条多肽链折叠形成蛋白质
几条多肽链折叠形成蛋白质
折叠盘曲成空间结构
(2)肽链的盘区、折叠方式及其空间结构千差万别
构成各种蛋白质的氨基酸的种类、氨基酸的数目、氨基酸的排列顺序以及多肽链盘曲、折叠的空间结构的不同是蛋白质多种多样的原因。
每一种蛋白质分子都有与它所承担功能相适应的独特结构,如果氨基酸序列改变或蛋白质的空间结构改变,就可能会影响其功能。
蛋白质功能多种多样的原因
蛋白质的结构决定功能
血红蛋白β链第6位氨基酸谷氨酸被缬氨酸代替,形成了异常的血红蛋白S,取代了正常血红蛋白,氧分压下降时血红蛋白S分子之间相互作用,聚合成为螺旋形多聚体,使红细胞扭曲成镰状细胞(即镰变现象),导致运输氧的能力大为削弱。
正常红细胞
镰状细胞
特定蛋白质的空间结构决定其具有的特定生理功能
下面是日常生活中的一些实例,你知道为什么吗
3. 含丰富蛋白质的食物最好煮熟后再食用。
2. 加酶的洗衣粉不宜用开水溶解。
1. 沾有血渍、牛奶的衣服不易用热水洗净。
血渍、牛奶的主要成分是蛋白质,一般温度下,蛋白质能以胶体的形态溶解于水中,一旦受热,它就会凝固起来,不易溶解于水。
绝大多数酶为蛋白质成分,蛋白质在高温时会变性,失去蛋白酶的功能。
加热以后,具备一定空间结构的螺旋形蛋白质分子链会松开,这是蛋白质的变性,蛋白质在变性后更加容易消化和吸收。
蛋白质的变性是指蛋白质在某些物理和化学因素作用下,其特定的空间构象被破坏,从而导致其理化性质的改变和生物活性丧失的现象。
致变因素:化学方法有加强酸、强碱、重金属盐、尿素、丙酮等;物理方法有加热(高温)、紫外线及X射线照射、超声波、剧烈振荡或搅拌等。
变性
5. 盐析与变性
(1)蛋白质变性
互动探究
?
鸡蛋是生吃还是熟吃更易消化吸收?
空间结构松散、伸展
肽键变了没?
①鸡蛋、肉类等经高温后蛋白质变性,更易消化。
②细菌、病毒经过加热、酸、重金属处理后因蛋白质变性而灭活。
③动物、昆虫标本固定保存、防腐。
④很多毒素是蛋白质,经甲醛固定,减毒、封闭毒性碱基团作类毒素抗原,制作抗毒素。
(2)蛋白质变性的应用
使蛋白质变性的因素:高温、酒精、紫外线、强酸、强碱、重金属盐。这也是消毒灭菌的原理。
生物世界
加5%卵清蛋白溶液5ml于试管中,再加等量的饱和硫酸铵溶液,混匀后静置数分钟析出球蛋白沉淀。倒出少量浑浊沉淀,加少量水,沉淀是否溶解,为什么
溶解,蛋白溶液加入浓无机盐溶液,导致蛋白质溶解度降低而析出,这是盐析过程,蛋白质只是沉淀,并未变性,加水后即恢复溶解。
【思考】
盐析是指在蛋白质水溶液中加入中性盐,随着盐浓度增大而使蛋白质沉淀出来的现象。得到的蛋白质一般不失活,一定条件下又可重新溶解。
盐析:
变化实质:物理变化(溶解度降低)
变化过程:可逆
用途:分离、提纯等
变性:
变化实质:化学变化(空间结构改变)
变化过程:不可逆
用途:杀菌、消毒等
(3)盐析与变性的区别
6. 蛋白质形成过程中的数量计算
肽键数=6-1
肽键数=8-1
肽链数为1时:肽键数 = 脱去水分子个数 = n-1
肽键数=14-2
肽链数为2时:肽键数 = 脱去水分子个数= n-2
肽键数 = 脱去水分子个数 = 氨基酸数-肽链条数= n-m
(n表示氨基酸数、m表示肽链数)
(1)肽键数和水分子数计算
—C
NH2
H
R1
—C—
O
N—
H
C
H
R2
—C—
O
N—
H
C—
COOH
H
R3
一条肽链至少含有____个羧基和_____个氨基。
一
一
m条肽链至少含有____个羧基和_____个氨基。
m
m
蛋白质中至少含有的游离的氨基或羧基数=肽链的条数。
(2)氨基数和羧基数的计算
蛋白质相对分子质量=氨基酸平均相对分子质量×氨基酸数量-失去水分子数×18
—C
NH2
H
R1
—C—
O
N—
H
C
H
R2
—C—
O
N—
H
C—
COOH
H
R3
(3)蛋白质相对分子量的计算
7. 检测生物组织中蛋白质的实验
(1)实验原理:蛋白质+双缩脲试剂→紫色反应
具有两个或两个以上肽键的化合物在碱性条件下与Cu2+反应生成紫色络合物
·本实验是显色反应,因此选用材料有两个要求:
·蛋白质的检测实验,我们使用的实验材料是稀蛋清,为什么用稀释了的鸡蛋清呢?
含有蛋白质、浅色系
浓度太大,反应不完全
A液 0.1 g/ml NaOH溶液
B液 0.01g/ml CuSO4溶液
使用方法:先滴加A液(制造碱性环境),再滴加B液,最后摇匀。
(2)实验试剂:双缩脲试剂
目的要求
1. 尝试用化学试剂检测生物组织中的糖类、蛋白质。
2. 分析实验现象,得出结论。
材料用具
供教师用的蛋白质溶液、淀粉溶液、葡萄糖溶液,供学生用的梨和白萝卜(或匀浆)、稀释的蛋清液、马铃薯块茎 (或匀浆),清水,双缩脲试剂A,双缩脲试剂B,本尼迪特试剂,碘-碘化钾溶液,试管若干支,10 mL的量筒,研钵,漏斗,滤纸,80~100汇的热水浴等。
方法步骤
1. 观察教师用指示剂分别检测蛋白质溶液、淀粉溶液和葡萄糖溶液的显色结果。
2.下表中的食物是否含有淀粉、蛋白质、还原糖?请将你对实验结果的预测填入表格中。
3. 将需要匀浆的生物组织材料剪碎,置于研钵中,加少量清水研磨,并将硏磨液过滤或静置使其中的固形物沉淀。各种材料单独进行操作。
4.检测。
( 1)检测淀粉:取2mL样本上清液,加入5滴碘一碘化钾溶液,与样本上清液比较,观察颜色变化并记录在下表的相应位置(“十”表示有,“一〞表示无)。
(2)检测蛋白质:取2mL样本上清液,加入2mL双缩脲试剂A,振荡试管,使样本与试剂A混合均匀,再加入5滴双缩服试剂B,与样本上清液比较,观察颜色变化并记录在下表的相应位置。
(3)检测还原糖:取2mL样本上清液,加入2mL本尼迪特试剂,振荡试管,使样本与本尼迪特试剂混合均匀,然后将试管置于热水浴中加热2~3 min,与样本上清液比较,观察颜色变化并记录在下表的相应位置。
选材:含蛋白质丰富的豆浆或鸡蛋清溶液。
黄豆浆滤液或蛋清稀释液
制备样液
呈色反应
组织样
液2 mL
双缩脲试剂A
双缩脲试剂B液5滴
摇匀后变成紫色
结论:组织样液中存在蛋白质。
(3)实验过程
巩固练习
1. 下列物质中,不是构成蛋白质的氨基酸( )
D
A.
B.
C.
D.
2.催产素、牛加压素、血管舒缓素等多肽化合物的氨基酸数量相同,但其生理功能却不同,原因有( )
①氨基酸种类不同 ②合成的场所不同
③氨基酸的排列顺序不同 ④肽链的折叠盘曲方式不同
A.①②③ B.①③④
C.②③④ D.①②③④
B
3. 胰岛素是含有51个氨基酸的蛋白质,相对分子质量为6000,胰岛素分子有A链(21个氨基酸)与B链(30个氨基酸)组成。问:胰岛素分子中总共含有多少个肽键?形成时脱去了多少个水分子?分子量减少了多少?
49
49
二硫键
二硫键
49×18+2×3 =888
脱氢缩合
4. 某五十肽中有丙氨酸(R基为-CH3)2个,现脱掉其中的丙氨酸(相应位置如右图)得到几种不同有机产物,其中脱下的氨基酸均以游离态正常存在。下列有关该过程产生的全部有机物中有关原子、基团或肽键数目的叙述,错误的是( )
A.肽键数目减少4个
B.氨基和羧基分别增加4个
C.氢原子数目增加8个
D.氧原子数目增加2个
D
丙氨酸
丙氨酸
新型冠状病毒(2019-nCoV)属于β属的冠状病毒,具有囊膜的单股正链RNA病毒。
目前正在通过核酸检测确定感染病例。新型冠状病毒是RNA病毒,不同的病毒核酸序列不同。标记新型冠状病毒的某个核酸片段,与核酸检测样本进行对比。
核酸的种类及其分布核酸脱氧核糖核酸核 糖 核 酸种类简称DNA简称RNA分布DNARNA真核生物原核生物主要分布在细胞核中;少量分布在线粒体、叶绿体中。主要分布在拟核中(环状DNA分子)主要分布在细胞质中。病毒只含一种核酸,DNA或者RNA。二、核酸储存与传递遗传信息
(一)核酸的基本单位——核苷酸
1. 组成元素:C、H、O、N、P
2. 组成单位:核苷酸
一个核苷酸 = 一分子(磷酸 + 五碳糖 + 含氮碱基)
五碳糖
含氮碱基
P
(二)核酸的分类
脱氧核苷酸
脱氧核苷酸连接成的长链
DNA分子
1. DNA(脱氧核糖核酸)
碱基
核糖核苷酸
核糖核苷酸连接成的长链
2. RNA(核糖核酸)
RNA分子
碱基
碱基:A、T、G、C
碱基:A、U、G、C
脱氧核苷酸
核糖核苷酸
碱基
碱基
①脱氧核糖核苷酸(4种)——DNA组成单位
p
T
p
G
腺嘌呤脱氧核苷酸
鸟嘌呤脱氧核苷酸
p
C
胞嘧啶脱氧核苷酸
胸腺嘧啶脱氧核苷酸
根据碱基种类不同,将核苷酸分为:
p
A
②核糖核苷酸(4种)——RNA组成单位
P
A
p
G
p
C
p
U
腺嘌呤核糖核苷酸
鸟嘌呤核糖核苷酸
胞嘧啶核糖核苷酸
尿嘧啶核糖核苷酸
RNA
DNA
核糖核苷酸
构成RNA
脱氧核糖核苷酸
构成DNA
脱氧核糖
胸腺嘧啶(T)
磷酸
腺嘌呤(A)
鸟嘌呤(G)
胞嘧啶(C)
核糖
尿嘧啶(U)
3. DNA与RNA的区别
(三)核酸的分布
DNA:真核细胞的DNA主要分布在细胞核中。线粒体、叶绿体中也有少量DNA。此外,原核细胞的拟核、质粒,DNA病毒中也有。
RNA:主要分布在细胞质中。RNA病毒中也有。
(四)核酸的功能
核酸是细胞中控制其生命活动的生物大分子。组成生物体的亿万个细胞中都有DNA和RNA。DNA中储藏的信息控制着细胞的所有活动,并且决定着细胞和整个生物体的遗传特性。RNA是合成蛋白质所必需的。
种类 真核生物及原核生物 病毒
五碳糖 2种(核糖和脱氧核糖) 1种(核糖或脱氧核糖)
碱基 5种(A、T、C、G、U) 4种(A、G、C、T
或A、G、C、U)
核苷酸 8种(4种脱氧核苷酸 和4种核糖核苷酸) 4种(4种脱氧核苷酸
或4种核糖核苷酸)
彻底水解产物 8种(1种磷酸+2种五碳糖+ 5种碱基) 6种(1种磷酸+1种五碳糖+
4种碱基)
小分子物质元素基本单位核苷酸链核酸相互连接脱水缩合磷酸五碳糖含氮碱基++C、H、O、N、P核苷酸RNADNA核苷酸之间也通过脱水缩合形成核苷酸链,核苷酸发生脱水缩合之后,通过磷酸二酯键结合。前一个核苷酸的羰基中的3碳上'—OH(羟基)和后一个核苷酸的5'—磷酸基形成酯键,此处的磷酸基同时与前后两个羟基形成酯键,故称磷酸二酯键。依次连下去,形成多核苷酸链,即核酸大分子链。核苷酸链之间通过氢键连接。两条链上的含氮碱基通过碱基互补以氢键相连。碱基互补配对原则中:A-T A-U G-C巩固练习
1. 噬菌体、烟草、HIV病毒的核酸中具有碱基和核苷酸的种类分别是( )
A.4种、8种、4种和4种、8种、4种
B.4种、5种、4种和4种、5种、4种
C.4种、5种、4种和4种、8种、4种
D.4种、8种、4种和4种、5种、4种
C
2. 有关DNA、RNA的说法,正确的是( )
A.均由C、H、O、N、P五种元素组成
B.DNA是大分子物质,RNA是小分子物质
C.DNA是主要的遗传物质,RNA不作为遗传物质
D.基本组成单位都是核糖核苷酸,但所含的碱基有所不同
A
3. 如下图所示,由1分子磷酸、1分子含氮碱基m和1分子化合物a构成了化合物b,下列叙述正确的是( )
A.若m为腺嘌呤,则b肯定为腺嘌呤脱氧核苷酸
B.若a为核糖,则b为DNA的基本组成单位
C.若m为尿嘧啶,则DNA中肯定不含b这种化合物
D.若由b构成的核酸为单链,则b一定为脱氧核苷酸
C
THANKS
同课章节目录
- 第一章 细胞的分子组成
- 第一节 水和无机盐是构成细胞的重要无机物
- 第二节 生物大分子以碳链为骨架
- 第二章 细胞的结构
- 第一节 细胞是生命的单位
- 第二节 细胞膜控制细胞与周围环境的联系
- 第三节 细胞质是多项生命活动的场所
- 第四节 细胞核是细胞生命活动的控制中心
- 第五节 细胞在结构和功能上是一个统一整体
- 第六节 原核细胞内无成形的细胞核
- 第三章 细胞的代谢
- 第一节 ATP是细胞内的“能量通货”
- 第二节 酶是生物催化剂
- 第三节 物质通过多种方式出入细胞
- 第四节 细胞呼吸为细胞生活提供能量
- 第五节 光合作用将光能转化为化学能
- 第四章 细胞的生命历程
- 第一节 细胞通过分裂增殖
- 第二节 细胞通过分化产生不同类型的细胞
- 第三节 细胞凋亡是编程性死亡
