【名师原创】2015年沪教版九年级下册精品备课课件:第七章 应用广泛的酸、碱、盐 本章总结提升(共27张PPT)
文档属性
| 名称 | 【名师原创】2015年沪教版九年级下册精品备课课件:第七章 应用广泛的酸、碱、盐 本章总结提升(共27张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 333.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2015-01-22 00:00:00 | ||
图片预览

文档简介
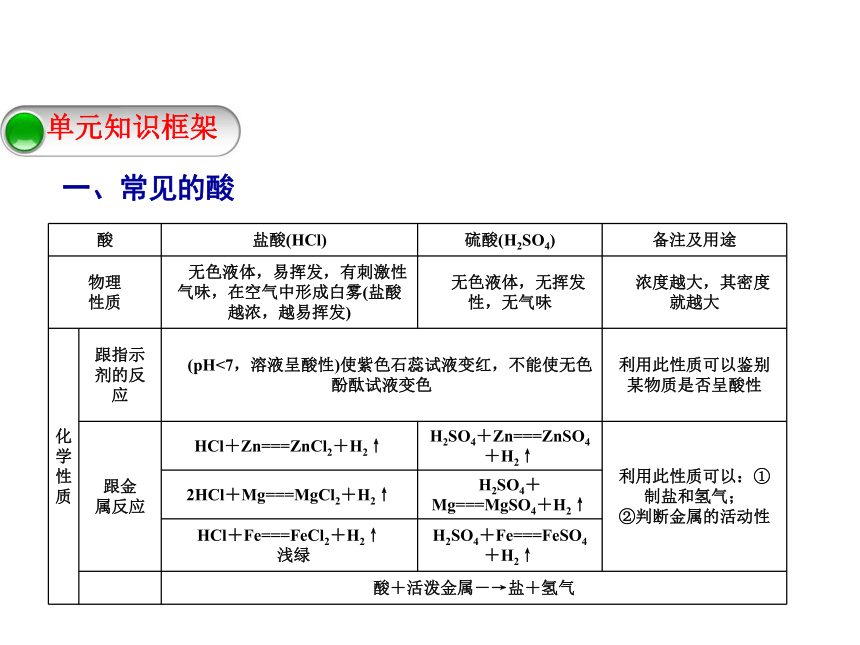
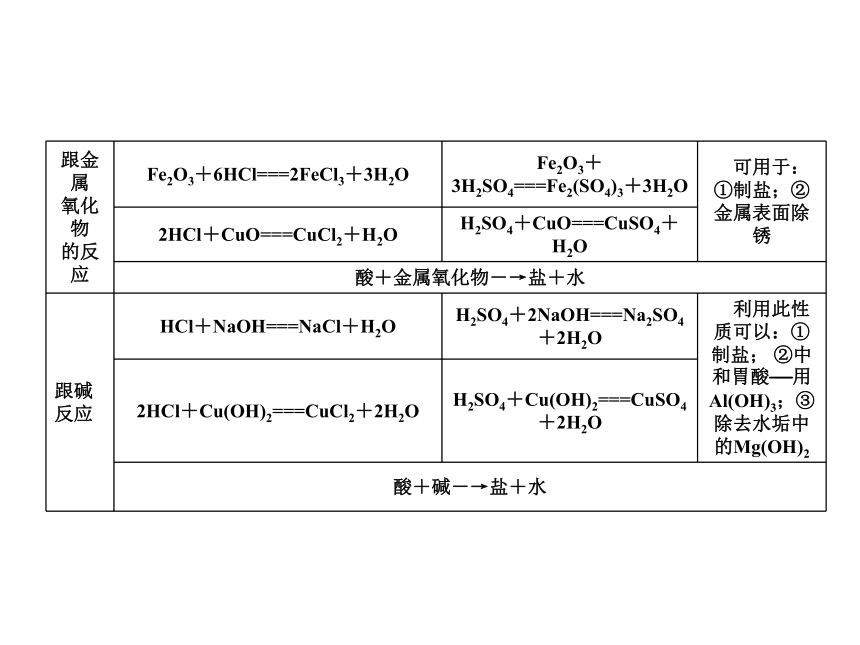
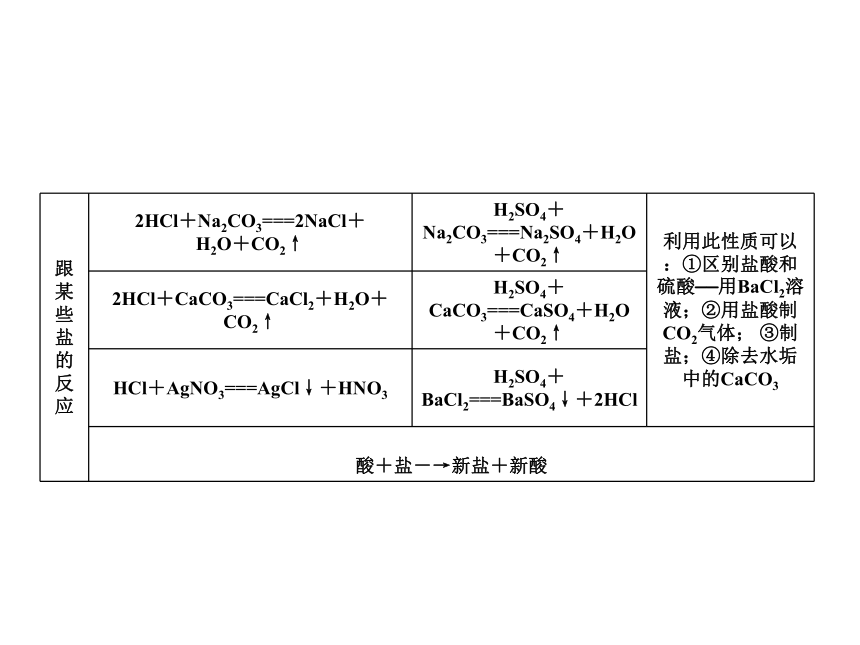
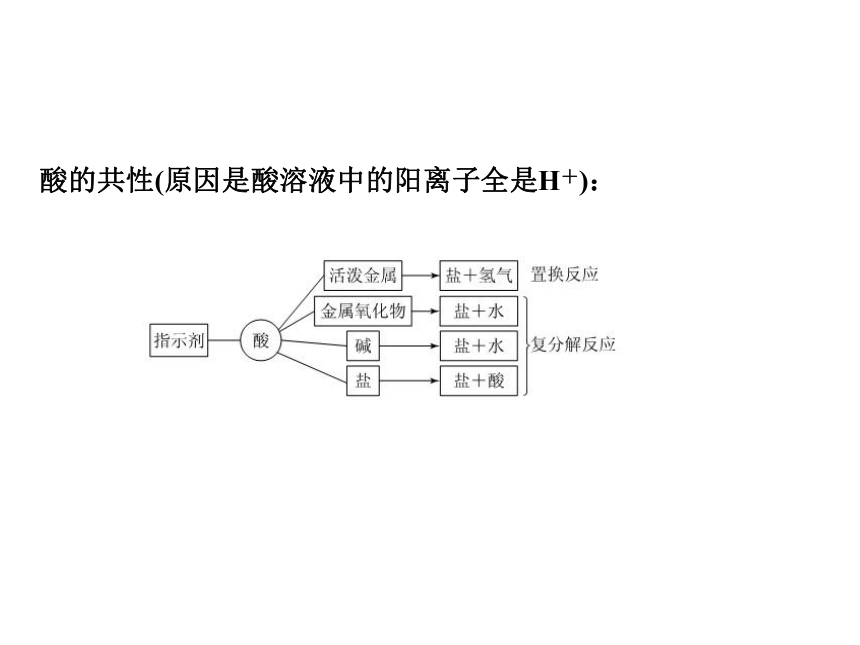
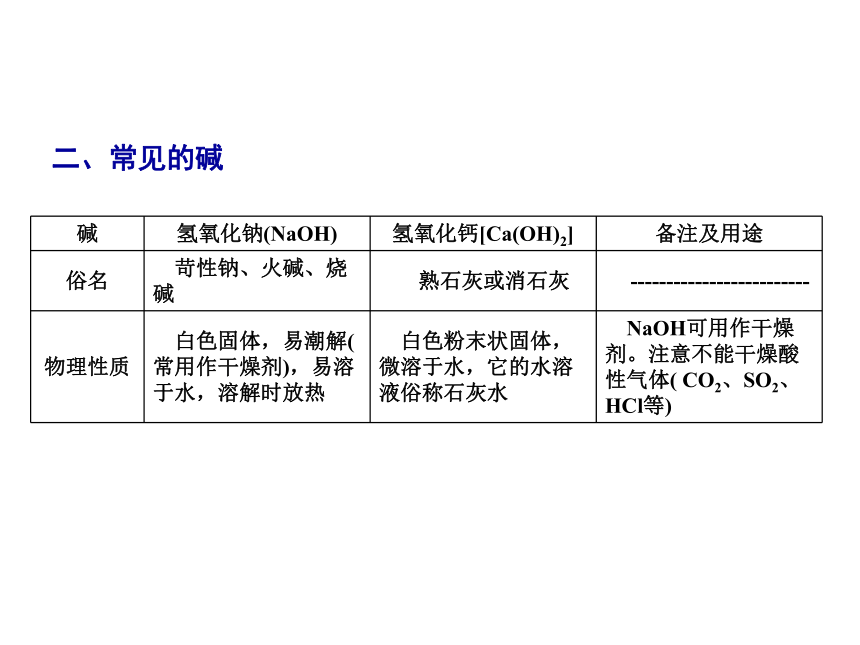
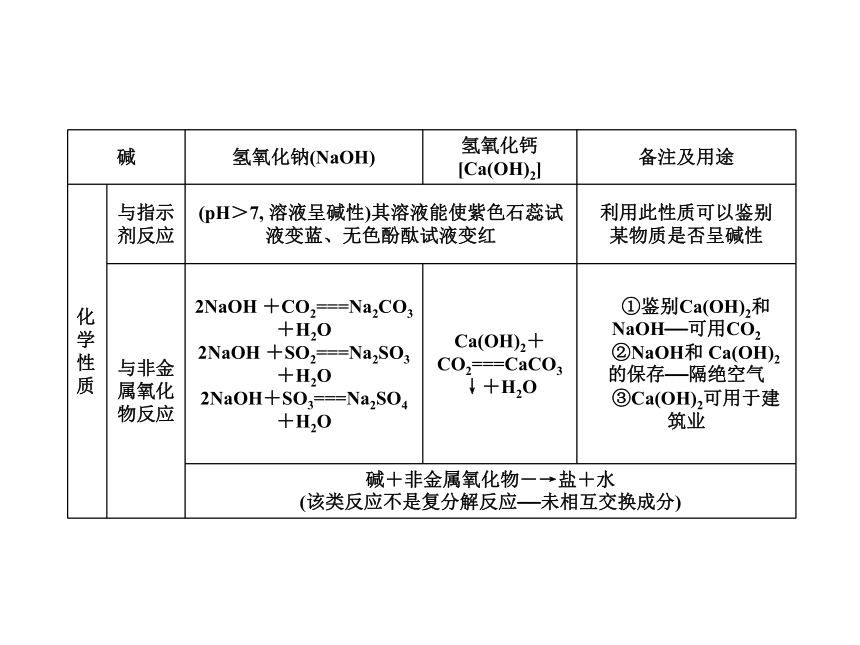
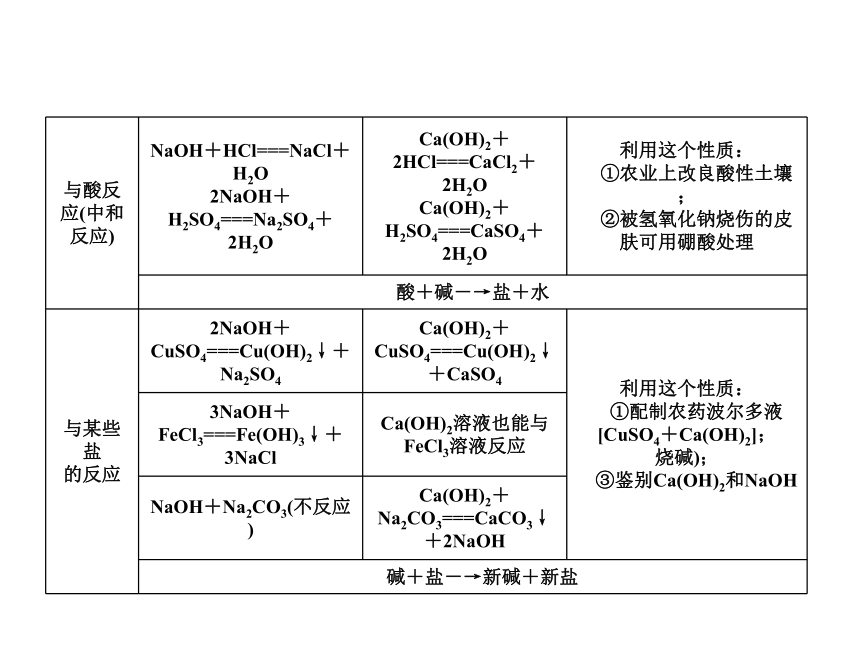
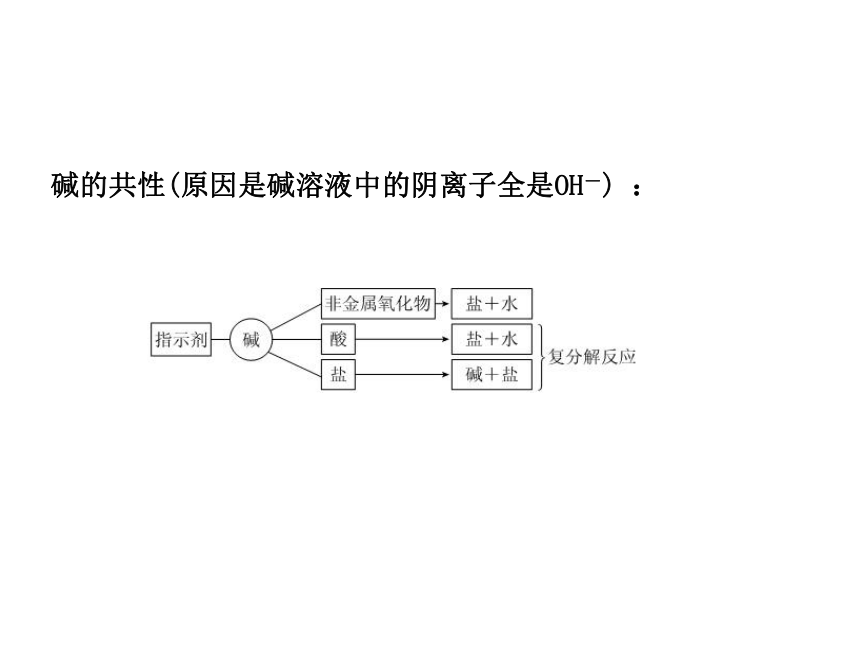
课件27张PPT。单元总结提升一、常见的酸第六章 溶解现象第六章 溶解现象第六章 溶解现象第六章 溶解现象酸的共性(原因是酸溶液中的阳离子全是H+):二、常见的碱第六章 溶解现象第六章 溶解现象第六章 溶解现象第六章 溶解现象碱的共性(原因是碱溶液中的阴离子全是OH-) : 第六章 溶解现象三、盐的性质(盐无共同的离子,故无共同的性质) 第六章 溶解现象例1 小梅同学学习了单质、氧化物、酸、碱、盐的性质后,发现许多不同类别的物质反应时能生成盐,于是她构建了如图7-T-3所示的知识网络图。铜及其化合物在工业上有重要的应用。请你借助网络图回答下列问题。类型一 正确判断酸、碱、盐之间的反应第六章 溶解现象 (1)写出用酸和碱生产硫酸铜的化学方程式:
__________________________________________。
(2)请你把图中①②处补充完整,要求不能与图中已有信息重复。
①________________;②____________________。
(3)根据网络图可制备物质。例如,某回收含铜电缆废料的工厂有下列制铜的方案。第六章 溶解现象 ①写出下列步骤中的化学方程式。
步骤Ⅲ:______________________________________。
步骤Ⅴ:___________________________________。
②上述方案中可能造成空气污染的步骤是___________。第六章 溶解现象[答案] (1)H2SO4+Cu(OH)2===CuSO4+2H2O (2)酸+盐 金属+盐(其他合理答案也可)
(3)①2NaOH+CuSO4===Cu(OH)2↓+Na2SO4
CO+CuOCu+CO2 ②步骤Ⅰ和步骤Ⅴ [解析] 含铜电缆废料在灼烧过程中会产生大气污染物;CO和CuO的反应中CO有毒,也会造成空气污染。第六章 溶解现象1.下列各组物质能按照关系图 (其中“―→”表示反应一步完成)相互转化的是( )针对训练[解析] B Ca(OH)2溶液加稀盐酸可生成CaCl2,Ca(OH)2溶液加Na2CO3溶液可生成CaCO3,CaCl2加Na2CO3溶液也可生成CaCO3。
第六章 溶解现象例2 一定条件下,下列物质的转化均可一步实现的是( )
A.CaCl2→CaCO3→Ca(OH)2
B.AgNO3→Fe(NO3)2→Zn(NO3)2
C.NaNO3→NaOH→Na2CO3
D.Fe2O3→FeSO4→Fe(OH)3类型二 熟悉酸、碱、盐之间的相互转化第六章 溶解现象[解析] B 2AgNO3+FeCl2===Fe(NO3)2+2AgCl↓,Fe(NO3)2+Zn===Zn(NO3)2+Fe。选项A中CaCO3不能一步转化为Ca(OH)2;选项C中NaNO3不能一步转化为NaOH;选项D中的两组转化皆不能一步实现。2.下表中各物质不能按照图7-T-5中关系(“―→”表示反应一步完成)转化的是( )针对训练第六章 溶解现象[解析] A 假设NaNO3可以一步转化为Na2SO4,则有复分解反应NaNO3+H2SO4―→Na2SO4+HNO3能够发生。显然Na2SO4和HNO3不是沉淀(所有的硝酸盐都能溶于水),该复分解反应不能发生,原假设错误,因此NaNO3不能一步转化为Na2SO4。第六章 溶解现象类型三 知道化肥的检验方法例3 化学实验室有一瓶化肥的标签已脱落,只知道它是NH4Cl、(NH4)2SO4、NH4HCO3和尿素[CO(NH2)2]中的一种。请你完成以下探究。
[猜想] 猜想①:该化肥是NH4Cl。
猜想②:该化肥是__________。
猜想③:该化肥是NH4HCO3。
猜想④:该化肥是尿素。
[实验探究] 第六章 溶解现象(1)取少量样品在研钵中与熟石灰研磨,有刺激性气味的气体放出,证明猜想________不成立;写出其中一种化肥发生该反应的化学方程式:____________________________。
(2)如图7-T-6中(a)所示,另取少量样品于试管中,滴加适量水振荡,再选图(b)中__________溶液滴入试管中,若无气泡放出,则猜想__________不成立。
(3)在步骤(2)的试管中再滴入图(b)中的________溶液,若________________,则猜想①成立;若______________,则猜想②成立,其反应的化学方程式为__________________。第六章 溶解现象[答案] [猜想] (NH4)2SO4(或硫酸铵)
[实验探究] (1)④ 2NH4Cl+Ca(OH)2===CaCl2+2H2O+2NH3↑[或(NH4)2SO4+Ca(OH)2===CaSO4+2H2O+2NH3↑,或NH4HCO3+Ca(OH)2===CaCO3↓+2H2O+NH3↑]
(2)HCl ③
(3)BaCl2 无白色沉淀 有白色沉淀
(NH4)2SO4+BaCl2===BaSO4↓+2NH4Cl第六章 溶解现象3.氮肥、磷肥、钾肥是农业生产中最主要的化肥,用简便的方法区别三种化肥,在农业生产中具有实用性。区别下列相关化肥的方法可行的是( )
A.NH4Cl与KCl:观察外观
B.NH4HCO3与KCl:加水
C.K2SO4与Ca3(PO4)2:闻气味
D.(NH4)2SO4与K2SO4:加熟石灰研磨后闻气味针对训练[解析] D (NH4)2SO4是铵盐,加熟石灰研磨后有刺激性气味,而K2SO4没有气味。第六章 溶解现象类型四 金属活动性强弱的判断 例4 图7-T-7为某学习小组探究金属化学性质时所做的四个实验,仔细分析后回答下列问题。
图7-T-7
(1)描述A中的实验现象:____。
(2)写出C中反应的化学方程式:_____。
(3)要证明Cu、Fe、Ag的活动性顺序,至少要做的实验是__________(填序号)。
(4)开始反应后D中溶液逐渐变为黄色,原因是_____。第六章 溶解现象第六章 溶解现象[答案] (1)铜丝表面附着一层银白色固体,溶液变为蓝色 (2)Zn+2HCl===ZnCl2+H2↑ (3)A、B (4)铁钉未打磨有铁锈[或溶液中有Fe2(SO4)3生成,其他合理答案均可][解析] 铜的活动性比银强,所以会在铜丝表面有银白色物质析出;要想确定金属的活动性顺序,必须做的实验即是可以保证看到不同的现象,能够直接得出活动性顺序的,避免重复无效的实验,从图示实验内容来看,A、B两个实验即可证明三种金属的活动性顺序。二价铁离子为浅绿色,黄色是三价铁离子的颜色,估计是铁钉表面有铁锈。针对训练4.下列实验方案能证明铁、铜、银三种金属活动性顺序的是( )
A.将铁丝、铜丝分别放入硝酸银溶液中,根据现象,判断结果
B.将铁丝分别放入硫酸铜、硝酸银溶液中,根据现象,判断结果
C.将铁、铜、银三种金属丝分别放入稀硫酸中,根据现象,判断结果
D.先将铁、铜、银三种金属丝分别放入稀硫酸中,再将铜丝放入硝酸银溶液中,根据现象,判断结果第六章 溶解现象[解析] D 方案A不能判断铁和铜的金属活动性强弱;方案B、C都不能判断铜和银的金属活动性强弱。
第六章 溶解现象
__________________________________________。
(2)请你把图中①②处补充完整,要求不能与图中已有信息重复。
①________________;②____________________。
(3)根据网络图可制备物质。例如,某回收含铜电缆废料的工厂有下列制铜的方案。第六章 溶解现象 ①写出下列步骤中的化学方程式。
步骤Ⅲ:______________________________________。
步骤Ⅴ:___________________________________。
②上述方案中可能造成空气污染的步骤是___________。第六章 溶解现象[答案] (1)H2SO4+Cu(OH)2===CuSO4+2H2O (2)酸+盐 金属+盐(其他合理答案也可)
(3)①2NaOH+CuSO4===Cu(OH)2↓+Na2SO4
CO+CuOCu+CO2 ②步骤Ⅰ和步骤Ⅴ [解析] 含铜电缆废料在灼烧过程中会产生大气污染物;CO和CuO的反应中CO有毒,也会造成空气污染。第六章 溶解现象1.下列各组物质能按照关系图 (其中“―→”表示反应一步完成)相互转化的是( )针对训练[解析] B Ca(OH)2溶液加稀盐酸可生成CaCl2,Ca(OH)2溶液加Na2CO3溶液可生成CaCO3,CaCl2加Na2CO3溶液也可生成CaCO3。
第六章 溶解现象例2 一定条件下,下列物质的转化均可一步实现的是( )
A.CaCl2→CaCO3→Ca(OH)2
B.AgNO3→Fe(NO3)2→Zn(NO3)2
C.NaNO3→NaOH→Na2CO3
D.Fe2O3→FeSO4→Fe(OH)3类型二 熟悉酸、碱、盐之间的相互转化第六章 溶解现象[解析] B 2AgNO3+FeCl2===Fe(NO3)2+2AgCl↓,Fe(NO3)2+Zn===Zn(NO3)2+Fe。选项A中CaCO3不能一步转化为Ca(OH)2;选项C中NaNO3不能一步转化为NaOH;选项D中的两组转化皆不能一步实现。2.下表中各物质不能按照图7-T-5中关系(“―→”表示反应一步完成)转化的是( )针对训练第六章 溶解现象[解析] A 假设NaNO3可以一步转化为Na2SO4,则有复分解反应NaNO3+H2SO4―→Na2SO4+HNO3能够发生。显然Na2SO4和HNO3不是沉淀(所有的硝酸盐都能溶于水),该复分解反应不能发生,原假设错误,因此NaNO3不能一步转化为Na2SO4。第六章 溶解现象类型三 知道化肥的检验方法例3 化学实验室有一瓶化肥的标签已脱落,只知道它是NH4Cl、(NH4)2SO4、NH4HCO3和尿素[CO(NH2)2]中的一种。请你完成以下探究。
[猜想] 猜想①:该化肥是NH4Cl。
猜想②:该化肥是__________。
猜想③:该化肥是NH4HCO3。
猜想④:该化肥是尿素。
[实验探究] 第六章 溶解现象(1)取少量样品在研钵中与熟石灰研磨,有刺激性气味的气体放出,证明猜想________不成立;写出其中一种化肥发生该反应的化学方程式:____________________________。
(2)如图7-T-6中(a)所示,另取少量样品于试管中,滴加适量水振荡,再选图(b)中__________溶液滴入试管中,若无气泡放出,则猜想__________不成立。
(3)在步骤(2)的试管中再滴入图(b)中的________溶液,若________________,则猜想①成立;若______________,则猜想②成立,其反应的化学方程式为__________________。第六章 溶解现象[答案] [猜想] (NH4)2SO4(或硫酸铵)
[实验探究] (1)④ 2NH4Cl+Ca(OH)2===CaCl2+2H2O+2NH3↑[或(NH4)2SO4+Ca(OH)2===CaSO4+2H2O+2NH3↑,或NH4HCO3+Ca(OH)2===CaCO3↓+2H2O+NH3↑]
(2)HCl ③
(3)BaCl2 无白色沉淀 有白色沉淀
(NH4)2SO4+BaCl2===BaSO4↓+2NH4Cl第六章 溶解现象3.氮肥、磷肥、钾肥是农业生产中最主要的化肥,用简便的方法区别三种化肥,在农业生产中具有实用性。区别下列相关化肥的方法可行的是( )
A.NH4Cl与KCl:观察外观
B.NH4HCO3与KCl:加水
C.K2SO4与Ca3(PO4)2:闻气味
D.(NH4)2SO4与K2SO4:加熟石灰研磨后闻气味针对训练[解析] D (NH4)2SO4是铵盐,加熟石灰研磨后有刺激性气味,而K2SO4没有气味。第六章 溶解现象类型四 金属活动性强弱的判断 例4 图7-T-7为某学习小组探究金属化学性质时所做的四个实验,仔细分析后回答下列问题。
图7-T-7
(1)描述A中的实验现象:____。
(2)写出C中反应的化学方程式:_____。
(3)要证明Cu、Fe、Ag的活动性顺序,至少要做的实验是__________(填序号)。
(4)开始反应后D中溶液逐渐变为黄色,原因是_____。第六章 溶解现象第六章 溶解现象[答案] (1)铜丝表面附着一层银白色固体,溶液变为蓝色 (2)Zn+2HCl===ZnCl2+H2↑ (3)A、B (4)铁钉未打磨有铁锈[或溶液中有Fe2(SO4)3生成,其他合理答案均可][解析] 铜的活动性比银强,所以会在铜丝表面有银白色物质析出;要想确定金属的活动性顺序,必须做的实验即是可以保证看到不同的现象,能够直接得出活动性顺序的,避免重复无效的实验,从图示实验内容来看,A、B两个实验即可证明三种金属的活动性顺序。二价铁离子为浅绿色,黄色是三价铁离子的颜色,估计是铁钉表面有铁锈。针对训练4.下列实验方案能证明铁、铜、银三种金属活动性顺序的是( )
A.将铁丝、铜丝分别放入硝酸银溶液中,根据现象,判断结果
B.将铁丝分别放入硫酸铜、硝酸银溶液中,根据现象,判断结果
C.将铁、铜、银三种金属丝分别放入稀硫酸中,根据现象,判断结果
D.先将铁、铜、银三种金属丝分别放入稀硫酸中,再将铜丝放入硝酸银溶液中,根据现象,判断结果第六章 溶解现象[解析] D 方案A不能判断铁和铜的金属活动性强弱;方案B、C都不能判断铜和银的金属活动性强弱。
第六章 溶解现象
