福建省上杭县蛟洋中学九年级化学教学课件:第七章第二节 常见的酸和碱(共39张PPT)
文档属性
| 名称 | 福建省上杭县蛟洋中学九年级化学教学课件:第七章第二节 常见的酸和碱(共39张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 371.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2015-03-22 00:00:00 | ||
图片预览











文档简介
课件39张PPT。常见的酸和碱
酸和碱的通性1、什么叫酸?由氢离子和酸根离子构成的化合物叫酸.2、什么叫碱?由金属离子和氢氧根离子构成的化合物叫碱。思考问题:如: 硫酸 盐酸 硝酸 . 碳酸 醋酸 .如: 氢氧化钠 氢氧化钙 .
氢氧化钾 氨水 .H2SO4HClHNO3 H2CO3CH3COOHNaOHCa(OH)2KOHNH3 H2O复习:常见的酸和碱
3、掌握酸的通性、碱的通性及有关化学方程 式。
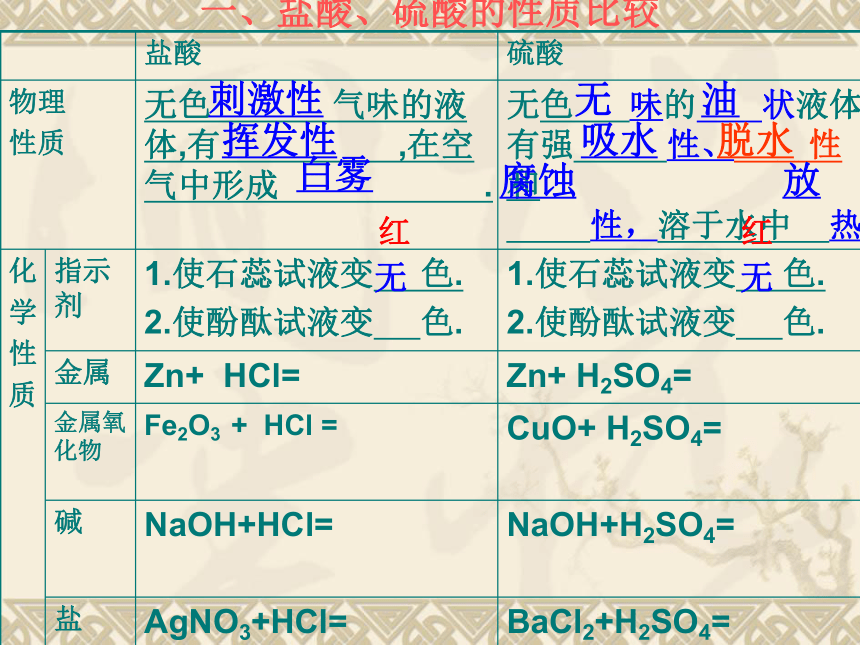
1、掌握盐酸、硫酸的物理性质和化学性质。2、掌握氢氧化钠、氢氧化钙物理和化学性质复习目标:一、盐酸、硫酸的性质比较红红无无刺激性挥发性白雾无吸水油腐蚀脱水放一、盐酸、硫酸的性质比较红红无无刺激性挥发性白雾无吸水油腐蚀脱水放
1.能使指示剂变色
2.酸+金属=盐+氢气3.酸+金属氧化物=盐+水4.酸+碱=盐+水(中和反应)5. 酸+盐=新酸+新盐酸能使石蕊变红, 能使酚酞变色 ,使PH试纸变棕--红色 条件:(1)金属指排在H
前面的活泼金属Zn+H2SO4=ZnSO4+H2↑
Fe +H2SO4=FeSO4+H2↑CuO+H2SO4=CuSO4+H2O Fe2O3+6HCl=2FeCl3+3H2ONaOH+HCl=NaCl+H2O Cu(OH)2+H2SO4=CuSO4+2H2O条件:生成物中有↑ 或↓或水
AgNO3+HCl=AgCl ↓ + HNO3
Ba(NO3)2+H2SO4=BaSO4 ↓+ 2HNO3
CaCO3+2HCl=CaCl2 + H2O + CO 2↑总结:酸的通性小明看见爸爸常常用稀盐酸给铁制器皿除锈,他自己想亲自试一试。于是,他找出一颗生锈铁钉出来,放入足量稀盐酸中,然后,美滋滋地去睡觉了……生活知多D可是,当他醒来之后,发现铁钉 不见了,你知道为什么吗?用两 个化学方程式表示出来。生锈铁钉消失的原因1、Fe2O3+6HCl == 2FeCl3+ 3H2O
2、 Fe + 2HCl ==FeCl2 + H2↑铁锈溶解 铁溶解 溶解完全 “雪碧”是一种无色的碳酸饮料,将少量“雪碧”滴入紫色石蕊试液中,然后再加热,溶液颜色的变化是( )
A.先变蓝后变紫B.变红后颜色不再改变
C.先变无色后变红 D.先变红后变紫生活知多DD提示: 雪碧中含碳酸H2CO3,它能使紫色石蕊溶液变红色,但加热时碳酸分解:H2CO3==H2O+CO2↑ 所以石蕊溶液又变回原来的紫色.苯甲酸(C6H5COOH)可用作食品防腐剂,其酸性比醋酸强,下列对苯甲酸性质的推测,不合理的是( )
A、苯甲酸能使石蕊试液变红色
B、苯甲酸不能使酚酞变色
C、苯甲酸溶液的pH>7
D、苯甲酸溶液的pH<7练习C火碱、烧碱、苛性钠消石灰、熟石灰、石灰浆1、—色—状—体, 2、—溶于水,放出——, 3、易—而—可以用作— 4、有—性1、—色—状—体, 2、—溶于水,它的水溶液俗称— 3、也有—性使石蕊试液变——色,使酚酞试液变——色蓝红使石蕊试液变——色 使酚酞试液变——色蓝红CO2+NaOH——
SO2+NaOH——CO2+Ca(OH)2 —NaOH+HCl——Ca(OH)2 + HCl—CuSO4+NaOH——Na2CO3+Ca(OH)2——火碱、烧碱、苛性钠消石灰、熟石灰、石灰浆1、白色块状固体, 2、易溶于水,放出热量, 3、易吸水而潮解,可以用作 干燥剂 4、有腐蚀性1、白色粉末状固体, 2、微溶于水,水溶液俗称石灰水 3、也有腐蚀性使石蕊试液变——色,使酚酞试液变——色蓝红使石蕊试液变——色 使酚酞试液变——色蓝红CO2+NaOH——
SO2+NaOH——CO2+Ca(OH)2 —NaOH+HCl——Ca(OH)2 + HCl—CuSO4+NaOH——Na2CO3+Ca(OH)2——1.能使指示剂变色 2.碱+非金属氧化物=盐+水 3.碱+酸=盐+水(中和反应)4.碱+盐=新碱+新盐CO2+Ca(OH)2=CaCO 3↓ +H2O
CO2+2NaOH=Na2CO3+H2O
SO2 +2NaOH=Na2SO3+H2O条件:(1)生成物中有↑ 或↓或水 (2)反应物均可溶CuSO4 + 2NaOH = Cu(OH)2 ↓ + Na2SO4
Ca(OH)2 + Na2CO3 = CaCO3 ↓ + 2NaOH
FeCl3 + 3NaOH = Fe(OH)3 ↓ + 3NaCl
NH4NO3 + NaOH = NH3 ↑ + H2O + NaNO3使紫色的石蕊试液变——色,使无色的酚酞试液变——色NaOH+HCl=NaCl+H2O Cu(OH)2+H2SO4=CuSO4+2H2O总结:碱的通性成份:氢氧化铝、碘甲基蛋氨酸等3HCl + Al(OH)3 == AlCl3 + 3H2O生活知多D用化学方程式表示斯达舒治疗胃酸过多症的原理:敞口的氢氧化钠固体质量会变化吗?动动脑答案: 会增大。因为氢氧化钠易吸水且与CO2反应:
2NaOH + CO2 === Na2CO3 + H2O
80 44 106 181、把纯水、稀硫酸和氢氧化钠三种无色溶液区别开的最简单的方法是( )
A:滴入酚酞试液 B:滴入石蕊试液
C:滴入氯化钡溶液 D:通入二氧化碳气体B2、下列物质不能和氢氧化钠溶液反应生成盐和水的是( )
A:三氧化硫 B:二氧化碳
C:氧化镁 D:稀硫酸C答案:_____C 2、混有少量水蒸气的下列气体,能用氢氧化钠固体干燥的是( )
A: CO2 B: H2 C: SO2 D: HClB3、下列物质长期露置在空气中,质量会减少的是( )
A:浓盐酸 B:固体烧碱
C:大理石 D:浓硫酸A4、下列四种物质中,在一定条件下能与其它三种物质发生反应的是( )
A: CuSO4 B:CO2
C:NaOH D:H2SO4C2NaOH + CuSO4 ===Cu(OH)2 ↓ + Na2SO4
2NaOH+ CO2=== Na2CO3 + H2O
2NaOH+H2SO4===Na2SO4+H2O3、在氯化铁溶液中滴入烧碱溶液,观察到的现象是( )
A:有白色沉淀 B:有红褐色沉淀
C:有气泡冒出 D:有蓝色沉淀产生BFeCl3 + 3NaOH=== Fe(OH)3 ↓ + 3NaCl 红褐色提示:H2SO4+Ba(OH)2==H2O↓+BaSO4↓DCaCO3+2HCl==CaCl2+H2O+CO2↑Ca(OH)2+2HCl==CaCl2+H2OCuO+2HCl==CuCl2+H2O6、下列各组物质混合后不产生沉淀和气体,能得到无色溶液的是( )
A:氢氧化钡溶液和稀硫酸
B:氧化铜和稀盐酸
C:大理石和稀盐酸
D:石灰水和稀盐酸
7、填空 氢氧化钠又名苛性钠,这是因为它有强烈的_________。氢氧化钠必须密封保存,是因为它能吸收空气中的_____,并能跟空气中的_____________起反应。腐蚀性水分二氧化碳2NaOH+ CO2=== Na2CO3 + H2O5、下列物质与稀硫酸反应不能产生氢气的是( )
A: 镁 B:银 C:铁 D:铝B 根据金属活动性顺序表知道: 镁>铝>铁>(氢)>银
银排在氢之后,所以它不能和稀硫酸反应.提示:酸→H++酸根离子 8、“物质的组成与结构决定物质的性质”是化学学科中的重要观点。按照这一观点讨论:
酸溶液具有一些共同的化学性质,是因为酸溶液中都含有 ;碱溶液也具有一些共同的化学性质,是因为碱溶液中都含有 。练习碱→金属离子+OH-H+OH-鱼胆弄破后会使鱼肉粘上难溶解于水的胆汁酸(一种酸)而变苦,要减少这种苦味,用来洗涤的最佳物质是( )。
A、水 B、食盐
C、纯碱 D、食醋C生活知多D 计算题
Na2CO3和Na2SO4的混合物12.4克与100克稀硫酸恰好完全反应,产生2.2克气体。求:
(1)原混合物中硫酸钠的质量分数?
(2)反应后溶液中硫酸钠的质量分数?
取NaOH溶液适量于小烧杯中,滴入几滴酚酞试液,然后再向该溶液中逐滴滴入稀HCl。溶液先由无色变红,再由红变无色。氢氧化钠溶液能与稀盐酸反应。动动脑一定条件下,同一化学反应进行的快慢与反应物的质量分数成正比。现用100克溶液质质量分数为30%的盐酸溶液与过量的锌粉反应,为了使反应慢点进行而又不生成氢气的总量,可向所用的盐酸中加入适量的( )。
A、氢氧化钠 B、水
C、氧化镁 D、碳酸钙练习B 现有白纸和几种溶液,有人用这些材料设计了一个名为“雨落叶出红花开”的趣味实验。实验的过程如下:先用洁净的毛笔蘸 (填序号,下同)在白纸上画上花,再用 画上叶,将白纸挂上墙壁,晾干后用 向纸上喷即成。
A、酚酞试液 B、石蕊试液
C、氢氧化钠溶液 D、稀盐酸练习用锌粒和盐酸反应制取的氢气中,常混有水蒸气和氯化氢气体,为了除去气体杂质,可使混合气体通过右图A、B两装置,气体通过两瓶的导管顺序正确的是( ) A、abcd B、dcba C、cdab D、bacd a b c d浓硫酸NaOH溶液练习CA B下列四种物质中,能和其他三种物质反应的是( )。
A、盐酸 B、锌
C、铁锈 D、氢氧化铜练习A下列四种物质中,能和其他三种物质反应的是( )。
A、盐酸 B、二氧化碳
C、硫酸铜 D、氢氧化钠练习D稀盐酸NaOH溶液紫色石蕊稀盐酸NaOH溶液无色酚酞一、稀盐酸、稀硫酸的化学性质:1、酸 + 指示剂 pH试纸:0——7——14
酸红—中黄—碱蓝金属活动性顺序表(强到弱)K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au思考题 煤是重要的化工原料,用煤做燃料,不仅是极大的浪费,而且因燃煤中含有硫的化合物燃烧时生成SO2气体造成环境污染。
假设一个有30万户居民的中等城市,每户每天烧煤5千克,这种煤中含硫的90%转化为SO2,则该城市每年排放到空气中的SO2的质量约为2.6吨。
试分析:我们可以采取哪些措施以减少SO2对空气的污染?
酸和碱的通性1、什么叫酸?由氢离子和酸根离子构成的化合物叫酸.2、什么叫碱?由金属离子和氢氧根离子构成的化合物叫碱。思考问题:如: 硫酸 盐酸 硝酸 . 碳酸 醋酸 .如: 氢氧化钠 氢氧化钙 .
氢氧化钾 氨水 .H2SO4HClHNO3 H2CO3CH3COOHNaOHCa(OH)2KOHNH3 H2O复习:常见的酸和碱
3、掌握酸的通性、碱的通性及有关化学方程 式。
1、掌握盐酸、硫酸的物理性质和化学性质。2、掌握氢氧化钠、氢氧化钙物理和化学性质复习目标:一、盐酸、硫酸的性质比较红红无无刺激性挥发性白雾无吸水油腐蚀脱水放一、盐酸、硫酸的性质比较红红无无刺激性挥发性白雾无吸水油腐蚀脱水放
1.能使指示剂变色
2.酸+金属=盐+氢气3.酸+金属氧化物=盐+水4.酸+碱=盐+水(中和反应)5. 酸+盐=新酸+新盐酸能使石蕊变红, 能使酚酞变色 ,使PH试纸变棕--红色 条件:(1)金属指排在H
前面的活泼金属Zn+H2SO4=ZnSO4+H2↑
Fe +H2SO4=FeSO4+H2↑CuO+H2SO4=CuSO4+H2O Fe2O3+6HCl=2FeCl3+3H2ONaOH+HCl=NaCl+H2O Cu(OH)2+H2SO4=CuSO4+2H2O条件:生成物中有↑ 或↓或水
AgNO3+HCl=AgCl ↓ + HNO3
Ba(NO3)2+H2SO4=BaSO4 ↓+ 2HNO3
CaCO3+2HCl=CaCl2 + H2O + CO 2↑总结:酸的通性小明看见爸爸常常用稀盐酸给铁制器皿除锈,他自己想亲自试一试。于是,他找出一颗生锈铁钉出来,放入足量稀盐酸中,然后,美滋滋地去睡觉了……生活知多D可是,当他醒来之后,发现铁钉 不见了,你知道为什么吗?用两 个化学方程式表示出来。生锈铁钉消失的原因1、Fe2O3+6HCl == 2FeCl3+ 3H2O
2、 Fe + 2HCl ==FeCl2 + H2↑铁锈溶解 铁溶解 溶解完全 “雪碧”是一种无色的碳酸饮料,将少量“雪碧”滴入紫色石蕊试液中,然后再加热,溶液颜色的变化是( )
A.先变蓝后变紫B.变红后颜色不再改变
C.先变无色后变红 D.先变红后变紫生活知多DD提示: 雪碧中含碳酸H2CO3,它能使紫色石蕊溶液变红色,但加热时碳酸分解:H2CO3==H2O+CO2↑ 所以石蕊溶液又变回原来的紫色.苯甲酸(C6H5COOH)可用作食品防腐剂,其酸性比醋酸强,下列对苯甲酸性质的推测,不合理的是( )
A、苯甲酸能使石蕊试液变红色
B、苯甲酸不能使酚酞变色
C、苯甲酸溶液的pH>7
D、苯甲酸溶液的pH<7练习C火碱、烧碱、苛性钠消石灰、熟石灰、石灰浆1、—色—状—体, 2、—溶于水,放出——, 3、易—而—可以用作— 4、有—性1、—色—状—体, 2、—溶于水,它的水溶液俗称— 3、也有—性使石蕊试液变——色,使酚酞试液变——色蓝红使石蕊试液变——色 使酚酞试液变——色蓝红CO2+NaOH——
SO2+NaOH——CO2+Ca(OH)2 —NaOH+HCl——Ca(OH)2 + HCl—CuSO4+NaOH——Na2CO3+Ca(OH)2——火碱、烧碱、苛性钠消石灰、熟石灰、石灰浆1、白色块状固体, 2、易溶于水,放出热量, 3、易吸水而潮解,可以用作 干燥剂 4、有腐蚀性1、白色粉末状固体, 2、微溶于水,水溶液俗称石灰水 3、也有腐蚀性使石蕊试液变——色,使酚酞试液变——色蓝红使石蕊试液变——色 使酚酞试液变——色蓝红CO2+NaOH——
SO2+NaOH——CO2+Ca(OH)2 —NaOH+HCl——Ca(OH)2 + HCl—CuSO4+NaOH——Na2CO3+Ca(OH)2——1.能使指示剂变色 2.碱+非金属氧化物=盐+水 3.碱+酸=盐+水(中和反应)4.碱+盐=新碱+新盐CO2+Ca(OH)2=CaCO 3↓ +H2O
CO2+2NaOH=Na2CO3+H2O
SO2 +2NaOH=Na2SO3+H2O条件:(1)生成物中有↑ 或↓或水 (2)反应物均可溶CuSO4 + 2NaOH = Cu(OH)2 ↓ + Na2SO4
Ca(OH)2 + Na2CO3 = CaCO3 ↓ + 2NaOH
FeCl3 + 3NaOH = Fe(OH)3 ↓ + 3NaCl
NH4NO3 + NaOH = NH3 ↑ + H2O + NaNO3使紫色的石蕊试液变——色,使无色的酚酞试液变——色NaOH+HCl=NaCl+H2O Cu(OH)2+H2SO4=CuSO4+2H2O总结:碱的通性成份:氢氧化铝、碘甲基蛋氨酸等3HCl + Al(OH)3 == AlCl3 + 3H2O生活知多D用化学方程式表示斯达舒治疗胃酸过多症的原理:敞口的氢氧化钠固体质量会变化吗?动动脑答案: 会增大。因为氢氧化钠易吸水且与CO2反应:
2NaOH + CO2 === Na2CO3 + H2O
80 44 106 181、把纯水、稀硫酸和氢氧化钠三种无色溶液区别开的最简单的方法是( )
A:滴入酚酞试液 B:滴入石蕊试液
C:滴入氯化钡溶液 D:通入二氧化碳气体B2、下列物质不能和氢氧化钠溶液反应生成盐和水的是( )
A:三氧化硫 B:二氧化碳
C:氧化镁 D:稀硫酸C答案:_____C 2、混有少量水蒸气的下列气体,能用氢氧化钠固体干燥的是( )
A: CO2 B: H2 C: SO2 D: HClB3、下列物质长期露置在空气中,质量会减少的是( )
A:浓盐酸 B:固体烧碱
C:大理石 D:浓硫酸A4、下列四种物质中,在一定条件下能与其它三种物质发生反应的是( )
A: CuSO4 B:CO2
C:NaOH D:H2SO4C2NaOH + CuSO4 ===Cu(OH)2 ↓ + Na2SO4
2NaOH+ CO2=== Na2CO3 + H2O
2NaOH+H2SO4===Na2SO4+H2O3、在氯化铁溶液中滴入烧碱溶液,观察到的现象是( )
A:有白色沉淀 B:有红褐色沉淀
C:有气泡冒出 D:有蓝色沉淀产生BFeCl3 + 3NaOH=== Fe(OH)3 ↓ + 3NaCl 红褐色提示:H2SO4+Ba(OH)2==H2O↓+BaSO4↓DCaCO3+2HCl==CaCl2+H2O+CO2↑Ca(OH)2+2HCl==CaCl2+H2OCuO+2HCl==CuCl2+H2O6、下列各组物质混合后不产生沉淀和气体,能得到无色溶液的是( )
A:氢氧化钡溶液和稀硫酸
B:氧化铜和稀盐酸
C:大理石和稀盐酸
D:石灰水和稀盐酸
7、填空 氢氧化钠又名苛性钠,这是因为它有强烈的_________。氢氧化钠必须密封保存,是因为它能吸收空气中的_____,并能跟空气中的_____________起反应。腐蚀性水分二氧化碳2NaOH+ CO2=== Na2CO3 + H2O5、下列物质与稀硫酸反应不能产生氢气的是( )
A: 镁 B:银 C:铁 D:铝B 根据金属活动性顺序表知道: 镁>铝>铁>(氢)>银
银排在氢之后,所以它不能和稀硫酸反应.提示:酸→H++酸根离子 8、“物质的组成与结构决定物质的性质”是化学学科中的重要观点。按照这一观点讨论:
酸溶液具有一些共同的化学性质,是因为酸溶液中都含有 ;碱溶液也具有一些共同的化学性质,是因为碱溶液中都含有 。练习碱→金属离子+OH-H+OH-鱼胆弄破后会使鱼肉粘上难溶解于水的胆汁酸(一种酸)而变苦,要减少这种苦味,用来洗涤的最佳物质是( )。
A、水 B、食盐
C、纯碱 D、食醋C生活知多D 计算题
Na2CO3和Na2SO4的混合物12.4克与100克稀硫酸恰好完全反应,产生2.2克气体。求:
(1)原混合物中硫酸钠的质量分数?
(2)反应后溶液中硫酸钠的质量分数?
取NaOH溶液适量于小烧杯中,滴入几滴酚酞试液,然后再向该溶液中逐滴滴入稀HCl。溶液先由无色变红,再由红变无色。氢氧化钠溶液能与稀盐酸反应。动动脑一定条件下,同一化学反应进行的快慢与反应物的质量分数成正比。现用100克溶液质质量分数为30%的盐酸溶液与过量的锌粉反应,为了使反应慢点进行而又不生成氢气的总量,可向所用的盐酸中加入适量的( )。
A、氢氧化钠 B、水
C、氧化镁 D、碳酸钙练习B 现有白纸和几种溶液,有人用这些材料设计了一个名为“雨落叶出红花开”的趣味实验。实验的过程如下:先用洁净的毛笔蘸 (填序号,下同)在白纸上画上花,再用 画上叶,将白纸挂上墙壁,晾干后用 向纸上喷即成。
A、酚酞试液 B、石蕊试液
C、氢氧化钠溶液 D、稀盐酸练习用锌粒和盐酸反应制取的氢气中,常混有水蒸气和氯化氢气体,为了除去气体杂质,可使混合气体通过右图A、B两装置,气体通过两瓶的导管顺序正确的是( ) A、abcd B、dcba C、cdab D、bacd a b c d浓硫酸NaOH溶液练习CA B下列四种物质中,能和其他三种物质反应的是( )。
A、盐酸 B、锌
C、铁锈 D、氢氧化铜练习A下列四种物质中,能和其他三种物质反应的是( )。
A、盐酸 B、二氧化碳
C、硫酸铜 D、氢氧化钠练习D稀盐酸NaOH溶液紫色石蕊稀盐酸NaOH溶液无色酚酞一、稀盐酸、稀硫酸的化学性质:1、酸 + 指示剂 pH试纸:0——7——14
酸红—中黄—碱蓝金属活动性顺序表(强到弱)K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au思考题 煤是重要的化工原料,用煤做燃料,不仅是极大的浪费,而且因燃煤中含有硫的化合物燃烧时生成SO2气体造成环境污染。
假设一个有30万户居民的中等城市,每户每天烧煤5千克,这种煤中含硫的90%转化为SO2,则该城市每年排放到空气中的SO2的质量约为2.6吨。
试分析:我们可以采取哪些措施以减少SO2对空气的污染?
