2024沪教版化学九年级下学期课时练--第2节 溶液组成的表示
文档属性
| 名称 | 2024沪教版化学九年级下学期课时练--第2节 溶液组成的表示 |  | |
| 格式 | docx | ||
| 文件大小 | 1.1MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-11-29 17:06:41 | ||
图片预览



文档简介
中小学教育资源及组卷应用平台
2024沪教版化学九年级下学期
第6章 溶解现象
第2节 溶液组成的表示
基础过关全练
知识点1 溶液的组成
1.(2023云南中考)下列溶液中,溶质不是固体的是 ( )
A.食盐溶液 B.硝酸钾溶液
C.酒精溶液 D.蔗糖溶液
2.(2023河北唐山路北期末)澄清石灰水中的溶质是( )
A.碳酸钙 B.水
C.氧化钙 D.氢氧化钙
3.将下列溶液中溶质的化学式填在相应的横线上。
(1)稀硫酸 ;
(2)食盐水 ;
(3)稀盐酸 ;
(4)锌和盐酸恰好完全反应后的溶液 ;
(5)硝酸钾溶液 ;
(6)白磷的二硫化碳溶液 。
知识点2 溶液浓度的表示
4.(2023辽宁沈阳一模)某医院要配制200 g 8%的CuSO4溶液检验糖尿病患者的尿液,需要硫酸铜的质量为(C9206002) ( )
A.184 g B.16 g C.20 g D.25 g
5.(2023河北滦州期末)按下列方法配制的溶液,其溶质质量分数为5%的是(水的密度为1 g/mL) ( )
A.称取5.0 g氯化钾,溶解在95 mL水中,充分搅拌
B.量取5.0 mL浓盐酸,倒入95 mL水中,充分搅拌
C.称取5.0 g碳酸钙,放入95 mL水中,充分搅拌
D.量取5.0 mL浓硫酸,倒入95 mL水中,充分搅拌
6.【教材变式·P15 T7】某同学在整理实验室时发现一瓶浓盐酸,标签如图。根据标签填空:
(1)该浓盐酸的溶质是 。
(2)这瓶浓盐酸的质量为 g。
(3)现要配制3 700 g溶质质量分数为10%的稀盐酸,需要这种浓盐酸的质量为 g,需加水的质量为 g。
7.【守恒法解题】(2023陕西中考A卷)学习小组同学利用下图实验,回收实验室废弃的铜粉与铁粉混合物中的铜粉。
请完成下列分析及计算:
(1)反应生成氢气的质量是 g。
(2)计算上述实验回收铜粉的质量。(忽略回收过程中铜粉的损失)
(3)上述实验所用稀硫酸的溶质质量分数 (填“可能”或“不可能”)是15%。
知识点3 配制一定溶质质量分数的溶液
8.(2023江苏苏州中考)在配制50 g溶质质量分数为2%的Na2CO3溶液的实验中,一定不需要用到的仪器是 ( )
A.漏斗 B.玻璃棒
C.50 mL量筒 D.烧杯
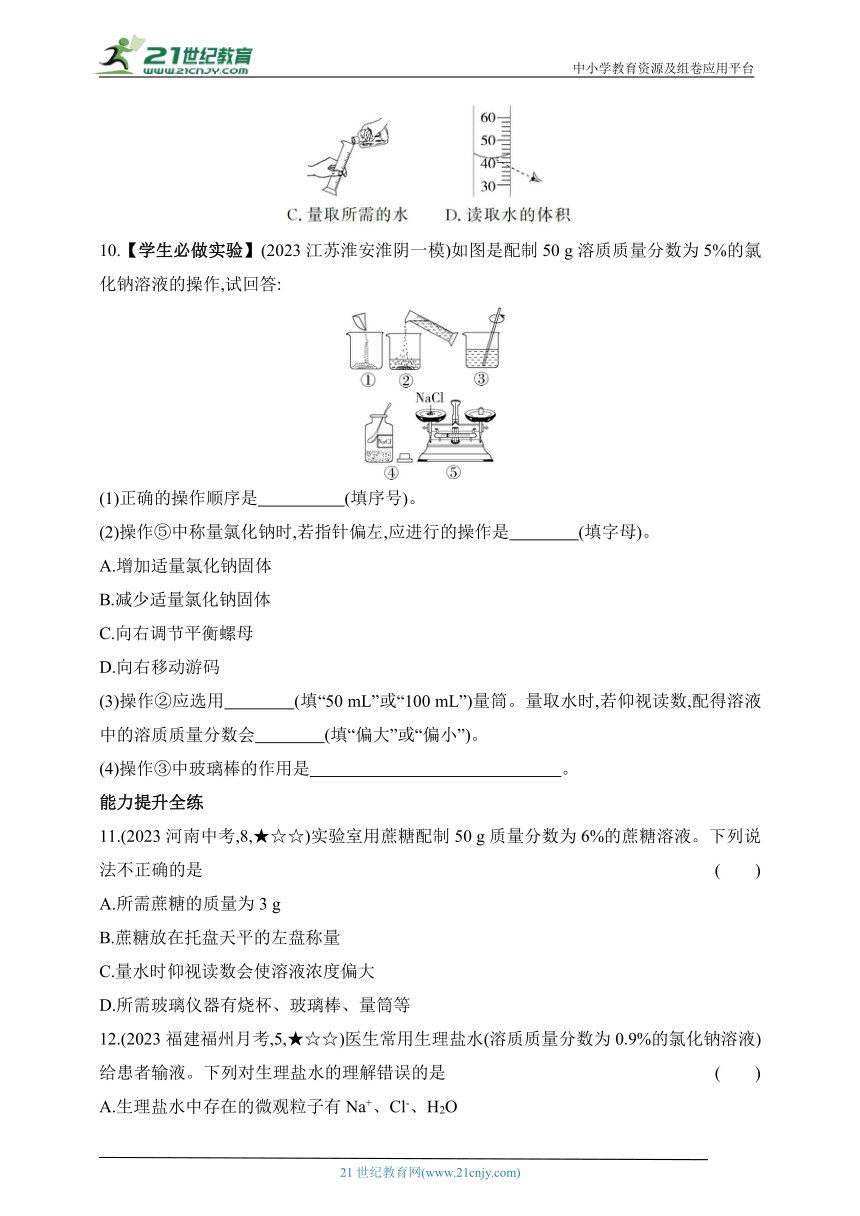
9.(2023安徽中考)为制作叶脉书签,某同学在实验室配制10%的NaOH溶液,部分操作如下,其中正确的是 ( )
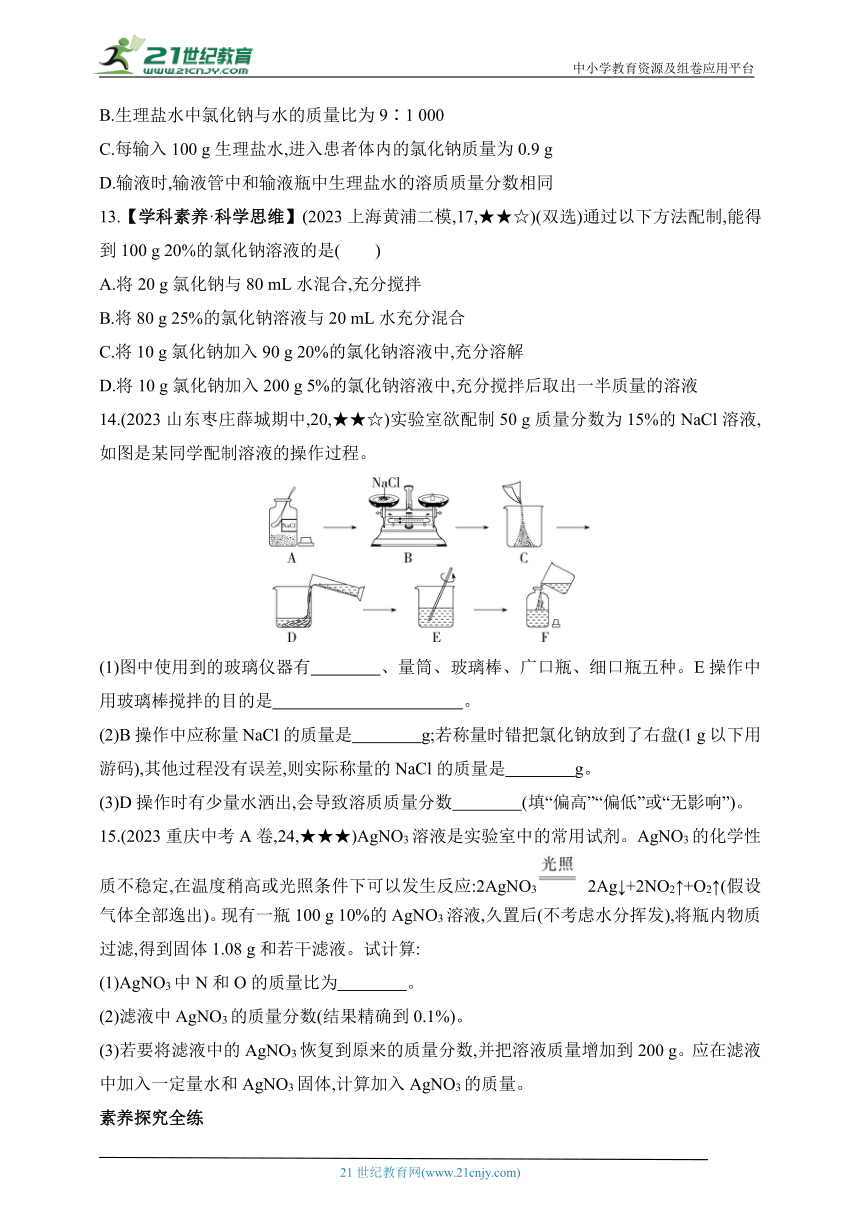
10.【学生必做实验】(2023江苏淮安淮阴一模)如图是配制50 g溶质质量分数为5%的氯化钠溶液的操作,试回答:
(1)正确的操作顺序是 (填序号)。
(2)操作⑤中称量氯化钠时,若指针偏左,应进行的操作是 (填字母)。
A.增加适量氯化钠固体
B.减少适量氯化钠固体
C.向右调节平衡螺母
D.向右移动游码
(3)操作②应选用 (填“50 mL”或“100 mL”)量筒。量取水时,若仰视读数,配得溶液中的溶质质量分数会 (填“偏大”或“偏小”)。
(4)操作③中玻璃棒的作用是 。
能力提升全练
11.(2023河南中考,8,★☆☆)实验室用蔗糖配制50 g质量分数为6%的蔗糖溶液。下列说法不正确的是 ( )
A.所需蔗糖的质量为3 g
B.蔗糖放在托盘天平的左盘称量
C.量水时仰视读数会使溶液浓度偏大
D.所需玻璃仪器有烧杯、玻璃棒、量筒等
12.(2023福建福州月考,5,★☆☆)医生常用生理盐水(溶质质量分数为0.9%的氯化钠溶液)给患者输液。下列对生理盐水的理解错误的是 ( )
A.生理盐水中存在的微观粒子有Na+、Cl-、H2O
B.生理盐水中氯化钠与水的质量比为9∶1 000
C.每输入100 g生理盐水,进入患者体内的氯化钠质量为0.9 g
D.输液时,输液管中和输液瓶中生理盐水的溶质质量分数相同
13.【学科素养·科学思维】(2023上海黄浦二模,17,★★☆)(双选)通过以下方法配制,能得到100 g 20%的氯化钠溶液的是( )
A.将20 g氯化钠与80 mL水混合,充分搅拌
B.将80 g 25%的氯化钠溶液与20 mL水充分混合
C.将10 g氯化钠加入90 g 20%的氯化钠溶液中,充分溶解
D.将10 g氯化钠加入200 g 5%的氯化钠溶液中,充分搅拌后取出一半质量的溶液
14.(2023山东枣庄薛城期中,20,★★☆)实验室欲配制50 g质量分数为15%的NaCl溶液,如图是某同学配制溶液的操作过程。
(1)图中使用到的玻璃仪器有 、量筒、玻璃棒、广口瓶、细口瓶五种。E操作中用玻璃棒搅拌的目的是 。
(2)B操作中应称量NaCl的质量是 g;若称量时错把氯化钠放到了右盘(1 g以下用游码),其他过程没有误差,则实际称量的NaCl的质量是 g。
(3)D操作时有少量水洒出,会导致溶质质量分数 (填“偏高”“偏低”或“无影响”)。
15.(2023重庆中考A卷,24,★★★)AgNO3溶液是实验室中的常用试剂。AgNO3的化学性质不稳定,在温度稍高或光照条件下可以发生反应:2AgNO3 2Ag↓+2NO2↑+O2↑(假设气体全部逸出)。现有一瓶100 g 10%的AgNO3溶液,久置后(不考虑水分挥发),将瓶内物质过滤,得到固体1.08 g和若干滤液。试计算:
(1)AgNO3中N和O的质量比为 。
(2)滤液中AgNO3的质量分数(结果精确到0.1%)。
(3)若要将滤液中的AgNO3恢复到原来的质量分数,并把溶液质量增加到200 g。应在滤液中加入一定量水和AgNO3固体,计算加入AgNO3的质量。
素养探究全练
16.【学科素养·科学思维】(2023福建石狮一模)某活动小组的同学以“我帮稻农选好种”为主题,开展如下学习活动。已知:20 ℃时,盐水的密度与溶质质量分数的对照表如下:
密度/(g/cm3) 1.0 1.03 1.07 1.09 1.10 1.12 1.13
溶质质量分数/% 2 4 8 12 14 16 18
(1)选种:水稻选种所用的盐水密度为1.10 g/cm3,选种时将稻种加入配好的盐水中,静置一段时间后,用漏勺捞去浮于上层的劣种。
①由表中信息可知,盐水的密度与溶质质量分数的关系是
。水稻选种时,需配制的盐水的溶质质量分数是 。
②漏勺孔径的大小 (填“大于”或“小于”)劣种的直径。
(2)浸种:选好的稻种置于4%的盐水中浸泡30分钟左右,可防细菌性病害。若要将50 g 14%的盐水稀释成4%的浸种盐水,需加水 g。
答案全解全析
基础过关全练
1.C 酒精溶液是酒精的水溶液,酒精是溶质,是液体。故选C。
2.D 石灰水是氢氧化钙溶于水形成的溶液,其溶质为氢氧化钙。
3.(1)H2SO4 (2)NaCl (3)HCl (4)ZnCl2
(5)KNO3 (6)P
解析 (1)稀硫酸中溶质是H2SO4,溶剂是水;(2)食盐水中溶质是氯化钠,溶剂是水;(3)稀盐酸中溶质是氯化氢气体,溶剂是水;(4)锌和盐酸恰好完全反应生成氯化锌和氢气,氢气逸散到空气中,所以溶液中溶质是氯化锌,溶剂是水;(5)硝酸钾溶液中溶质是硝酸钾,溶剂是水;(6)白磷的二硫化碳溶液中溶质是白磷,溶剂是二硫化碳。
4.B 200 g溶质质量分数为8%的CuSO4溶液中硫酸铜的质量为200 g×8%=16 g。
5.A 5.0 g氯化钾溶解在95 mL(合95 g)水中,溶质质量分数为5 g÷(5 g+95 g)×100%=5%;5.0 mL是浓盐酸的体积,不能得出溶质氯化氢的质量,故不能求得溶质质量分数;碳酸钙不溶于水,不能得到溶液;5.0 mL是浓硫酸的体积,不能得出溶质硫酸的质量,故不能求得溶质质量分数。
6.(1)氯化氢 (2)590 (3)1 000 2 700
解析 (1)氯化氢溶于水形成盐酸,所以该浓盐酸的溶质是氯化氢。(2)浓盐酸的质量为500 mL×1.18 g/mL=590 g。(3)配制3 700 g溶质质量分数为10%的稀盐酸,需要题述浓盐酸的质量为=1 000 g,需加水的质量为3 700 g-1 000 g=2 700 g。
7.(1)0.4
(2)解:设混合物中铁粉的质量为x,消耗硫酸的质量为y。
Fe + H2SO4 FeSO4+H2↑
56 98 2
x y 0.4 g
x=11.2 g
y=19.6 g
混合物中铜粉的质量为30 g-11.2 g=18.8 g
答:实验回收铜粉的质量为18.8 g。
(3)不可能
解析 (1)根据质量守恒定律,反应生成氢气的质量是30 g+100 g-129.6 g=0.4 g。(2)根据生成氢气的质量和化学方程式的计算,可求得参加反应的铁和硫酸的质量,从而求出混合物中铜的质量。(3)实验所用稀硫酸的溶质质量分数至少为×100%=19.6%,所以所用稀硫酸的溶质质量分数不可能是15%。
8.A 托盘天平用于称取碳酸钠、50 mL量筒与胶头滴管用于准确量取水、烧杯用于完成溶解操作、玻璃棒用于溶解时的搅拌,一定不需要用到的仪器是漏斗。
9.C 取用粉末状固体药品时,瓶塞要倒放,A错误;氢氧化钠具有腐蚀性,应放在玻璃器皿中称量,B错误;向量筒中倾倒液体药品时,标签要朝向手心,瓶口紧挨量筒口,C正确;量取液体读数时,视线应与液体凹液面的最低处保持水平,D错误。
10.(1)④⑤①②③ (2)B (3)50 mL 偏小 (4)搅拌,加速溶解
解析 (1)配制溶液的正确步骤是计算→称量→量取→溶解→装瓶,故题图实验的正确操作顺序是④⑤①②③。(2)称量NaCl时指针偏左,说明氯化钠质量偏大,应减少适量氯化钠固体。(3)需要水的质量为
50 g-50 g×5%=47.5 g,需要水的体积为=47.5 mL,因此应选择
50 mL的量筒;量取水时仰视读数,会造成量取液体体积偏大,所配溶液溶质质量分数偏小。(4)在溶解时,玻璃棒的作用是搅拌,加速溶解。
能力提升全练
11.C 所需蔗糖的质量为50 g×6%=3 g,A正确;用托盘天平称量物质的质量时,应遵循“左物右码”的原则,B正确;量取水时仰视读数,量取的水偏多,导致溶液浓度偏小,C错误;配制溶液需要的玻璃仪器有烧杯、玻璃棒、量筒等,D正确。
12.B 生理盐水是溶质质量分数为0.9%的氯化钠溶液,含义是每100份质量的生理盐水中含有0.9份质量的氯化钠,则生理盐水中氯化钠与水的质量比为0.9∶(100-0.9)=9∶991,B错误。
13.AB 将20 g氯化钠与80 mL(合80 g)水混合,充分搅拌,所得溶液中氯化钠的质量分数为×100%=20%;将80 g 25%的氯化钠溶液与20 mL(合20 g)水充分混合,所得溶液中氯化钠的质量分数为×100%=20%;在20%的氯化钠溶液中加入氯化钠并溶解,所得溶液的溶质质量分数超过20%;将10 g氯化钠加入200 g 5%的氯化钠溶液中,所得溶液中氯化钠的质量分数为×100%≈9.5%,因为溶液具有均一性,取出一半质量的溶液,溶质质量分数不变。
14.(1)烧杯 加速溶解 (2)7.5 6.5 (3)偏高
解析 (1)题图中配制溶液过程中使用到的玻璃仪器有烧杯、量筒、玻璃棒、广口瓶、细口瓶五种;E操作是溶解操作,用玻璃棒搅拌的目的是加速溶解。(2)称量NaCl的质量为50 g×15%=7.5 g;若称量时错把氯化钠放到了右盘(1 g以下用游码),则实际称量的NaCl的质量是7 g-0.5 g=6.5 g。(3)D操作时有少量水洒出,导致溶剂质量减少,所以会导致溶质质量分数偏高。
15.(1)7∶24
(2)解:设参加反应的硝酸银的质量为x,生成二氧化氮的质量为y,生成氧气的质量为z。
2AgNO3 2Ag↓+2NO2↑+O2↑
340 216 92 32
x 1.08 g y z
x=1.7 g
y=0.46 g
z=0.16 g
滤液中AgNO3的质量分数为×100%≈8.4%。
答:滤液中AgNO3的质量分数为8.4%。
(3)加入AgNO3的质量为200 g×10%-(100 g×10%-1.7 g)=11.7 g。
答:加入AgNO3的质量为11.7 g。
解析 (1)AgNO3中N和O的质量比为14∶(16×3)=7∶24。(2)根据生成银的质量,由反应的化学方程式计算出参加反应的硝酸银的质量、生成二氧化氮和氧气的质量,进而计算出滤液中AgNO3的质量分数。
素养探究全练
16.(1)①盐水的密度越大,溶质质量分数越大 14% ②小于 (2)125
解析 (1)①根据题表中信息可知,随着盐水密度的增大,溶质质量分数不断增大;由题意与表中信息可知,20 ℃时水稻选种所用的盐水密度为1.10 g/cm3,溶质的质量分数为14%。②根据可用漏勺捞去浮于上层的劣种可知,漏勺孔径的大小小于劣种的直径。(2)设加水的质量为x,根据稀释前后溶质质量不变可得50 g×14%=(50 g+x)×4%,x=125 g,故需加水125 g。
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网(www.21cnjy.com)
2024沪教版化学九年级下学期
第6章 溶解现象
第2节 溶液组成的表示
基础过关全练
知识点1 溶液的组成
1.(2023云南中考)下列溶液中,溶质不是固体的是 ( )
A.食盐溶液 B.硝酸钾溶液
C.酒精溶液 D.蔗糖溶液
2.(2023河北唐山路北期末)澄清石灰水中的溶质是( )
A.碳酸钙 B.水
C.氧化钙 D.氢氧化钙
3.将下列溶液中溶质的化学式填在相应的横线上。
(1)稀硫酸 ;
(2)食盐水 ;
(3)稀盐酸 ;
(4)锌和盐酸恰好完全反应后的溶液 ;
(5)硝酸钾溶液 ;
(6)白磷的二硫化碳溶液 。
知识点2 溶液浓度的表示
4.(2023辽宁沈阳一模)某医院要配制200 g 8%的CuSO4溶液检验糖尿病患者的尿液,需要硫酸铜的质量为(C9206002) ( )
A.184 g B.16 g C.20 g D.25 g
5.(2023河北滦州期末)按下列方法配制的溶液,其溶质质量分数为5%的是(水的密度为1 g/mL) ( )
A.称取5.0 g氯化钾,溶解在95 mL水中,充分搅拌
B.量取5.0 mL浓盐酸,倒入95 mL水中,充分搅拌
C.称取5.0 g碳酸钙,放入95 mL水中,充分搅拌
D.量取5.0 mL浓硫酸,倒入95 mL水中,充分搅拌
6.【教材变式·P15 T7】某同学在整理实验室时发现一瓶浓盐酸,标签如图。根据标签填空:
(1)该浓盐酸的溶质是 。
(2)这瓶浓盐酸的质量为 g。
(3)现要配制3 700 g溶质质量分数为10%的稀盐酸,需要这种浓盐酸的质量为 g,需加水的质量为 g。
7.【守恒法解题】(2023陕西中考A卷)学习小组同学利用下图实验,回收实验室废弃的铜粉与铁粉混合物中的铜粉。
请完成下列分析及计算:
(1)反应生成氢气的质量是 g。
(2)计算上述实验回收铜粉的质量。(忽略回收过程中铜粉的损失)
(3)上述实验所用稀硫酸的溶质质量分数 (填“可能”或“不可能”)是15%。
知识点3 配制一定溶质质量分数的溶液
8.(2023江苏苏州中考)在配制50 g溶质质量分数为2%的Na2CO3溶液的实验中,一定不需要用到的仪器是 ( )
A.漏斗 B.玻璃棒
C.50 mL量筒 D.烧杯
9.(2023安徽中考)为制作叶脉书签,某同学在实验室配制10%的NaOH溶液,部分操作如下,其中正确的是 ( )
10.【学生必做实验】(2023江苏淮安淮阴一模)如图是配制50 g溶质质量分数为5%的氯化钠溶液的操作,试回答:
(1)正确的操作顺序是 (填序号)。
(2)操作⑤中称量氯化钠时,若指针偏左,应进行的操作是 (填字母)。
A.增加适量氯化钠固体
B.减少适量氯化钠固体
C.向右调节平衡螺母
D.向右移动游码
(3)操作②应选用 (填“50 mL”或“100 mL”)量筒。量取水时,若仰视读数,配得溶液中的溶质质量分数会 (填“偏大”或“偏小”)。
(4)操作③中玻璃棒的作用是 。
能力提升全练
11.(2023河南中考,8,★☆☆)实验室用蔗糖配制50 g质量分数为6%的蔗糖溶液。下列说法不正确的是 ( )
A.所需蔗糖的质量为3 g
B.蔗糖放在托盘天平的左盘称量
C.量水时仰视读数会使溶液浓度偏大
D.所需玻璃仪器有烧杯、玻璃棒、量筒等
12.(2023福建福州月考,5,★☆☆)医生常用生理盐水(溶质质量分数为0.9%的氯化钠溶液)给患者输液。下列对生理盐水的理解错误的是 ( )
A.生理盐水中存在的微观粒子有Na+、Cl-、H2O
B.生理盐水中氯化钠与水的质量比为9∶1 000
C.每输入100 g生理盐水,进入患者体内的氯化钠质量为0.9 g
D.输液时,输液管中和输液瓶中生理盐水的溶质质量分数相同
13.【学科素养·科学思维】(2023上海黄浦二模,17,★★☆)(双选)通过以下方法配制,能得到100 g 20%的氯化钠溶液的是( )
A.将20 g氯化钠与80 mL水混合,充分搅拌
B.将80 g 25%的氯化钠溶液与20 mL水充分混合
C.将10 g氯化钠加入90 g 20%的氯化钠溶液中,充分溶解
D.将10 g氯化钠加入200 g 5%的氯化钠溶液中,充分搅拌后取出一半质量的溶液
14.(2023山东枣庄薛城期中,20,★★☆)实验室欲配制50 g质量分数为15%的NaCl溶液,如图是某同学配制溶液的操作过程。
(1)图中使用到的玻璃仪器有 、量筒、玻璃棒、广口瓶、细口瓶五种。E操作中用玻璃棒搅拌的目的是 。
(2)B操作中应称量NaCl的质量是 g;若称量时错把氯化钠放到了右盘(1 g以下用游码),其他过程没有误差,则实际称量的NaCl的质量是 g。
(3)D操作时有少量水洒出,会导致溶质质量分数 (填“偏高”“偏低”或“无影响”)。
15.(2023重庆中考A卷,24,★★★)AgNO3溶液是实验室中的常用试剂。AgNO3的化学性质不稳定,在温度稍高或光照条件下可以发生反应:2AgNO3 2Ag↓+2NO2↑+O2↑(假设气体全部逸出)。现有一瓶100 g 10%的AgNO3溶液,久置后(不考虑水分挥发),将瓶内物质过滤,得到固体1.08 g和若干滤液。试计算:
(1)AgNO3中N和O的质量比为 。
(2)滤液中AgNO3的质量分数(结果精确到0.1%)。
(3)若要将滤液中的AgNO3恢复到原来的质量分数,并把溶液质量增加到200 g。应在滤液中加入一定量水和AgNO3固体,计算加入AgNO3的质量。
素养探究全练
16.【学科素养·科学思维】(2023福建石狮一模)某活动小组的同学以“我帮稻农选好种”为主题,开展如下学习活动。已知:20 ℃时,盐水的密度与溶质质量分数的对照表如下:
密度/(g/cm3) 1.0 1.03 1.07 1.09 1.10 1.12 1.13
溶质质量分数/% 2 4 8 12 14 16 18
(1)选种:水稻选种所用的盐水密度为1.10 g/cm3,选种时将稻种加入配好的盐水中,静置一段时间后,用漏勺捞去浮于上层的劣种。
①由表中信息可知,盐水的密度与溶质质量分数的关系是
。水稻选种时,需配制的盐水的溶质质量分数是 。
②漏勺孔径的大小 (填“大于”或“小于”)劣种的直径。
(2)浸种:选好的稻种置于4%的盐水中浸泡30分钟左右,可防细菌性病害。若要将50 g 14%的盐水稀释成4%的浸种盐水,需加水 g。
答案全解全析
基础过关全练
1.C 酒精溶液是酒精的水溶液,酒精是溶质,是液体。故选C。
2.D 石灰水是氢氧化钙溶于水形成的溶液,其溶质为氢氧化钙。
3.(1)H2SO4 (2)NaCl (3)HCl (4)ZnCl2
(5)KNO3 (6)P
解析 (1)稀硫酸中溶质是H2SO4,溶剂是水;(2)食盐水中溶质是氯化钠,溶剂是水;(3)稀盐酸中溶质是氯化氢气体,溶剂是水;(4)锌和盐酸恰好完全反应生成氯化锌和氢气,氢气逸散到空气中,所以溶液中溶质是氯化锌,溶剂是水;(5)硝酸钾溶液中溶质是硝酸钾,溶剂是水;(6)白磷的二硫化碳溶液中溶质是白磷,溶剂是二硫化碳。
4.B 200 g溶质质量分数为8%的CuSO4溶液中硫酸铜的质量为200 g×8%=16 g。
5.A 5.0 g氯化钾溶解在95 mL(合95 g)水中,溶质质量分数为5 g÷(5 g+95 g)×100%=5%;5.0 mL是浓盐酸的体积,不能得出溶质氯化氢的质量,故不能求得溶质质量分数;碳酸钙不溶于水,不能得到溶液;5.0 mL是浓硫酸的体积,不能得出溶质硫酸的质量,故不能求得溶质质量分数。
6.(1)氯化氢 (2)590 (3)1 000 2 700
解析 (1)氯化氢溶于水形成盐酸,所以该浓盐酸的溶质是氯化氢。(2)浓盐酸的质量为500 mL×1.18 g/mL=590 g。(3)配制3 700 g溶质质量分数为10%的稀盐酸,需要题述浓盐酸的质量为=1 000 g,需加水的质量为3 700 g-1 000 g=2 700 g。
7.(1)0.4
(2)解:设混合物中铁粉的质量为x,消耗硫酸的质量为y。
Fe + H2SO4 FeSO4+H2↑
56 98 2
x y 0.4 g
x=11.2 g
y=19.6 g
混合物中铜粉的质量为30 g-11.2 g=18.8 g
答:实验回收铜粉的质量为18.8 g。
(3)不可能
解析 (1)根据质量守恒定律,反应生成氢气的质量是30 g+100 g-129.6 g=0.4 g。(2)根据生成氢气的质量和化学方程式的计算,可求得参加反应的铁和硫酸的质量,从而求出混合物中铜的质量。(3)实验所用稀硫酸的溶质质量分数至少为×100%=19.6%,所以所用稀硫酸的溶质质量分数不可能是15%。
8.A 托盘天平用于称取碳酸钠、50 mL量筒与胶头滴管用于准确量取水、烧杯用于完成溶解操作、玻璃棒用于溶解时的搅拌,一定不需要用到的仪器是漏斗。
9.C 取用粉末状固体药品时,瓶塞要倒放,A错误;氢氧化钠具有腐蚀性,应放在玻璃器皿中称量,B错误;向量筒中倾倒液体药品时,标签要朝向手心,瓶口紧挨量筒口,C正确;量取液体读数时,视线应与液体凹液面的最低处保持水平,D错误。
10.(1)④⑤①②③ (2)B (3)50 mL 偏小 (4)搅拌,加速溶解
解析 (1)配制溶液的正确步骤是计算→称量→量取→溶解→装瓶,故题图实验的正确操作顺序是④⑤①②③。(2)称量NaCl时指针偏左,说明氯化钠质量偏大,应减少适量氯化钠固体。(3)需要水的质量为
50 g-50 g×5%=47.5 g,需要水的体积为=47.5 mL,因此应选择
50 mL的量筒;量取水时仰视读数,会造成量取液体体积偏大,所配溶液溶质质量分数偏小。(4)在溶解时,玻璃棒的作用是搅拌,加速溶解。
能力提升全练
11.C 所需蔗糖的质量为50 g×6%=3 g,A正确;用托盘天平称量物质的质量时,应遵循“左物右码”的原则,B正确;量取水时仰视读数,量取的水偏多,导致溶液浓度偏小,C错误;配制溶液需要的玻璃仪器有烧杯、玻璃棒、量筒等,D正确。
12.B 生理盐水是溶质质量分数为0.9%的氯化钠溶液,含义是每100份质量的生理盐水中含有0.9份质量的氯化钠,则生理盐水中氯化钠与水的质量比为0.9∶(100-0.9)=9∶991,B错误。
13.AB 将20 g氯化钠与80 mL(合80 g)水混合,充分搅拌,所得溶液中氯化钠的质量分数为×100%=20%;将80 g 25%的氯化钠溶液与20 mL(合20 g)水充分混合,所得溶液中氯化钠的质量分数为×100%=20%;在20%的氯化钠溶液中加入氯化钠并溶解,所得溶液的溶质质量分数超过20%;将10 g氯化钠加入200 g 5%的氯化钠溶液中,所得溶液中氯化钠的质量分数为×100%≈9.5%,因为溶液具有均一性,取出一半质量的溶液,溶质质量分数不变。
14.(1)烧杯 加速溶解 (2)7.5 6.5 (3)偏高
解析 (1)题图中配制溶液过程中使用到的玻璃仪器有烧杯、量筒、玻璃棒、广口瓶、细口瓶五种;E操作是溶解操作,用玻璃棒搅拌的目的是加速溶解。(2)称量NaCl的质量为50 g×15%=7.5 g;若称量时错把氯化钠放到了右盘(1 g以下用游码),则实际称量的NaCl的质量是7 g-0.5 g=6.5 g。(3)D操作时有少量水洒出,导致溶剂质量减少,所以会导致溶质质量分数偏高。
15.(1)7∶24
(2)解:设参加反应的硝酸银的质量为x,生成二氧化氮的质量为y,生成氧气的质量为z。
2AgNO3 2Ag↓+2NO2↑+O2↑
340 216 92 32
x 1.08 g y z
x=1.7 g
y=0.46 g
z=0.16 g
滤液中AgNO3的质量分数为×100%≈8.4%。
答:滤液中AgNO3的质量分数为8.4%。
(3)加入AgNO3的质量为200 g×10%-(100 g×10%-1.7 g)=11.7 g。
答:加入AgNO3的质量为11.7 g。
解析 (1)AgNO3中N和O的质量比为14∶(16×3)=7∶24。(2)根据生成银的质量,由反应的化学方程式计算出参加反应的硝酸银的质量、生成二氧化氮和氧气的质量,进而计算出滤液中AgNO3的质量分数。
素养探究全练
16.(1)①盐水的密度越大,溶质质量分数越大 14% ②小于 (2)125
解析 (1)①根据题表中信息可知,随着盐水密度的增大,溶质质量分数不断增大;由题意与表中信息可知,20 ℃时水稻选种所用的盐水密度为1.10 g/cm3,溶质的质量分数为14%。②根据可用漏勺捞去浮于上层的劣种可知,漏勺孔径的大小小于劣种的直径。(2)设加水的质量为x,根据稀释前后溶质质量不变可得50 g×14%=(50 g+x)×4%,x=125 g,故需加水125 g。
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网(www.21cnjy.com)
