2024沪教版化学九年级下学期课时练--第6章 素养综合检测
文档属性
| 名称 | 2024沪教版化学九年级下学期课时练--第6章 素养综合检测 |

|
|
| 格式 | docx | ||
| 文件大小 | 1.3MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-11-29 00:00:00 | ||
图片预览


文档简介
中小学教育资源及组卷应用平台
2024沪教版化学九年级下学期
第6章·素养综合检测
(满分100分,限时45分钟)
一、选择题(每小题4分,共40分)
1.(2023湖南永州中考)下列溶液中,溶剂不是水的是 ( )
A.稀硫酸 B.生理盐水
C.蔗糖溶液 D.碘的酒精溶液
2.【学科素养·化学观念】(2023四川自贡中考)溶液用途广泛,与人们的生活息息相关。下列说法正确的是 ( )
A.溶液是由溶质和溶剂组成的
B.溶液都是无色透明的液体
C.溶液是具有均一性、稳定性的纯净物
D.饱和溶液一定是浓溶液,不饱和溶液一定是稀溶液
3.【新素材·航空航天】(2023江苏南京期中)王亚平在太空做了油和水“难分难舍”的神奇实验:她用力摇晃装有油和水的瓶子,让油水充分混合、静置,发现油水不分层。下列说法不正确的是 ( )
A.在地面油水混合物会产生分层现象
B.太空中水的化学性质与地面的水不同
C.在不同环境中同一实验现象可能不同
D.在地面向油水混合物中加入洗涤剂会产生乳化现象
4.【教材变式·P16实验】为了探究影响物质溶解性的因素,设计了如图实验:
实验
现象 固体溶解,形成紫红色溶液 固体几乎不溶解 固体溶解,形成紫红色溶液
下列说法错误的是 ( )
A.物质的溶解性受到溶质与溶剂性质的影响
B.②号试管所得液体是乳浊液
C.不同溶质在同一种溶剂中的溶解性不同
D.同种溶质在不同溶剂中的溶解性不同
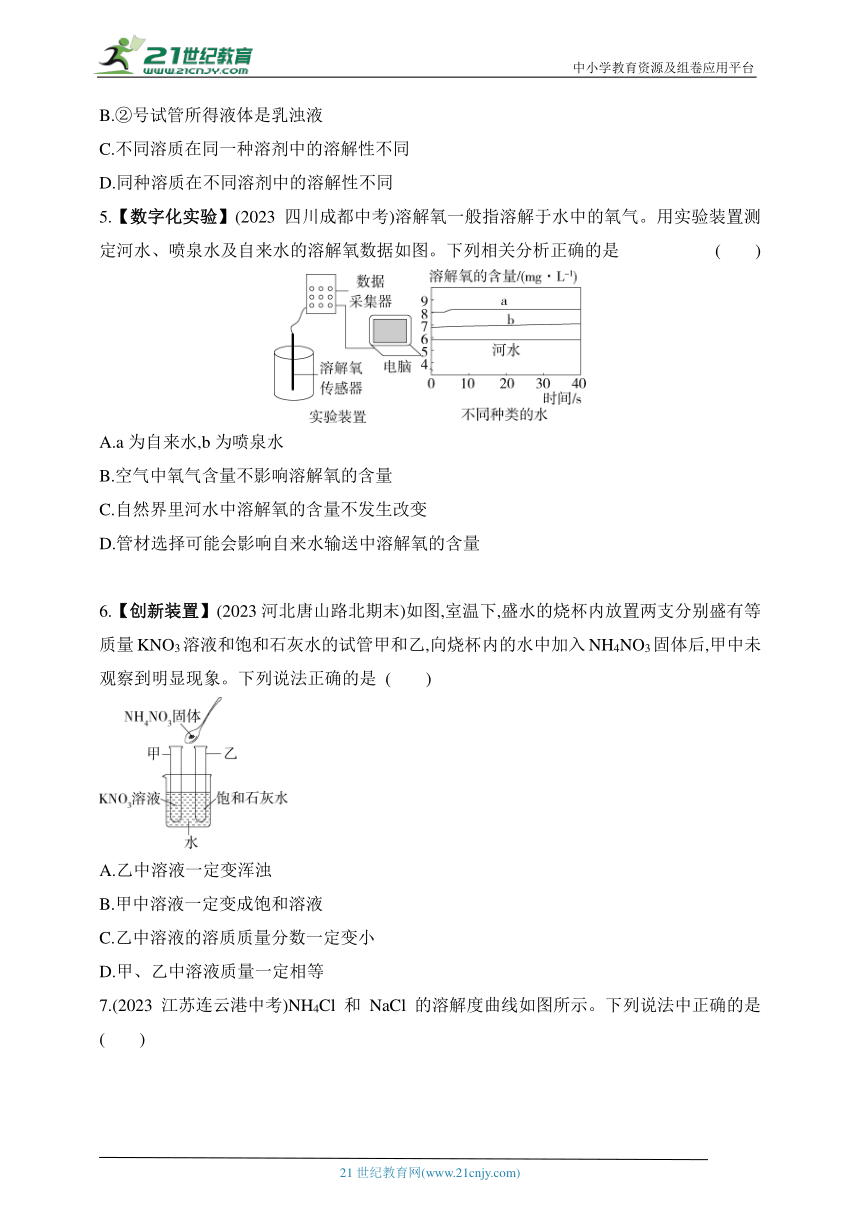
5.【数字化实验】(2023四川成都中考)溶解氧一般指溶解于水中的氧气。用实验装置测定河水、喷泉水及自来水的溶解氧数据如图。下列相关分析正确的是 ( )
A.a为自来水,b为喷泉水
B.空气中氧气含量不影响溶解氧的含量
C.自然界里河水中溶解氧的含量不发生改变
D.管材选择可能会影响自来水输送中溶解氧的含量
6.【创新装置】(2023河北唐山路北期末)如图,室温下,盛水的烧杯内放置两支分别盛有等质量KNO3溶液和饱和石灰水的试管甲和乙,向烧杯内的水中加入NH4NO3固体后,甲中未观察到明显现象。下列说法正确的是 ( )
A.乙中溶液一定变浑浊
B.甲中溶液一定变成饱和溶液
C.乙中溶液的溶质质量分数一定变小
D.甲、乙中溶液质量一定相等
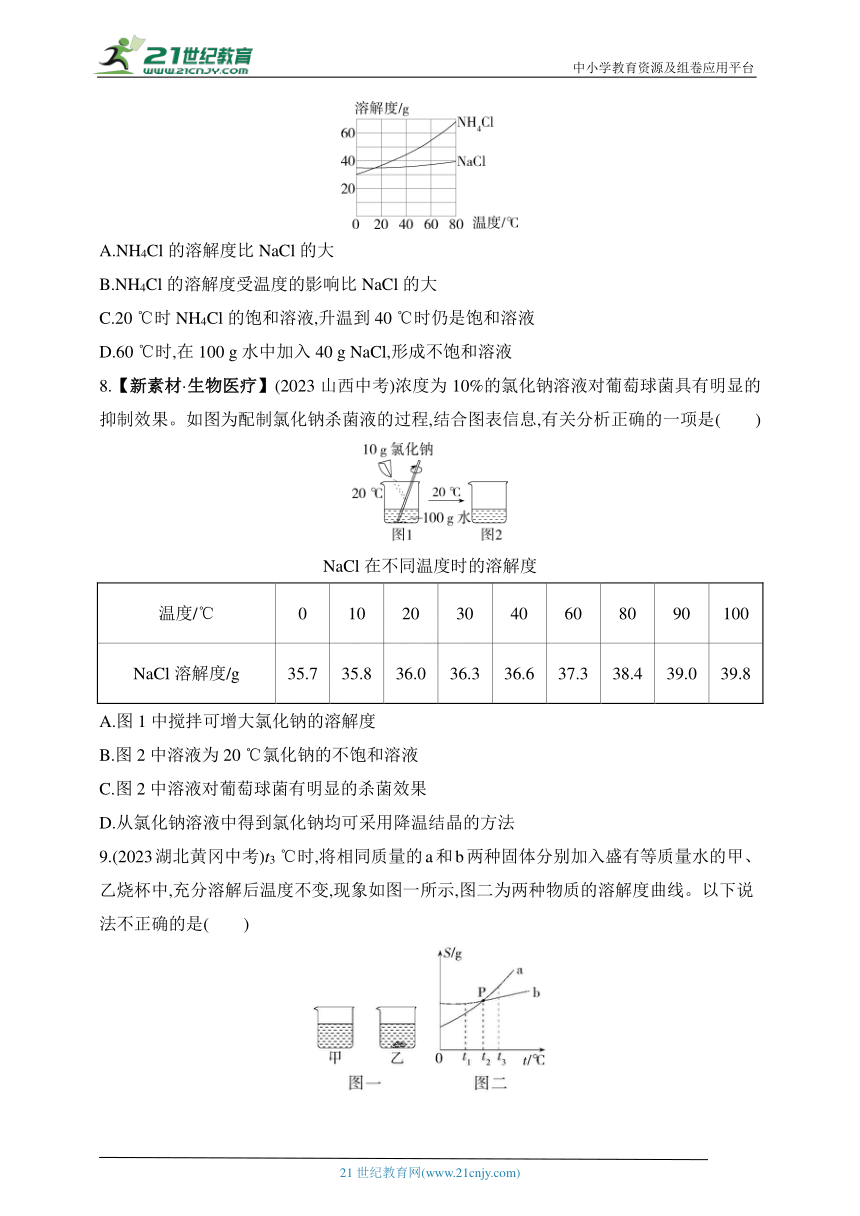
7.(2023江苏连云港中考)NH4Cl和NaCl的溶解度曲线如图所示。下列说法中正确的是 ( )
A.NH4Cl的溶解度比NaCl的大
B.NH4Cl的溶解度受温度的影响比NaCl的大
C.20 ℃时NH4Cl的饱和溶液,升温到40 ℃时仍是饱和溶液
D.60 ℃时,在100 g水中加入40 g NaCl,形成不饱和溶液
8.【新素材·生物医疗】(2023山西中考)浓度为10%的氯化钠溶液对葡萄球菌具有明显的抑制效果。如图为配制氯化钠杀菌液的过程,结合图表信息,有关分析正确的一项是 ( )
NaCl在不同温度时的溶解度
温度/℃ 0 10 20 30 40 60 80 90 100
NaCl溶解度/g 35.7 35.8 36.0 36.3 36.6 37.3 38.4 39.0 39.8
A.图1中搅拌可增大氯化钠的溶解度
B.图2中溶液为20 ℃氯化钠的不饱和溶液
C.图2中溶液对葡萄球菌有明显的杀菌效果
D.从氯化钠溶液中得到氯化钠均可采用降温结晶的方法
9.(2023湖北黄冈中考)t3 ℃时,将相同质量的a和b两种固体分别加入盛有等质量水的甲、乙烧杯中,充分溶解后温度不变,现象如图一所示,图二为两种物质的溶解度曲线。以下说法不正确的是( )
A.乙烧杯中的溶质为b
B.甲烧杯中形成的溶液一定是不饱和溶液
C.若将温度降到t2 ℃,甲、乙两烧杯中溶液的质量相等
D.t1 ℃时,b的溶解度比a的大
10.(2023河南平顶山一模)甲、乙两同学在室温下各取50 g某溶液分别做制晶体实验。甲同学将溶液蒸发掉10 g水后冷却至室温,得到1.2 g晶体(晶体不含结晶水);乙同学将溶液蒸发掉15 g水后冷却至室温,得到2.4 g晶体。若两人实验结果都正确,则原50 g某溶液中溶质的质量分数为( )
A.1.1% B.17.4% C.22.2% D.36.1%
二、填空题(共38分)
11.(6分)碳酸饮料易拉罐拉环若被拉断后,可用A4纸多次对折形成的硬尖角来回摩擦接口凹槽(如图,图中拉环未被拉断),使其爆开。
(1)操作中,用硬尖角能使接口凹槽处受到的压强增大,其原因是 。
(2)为了确定饮料的口味,只需倒出少量品尝。这体现了溶液的
性。
(3)易拉罐打开后,罐内气压突然减小,有大量气泡冒出。这说明气体的溶解度随气压的减小而 (填“变大”或“变小”)。
12.【新素材·革命文化】(2023四川眉山中考节选)(8分)红色经典影片《闪闪的红星》中有一段儿童团员潘冬子给红军送盐的故事。冬子开始把食盐装在竹筒中,打算扮作上山砍柴的人将食盐送给红军。途中发现敌人盘查严格,冬子急中生智跑到河边,把竹筒里的食盐全部溶成盐水,再用棉袄吸收,最终顺利地将食盐送给了红军。
回答下列问题:
(1)从物质分类的角度分析,盐水属于 (填“纯净物”或“混合物”);从物质变化的角度分析,食盐溶成盐水属于 (填“物理变化”或“化学变化”)。
(2)从棉袄中挤出盐水,过滤,蒸发得到食盐。其中用到的玻璃仪器有烧杯、玻璃棒、酒精灯和 。
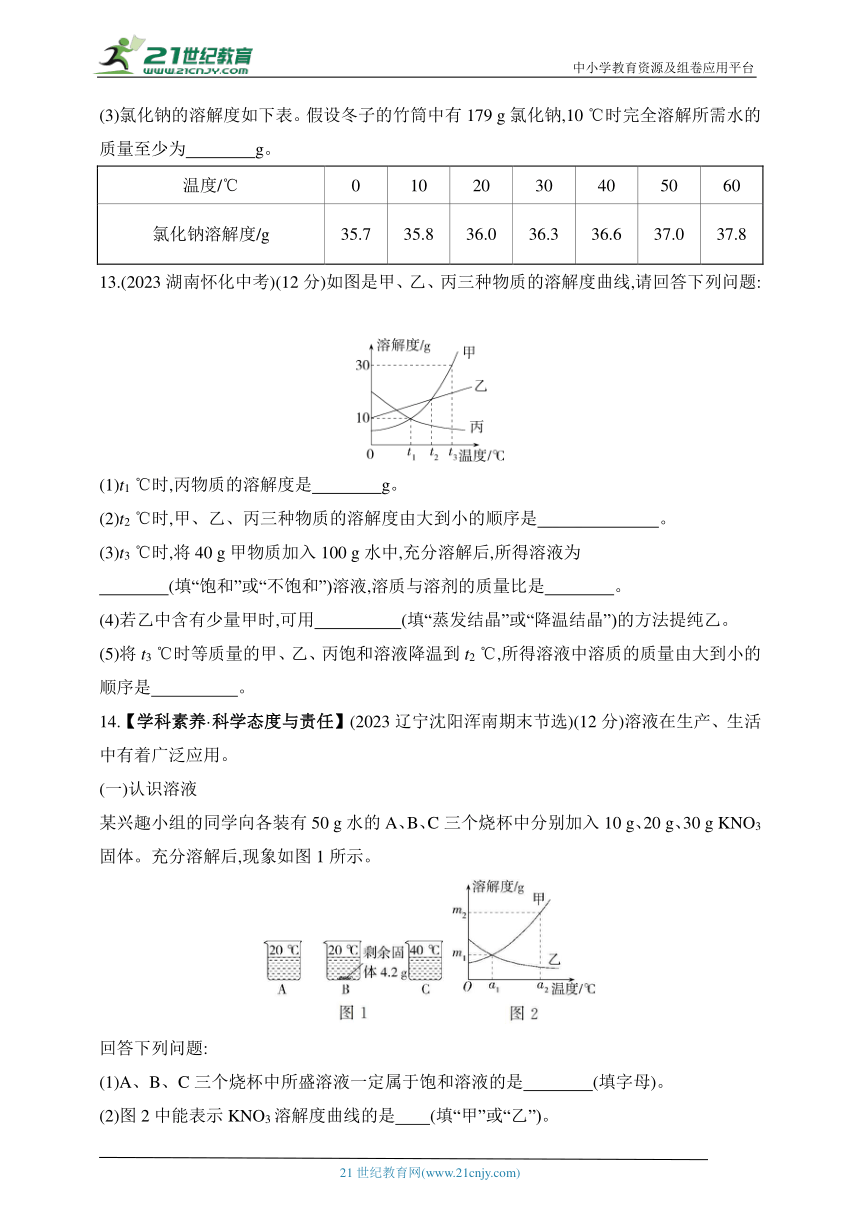
(3)氯化钠的溶解度如下表。假设冬子的竹筒中有179 g氯化钠,10 ℃时完全溶解所需水的质量至少为 g。
温度/℃ 0 10 20 30 40 50 60
氯化钠溶解度/g 35.7 35.8 36.0 36.3 36.6 37.0 37.8
13.(2023湖南怀化中考)(12分)如图是甲、乙、丙三种物质的溶解度曲线,请回答下列问题:
(1)t1 ℃时,丙物质的溶解度是 g。
(2)t2 ℃时,甲、乙、丙三种物质的溶解度由大到小的顺序是 。
(3)t3 ℃时,将40 g甲物质加入100 g水中,充分溶解后,所得溶液为
(填“饱和”或“不饱和”)溶液,溶质与溶剂的质量比是 。
(4)若乙中含有少量甲时,可用 (填“蒸发结晶”或“降温结晶”)的方法提纯乙。
(5)将t3 ℃时等质量的甲、乙、丙饱和溶液降温到t2 ℃,所得溶液中溶质的质量由大到小的顺序是 。
14.【学科素养·科学态度与责任】(2023辽宁沈阳浑南期末节选)(12分)溶液在生产、生活中有着广泛应用。
(一)认识溶液
某兴趣小组的同学向各装有50 g水的A、B、C三个烧杯中分别加入10 g、20 g、30 g KNO3固体。充分溶解后,现象如图1所示。
回答下列问题:
(1)A、B、C三个烧杯中所盛溶液一定属于饱和溶液的是 (填字母)。
(2)图2中能表示KNO3溶解度曲线的是 (填“甲”或“乙”)。
(3)在20 ℃时KNO3的溶解度为 。
(4)20 ℃时,要使B烧杯中剩余固体继续溶解,可采用的方法是 。
(二)物质的分离
利用海水提取粗盐的过程如图所示。
回答下列问题:
(5)将一定质量的海水通过贮水池引入蒸发池中,在引入结晶池之前的蒸发过程中,蒸发池中氯化钠的质量 (填“增大”“不变”或“减小”)。
(6)从海水中提取的粗盐常含有难溶性杂质。欲从粗盐中得到精盐,应进行的实验操作是 。
三、实验探究题(共12分)
15.(2023江苏淮安二模)(12分)某化学兴趣小组的同学做粗盐(含有难溶性杂质)提纯实验,并用所得的精盐配制100 g溶质质量分数为15%的氯化钠溶液。(天平称量时1 g以下使用游码)
【实验一】如图是同学们做粗盐提纯实验的操作示意图。请回答下列问题:
(1)粗盐提纯的操作顺序为 (填字母)、称量精盐、计算产率。
A.①⑤③⑥②④
B.①⑤②③⑥④
C.①②③⑤⑥④
D.①⑤②⑥③④
(2)进行操作④时,当观察到 时,停止加热。
【实验二】用提纯得到的精盐配制100 g溶质质量分数为15%的氯化钠溶液。
(3)用已调平的天平称取氯化钠固体时,发现指针偏右,接下来的操作是 。
(4)经检测,配制好的溶液溶质质量分数偏小,其原因可能是
(填字母)。
A.氯化钠固体不纯
B.称量时将砝码放在左盘,食盐放在右盘(未使用游码)
C.量取水时,俯视读数
D.将氯化钠固体倒入烧杯中时,有少量固体撒出
四、计算题(共10分)
16.【守恒法解题】(2023河北成安一模)(10分)硫酸亚铁是养殖花卉过程中常见的肥料,适合杜鹃、茉莉、栀子花等的养殖。某同学取100 g稀硫酸与足量的废铁屑充分反应制取硫酸亚铁,测得生成氢气0.1 g。
(1)根据化学方程式计算生成硫酸亚铁的质量。
(2)若将上述所得硫酸亚铁溶液稀释成0.1%的溶液作为花肥,计算需要加水的质量。
答案全解全析
1.D 碘的酒精溶液中,溶质是碘,溶剂是酒精。
2.A 溶液不一定都是无色透明的液体,如硫酸铜溶液是蓝色的,B错误;溶液是具有均一性、稳定性的混合物,C错误;溶液是否饱和与溶液的浓稀没有必然联系,饱和溶液不一定是浓溶液,不饱和溶液不一定是稀溶液,D错误。
3.B 在地面上油是不溶于水的,因此在地面油水混合物会产生分层现象,A正确;太空中水的化学性质与地面的水相同,B错误;由题干信息可知,在不同环境中同一实验现象可能不同,C正确;洗涤剂对油污有乳化作用,因此在地面向油水混合物中加入洗涤剂会产生乳化现象,D正确。
4.B ②号试管中的高锰酸钾固体不溶于汽油,以细小固体颗粒的形式分散于汽油中,形成悬浊液,故B错误。
5.D 喷泉水与空气接触最充分,溶解氧的含量最大,因此a为喷泉水,b为自来水,A错误;空气中氧气含量会影响溶解氧的含量,B错误;自然界气温升高时,河水中氧气的溶解度降低,即河水中溶解氧的含量下降,C错误;管材中含有铁时,会与自来水中的溶解氧发生反应,使自来水输送中溶解氧的含量减少,D正确。
6.D 氢氧化钙的溶解度随着温度的升高而减小,硝酸铵溶于水吸热,使温度降低,乙中溶液不会有氢氧化钙析出,溶液的组成不变,溶液的溶质质量分数不变,A、C错误;甲中未观察到明显现象,甲中溶液不一定变成饱和溶液,也可能是不饱和溶液,B错误;甲、乙中溶液的组成均没有发生改变,则甲、乙中溶液质量一定相等,D正确。
7.B 比较氯化铵和氯化钠的溶解度大小需要指明温度,A错误;由溶解度曲线图可知,氯化铵和氯化钠的溶解度均随温度的升高而增大,氯化铵的溶解度受温度的影响变化比氯化钠大,B正确;20 ℃时氯化铵的饱和溶液,升温到40 ℃,氯化铵的溶解度增大,其溶液会变为不饱和溶液,C错误;60 ℃时,氯化钠的溶解度小于40 g,在100 g水中加入40 g氯化钠,固体不能全部溶解,形成的是饱和溶液,D错误。
8.B 搅拌只能加速溶解,不能改变相应温度下物质的溶解度,A错误;根据溶解度表可知,20 ℃时氯化钠的溶解度为36.0 g,即在100 g水中最多能溶解36.0 g NaCl,达到饱和状态,图2中100 g水里只溶解了10 g NaCl,故未达到饱和状态,B正确;根据题意可知,10%的氯化钠溶液对葡萄球菌有明显的抑制作用,图2中NaCl溶液的溶质质量分数为×100%≈9.1%,故无明显的杀菌效果,C错误;根据溶解度表可知,氯化钠的溶解度受温度变化影响不大,故从氯化钠溶液中得到氯化钠固体应采用的方法是蒸发结晶,D错误。
9.B t3 ℃时,a物质的溶解度大于b物质的溶解度,将相同质量的a和b两种固体分别加入盛有等质量水的甲、乙烧杯中,乙烧杯中有固体未溶解,则乙烧杯中的溶质为b,A正确;甲烧杯中的溶液可能是不饱和溶液,也可能是恰好饱和的溶液,B错误;温度降低至t2 ℃时,a、b物质的溶解度相等,且甲、乙烧杯中水的质量相等,则两烧杯中溶液的质量相等,C正确;根据题图二可知,t1 ℃时,b的溶解度大于a的溶解度,D正确。
10.B 根据题意可知,可以将乙同学蒸发的过程表示为:50 g溶液 析出1.2 g晶体 析出1.2 g晶体,说明原溶液若蒸发掉5 g水,则剩余的45 g溶液应为恰好饱和的溶液,由图示可知,1.2 g溶质溶解在5 g水中恰好达到饱和形成6.2 g溶液,则设45 g饱和溶液中溶质的质量为x,则
x=≈8.7 g
则原溶液中溶质的质量分数约为×100%=17.4%。
11.(1)通过做功,使接口凹槽处温度升高,罐内气压增大,罐内气体对接口凹槽处压力增大,压强增大 (2)均一 (3)变小
解析 (2)溶液具有均一性,倒出的少量饮料与整罐饮料的口味是一致的。(3)易拉罐打开后,罐内气压突然减小,有大量气泡冒出,这说明气体的溶解度随气压的减小而变小。
12.(1)混合物 物理变化 (2)漏斗 (3)500
解析 (1)盐水中含有氯化钠、水,属于混合物;食盐溶成盐水,没有新物质生成,属于物理变化。(2)过滤操作需要用到的玻璃仪器有烧杯、玻璃棒、漏斗;蒸发操作需要用到的玻璃仪器有玻璃棒和酒精灯。(3)由题表可知,10 ℃时氯化钠的溶解度为35.8 g,若冬子的竹筒中有179 g氯化钠,10 ℃时完全溶解所需水的质量至少为100 g×=500 g。
13.(1)10 (2)甲=乙>丙 (3)饱和 3∶10 (4)蒸发结晶 (5)乙>甲>丙
解析 (3)t3 ℃时,甲物质的溶解度是30 g,即t3 ℃时100 g水中溶解30 g甲物质达到饱和状态,将40 g甲物质加入100 g水中,充分溶解后,所得溶液为饱和溶液,溶质与溶剂的质量比是3∶10。(4)乙物质的溶解度受温度变化影响较小,甲物质的溶解度受温度变化影响较大,若乙中含有少量的甲,可用蒸发结晶的方法提纯乙。(5)t3 ℃时,溶解度:甲>乙>丙,故等质量的甲、乙、丙饱和溶液中,溶质质量:甲>乙>丙,溶剂质量:丙>乙>甲。将t3 ℃等质量的甲、乙、丙饱和溶液降温到t2 ℃,甲、乙的溶解度减小,且在t2 ℃时甲、乙的溶解度相等,故甲、乙溶液仍为饱和溶液,且溶质质量分数相等,但溶剂质量:乙>甲,故溶质质量:乙>甲;丙的溶解度增大,溶液组成不变,因为甲、乙在t2 ℃时的溶解度大于丙在t3 ℃时的溶解度,故溶质质量:乙>甲>丙。
14.(1)B (2)甲 (3)31.6 g (4)加水 (5)不变 (6)溶解、过滤、蒸发结晶
解析 (1)B烧杯所盛溶液中有未溶解的固体,则其一定属于饱和溶液。(2)根据题图1,可确定硝酸钾的溶解度随温度的升高而增大,故题图2中表示KNO3溶解度曲线的是甲。(3)20 ℃时,50 g水中最多溶解的硝酸钾的质量为20 g-4.2 g=15.8 g,则100 g水中最多溶解硝酸钾31.6 g,所以20 ℃时KNO3的溶解度为31.6 g。(4)20 ℃时,要使B烧杯中剩余固体继续溶解,可采用的方法是加水。(5)蒸发过程中,蒸发池中水的质量减少,氯化钠的质量不变。
15.(1)B (2)蒸发皿中出现较多固体 (3)继续向左盘添加氯化钠,直至天平平衡 (4)AD
解析 (1)粗盐提纯的实验步骤为:溶解(用托盘天平称取适量粗盐,倒入烧杯中,量取适量水,倒入烧杯中进行溶解)、过滤、蒸发,所以顺序为①⑤②③⑥④。(2)操作④为蒸发,蒸发时,当观察到蒸发皿中出现较多固体时,停止加热,利用余热将剩余滤液蒸干。(3)用已调平的天平称取氯化钠固体时,发现指针偏右,说明氯化钠质量偏小,则应继续向左盘添加氯化钠,直至天平平衡。(4)氯化钠固体不纯,导致溶质质量偏小,溶质质量分数偏小;称量时将砝码放在左盘,食盐放在右盘,称量过程中没有用到游码,不影响称取的溶质质量,溶质质量分数不受影响;量取水时,俯视读数,会导致量取水的体积偏小,溶质质量分数偏大;将氯化钠固体倒入烧杯中时有少量固体撒出,会导致溶质质量偏小,溶质质量分数偏小。故选AD。
16.(1)解:设生成硫酸亚铁的质量为x,参与反应的铁的质量为y。
Fe+H2SO4 FeSO4+H2↑
56 152 2
y x 0.1 g
,x=7.6 g
,y=2.8 g
答:生成硫酸亚铁的质量为7.6 g。
(2)反应后得到的硫酸亚铁溶液的质量为2.8 g+100 g-0.1 g=102.7 g,
解:设将所得的硫酸亚铁溶液稀释成0.1%的溶液需要加水的质量为z。
7.6 g=(102.7 g+z)×0.1%
z=7 497.3 g
答:需要加水的质量为7 497.3 g。
解析 (1)根据氢气的质量与化学方程式可求得参加反应的铁和生成硫酸亚铁的质量。(2)根据稀释前后溶质的质量不变可求得加水的质量。
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网(www.21cnjy.com)
2024沪教版化学九年级下学期
第6章·素养综合检测
(满分100分,限时45分钟)
一、选择题(每小题4分,共40分)
1.(2023湖南永州中考)下列溶液中,溶剂不是水的是 ( )
A.稀硫酸 B.生理盐水
C.蔗糖溶液 D.碘的酒精溶液
2.【学科素养·化学观念】(2023四川自贡中考)溶液用途广泛,与人们的生活息息相关。下列说法正确的是 ( )
A.溶液是由溶质和溶剂组成的
B.溶液都是无色透明的液体
C.溶液是具有均一性、稳定性的纯净物
D.饱和溶液一定是浓溶液,不饱和溶液一定是稀溶液
3.【新素材·航空航天】(2023江苏南京期中)王亚平在太空做了油和水“难分难舍”的神奇实验:她用力摇晃装有油和水的瓶子,让油水充分混合、静置,发现油水不分层。下列说法不正确的是 ( )
A.在地面油水混合物会产生分层现象
B.太空中水的化学性质与地面的水不同
C.在不同环境中同一实验现象可能不同
D.在地面向油水混合物中加入洗涤剂会产生乳化现象
4.【教材变式·P16实验】为了探究影响物质溶解性的因素,设计了如图实验:
实验
现象 固体溶解,形成紫红色溶液 固体几乎不溶解 固体溶解,形成紫红色溶液
下列说法错误的是 ( )
A.物质的溶解性受到溶质与溶剂性质的影响
B.②号试管所得液体是乳浊液
C.不同溶质在同一种溶剂中的溶解性不同
D.同种溶质在不同溶剂中的溶解性不同
5.【数字化实验】(2023四川成都中考)溶解氧一般指溶解于水中的氧气。用实验装置测定河水、喷泉水及自来水的溶解氧数据如图。下列相关分析正确的是 ( )
A.a为自来水,b为喷泉水
B.空气中氧气含量不影响溶解氧的含量
C.自然界里河水中溶解氧的含量不发生改变
D.管材选择可能会影响自来水输送中溶解氧的含量
6.【创新装置】(2023河北唐山路北期末)如图,室温下,盛水的烧杯内放置两支分别盛有等质量KNO3溶液和饱和石灰水的试管甲和乙,向烧杯内的水中加入NH4NO3固体后,甲中未观察到明显现象。下列说法正确的是 ( )
A.乙中溶液一定变浑浊
B.甲中溶液一定变成饱和溶液
C.乙中溶液的溶质质量分数一定变小
D.甲、乙中溶液质量一定相等
7.(2023江苏连云港中考)NH4Cl和NaCl的溶解度曲线如图所示。下列说法中正确的是 ( )
A.NH4Cl的溶解度比NaCl的大
B.NH4Cl的溶解度受温度的影响比NaCl的大
C.20 ℃时NH4Cl的饱和溶液,升温到40 ℃时仍是饱和溶液
D.60 ℃时,在100 g水中加入40 g NaCl,形成不饱和溶液
8.【新素材·生物医疗】(2023山西中考)浓度为10%的氯化钠溶液对葡萄球菌具有明显的抑制效果。如图为配制氯化钠杀菌液的过程,结合图表信息,有关分析正确的一项是 ( )
NaCl在不同温度时的溶解度
温度/℃ 0 10 20 30 40 60 80 90 100
NaCl溶解度/g 35.7 35.8 36.0 36.3 36.6 37.3 38.4 39.0 39.8
A.图1中搅拌可增大氯化钠的溶解度
B.图2中溶液为20 ℃氯化钠的不饱和溶液
C.图2中溶液对葡萄球菌有明显的杀菌效果
D.从氯化钠溶液中得到氯化钠均可采用降温结晶的方法
9.(2023湖北黄冈中考)t3 ℃时,将相同质量的a和b两种固体分别加入盛有等质量水的甲、乙烧杯中,充分溶解后温度不变,现象如图一所示,图二为两种物质的溶解度曲线。以下说法不正确的是( )
A.乙烧杯中的溶质为b
B.甲烧杯中形成的溶液一定是不饱和溶液
C.若将温度降到t2 ℃,甲、乙两烧杯中溶液的质量相等
D.t1 ℃时,b的溶解度比a的大
10.(2023河南平顶山一模)甲、乙两同学在室温下各取50 g某溶液分别做制晶体实验。甲同学将溶液蒸发掉10 g水后冷却至室温,得到1.2 g晶体(晶体不含结晶水);乙同学将溶液蒸发掉15 g水后冷却至室温,得到2.4 g晶体。若两人实验结果都正确,则原50 g某溶液中溶质的质量分数为( )
A.1.1% B.17.4% C.22.2% D.36.1%
二、填空题(共38分)
11.(6分)碳酸饮料易拉罐拉环若被拉断后,可用A4纸多次对折形成的硬尖角来回摩擦接口凹槽(如图,图中拉环未被拉断),使其爆开。
(1)操作中,用硬尖角能使接口凹槽处受到的压强增大,其原因是 。
(2)为了确定饮料的口味,只需倒出少量品尝。这体现了溶液的
性。
(3)易拉罐打开后,罐内气压突然减小,有大量气泡冒出。这说明气体的溶解度随气压的减小而 (填“变大”或“变小”)。
12.【新素材·革命文化】(2023四川眉山中考节选)(8分)红色经典影片《闪闪的红星》中有一段儿童团员潘冬子给红军送盐的故事。冬子开始把食盐装在竹筒中,打算扮作上山砍柴的人将食盐送给红军。途中发现敌人盘查严格,冬子急中生智跑到河边,把竹筒里的食盐全部溶成盐水,再用棉袄吸收,最终顺利地将食盐送给了红军。
回答下列问题:
(1)从物质分类的角度分析,盐水属于 (填“纯净物”或“混合物”);从物质变化的角度分析,食盐溶成盐水属于 (填“物理变化”或“化学变化”)。
(2)从棉袄中挤出盐水,过滤,蒸发得到食盐。其中用到的玻璃仪器有烧杯、玻璃棒、酒精灯和 。
(3)氯化钠的溶解度如下表。假设冬子的竹筒中有179 g氯化钠,10 ℃时完全溶解所需水的质量至少为 g。
温度/℃ 0 10 20 30 40 50 60
氯化钠溶解度/g 35.7 35.8 36.0 36.3 36.6 37.0 37.8
13.(2023湖南怀化中考)(12分)如图是甲、乙、丙三种物质的溶解度曲线,请回答下列问题:
(1)t1 ℃时,丙物质的溶解度是 g。
(2)t2 ℃时,甲、乙、丙三种物质的溶解度由大到小的顺序是 。
(3)t3 ℃时,将40 g甲物质加入100 g水中,充分溶解后,所得溶液为
(填“饱和”或“不饱和”)溶液,溶质与溶剂的质量比是 。
(4)若乙中含有少量甲时,可用 (填“蒸发结晶”或“降温结晶”)的方法提纯乙。
(5)将t3 ℃时等质量的甲、乙、丙饱和溶液降温到t2 ℃,所得溶液中溶质的质量由大到小的顺序是 。
14.【学科素养·科学态度与责任】(2023辽宁沈阳浑南期末节选)(12分)溶液在生产、生活中有着广泛应用。
(一)认识溶液
某兴趣小组的同学向各装有50 g水的A、B、C三个烧杯中分别加入10 g、20 g、30 g KNO3固体。充分溶解后,现象如图1所示。
回答下列问题:
(1)A、B、C三个烧杯中所盛溶液一定属于饱和溶液的是 (填字母)。
(2)图2中能表示KNO3溶解度曲线的是 (填“甲”或“乙”)。
(3)在20 ℃时KNO3的溶解度为 。
(4)20 ℃时,要使B烧杯中剩余固体继续溶解,可采用的方法是 。
(二)物质的分离
利用海水提取粗盐的过程如图所示。
回答下列问题:
(5)将一定质量的海水通过贮水池引入蒸发池中,在引入结晶池之前的蒸发过程中,蒸发池中氯化钠的质量 (填“增大”“不变”或“减小”)。
(6)从海水中提取的粗盐常含有难溶性杂质。欲从粗盐中得到精盐,应进行的实验操作是 。
三、实验探究题(共12分)
15.(2023江苏淮安二模)(12分)某化学兴趣小组的同学做粗盐(含有难溶性杂质)提纯实验,并用所得的精盐配制100 g溶质质量分数为15%的氯化钠溶液。(天平称量时1 g以下使用游码)
【实验一】如图是同学们做粗盐提纯实验的操作示意图。请回答下列问题:
(1)粗盐提纯的操作顺序为 (填字母)、称量精盐、计算产率。
A.①⑤③⑥②④
B.①⑤②③⑥④
C.①②③⑤⑥④
D.①⑤②⑥③④
(2)进行操作④时,当观察到 时,停止加热。
【实验二】用提纯得到的精盐配制100 g溶质质量分数为15%的氯化钠溶液。
(3)用已调平的天平称取氯化钠固体时,发现指针偏右,接下来的操作是 。
(4)经检测,配制好的溶液溶质质量分数偏小,其原因可能是
(填字母)。
A.氯化钠固体不纯
B.称量时将砝码放在左盘,食盐放在右盘(未使用游码)
C.量取水时,俯视读数
D.将氯化钠固体倒入烧杯中时,有少量固体撒出
四、计算题(共10分)
16.【守恒法解题】(2023河北成安一模)(10分)硫酸亚铁是养殖花卉过程中常见的肥料,适合杜鹃、茉莉、栀子花等的养殖。某同学取100 g稀硫酸与足量的废铁屑充分反应制取硫酸亚铁,测得生成氢气0.1 g。
(1)根据化学方程式计算生成硫酸亚铁的质量。
(2)若将上述所得硫酸亚铁溶液稀释成0.1%的溶液作为花肥,计算需要加水的质量。
答案全解全析
1.D 碘的酒精溶液中,溶质是碘,溶剂是酒精。
2.A 溶液不一定都是无色透明的液体,如硫酸铜溶液是蓝色的,B错误;溶液是具有均一性、稳定性的混合物,C错误;溶液是否饱和与溶液的浓稀没有必然联系,饱和溶液不一定是浓溶液,不饱和溶液不一定是稀溶液,D错误。
3.B 在地面上油是不溶于水的,因此在地面油水混合物会产生分层现象,A正确;太空中水的化学性质与地面的水相同,B错误;由题干信息可知,在不同环境中同一实验现象可能不同,C正确;洗涤剂对油污有乳化作用,因此在地面向油水混合物中加入洗涤剂会产生乳化现象,D正确。
4.B ②号试管中的高锰酸钾固体不溶于汽油,以细小固体颗粒的形式分散于汽油中,形成悬浊液,故B错误。
5.D 喷泉水与空气接触最充分,溶解氧的含量最大,因此a为喷泉水,b为自来水,A错误;空气中氧气含量会影响溶解氧的含量,B错误;自然界气温升高时,河水中氧气的溶解度降低,即河水中溶解氧的含量下降,C错误;管材中含有铁时,会与自来水中的溶解氧发生反应,使自来水输送中溶解氧的含量减少,D正确。
6.D 氢氧化钙的溶解度随着温度的升高而减小,硝酸铵溶于水吸热,使温度降低,乙中溶液不会有氢氧化钙析出,溶液的组成不变,溶液的溶质质量分数不变,A、C错误;甲中未观察到明显现象,甲中溶液不一定变成饱和溶液,也可能是不饱和溶液,B错误;甲、乙中溶液的组成均没有发生改变,则甲、乙中溶液质量一定相等,D正确。
7.B 比较氯化铵和氯化钠的溶解度大小需要指明温度,A错误;由溶解度曲线图可知,氯化铵和氯化钠的溶解度均随温度的升高而增大,氯化铵的溶解度受温度的影响变化比氯化钠大,B正确;20 ℃时氯化铵的饱和溶液,升温到40 ℃,氯化铵的溶解度增大,其溶液会变为不饱和溶液,C错误;60 ℃时,氯化钠的溶解度小于40 g,在100 g水中加入40 g氯化钠,固体不能全部溶解,形成的是饱和溶液,D错误。
8.B 搅拌只能加速溶解,不能改变相应温度下物质的溶解度,A错误;根据溶解度表可知,20 ℃时氯化钠的溶解度为36.0 g,即在100 g水中最多能溶解36.0 g NaCl,达到饱和状态,图2中100 g水里只溶解了10 g NaCl,故未达到饱和状态,B正确;根据题意可知,10%的氯化钠溶液对葡萄球菌有明显的抑制作用,图2中NaCl溶液的溶质质量分数为×100%≈9.1%,故无明显的杀菌效果,C错误;根据溶解度表可知,氯化钠的溶解度受温度变化影响不大,故从氯化钠溶液中得到氯化钠固体应采用的方法是蒸发结晶,D错误。
9.B t3 ℃时,a物质的溶解度大于b物质的溶解度,将相同质量的a和b两种固体分别加入盛有等质量水的甲、乙烧杯中,乙烧杯中有固体未溶解,则乙烧杯中的溶质为b,A正确;甲烧杯中的溶液可能是不饱和溶液,也可能是恰好饱和的溶液,B错误;温度降低至t2 ℃时,a、b物质的溶解度相等,且甲、乙烧杯中水的质量相等,则两烧杯中溶液的质量相等,C正确;根据题图二可知,t1 ℃时,b的溶解度大于a的溶解度,D正确。
10.B 根据题意可知,可以将乙同学蒸发的过程表示为:50 g溶液 析出1.2 g晶体 析出1.2 g晶体,说明原溶液若蒸发掉5 g水,则剩余的45 g溶液应为恰好饱和的溶液,由图示可知,1.2 g溶质溶解在5 g水中恰好达到饱和形成6.2 g溶液,则设45 g饱和溶液中溶质的质量为x,则
x=≈8.7 g
则原溶液中溶质的质量分数约为×100%=17.4%。
11.(1)通过做功,使接口凹槽处温度升高,罐内气压增大,罐内气体对接口凹槽处压力增大,压强增大 (2)均一 (3)变小
解析 (2)溶液具有均一性,倒出的少量饮料与整罐饮料的口味是一致的。(3)易拉罐打开后,罐内气压突然减小,有大量气泡冒出,这说明气体的溶解度随气压的减小而变小。
12.(1)混合物 物理变化 (2)漏斗 (3)500
解析 (1)盐水中含有氯化钠、水,属于混合物;食盐溶成盐水,没有新物质生成,属于物理变化。(2)过滤操作需要用到的玻璃仪器有烧杯、玻璃棒、漏斗;蒸发操作需要用到的玻璃仪器有玻璃棒和酒精灯。(3)由题表可知,10 ℃时氯化钠的溶解度为35.8 g,若冬子的竹筒中有179 g氯化钠,10 ℃时完全溶解所需水的质量至少为100 g×=500 g。
13.(1)10 (2)甲=乙>丙 (3)饱和 3∶10 (4)蒸发结晶 (5)乙>甲>丙
解析 (3)t3 ℃时,甲物质的溶解度是30 g,即t3 ℃时100 g水中溶解30 g甲物质达到饱和状态,将40 g甲物质加入100 g水中,充分溶解后,所得溶液为饱和溶液,溶质与溶剂的质量比是3∶10。(4)乙物质的溶解度受温度变化影响较小,甲物质的溶解度受温度变化影响较大,若乙中含有少量的甲,可用蒸发结晶的方法提纯乙。(5)t3 ℃时,溶解度:甲>乙>丙,故等质量的甲、乙、丙饱和溶液中,溶质质量:甲>乙>丙,溶剂质量:丙>乙>甲。将t3 ℃等质量的甲、乙、丙饱和溶液降温到t2 ℃,甲、乙的溶解度减小,且在t2 ℃时甲、乙的溶解度相等,故甲、乙溶液仍为饱和溶液,且溶质质量分数相等,但溶剂质量:乙>甲,故溶质质量:乙>甲;丙的溶解度增大,溶液组成不变,因为甲、乙在t2 ℃时的溶解度大于丙在t3 ℃时的溶解度,故溶质质量:乙>甲>丙。
14.(1)B (2)甲 (3)31.6 g (4)加水 (5)不变 (6)溶解、过滤、蒸发结晶
解析 (1)B烧杯所盛溶液中有未溶解的固体,则其一定属于饱和溶液。(2)根据题图1,可确定硝酸钾的溶解度随温度的升高而增大,故题图2中表示KNO3溶解度曲线的是甲。(3)20 ℃时,50 g水中最多溶解的硝酸钾的质量为20 g-4.2 g=15.8 g,则100 g水中最多溶解硝酸钾31.6 g,所以20 ℃时KNO3的溶解度为31.6 g。(4)20 ℃时,要使B烧杯中剩余固体继续溶解,可采用的方法是加水。(5)蒸发过程中,蒸发池中水的质量减少,氯化钠的质量不变。
15.(1)B (2)蒸发皿中出现较多固体 (3)继续向左盘添加氯化钠,直至天平平衡 (4)AD
解析 (1)粗盐提纯的实验步骤为:溶解(用托盘天平称取适量粗盐,倒入烧杯中,量取适量水,倒入烧杯中进行溶解)、过滤、蒸发,所以顺序为①⑤②③⑥④。(2)操作④为蒸发,蒸发时,当观察到蒸发皿中出现较多固体时,停止加热,利用余热将剩余滤液蒸干。(3)用已调平的天平称取氯化钠固体时,发现指针偏右,说明氯化钠质量偏小,则应继续向左盘添加氯化钠,直至天平平衡。(4)氯化钠固体不纯,导致溶质质量偏小,溶质质量分数偏小;称量时将砝码放在左盘,食盐放在右盘,称量过程中没有用到游码,不影响称取的溶质质量,溶质质量分数不受影响;量取水时,俯视读数,会导致量取水的体积偏小,溶质质量分数偏大;将氯化钠固体倒入烧杯中时有少量固体撒出,会导致溶质质量偏小,溶质质量分数偏小。故选AD。
16.(1)解:设生成硫酸亚铁的质量为x,参与反应的铁的质量为y。
Fe+H2SO4 FeSO4+H2↑
56 152 2
y x 0.1 g
,x=7.6 g
,y=2.8 g
答:生成硫酸亚铁的质量为7.6 g。
(2)反应后得到的硫酸亚铁溶液的质量为2.8 g+100 g-0.1 g=102.7 g,
解:设将所得的硫酸亚铁溶液稀释成0.1%的溶液需要加水的质量为z。
7.6 g=(102.7 g+z)×0.1%
z=7 497.3 g
答:需要加水的质量为7 497.3 g。
解析 (1)根据氢气的质量与化学方程式可求得参加反应的铁和生成硫酸亚铁的质量。(2)根据稀释前后溶质的质量不变可求得加水的质量。
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网(www.21cnjy.com)
