6.2.1 溶液组成的表示课件(共19张PPT) 沪教版(全国) 九年级下册
文档属性
| 名称 | 6.2.1 溶液组成的表示课件(共19张PPT) 沪教版(全国) 九年级下册 |

|
|
| 格式 | ppt | ||
| 文件大小 | 1.0MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-12-26 00:00:00 | ||
图片预览






文档简介
(共19张PPT)
第1课时 溶液的组成
溶液浓度的表示
第2节 物质组成的表示
第六单元 溶解现象
蔗糖溶解
被分散的物质是什么?
分散别的物质的是什么?
形成的混合物叫什么?
一、溶液的组成
一、溶液的组成
1.溶质、溶剂
溶质:被溶解的物质
溶剂:溶解溶质的物质。
请你说出食盐水溶液中的溶质和溶剂
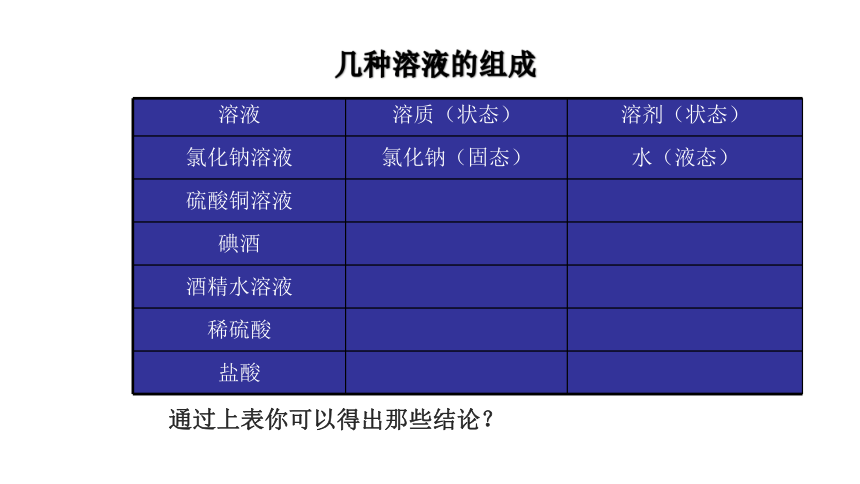
溶液 溶质(状态) 溶剂(状态)
氯化钠溶液 氯化钠(固态) 水(液态)
硫酸铜溶液
碘酒
酒精水溶液
稀硫酸
盐酸
通过上表你可以得出那些结论?
2.注意:
(1)溶质的状态可以固态、液态和气态。
(2)水是常用的溶剂。若溶液中未指明溶剂,一般的溶液都是指水溶液。
(3)当溶液中有水存在时,无论水的量是多少,水就是溶剂。
(4)当两种液体互溶时,一般把量多的物质叫做溶剂。
你知道左图瓶中标签是什么意思吗?
化学纯 500mL
浓盐酸(HCl)
含HCl 37%
密度为1.18 g/cm3
下面我们就来学习溶液组成的表示方法。
二、溶液浓度的表示
从定性上我们知道溶液溶质和溶剂组成的.
溶质
溶剂
溶液质量 = 溶质质量 + 溶剂质量
溶液
你知道它们之间的质量有什么关系?
这两杯氯化钠溶液又有什么不同?
盐加的越多,溶液越咸,此时浓度越大。
溶液的浓与稀是指溶质含量的相对多少,它不能准确的表明一定量的溶液中所含溶质的多少。
怎样确切的表示一定量的溶液中含多少溶质呢?
二、溶液浓度的表示
溶质质量
溶液质量
×100%
溶质的质量分数=
( ω)
=
溶质质量
溶质质量+溶剂质量
×100%
计算:
定义:溶质的质量与溶液的质量之比。
溶质质量
溶液质量
×100%
溶质的质量分数=
食盐 水 食盐水 盐水的溶质质量分数
1克 99克 ?
10克 190克 ?
5克 95克 ?
20克 180克 ?
二、溶液浓度的表示
〖例〗从一瓶氯化钾溶液中取出20 g溶液,蒸干后得到
2.8 g氯化钾固体。试确定这瓶溶液中溶质的质
量分数。
解:这瓶溶液中溶质的质量分数为:
答:这瓶溶液中氯化钾的质量分数为14%。
2.8g
20g
×100%=14%
溶质质量
溶液质量
×100%
溶质的质量分数=
溶质质量 溶剂质量 溶液质量 溶质质量分数
不变 增加
不变 减少
增加 不变
减少 不变
二、溶液浓度的表示
向100 g溶质质量分数为5%的氢氧化钠溶液中:
(1)加入5 g氢氧化钠固体;
(2)加入100 g水;
(3)蒸发50 g水;
(4)取出20 g溶液。
计算以上方法所得溶液中溶质的质量分数。
通过以上的计算,你能得出那些规律?
你有办法解决下列问题吗?
小结:
当一瓶溶液中的溶质或溶剂的质量发生改变时,溶质的质量分数会发生改变;
若溶质和溶剂的质量成比例增加或减少时,质量分数不变。
请你来判断:
1、在100g水中溶解20g食盐,其溶质的质量分数为20 %
2、从质量分数为20%的100gNa2CO3 溶液中取出10g溶液,
则取出的溶液中溶质的质量分数为2%
3、100gCuSO4溶液里含有17gCuSO4,若向其中加入3g无
水CuSO4,使其完全溶解,则溶质的质量分数变为20 %
三、溶质质量分数的计算
我来独立完成
1.可以作为溶质的是( )
A.只有固体 B.只有液体
C.只有气体 D.气、液、固体均可
2.20%的蔗糖溶液中溶质、溶剂、溶液之间的质量比是( )
A. 1∶4∶5 B. 5∶4∶1
C. 4∶1∶5 D. 1∶5∶4
3.在常温下,向100 g5%的氯化钠溶液中加入5 g硝酸钾粉末
完全溶解后,氯化钠的溶质质量分数将 ( )
A.增大 B.减小
C.不变 D.无法确定
D
A
B
4.溶质质量分数是表示 的一种方法,其数
学意义是 之比。现有溶质质量分
数为20%的氯化钠溶液,其20%表示的含义就是每 g
氯化钠溶液中含有氯化钠 g。
5.医疗上的生理盐水是溶质质量分数约为0.9%的氯化钠
溶液,现用1000g生理盐水给某病人输液,则有 克
氯化钠和 克水进入病人体内。
我来独立完成
使一瓶100 g10%的NaOH溶液的溶质质量分数发生改变,你有办法吗?看谁想的办法多?
放飞你想象的翅膀
我来独立完成
第1课时 溶液的组成
溶液浓度的表示
第2节 物质组成的表示
第六单元 溶解现象
蔗糖溶解
被分散的物质是什么?
分散别的物质的是什么?
形成的混合物叫什么?
一、溶液的组成
一、溶液的组成
1.溶质、溶剂
溶质:被溶解的物质
溶剂:溶解溶质的物质。
请你说出食盐水溶液中的溶质和溶剂
溶液 溶质(状态) 溶剂(状态)
氯化钠溶液 氯化钠(固态) 水(液态)
硫酸铜溶液
碘酒
酒精水溶液
稀硫酸
盐酸
通过上表你可以得出那些结论?
2.注意:
(1)溶质的状态可以固态、液态和气态。
(2)水是常用的溶剂。若溶液中未指明溶剂,一般的溶液都是指水溶液。
(3)当溶液中有水存在时,无论水的量是多少,水就是溶剂。
(4)当两种液体互溶时,一般把量多的物质叫做溶剂。
你知道左图瓶中标签是什么意思吗?
化学纯 500mL
浓盐酸(HCl)
含HCl 37%
密度为1.18 g/cm3
下面我们就来学习溶液组成的表示方法。
二、溶液浓度的表示
从定性上我们知道溶液溶质和溶剂组成的.
溶质
溶剂
溶液质量 = 溶质质量 + 溶剂质量
溶液
你知道它们之间的质量有什么关系?
这两杯氯化钠溶液又有什么不同?
盐加的越多,溶液越咸,此时浓度越大。
溶液的浓与稀是指溶质含量的相对多少,它不能准确的表明一定量的溶液中所含溶质的多少。
怎样确切的表示一定量的溶液中含多少溶质呢?
二、溶液浓度的表示
溶质质量
溶液质量
×100%
溶质的质量分数=
( ω)
=
溶质质量
溶质质量+溶剂质量
×100%
计算:
定义:溶质的质量与溶液的质量之比。
溶质质量
溶液质量
×100%
溶质的质量分数=
食盐 水 食盐水 盐水的溶质质量分数
1克 99克 ?
10克 190克 ?
5克 95克 ?
20克 180克 ?
二、溶液浓度的表示
〖例〗从一瓶氯化钾溶液中取出20 g溶液,蒸干后得到
2.8 g氯化钾固体。试确定这瓶溶液中溶质的质
量分数。
解:这瓶溶液中溶质的质量分数为:
答:这瓶溶液中氯化钾的质量分数为14%。
2.8g
20g
×100%=14%
溶质质量
溶液质量
×100%
溶质的质量分数=
溶质质量 溶剂质量 溶液质量 溶质质量分数
不变 增加
不变 减少
增加 不变
减少 不变
二、溶液浓度的表示
向100 g溶质质量分数为5%的氢氧化钠溶液中:
(1)加入5 g氢氧化钠固体;
(2)加入100 g水;
(3)蒸发50 g水;
(4)取出20 g溶液。
计算以上方法所得溶液中溶质的质量分数。
通过以上的计算,你能得出那些规律?
你有办法解决下列问题吗?
小结:
当一瓶溶液中的溶质或溶剂的质量发生改变时,溶质的质量分数会发生改变;
若溶质和溶剂的质量成比例增加或减少时,质量分数不变。
请你来判断:
1、在100g水中溶解20g食盐,其溶质的质量分数为20 %
2、从质量分数为20%的100gNa2CO3 溶液中取出10g溶液,
则取出的溶液中溶质的质量分数为2%
3、100gCuSO4溶液里含有17gCuSO4,若向其中加入3g无
水CuSO4,使其完全溶解,则溶质的质量分数变为20 %
三、溶质质量分数的计算
我来独立完成
1.可以作为溶质的是( )
A.只有固体 B.只有液体
C.只有气体 D.气、液、固体均可
2.20%的蔗糖溶液中溶质、溶剂、溶液之间的质量比是( )
A. 1∶4∶5 B. 5∶4∶1
C. 4∶1∶5 D. 1∶5∶4
3.在常温下,向100 g5%的氯化钠溶液中加入5 g硝酸钾粉末
完全溶解后,氯化钠的溶质质量分数将 ( )
A.增大 B.减小
C.不变 D.无法确定
D
A
B
4.溶质质量分数是表示 的一种方法,其数
学意义是 之比。现有溶质质量分
数为20%的氯化钠溶液,其20%表示的含义就是每 g
氯化钠溶液中含有氯化钠 g。
5.医疗上的生理盐水是溶质质量分数约为0.9%的氯化钠
溶液,现用1000g生理盐水给某病人输液,则有 克
氯化钠和 克水进入病人体内。
我来独立完成
使一瓶100 g10%的NaOH溶液的溶质质量分数发生改变,你有办法吗?看谁想的办法多?
放飞你想象的翅膀
我来独立完成
