6.3 物质的溶解性 课件(共33张PPT)沪教版(全国) 九年级下册
文档属性
| 名称 | 6.3 物质的溶解性 课件(共33张PPT)沪教版(全国) 九年级下册 |

|
|
| 格式 | ppt | ||
| 文件大小 | 2.5MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-12-26 00:00:00 | ||
图片预览











文档简介
(共33张PPT)
第六单元 溶解现象
什么是物质的溶解性?
通常把一种物质(溶质)溶解在另一种物质(溶剂)里的能力叫做溶解性
一、影响物质溶解性的因素
实验探究
实验1:用量筒分别量取5 mL水加入A、B、C 3支试管中,再
分别加入食盐、蔗糖、消石灰各2 g,振荡片刻、静置,
观察物质的溶解情况。
问题:
1、你观察到现象是什么?
2、三种物质溶解性的大小顺序如何?
3、你能得出什么结论?
归纳小结:不同物质在同一溶剂中的溶解性不同
实验2:如图所示,取A、B两支试管,分别滴入少量食用油。
往试管A中加入少量水,往试管B中加入少量汽油,振
荡试管,观察现象。
归纳小结:同一物质在不同溶剂中的溶解能力不同
问题:
1、你观察到什么现象?
2、食用油在水和汽油中溶解能力大?
3、你能得出什么结论?
实验3:取两支试管,分别加入5mL水,将其中 1支试管加热
至沸腾,然后分别加入5g硝酸钾,充分振荡试管,观
察硝酸钾是否完全溶解。
归纳小结:同一溶质在同一溶剂中的溶解能力与温度有关
问题:
1、加热前观察到什么现象?
2、加热后又观察到什么现象?
3、你能得出什么结论?
1 、溶剂的性质
2 、溶质的性质
3 、温度
内部条件
外部条件
影响物质溶解性的因素为
2、下列各因素中不会影响物质溶解性的是( )
A、溶剂的性质 B、溶质的性质
C、溶剂的量 D、温度的变化
1、下列各物质中,在水中溶解性最大的是( )
A、面粉 B 、碳酸钠 C、油脂 D、碳酸钙
B
C
练习
物质能不能无限制地溶解在一定量的水中?
操作
现象
结论: 温度和溶剂一定时,物质溶解有一最大限度
加入5克氯化钠,搅拌
再加入5克氯化钠,搅拌
全部溶解
部分不溶
加入5克硝酸钾,搅拌
再加入5克硝酸钾,搅拌
全部溶解
部分不溶
二、饱和溶液与不饱和溶液
定义
饱和溶液:在一定温度下,在一定量的溶剂里不能再溶解某种
溶质的溶液叫做这种溶质的饱和溶液
不饱和溶液:还能再继续溶解某种溶质的溶液
想一想:
上述概念中的红字应如何把握?
议一议
1 如何判断一种溶液是否饱和
2 饱和溶液和不饱和溶液如何转化
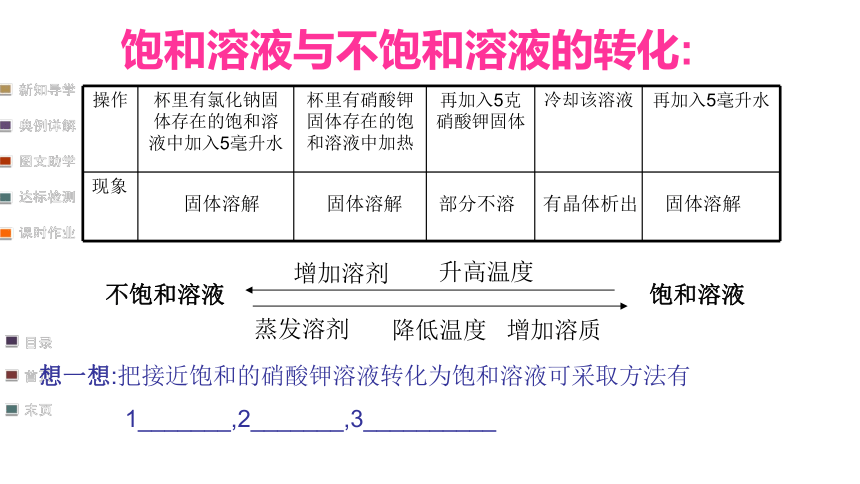
饱和溶液与不饱和溶液的转化:
操作 杯里有氯化钠固体存在的饱和溶液中加入5毫升水 杯里有硝酸钾固体存在的饱和溶液中加热 再加入5克硝酸钾固体 冷却该溶液 再加入5毫升水
现象
降低温度
饱和溶液
增加溶剂
升高温度
蒸发溶剂
增加溶质
不饱和溶液
想一想:把接近饱和的硝酸钾溶液转化为饱和溶液可采取方法有
1_______,2_______,3__________
固体溶解
固体溶解
部分不溶
有晶体析出
固体溶解
讨论:在上面的活动与探究中,用的水都是20 mL,其中溶解氯化钠和硝酸钾的质量是否相同?
在同一条件下,(相同温度,一定量的水),它们在水中溶解的最多量接近相同,但是随着温度的上升,水中溶解的硝酸钾的质量比氯化钠的质量要大得多。
三、溶解度
1、固体溶解度
在 下,某固体物质在 里达到 状态时所溶解的的质量。
一定温度
100g溶剂
饱和
条件:
一定温度
标准:
100g溶剂(一般指水)
状态:
饱和
单位:
克
讨论:20℃时硝酸钾的溶解度为31.6g,这句话的含义
温度
溶质的质量
溶剂的质量
饱和溶液的质量
20 ℃
31.6g
100g
131.6g
其含义是:在20 ℃时,硝酸钾在100克水中达到饱和状态时溶解的质量为31.6克。
或说:在20 ℃时,硝酸钾在100克水中最多能溶解31.6克。
例:判断正误:
1.l00g水中最多溶解38g氯化钠,所以氯化钠在水中的溶解度是38g。( )
2.在10℃时,烧杯内水中最多溶有140g硝酸铵,所以硝酸铵在水中的溶解度是140g。( )
3.在60℃,100g水中溶有75g硝酸钾,所以60℃时硝酸钾的溶解度为75g。( )
4.60℃,100g水中最多溶解124g硝酸钾,所以硝酸钾在这温度下的溶解度是124。( )
×
×
×
×
练习:
1、在20℃时,100g水中溶解36g氯化钠溶液达到饱 和,则20 ℃时氯化钠溶解度是____g。
36
2、在0℃时,100g水中最多可溶解13.3g硝酸钾,则0℃时硝酸钾溶解度是____g。
13.3
3、20℃时硝酸钾的溶解度是31.6g,这句话的含义是什么?将其关系代入下表:
温度 溶质的质量 溶剂的质量 溶液的质量
20℃
31.6g
100g
131.6g
2、溶解度与溶解性的关系
溶解性
溶解度/g (20℃)
易溶
可溶
微溶
难(不)溶
练习:
1、不溶物就是绝对不溶于水的物质。此话是否正确? 2、20℃时碳酸钙的溶解度是0.0013g,所以碳酸钙是___溶物质。 3、20℃时氯化钠的溶解度是36g,则氯化钠属于( )
A.易溶 物质 B.可溶物质 C.微溶物质 D.难溶物质
难
>10g
>1g
<1g
<0.01g
A
.
.
.
0.01g
1g
10g
易溶
可溶
微溶
难(不)溶
.
.
.
.
溶解度/
g
200
100
60
70
50
10
20
30
40
80
90
100
110
180
170
160
150
140
130
120
190
50
10
20
30
40
0
90
60
70
80
温度/℃
.
硝酸钾
.
.
.
.
温度/℃ 0 10 20 30 40 50 60 70 80 90 100
溶解度/g
硝酸钾在不同温度时的溶解度:
13.3
31.6
20.9
45.8
63.9
85.5
110
138
168
202
246
3、溶解度的表示方法:
(1)列表法:
(2)溶解度曲线(如图)
.A
1:曲线上的点表示物质在该点所示温度下的溶解度;两曲线上的交点表示两物质在该点所示温度下的溶解度相同
溶解度(克)
温度(t)
160
150
140
130
120
110
100
90
80
70
60
50
40
30
20
10
200
190
180
170
10
100
90
80
70
60
50
40
30
20
0
硝酸铵
硝酸钾
硝酸钠
氯化铵
氯化钠
硼酸
固体溶解度曲线
2:曲线表示同一种物质在不同温度下的溶解度或溶解度随温度变化的情况
3:曲线上面所表示的溶液为饱和溶液;曲线下面所表示的溶液为不饱和溶液
找一找:50℃时各物质的溶解度
100
硼酸
硝酸铵
硝酸钠
硝酸钾
氯化铵
氯化钾
氯化钠
60
70
50
10
20
30
40
80
90
100
110
180
170
160
150
140
130
120
190
200
50
10
20
30
40
0
90
60
70
80
溶解度/
g
温度/℃
温度/℃
0.05
0.10
0.15
0.20
90
70
40
0
10
20
50
60
80
100
30
溶解度/
g
0.05
0.10
0.15
0.20
90
70
40
0
10
20
50
60
80
100
30
熟石灰的溶解度曲线:
讨论:
固体物质溶解度受温度变化影响情况:
大多数固体物质溶解度随温度升高而增大,例如 硝酸钾等。
少数固体物质溶解度受温度影响不大,例如食盐。
极少数固体物质溶解度随温度升高反而减小,例如熟石灰。
100
硼酸
硝酸 铵
硝酸钠
硝酸钾
氯化铵
氯化钾
氯化钠
60
70
50
10
20
30
40
80
90
100
110
180
170
160
150
140
130
120
190
200
50
10
20
30
40
0
90
60
70
80
溶解度/
g
温度/℃
1、横坐标60,纵坐标110 的交点表示什么意义?
练习:
A.
.
2、比较硝酸钠与硝酸钾的溶解度大小
在68 ℃时,NaNO3与KNO3的溶解度相等
温度大于68 ℃时, KNO3的溶解度大于NaNO3
温度小于68 ℃时,NaNO3的溶解度大于KNO3
100
硼酸
硝酸铵
硝酸钠
硝酸钾
氯化铵
氯化钾
氯化钠
60
70
50
10
20
30
40
80
90
100
110
180
170
160
150
140
130
120
190
200
50
10
20
30
40
0
90
60
70
80
溶解度/
g
温度/℃
68
134g
小于
B.
4、在40℃时,硝酸钾的溶解度____ (填大于、小于)硝酸钠的溶解度。
练习:
3、在___℃时硝酸钾和硝酸钠的溶解度相同,都约为______。
5、在80℃时氯化钠、氯化钾、氯化铵、硼酸的溶解度由大到小的顺序是_______________________________。
氯化铵、氯化钾、氯化钠、硼酸
[讨论1] 天气闷热时,鱼儿为什么总爱在水面上进行呼吸?
(1)打开汽水盖时,汽水会自动喷出来。这说明气体在水中的溶解度与什么有关?
(2)喝了汽水以后,常常会打嗝。这说明气体的溶解度还与什么有关?
气体的溶解度与温度、压强有关,温度越高,溶解度越小;压强越大溶解度越大。
[讨论2]:
2、气体溶解度:
通常讲的气体溶解度是指该气体在压强为101KPa, 一定温度时溶解在1体积水里达到饱和状态时的气体体积。
0 ℃时,氧气的溶解度为0.049的含义是什么?
在0 ℃,氧气压强为101 kPa时,1体积水最多能溶解0. 049体积氧气
想一想:
1标准大气压下,20 ℃时部分气体的溶解度
是一个比值,无单位。
怎样从海水中把氯化钠提取出来呢?
四、结晶
[实验1] 用玻璃棒蘸取少量浓的氯化钠溶液,用酒精灯加热,观察实验现象。
玻璃棒附有白色的食盐晶体
结论:在一定条件下,可以使固体物质从它的水溶液中析出
晶体的过程叫做结晶。
要使晶体从溶液中析出有那些方法呢?
⑴蒸发溶剂法:
适用于溶解度受温度影响较小的的固体溶质,即缓升型的物质。如蒸发海水获得食盐;
如盐场用海水晒盐
把海水引入海滩
使水分蒸发
从而得到食盐
借助日光
和风力
⑵冷却热饱和溶液法:或称降温结晶法。
适用于溶解度受温度影响较大的固体溶质。如冷却热的硝酸钾饱和溶液来获取硝酸钾晶体
硝酸钾的溶解度曲线
1、下列混合物可以用结晶方法分离的是( )
A. 木炭粉和二氧化锰
B. 氯酸钾中含有泥沙
C. 硝酸钾中混有少量食盐
D. 在加热完全分解的高锰酸钾的产物中提取二氧化锰
2、海水晒盐的原理是( )
A.利用阳光和风力,使氯化钠蒸发
B.利用阳光和风力,使水分蒸发
C.利用日晒,使海水分解
D.利用日晒,使氯化钠的溶解度减小
随堂练习:
C
B
3、粗盐的杂质主要是氯化镁(能溶于水)。工业上常把粗盐粉碎后用饱
和食盐水浸洗,再过滤出食盐。对这一过程认识正确的是( )
A .浸洗前后,被浸洗的粗盐中的氯化镁的含量基本不变
B .浸洗前后,食盐水中氯化钠的质量基本不变
C .浸洗后,食盐水中氯化钠的质量分数增大
D .浸洗用的饱和食盐水可以无限次地使用下去
4、某物质结晶后的溶液( )
A.一定是该物质的浓溶液
B.可能是该物质的浓溶液
C.一定是该物质的饱和溶液
D.可能是该物质的饱和溶液,也可能是浓溶液
B
C
5、20℃时, 200gA溶液蒸发掉10g水后析出2g晶体,同样温度下再蒸发
掉10g水时,下列推论正确的是( )
A. 又会析出2g晶体
B. 析出晶体的质量一定大于2g
C.物质A的溶解度变小
D .析出晶体后的溶液的质量分数不变
D
第六单元 溶解现象
什么是物质的溶解性?
通常把一种物质(溶质)溶解在另一种物质(溶剂)里的能力叫做溶解性
一、影响物质溶解性的因素
实验探究
实验1:用量筒分别量取5 mL水加入A、B、C 3支试管中,再
分别加入食盐、蔗糖、消石灰各2 g,振荡片刻、静置,
观察物质的溶解情况。
问题:
1、你观察到现象是什么?
2、三种物质溶解性的大小顺序如何?
3、你能得出什么结论?
归纳小结:不同物质在同一溶剂中的溶解性不同
实验2:如图所示,取A、B两支试管,分别滴入少量食用油。
往试管A中加入少量水,往试管B中加入少量汽油,振
荡试管,观察现象。
归纳小结:同一物质在不同溶剂中的溶解能力不同
问题:
1、你观察到什么现象?
2、食用油在水和汽油中溶解能力大?
3、你能得出什么结论?
实验3:取两支试管,分别加入5mL水,将其中 1支试管加热
至沸腾,然后分别加入5g硝酸钾,充分振荡试管,观
察硝酸钾是否完全溶解。
归纳小结:同一溶质在同一溶剂中的溶解能力与温度有关
问题:
1、加热前观察到什么现象?
2、加热后又观察到什么现象?
3、你能得出什么结论?
1 、溶剂的性质
2 、溶质的性质
3 、温度
内部条件
外部条件
影响物质溶解性的因素为
2、下列各因素中不会影响物质溶解性的是( )
A、溶剂的性质 B、溶质的性质
C、溶剂的量 D、温度的变化
1、下列各物质中,在水中溶解性最大的是( )
A、面粉 B 、碳酸钠 C、油脂 D、碳酸钙
B
C
练习
物质能不能无限制地溶解在一定量的水中?
操作
现象
结论: 温度和溶剂一定时,物质溶解有一最大限度
加入5克氯化钠,搅拌
再加入5克氯化钠,搅拌
全部溶解
部分不溶
加入5克硝酸钾,搅拌
再加入5克硝酸钾,搅拌
全部溶解
部分不溶
二、饱和溶液与不饱和溶液
定义
饱和溶液:在一定温度下,在一定量的溶剂里不能再溶解某种
溶质的溶液叫做这种溶质的饱和溶液
不饱和溶液:还能再继续溶解某种溶质的溶液
想一想:
上述概念中的红字应如何把握?
议一议
1 如何判断一种溶液是否饱和
2 饱和溶液和不饱和溶液如何转化
饱和溶液与不饱和溶液的转化:
操作 杯里有氯化钠固体存在的饱和溶液中加入5毫升水 杯里有硝酸钾固体存在的饱和溶液中加热 再加入5克硝酸钾固体 冷却该溶液 再加入5毫升水
现象
降低温度
饱和溶液
增加溶剂
升高温度
蒸发溶剂
增加溶质
不饱和溶液
想一想:把接近饱和的硝酸钾溶液转化为饱和溶液可采取方法有
1_______,2_______,3__________
固体溶解
固体溶解
部分不溶
有晶体析出
固体溶解
讨论:在上面的活动与探究中,用的水都是20 mL,其中溶解氯化钠和硝酸钾的质量是否相同?
在同一条件下,(相同温度,一定量的水),它们在水中溶解的最多量接近相同,但是随着温度的上升,水中溶解的硝酸钾的质量比氯化钠的质量要大得多。
三、溶解度
1、固体溶解度
在 下,某固体物质在 里达到 状态时所溶解的的质量。
一定温度
100g溶剂
饱和
条件:
一定温度
标准:
100g溶剂(一般指水)
状态:
饱和
单位:
克
讨论:20℃时硝酸钾的溶解度为31.6g,这句话的含义
温度
溶质的质量
溶剂的质量
饱和溶液的质量
20 ℃
31.6g
100g
131.6g
其含义是:在20 ℃时,硝酸钾在100克水中达到饱和状态时溶解的质量为31.6克。
或说:在20 ℃时,硝酸钾在100克水中最多能溶解31.6克。
例:判断正误:
1.l00g水中最多溶解38g氯化钠,所以氯化钠在水中的溶解度是38g。( )
2.在10℃时,烧杯内水中最多溶有140g硝酸铵,所以硝酸铵在水中的溶解度是140g。( )
3.在60℃,100g水中溶有75g硝酸钾,所以60℃时硝酸钾的溶解度为75g。( )
4.60℃,100g水中最多溶解124g硝酸钾,所以硝酸钾在这温度下的溶解度是124。( )
×
×
×
×
练习:
1、在20℃时,100g水中溶解36g氯化钠溶液达到饱 和,则20 ℃时氯化钠溶解度是____g。
36
2、在0℃时,100g水中最多可溶解13.3g硝酸钾,则0℃时硝酸钾溶解度是____g。
13.3
3、20℃时硝酸钾的溶解度是31.6g,这句话的含义是什么?将其关系代入下表:
温度 溶质的质量 溶剂的质量 溶液的质量
20℃
31.6g
100g
131.6g
2、溶解度与溶解性的关系
溶解性
溶解度/g (20℃)
易溶
可溶
微溶
难(不)溶
练习:
1、不溶物就是绝对不溶于水的物质。此话是否正确? 2、20℃时碳酸钙的溶解度是0.0013g,所以碳酸钙是___溶物质。 3、20℃时氯化钠的溶解度是36g,则氯化钠属于( )
A.易溶 物质 B.可溶物质 C.微溶物质 D.难溶物质
难
>10g
>1g
<1g
<0.01g
A
.
.
.
0.01g
1g
10g
易溶
可溶
微溶
难(不)溶
.
.
.
.
溶解度/
g
200
100
60
70
50
10
20
30
40
80
90
100
110
180
170
160
150
140
130
120
190
50
10
20
30
40
0
90
60
70
80
温度/℃
.
硝酸钾
.
.
.
.
温度/℃ 0 10 20 30 40 50 60 70 80 90 100
溶解度/g
硝酸钾在不同温度时的溶解度:
13.3
31.6
20.9
45.8
63.9
85.5
110
138
168
202
246
3、溶解度的表示方法:
(1)列表法:
(2)溶解度曲线(如图)
.A
1:曲线上的点表示物质在该点所示温度下的溶解度;两曲线上的交点表示两物质在该点所示温度下的溶解度相同
溶解度(克)
温度(t)
160
150
140
130
120
110
100
90
80
70
60
50
40
30
20
10
200
190
180
170
10
100
90
80
70
60
50
40
30
20
0
硝酸铵
硝酸钾
硝酸钠
氯化铵
氯化钠
硼酸
固体溶解度曲线
2:曲线表示同一种物质在不同温度下的溶解度或溶解度随温度变化的情况
3:曲线上面所表示的溶液为饱和溶液;曲线下面所表示的溶液为不饱和溶液
找一找:50℃时各物质的溶解度
100
硼酸
硝酸铵
硝酸钠
硝酸钾
氯化铵
氯化钾
氯化钠
60
70
50
10
20
30
40
80
90
100
110
180
170
160
150
140
130
120
190
200
50
10
20
30
40
0
90
60
70
80
溶解度/
g
温度/℃
温度/℃
0.05
0.10
0.15
0.20
90
70
40
0
10
20
50
60
80
100
30
溶解度/
g
0.05
0.10
0.15
0.20
90
70
40
0
10
20
50
60
80
100
30
熟石灰的溶解度曲线:
讨论:
固体物质溶解度受温度变化影响情况:
大多数固体物质溶解度随温度升高而增大,例如 硝酸钾等。
少数固体物质溶解度受温度影响不大,例如食盐。
极少数固体物质溶解度随温度升高反而减小,例如熟石灰。
100
硼酸
硝酸 铵
硝酸钠
硝酸钾
氯化铵
氯化钾
氯化钠
60
70
50
10
20
30
40
80
90
100
110
180
170
160
150
140
130
120
190
200
50
10
20
30
40
0
90
60
70
80
溶解度/
g
温度/℃
1、横坐标60,纵坐标110 的交点表示什么意义?
练习:
A.
.
2、比较硝酸钠与硝酸钾的溶解度大小
在68 ℃时,NaNO3与KNO3的溶解度相等
温度大于68 ℃时, KNO3的溶解度大于NaNO3
温度小于68 ℃时,NaNO3的溶解度大于KNO3
100
硼酸
硝酸铵
硝酸钠
硝酸钾
氯化铵
氯化钾
氯化钠
60
70
50
10
20
30
40
80
90
100
110
180
170
160
150
140
130
120
190
200
50
10
20
30
40
0
90
60
70
80
溶解度/
g
温度/℃
68
134g
小于
B.
4、在40℃时,硝酸钾的溶解度____ (填大于、小于)硝酸钠的溶解度。
练习:
3、在___℃时硝酸钾和硝酸钠的溶解度相同,都约为______。
5、在80℃时氯化钠、氯化钾、氯化铵、硼酸的溶解度由大到小的顺序是_______________________________。
氯化铵、氯化钾、氯化钠、硼酸
[讨论1] 天气闷热时,鱼儿为什么总爱在水面上进行呼吸?
(1)打开汽水盖时,汽水会自动喷出来。这说明气体在水中的溶解度与什么有关?
(2)喝了汽水以后,常常会打嗝。这说明气体的溶解度还与什么有关?
气体的溶解度与温度、压强有关,温度越高,溶解度越小;压强越大溶解度越大。
[讨论2]:
2、气体溶解度:
通常讲的气体溶解度是指该气体在压强为101KPa, 一定温度时溶解在1体积水里达到饱和状态时的气体体积。
0 ℃时,氧气的溶解度为0.049的含义是什么?
在0 ℃,氧气压强为101 kPa时,1体积水最多能溶解0. 049体积氧气
想一想:
1标准大气压下,20 ℃时部分气体的溶解度
是一个比值,无单位。
怎样从海水中把氯化钠提取出来呢?
四、结晶
[实验1] 用玻璃棒蘸取少量浓的氯化钠溶液,用酒精灯加热,观察实验现象。
玻璃棒附有白色的食盐晶体
结论:在一定条件下,可以使固体物质从它的水溶液中析出
晶体的过程叫做结晶。
要使晶体从溶液中析出有那些方法呢?
⑴蒸发溶剂法:
适用于溶解度受温度影响较小的的固体溶质,即缓升型的物质。如蒸发海水获得食盐;
如盐场用海水晒盐
把海水引入海滩
使水分蒸发
从而得到食盐
借助日光
和风力
⑵冷却热饱和溶液法:或称降温结晶法。
适用于溶解度受温度影响较大的固体溶质。如冷却热的硝酸钾饱和溶液来获取硝酸钾晶体
硝酸钾的溶解度曲线
1、下列混合物可以用结晶方法分离的是( )
A. 木炭粉和二氧化锰
B. 氯酸钾中含有泥沙
C. 硝酸钾中混有少量食盐
D. 在加热完全分解的高锰酸钾的产物中提取二氧化锰
2、海水晒盐的原理是( )
A.利用阳光和风力,使氯化钠蒸发
B.利用阳光和风力,使水分蒸发
C.利用日晒,使海水分解
D.利用日晒,使氯化钠的溶解度减小
随堂练习:
C
B
3、粗盐的杂质主要是氯化镁(能溶于水)。工业上常把粗盐粉碎后用饱
和食盐水浸洗,再过滤出食盐。对这一过程认识正确的是( )
A .浸洗前后,被浸洗的粗盐中的氯化镁的含量基本不变
B .浸洗前后,食盐水中氯化钠的质量基本不变
C .浸洗后,食盐水中氯化钠的质量分数增大
D .浸洗用的饱和食盐水可以无限次地使用下去
4、某物质结晶后的溶液( )
A.一定是该物质的浓溶液
B.可能是该物质的浓溶液
C.一定是该物质的饱和溶液
D.可能是该物质的饱和溶液,也可能是浓溶液
B
C
5、20℃时, 200gA溶液蒸发掉10g水后析出2g晶体,同样温度下再蒸发
掉10g水时,下列推论正确的是( )
A. 又会析出2g晶体
B. 析出晶体的质量一定大于2g
C.物质A的溶解度变小
D .析出晶体后的溶液的质量分数不变
D
