第3章 空气和生命复习课(空气、氧气、二氧化碳部分)
文档属性
| 名称 | 第3章 空气和生命复习课(空气、氧气、二氧化碳部分) |

|
|
| 格式 | zip | ||
| 文件大小 | 1.7MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2015-06-23 00:00:00 | ||
图片预览





文档简介
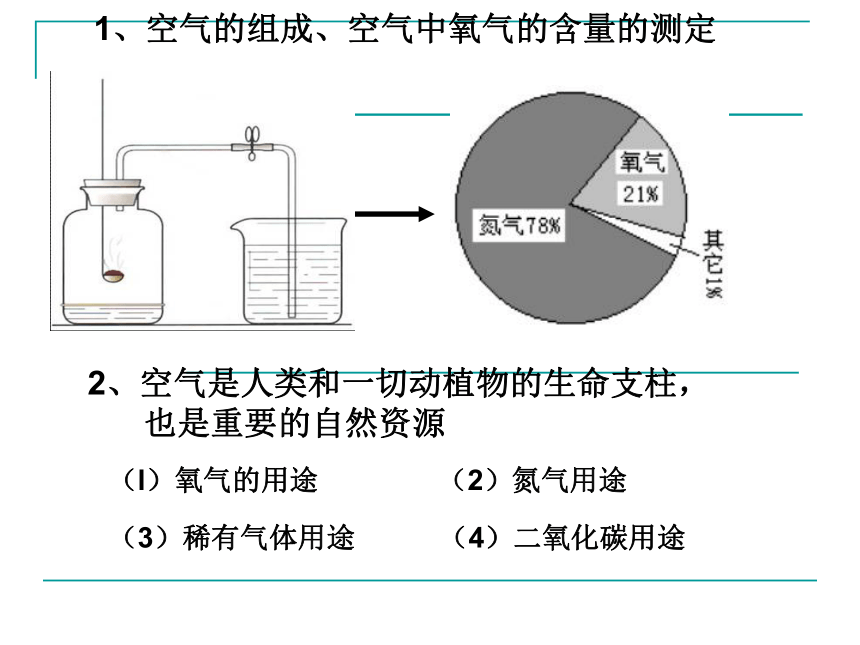
课件29张PPT。第3章 空气和生命 复习(1)1、空气的组成、空气中氧气的含量的测定 2、空气是人类和一切动植物的生命支柱,
也是重要的自然资源 (l)氧气的用途 (2)氮气用途(3)稀有气体用途(4)二氧化碳用途 性质物理性质:化学性质:无色、无味常温下呈气态
密度比空气大,不易溶于水。
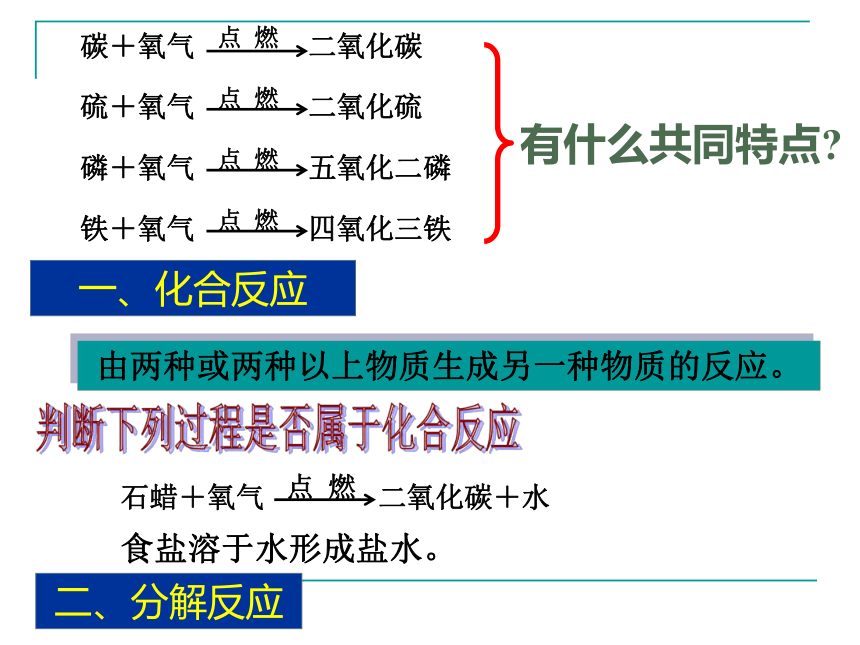
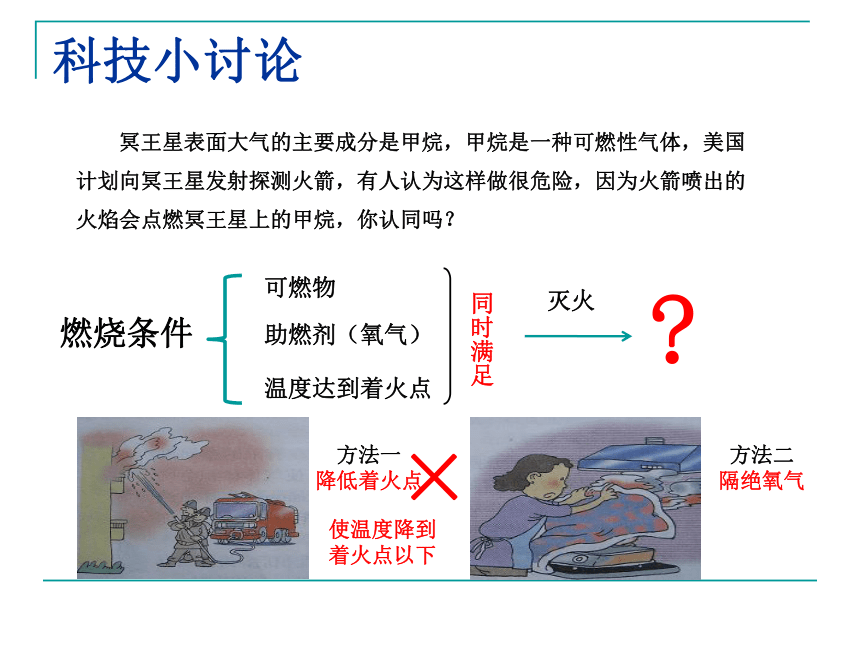
比较活泼S + O2 SO2点燃 明亮的蓝紫色火焰,生成具有刺激性气味的气体现象:氧化反应氧化物由两种元素构成,其中一种元素是氧的化合物碳磷铁丝说一说 反应现象 写一写化学方程式由两种或两种以上物质生成另一种物质的反应。 一、化合反应判断下列过程是否属于化合反应食盐溶于水形成盐水。二、分解反应 你能说说氧气有什么用途?助燃供给呼吸科技小讨论 冥王星表面大气的主要成分是甲烷,甲烷是一种可燃性气体,美国计划向冥王星发射探测火箭,有人认为这样做很危险,因为火箭喷出的
火焰会点燃冥王星上的甲烷,你认同吗?燃烧条件可燃物助燃剂(氧气)温度达到着火点灭火同时满足?方法一
降低着火点方法二
隔绝氧气×使温度降到
着火点以下氧化反应
(放 热)燃烧 缓慢氧化 有限空间内进行 爆炸不及时散热自燃1、燃烧:可燃物跟空气中氧气发生的一种发光发热的剧烈的氧化反应。
2、爆炸:可燃物在有限空间里急速燃烧
3、缓慢氧化:进行得很慢甚至不易被觉察的氧化反应
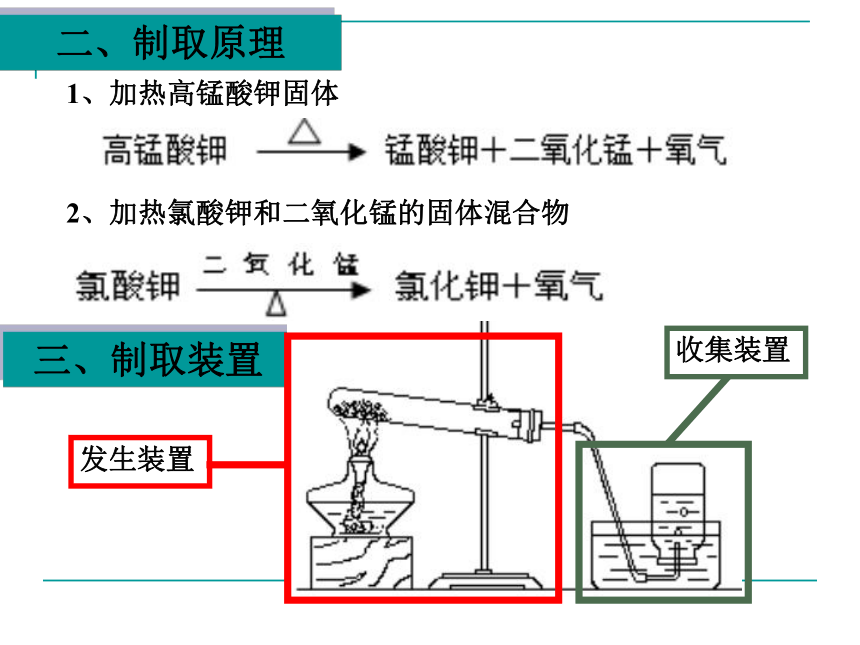
4、自燃:由缓慢氧化而引起的自发燃烧四个概念的区别和联系二、制取原理1、加热高锰酸钾固体2、加热氯酸钾和二氧化锰的固体混合物三、制取装置氧气实验室制法(固固加热型)本实验装置易错处:1)试管口应略向下2)导管应稍露出橡皮塞3)酒精灯应用外焰加热4)铁夹应夹在离试管口1/3处5)火焰应加热在试管底部6)酒精量不少于1/4,不多于2/37)排水收集时导管不能太长四、制取操作步骤1、检查气密性2、装入药品3、固定装置4、加热5、收集6、将导管移出水面7、撤去酒精灯如果1和2、6和7互相换位,结果会怎样五、氧气的收集方法1、排水法2、向上排空气法制取2KMnO4 K2MnO4+MnO2+O2↑ ?2KClO3 2KCl + 3O2↑ MnO2
?H2O2 H2 ↑ + O2 ↑MnO2 2H2O2 2H2O + O2 ↑MnO2 方法一:加热高锰酸钾方法二:加热氯酸钾和二氧化锰方法三:分解过氧化氢(固态)(固态)(液态)二、分解反应收集不易溶于水
密度比空气大能溶于水
密度比空气大难溶于水
密度比空气小O2CO2H2排水集气法向上排空气法向下排空气法?O2O2空气空气O2O2水思考:如何正确使用“万能集气瓶”?H2空气空气H2向上排空气法向下排空气法排水法验证 用带火星的木条伸入集气瓶内 ,木条复燃,
说明是氧气。把带火星的木条放到集气瓶口,木条复燃,说明已经收集满。是不是氧气呢?满了吗?能否说明氧气也具有可燃性?应用例1、实验室用过氧化氢制取氧气,现欲制氧气3.2克?问:需过氧化氢多少克?
解:2H2O2 2H2O + O2↑MnO2X3.268
X32
3.2X = 6.8g68 32 解题步聚
写出方程式
对应数据比
列出比例式
算出答案设需过氧化氢的质量为X例2、实验室用过氧化氢制取氧气,现欲制氧气2.24升 (氧气在常温下的密度为1.429克/升)。问:需过氧化氢多少克? 2H2O2 2H2O + O2↑MnO2X3.268 32 解:m = ρv =1.429x2.24 = 3.2g68
X32
3.2X = 6.8g例3、如图所示,实验室用过氧化氢制取氧气,烧瓶内的物质的质量在完全反应前后如右图所示,问:实验前加入过氧化氢多少克? 2H2O2 2H2O + O2↑MnO2X3.268 32 68
X32
3.2X = 6.8g解:氧气质量
100 – 96.8 = 3.2g 例4、实验室用100克过氧化氢溶液制取氧气,完全反应后生成氧气3.2克?问:原氧化氢溶液的质量分数是多少? 2H2O2 2H2O + O2↑MnO2X3.268 32 68
X32
3.2X = 6.8g解:6.8
100100%6.8%小结:题型变换分析例1 直接给出氧气的质量
例2 给出氧气的密度和体积
例3 利用图表给出信息
例4 隐藏了待求物过氧化氢实验室用过氧化氢制取氧气,现欲 制氧气3.2克?问:需质量分数为10%的过氧化氢溶液多少克?
练习:二氧化碳1.二氧化碳的物理性质。(通常情况下)无色无味的气体密度比空气大微溶于水三态变化,固体称干冰2.二氧化碳的化学性质:一般情况不能提供呼吸一般情况下,不能燃烧也支持燃烧与水反应:CO2+H2O H2CO3
与澄清石灰水反应:CO2+Ca(OH)2 CaCO3 +H2O
(检查二氧化碳的方法)3.二氧化碳的用途.灭火作化工原料,制纯碱,汽水等植物进行光合作用原料一、二氧化碳的实验室制法1、制法原理CaCO3+2HCl==CaCl2 + H2O + CO2↑原料选择:a为什么不用碳酸钠? 速度太快,不易控制石灰石或大理石、稀盐酸b为什么不用稀硫酸? 生成硫酸钙是微溶物质,附着在石灰石表面,使之与稀硫酸隔绝,阻碍反应进行。c、为什么不用浓盐酸因为浓盐酸有挥发性,生成的二氧化碳中含有大量的氯化氢气体制氢气适用范围
a、固液反应;
b、不需加热。2、发生装置选择:——启普发生器或简易装置思考:如何检查装置的气密性?制二氧化碳装置注意点液封要加热吗?导气管稍露出橡皮塞即可3、收集装置与收集方法收集方法:排水集气法 向上排空法3、二氧化碳的检验1、验证方法:通入澄清石灰水中,石灰水变混浊。2、验满方法:燃着的木条伸到瓶口,如果熄灭,说明已满二、二氧化碳的工业制法三、二氧化碳的用途。结合自己的生活常识,试举例说出二氧化碳有哪些用途。1、干冰:可做致冷剂,保存食品和人工降雨,可做灭火剂2、气体肥料:促进光合作用3、化工原料:制纯碱、汽水4、灭火好清新的空气
请爱护她石门中学 徐 飞
也是重要的自然资源 (l)氧气的用途 (2)氮气用途(3)稀有气体用途(4)二氧化碳用途 性质物理性质:化学性质:无色、无味常温下呈气态
密度比空气大,不易溶于水。
比较活泼S + O2 SO2点燃 明亮的蓝紫色火焰,生成具有刺激性气味的气体现象:氧化反应氧化物由两种元素构成,其中一种元素是氧的化合物碳磷铁丝说一说 反应现象 写一写化学方程式由两种或两种以上物质生成另一种物质的反应。 一、化合反应判断下列过程是否属于化合反应食盐溶于水形成盐水。二、分解反应 你能说说氧气有什么用途?助燃供给呼吸科技小讨论 冥王星表面大气的主要成分是甲烷,甲烷是一种可燃性气体,美国计划向冥王星发射探测火箭,有人认为这样做很危险,因为火箭喷出的
火焰会点燃冥王星上的甲烷,你认同吗?燃烧条件可燃物助燃剂(氧气)温度达到着火点灭火同时满足?方法一
降低着火点方法二
隔绝氧气×使温度降到
着火点以下氧化反应
(放 热)燃烧 缓慢氧化 有限空间内进行 爆炸不及时散热自燃1、燃烧:可燃物跟空气中氧气发生的一种发光发热的剧烈的氧化反应。
2、爆炸:可燃物在有限空间里急速燃烧
3、缓慢氧化:进行得很慢甚至不易被觉察的氧化反应
4、自燃:由缓慢氧化而引起的自发燃烧四个概念的区别和联系二、制取原理1、加热高锰酸钾固体2、加热氯酸钾和二氧化锰的固体混合物三、制取装置氧气实验室制法(固固加热型)本实验装置易错处:1)试管口应略向下2)导管应稍露出橡皮塞3)酒精灯应用外焰加热4)铁夹应夹在离试管口1/3处5)火焰应加热在试管底部6)酒精量不少于1/4,不多于2/37)排水收集时导管不能太长四、制取操作步骤1、检查气密性2、装入药品3、固定装置4、加热5、收集6、将导管移出水面7、撤去酒精灯如果1和2、6和7互相换位,结果会怎样五、氧气的收集方法1、排水法2、向上排空气法制取2KMnO4 K2MnO4+MnO2+O2↑ ?2KClO3 2KCl + 3O2↑ MnO2
?H2O2 H2 ↑ + O2 ↑MnO2 2H2O2 2H2O + O2 ↑MnO2 方法一:加热高锰酸钾方法二:加热氯酸钾和二氧化锰方法三:分解过氧化氢(固态)(固态)(液态)二、分解反应收集不易溶于水
密度比空气大能溶于水
密度比空气大难溶于水
密度比空气小O2CO2H2排水集气法向上排空气法向下排空气法?O2O2空气空气O2O2水思考:如何正确使用“万能集气瓶”?H2空气空气H2向上排空气法向下排空气法排水法验证 用带火星的木条伸入集气瓶内 ,木条复燃,
说明是氧气。把带火星的木条放到集气瓶口,木条复燃,说明已经收集满。是不是氧气呢?满了吗?能否说明氧气也具有可燃性?应用例1、实验室用过氧化氢制取氧气,现欲制氧气3.2克?问:需过氧化氢多少克?
解:2H2O2 2H2O + O2↑MnO2X3.268
X32
3.2X = 6.8g68 32 解题步聚
写出方程式
对应数据比
列出比例式
算出答案设需过氧化氢的质量为X例2、实验室用过氧化氢制取氧气,现欲制氧气2.24升 (氧气在常温下的密度为1.429克/升)。问:需过氧化氢多少克? 2H2O2 2H2O + O2↑MnO2X3.268 32 解:m = ρv =1.429x2.24 = 3.2g68
X32
3.2X = 6.8g例3、如图所示,实验室用过氧化氢制取氧气,烧瓶内的物质的质量在完全反应前后如右图所示,问:实验前加入过氧化氢多少克? 2H2O2 2H2O + O2↑MnO2X3.268 32 68
X32
3.2X = 6.8g解:氧气质量
100 – 96.8 = 3.2g 例4、实验室用100克过氧化氢溶液制取氧气,完全反应后生成氧气3.2克?问:原氧化氢溶液的质量分数是多少? 2H2O2 2H2O + O2↑MnO2X3.268 32 68
X32
3.2X = 6.8g解:6.8
100100%6.8%小结:题型变换分析例1 直接给出氧气的质量
例2 给出氧气的密度和体积
例3 利用图表给出信息
例4 隐藏了待求物过氧化氢实验室用过氧化氢制取氧气,现欲 制氧气3.2克?问:需质量分数为10%的过氧化氢溶液多少克?
练习:二氧化碳1.二氧化碳的物理性质。(通常情况下)无色无味的气体密度比空气大微溶于水三态变化,固体称干冰2.二氧化碳的化学性质:一般情况不能提供呼吸一般情况下,不能燃烧也支持燃烧与水反应:CO2+H2O H2CO3
与澄清石灰水反应:CO2+Ca(OH)2 CaCO3 +H2O
(检查二氧化碳的方法)3.二氧化碳的用途.灭火作化工原料,制纯碱,汽水等植物进行光合作用原料一、二氧化碳的实验室制法1、制法原理CaCO3+2HCl==CaCl2 + H2O + CO2↑原料选择:a为什么不用碳酸钠? 速度太快,不易控制石灰石或大理石、稀盐酸b为什么不用稀硫酸? 生成硫酸钙是微溶物质,附着在石灰石表面,使之与稀硫酸隔绝,阻碍反应进行。c、为什么不用浓盐酸因为浓盐酸有挥发性,生成的二氧化碳中含有大量的氯化氢气体制氢气适用范围
a、固液反应;
b、不需加热。2、发生装置选择:——启普发生器或简易装置思考:如何检查装置的气密性?制二氧化碳装置注意点液封要加热吗?导气管稍露出橡皮塞即可3、收集装置与收集方法收集方法:排水集气法 向上排空法3、二氧化碳的检验1、验证方法:通入澄清石灰水中,石灰水变混浊。2、验满方法:燃着的木条伸到瓶口,如果熄灭,说明已满二、二氧化碳的工业制法三、二氧化碳的用途。结合自己的生活常识,试举例说出二氧化碳有哪些用途。1、干冰:可做致冷剂,保存食品和人工降雨,可做灭火剂2、气体肥料:促进光合作用3、化工原料:制纯碱、汽水4、灭火好清新的空气
请爱护她石门中学 徐 飞
同课章节目录
- 第1章 电与磁
- 第1节 指南针为什么能指方向
- 第2节 电生磁
- 第3节 电磁铁的应用
- 第4节 电动机
- 第5节 磁生电
- 第6节 家庭用电
- 第7节 电的安全使用
- 第2章 微粒的模型与符号
- 第1节 模型、符号的建立与作用
- 第2节 物质的微观粒子模型
- 第3节 原子结构的模型
- 第4节 组成物质的元素
- 第5节 表示元素的符号
- 第6节 表示物质的符号
- 第7节 元素符号表示的量
- 第3章 空气与生命
- 第1节 空气与氧气
- 第2节 氧化和燃烧
- 第3节 化学方程式
- 第4节 二氧化碳
- 第5节 生物的呼吸和呼吸作用
- 第6节 光合作用
- 第7节 自然界中的氧循环和碳循环
- 第8节 空气污染与保护
- 第4章 植物与土壤
- 第1节 土壤的成分
- 第2节 各种各样的土壤
- 第3节 植物的根与物质吸收
- 第4节 植物的茎与物质运输
- 第5节 植物的叶与蒸腾作用
- 第6节 保护土壤
- 研究性学习课题
- 一 设计简单的电磁控制电路
- 二 化学反应中质量守恒的研究
- 三 研究植物的呼吸
- 四 当地水土状况调查
