7.2.3常见的碱课件(共32张PPT内嵌视频)2023-2024学年度沪教版化学九年级下册
文档属性
| 名称 | 7.2.3常见的碱课件(共32张PPT内嵌视频)2023-2024学年度沪教版化学九年级下册 |

|
|
| 格式 | pptx | ||
| 文件大小 | 30.4MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-01-17 00:00:00 | ||
图片预览










文档简介
(共32张PPT)
课时3 常见的碱
九年级下册
沪教版
学习目标
新课引入
新知学习
课堂小结
1
2
3
4
1.认识碱的组成,知道两种常见碱的主要物理性质和用途。
2.认识碱的化学性质,知道碱能使指示剂变色、能够与非金属氧化物反应、能与某些盐溶液反应。
3.初步认识复分解反应。
重难点
重点
重点
人类社会除了需要酸,同样也离不开碱,它们在生产生活中有哪些应用?
炉具清洁剂和肥皂中含有碱
使用石灰浆保护树木,防止冻伤,并防止害虫生卵。
实验室中常用的碱有哪些?它们都有哪些基本的性质?
氢氧化钠NaOH
氢氧化钙Ca(OH)2
氨水NH3.H2O
俗称烧碱、火碱或苛性钠
俗称熟石灰、消石灰
氢氧化钠固体在空气中的变化
现象:白色的固体,当曝露在空气中一段时间后,表面潮湿并逐渐溶解
分析:吸收空气中的水分
观察氢氧化钠固体的颜色、状态。在表面皿中放一些氢氧化钠固体,露置在空气中一段时间, 观察它发生的变化。
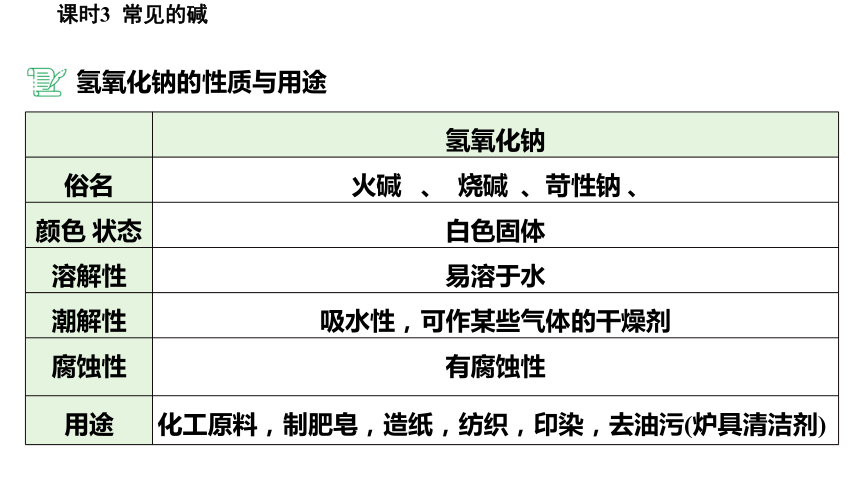
氢氧化钠的性质和用途
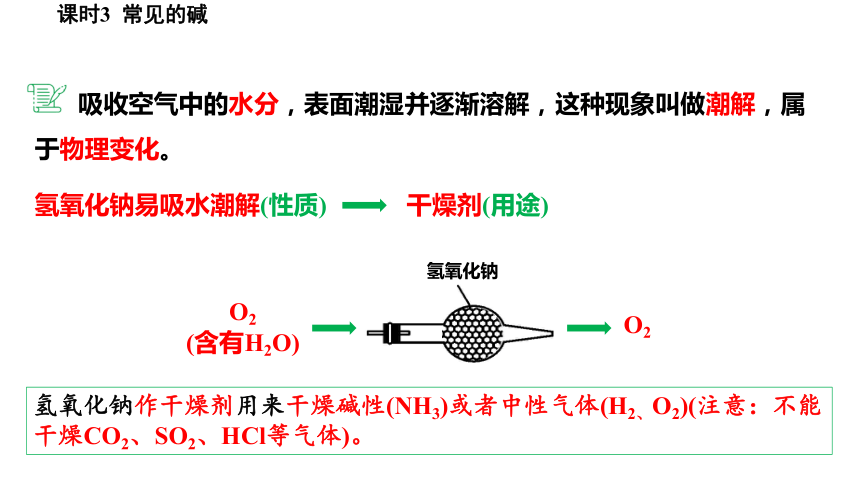
吸收空气中的水分,表面潮湿并逐渐溶解,这种现象叫做潮解,属于物理变化。
O2
(含有H2O)
O2
氢氧化钠易吸水潮解(性质)
干燥剂(用途)
氢氧化钠作干燥剂用来干燥碱性(NH3)或者中性气体(H2、O2)(注意:不能干燥CO2、SO2、HCl等气体)。
氢氧化钠
现象:氢氧化钠极易溶于水,溶液温度明显升高
分析:氢氧化钠溶解时放出大量的热
你还记得氢氧化钠固体溶于水的现象吗?
氢氧化钠还具有强烈的腐蚀性,利用它的腐蚀性,我们可以用氢氧化钠溶液浸泡叶子,自制美丽的“叶脉书签”。使用氢氧化钠时一定要小心,防止眼睛、皮肤、衣服等被它腐蚀。实验时要戴护目镜。如果不慎沾到皮肤上,要用大量水冲洗,再涂上硼酸溶液。
因为氢氧化钠的腐蚀性很强,所以人们俗称它为“火碱”、“烧碱”、“苛性钠”。
自制叶脉书签
NaOH由于易潮解、强腐蚀性”须在玻璃器皿中称量。
在工业上,氢氧化钠是一种重要的化工原料,广泛应用于制取肥皂,以及石油、造纸、纺织和印染等工业。
肥皂
造纸
纺织
印染
石油
氢氧化钠还能与油脂反应,在生活中可以用来去除油污,这就是炉具清洁剂中含有氢氧化钠的原因。
氢氧化钠
俗名 火碱 、 烧碱 、苛性钠 、
颜色 状态 白色固体
溶解性 易溶于水
潮解性 吸水性,可作某些气体的干燥剂
腐蚀性 有腐蚀性
用途 化工原料,制肥皂,造纸,纺织,印染,去油污(炉具清洁剂)
氢氧化钠的性质与用途
氢氧化钙的性质和用途
观察氢氧化钙固体的颜色、状态。在烧杯中加一些固体氢氧化钙,加入水,振荡,观察它的溶解过程,
现象:白色粉末状固体,部分溶解,液体浑浊
结论:微溶于水
Ca(OH)2是白色粉末状固体,微溶于水,其水溶液俗称石灰水。当石灰水中存在较多未溶解的熟石灰时,就称为石灰乳或石灰浆。
氢氧化钙对皮肤、衣服等有腐蚀作用,使用时要注意安全。
Ca(OH)2微溶于水,结合以前所学知识,你能设计实验证明水中已溶有 Ca(OH)2吗?
粉刷墙壁作建筑材料
改良酸性土壤
配制农药波尔多液
涂刷树木防虫防病
氢氧化钙在生产中有着广泛的用途
工业上是如何制得 Ca(OH)2的呢?
氢氧化钙可由生石灰与水反应得到:
CaO+H2O Ca(OH)2
生石灰:俗称氧化钙;具有强烈的吸水性,极易与水发生反应——常作为食品干燥剂;生石灰与水反应生成熟石灰的过程会放出大量的热。
生石灰与水反应放出的热量可以煮熟鸡蛋
生石灰可干燥某些碱性(NH3)或者中性气体(H2、O2);不能干燥CO2、SO2、HCl等酸性气体。
氢氧化钙
俗名 熟石灰 、 消石灰
颜色 状态 白色粉末状固体
溶解性 微溶于水
腐蚀性 有腐蚀性
用途 石灰浆,石灰乳,用于粉刷墙壁;配制农药波尔多液;与硫磺混合涂在树干上防止病虫害;熟石灰改良酸性土壤。
制取
CaO+H2O Ca(OH)2
氢氧化钙的性质与用途
实验室其他常见的碱
氨水(NH3·H2O)
无色液体,具有氨臭味,易挥发
氢氧化铜Cu(OH)2
氢氧化铁Fe(OH)3
氢氧化镁 Mg(OH)2
氢氧化钾KOH
氢氧化钠和氢氧化钙、氢氧化钾、氢氧化钡、氨水等,它们在组成上都有 OH—。
我们都知道:结构决定性质。碱中相同的结构,决定了它们具有哪些相似的性质呢?
——与酸碱指示剂作用
紫色石蕊溶液 无色酚酞溶液
氢氧化钠溶液
氢氧化钙溶液
碱溶液(可溶性碱)能使无色酚酞溶液变红,使紫色石蕊溶液变蓝。
变红
变红
变蓝
变蓝
碱的化学性质
你还记得实验室检验二氧化碳的方法吗
碱的化学性质
Ca(OH)2+CO2 === CaCO3↓ +H2O
氢氧化钠在空气中不仅易潮解吸收水分,也会发生类似的反应(变质):
2NaOH+CO2 === Na2CO3 +H2O(浓氢氧化钠溶液可用于吸收二氧化碳)
氢氧化钠必需密封保存!
碱溶液也能与SO3反应生成盐和水:
2NaOH+SO3 === Na2SO4 +H2O
——与非金属氧化物反应
碱溶液能与某些非金属氧化物反应,生成盐和水
碱 + 非金属氧化物 盐 + 水
Ca(OH)2 + CO2 === CaCO3↓ + H2O
2NaOH + CO2 === Na2CO3 + H2O
2NaOH + SO3 === Na2SO4 + H2O
从物质类别的角度看,这三个反应有什么相同点?
并不是所有的非金属氧化物都能与碱发生反应,如CO就不能与碱反应。
Ca(OH)2 + CO2 === CaCO3↓ + H2O
2NaOH + CO2 === Na2CO3 + H2O
2NaOH + SO3 === Na2SO4 + H2O
这类反应中,反应前后每一种元素的化合价都没有变化
这类非金属氧化物恰好有“对应价态的酸根离子”
-2
-2
-2
+4
+2
+4
+4
+6
+6
+4
-2
-2
-2
+1
+1
+1
+1
+1
+2
+1
+1
+1
+1
+1
你有什么发现?
碱的化学性质
——与盐反应
在烧碱溶液、石灰水中分别滴加硫酸铜溶液,会有什么现象?
现象 化学方程式
CuSO4溶液 +烧碱溶液
CuSO4溶液 +石灰水
CuSO4 + 2NaOH === Cu(OH)2↓+Na2SO4
CuSO4 + Ca(OH)2 === Cu(OH)2↓+CaSO4
产生蓝色沉淀
产生蓝色沉淀
2NaOH + CuSO4 === Cu(OH)2↓ + Na2SO4
Ca(OH)2 + CuSO4 === Cu(OH)2↓ + CaSO4
碱溶液 + 盐溶液 新碱 + 新盐
碱溶液能与某些盐溶液反应,生成新碱和新盐
氢氧化钠、氢氧化钙等碱在水溶液中都能产生氢氧根离子,所以碱溶液具有许多共同的化学性质
与酸碱指示剂作用
生成盐和水
与非金属氧化物
反应
与盐反应
碱的通性
生成沉淀
石蕊溶液遇碱变蓝色
酚酞溶液遇碱变红色
碱的化学性质
2NaOH + CuSO4 === Cu(OH)2↓ + Na2SO4
Ca(OH)2 + CuSO4 === Cu(OH)2↓ + CaSO4
由两种化合物相互交换成分,生成两种新的化合物的反应。
复分解反应
AB + CD → AD + CB
特点:“双交换,价不变”
观察以下方程式有什么特点?
碱的组成
(都含有OH—)
1.与指示剂作用
碱溶液化学性质
(碱性)
2.碱+非金属氧化物→盐+水
3.碱+盐→新盐+新盐
复分解反应
AB + CD → AD + CB(互交换,价不变)
常见的碱
氢氧化钠、氢氧化钙、氨水等的性质与用途
组成
性质
决定
1. 下列物质中,不用密封保存的是( )
A.浓硫酸 B.氯化钠固体 C.浓盐酸 D.烧碱固体
2.盛放在敞口瓶内的下列物质长期暴露在空气中,瓶内物质的质量会减少的是( )
A.盐酸 B. 生石灰
C.浓硫酸 D.烧碱固体
B
A
3.下列气体中,既能用固体NaOH干燥又能用浓H2SO4干燥的是( )
A. CO2 B. HCl C. SO2 D. O2
D
4. 碱溶液中都含有OH-,因此不同碱会表现出一些共同性质,下列有关氢氧化钙的描述中不能体现碱的共同性质的是( )
A. 能使无色酚酞试液变为红色
B. 能与碳酸钠反应生成碳酸钙沉淀
C. 能与氯化铜溶液反应生成氢氧化铜沉淀
D. 能与酸反应生成水
B
5. 下列反应中不属于复分解反应的是( )
A. H2SO4 + Ca(OH)2 === CaSO4 + 2H2O
B. H2SO4 + BaCl2 === BaSO4↓ + 2HCl
C. 2HCl + Fe === FeCl2 + H2 ↑
D. 2HCl + CaCO3 === CaCl2 + CO2 ↑ +H2O
C
6.如图所示,锥形瓶内盛有气体X,滴管内盛有液体Y。若挤压胶头滴管,使液体Y滴入锥形瓶中,充分振荡,观察到小气球膨胀起来。则气体X和液体Y不可能是( )
A.HCl、水
B.SO2、NaOH溶液
C.CO、稀硫酸
D.CO2、KOH溶液
C
7. 同学们为验证氢氧化钙的化学性质,做了以下实验(试管中均盛有氢氧化钙溶液)。
(1)将酚酞试液滴入氢氧化钙溶液中,溶液由无色变成红色,原因是其在水溶液中能解离出________(填离子符号)。
(2)B试管中发生反应的化学方程式为_______________________________。
OH-
Ca(OH) 2+CO2===CaCO3↓+ H2O
(3)C试管中可观察到的现象是______________。
(4)将B、C试管中反应后的物质过滤,将滤液倒入同一个大烧杯中,观察到有蓝色沉淀产生,由此可得出C试管反应后溶液中的溶质为______________(填化学式)。
产生蓝色沉淀
CuCl2、CaCl2
课时3 常见的碱
九年级下册
沪教版
学习目标
新课引入
新知学习
课堂小结
1
2
3
4
1.认识碱的组成,知道两种常见碱的主要物理性质和用途。
2.认识碱的化学性质,知道碱能使指示剂变色、能够与非金属氧化物反应、能与某些盐溶液反应。
3.初步认识复分解反应。
重难点
重点
重点
人类社会除了需要酸,同样也离不开碱,它们在生产生活中有哪些应用?
炉具清洁剂和肥皂中含有碱
使用石灰浆保护树木,防止冻伤,并防止害虫生卵。
实验室中常用的碱有哪些?它们都有哪些基本的性质?
氢氧化钠NaOH
氢氧化钙Ca(OH)2
氨水NH3.H2O
俗称烧碱、火碱或苛性钠
俗称熟石灰、消石灰
氢氧化钠固体在空气中的变化
现象:白色的固体,当曝露在空气中一段时间后,表面潮湿并逐渐溶解
分析:吸收空气中的水分
观察氢氧化钠固体的颜色、状态。在表面皿中放一些氢氧化钠固体,露置在空气中一段时间, 观察它发生的变化。
氢氧化钠的性质和用途
吸收空气中的水分,表面潮湿并逐渐溶解,这种现象叫做潮解,属于物理变化。
O2
(含有H2O)
O2
氢氧化钠易吸水潮解(性质)
干燥剂(用途)
氢氧化钠作干燥剂用来干燥碱性(NH3)或者中性气体(H2、O2)(注意:不能干燥CO2、SO2、HCl等气体)。
氢氧化钠
现象:氢氧化钠极易溶于水,溶液温度明显升高
分析:氢氧化钠溶解时放出大量的热
你还记得氢氧化钠固体溶于水的现象吗?
氢氧化钠还具有强烈的腐蚀性,利用它的腐蚀性,我们可以用氢氧化钠溶液浸泡叶子,自制美丽的“叶脉书签”。使用氢氧化钠时一定要小心,防止眼睛、皮肤、衣服等被它腐蚀。实验时要戴护目镜。如果不慎沾到皮肤上,要用大量水冲洗,再涂上硼酸溶液。
因为氢氧化钠的腐蚀性很强,所以人们俗称它为“火碱”、“烧碱”、“苛性钠”。
自制叶脉书签
NaOH由于易潮解、强腐蚀性”须在玻璃器皿中称量。
在工业上,氢氧化钠是一种重要的化工原料,广泛应用于制取肥皂,以及石油、造纸、纺织和印染等工业。
肥皂
造纸
纺织
印染
石油
氢氧化钠还能与油脂反应,在生活中可以用来去除油污,这就是炉具清洁剂中含有氢氧化钠的原因。
氢氧化钠
俗名 火碱 、 烧碱 、苛性钠 、
颜色 状态 白色固体
溶解性 易溶于水
潮解性 吸水性,可作某些气体的干燥剂
腐蚀性 有腐蚀性
用途 化工原料,制肥皂,造纸,纺织,印染,去油污(炉具清洁剂)
氢氧化钠的性质与用途
氢氧化钙的性质和用途
观察氢氧化钙固体的颜色、状态。在烧杯中加一些固体氢氧化钙,加入水,振荡,观察它的溶解过程,
现象:白色粉末状固体,部分溶解,液体浑浊
结论:微溶于水
Ca(OH)2是白色粉末状固体,微溶于水,其水溶液俗称石灰水。当石灰水中存在较多未溶解的熟石灰时,就称为石灰乳或石灰浆。
氢氧化钙对皮肤、衣服等有腐蚀作用,使用时要注意安全。
Ca(OH)2微溶于水,结合以前所学知识,你能设计实验证明水中已溶有 Ca(OH)2吗?
粉刷墙壁作建筑材料
改良酸性土壤
配制农药波尔多液
涂刷树木防虫防病
氢氧化钙在生产中有着广泛的用途
工业上是如何制得 Ca(OH)2的呢?
氢氧化钙可由生石灰与水反应得到:
CaO+H2O Ca(OH)2
生石灰:俗称氧化钙;具有强烈的吸水性,极易与水发生反应——常作为食品干燥剂;生石灰与水反应生成熟石灰的过程会放出大量的热。
生石灰与水反应放出的热量可以煮熟鸡蛋
生石灰可干燥某些碱性(NH3)或者中性气体(H2、O2);不能干燥CO2、SO2、HCl等酸性气体。
氢氧化钙
俗名 熟石灰 、 消石灰
颜色 状态 白色粉末状固体
溶解性 微溶于水
腐蚀性 有腐蚀性
用途 石灰浆,石灰乳,用于粉刷墙壁;配制农药波尔多液;与硫磺混合涂在树干上防止病虫害;熟石灰改良酸性土壤。
制取
CaO+H2O Ca(OH)2
氢氧化钙的性质与用途
实验室其他常见的碱
氨水(NH3·H2O)
无色液体,具有氨臭味,易挥发
氢氧化铜Cu(OH)2
氢氧化铁Fe(OH)3
氢氧化镁 Mg(OH)2
氢氧化钾KOH
氢氧化钠和氢氧化钙、氢氧化钾、氢氧化钡、氨水等,它们在组成上都有 OH—。
我们都知道:结构决定性质。碱中相同的结构,决定了它们具有哪些相似的性质呢?
——与酸碱指示剂作用
紫色石蕊溶液 无色酚酞溶液
氢氧化钠溶液
氢氧化钙溶液
碱溶液(可溶性碱)能使无色酚酞溶液变红,使紫色石蕊溶液变蓝。
变红
变红
变蓝
变蓝
碱的化学性质
你还记得实验室检验二氧化碳的方法吗
碱的化学性质
Ca(OH)2+CO2 === CaCO3↓ +H2O
氢氧化钠在空气中不仅易潮解吸收水分,也会发生类似的反应(变质):
2NaOH+CO2 === Na2CO3 +H2O(浓氢氧化钠溶液可用于吸收二氧化碳)
氢氧化钠必需密封保存!
碱溶液也能与SO3反应生成盐和水:
2NaOH+SO3 === Na2SO4 +H2O
——与非金属氧化物反应
碱溶液能与某些非金属氧化物反应,生成盐和水
碱 + 非金属氧化物 盐 + 水
Ca(OH)2 + CO2 === CaCO3↓ + H2O
2NaOH + CO2 === Na2CO3 + H2O
2NaOH + SO3 === Na2SO4 + H2O
从物质类别的角度看,这三个反应有什么相同点?
并不是所有的非金属氧化物都能与碱发生反应,如CO就不能与碱反应。
Ca(OH)2 + CO2 === CaCO3↓ + H2O
2NaOH + CO2 === Na2CO3 + H2O
2NaOH + SO3 === Na2SO4 + H2O
这类反应中,反应前后每一种元素的化合价都没有变化
这类非金属氧化物恰好有“对应价态的酸根离子”
-2
-2
-2
+4
+2
+4
+4
+6
+6
+4
-2
-2
-2
+1
+1
+1
+1
+1
+2
+1
+1
+1
+1
+1
你有什么发现?
碱的化学性质
——与盐反应
在烧碱溶液、石灰水中分别滴加硫酸铜溶液,会有什么现象?
现象 化学方程式
CuSO4溶液 +烧碱溶液
CuSO4溶液 +石灰水
CuSO4 + 2NaOH === Cu(OH)2↓+Na2SO4
CuSO4 + Ca(OH)2 === Cu(OH)2↓+CaSO4
产生蓝色沉淀
产生蓝色沉淀
2NaOH + CuSO4 === Cu(OH)2↓ + Na2SO4
Ca(OH)2 + CuSO4 === Cu(OH)2↓ + CaSO4
碱溶液 + 盐溶液 新碱 + 新盐
碱溶液能与某些盐溶液反应,生成新碱和新盐
氢氧化钠、氢氧化钙等碱在水溶液中都能产生氢氧根离子,所以碱溶液具有许多共同的化学性质
与酸碱指示剂作用
生成盐和水
与非金属氧化物
反应
与盐反应
碱的通性
生成沉淀
石蕊溶液遇碱变蓝色
酚酞溶液遇碱变红色
碱的化学性质
2NaOH + CuSO4 === Cu(OH)2↓ + Na2SO4
Ca(OH)2 + CuSO4 === Cu(OH)2↓ + CaSO4
由两种化合物相互交换成分,生成两种新的化合物的反应。
复分解反应
AB + CD → AD + CB
特点:“双交换,价不变”
观察以下方程式有什么特点?
碱的组成
(都含有OH—)
1.与指示剂作用
碱溶液化学性质
(碱性)
2.碱+非金属氧化物→盐+水
3.碱+盐→新盐+新盐
复分解反应
AB + CD → AD + CB(互交换,价不变)
常见的碱
氢氧化钠、氢氧化钙、氨水等的性质与用途
组成
性质
决定
1. 下列物质中,不用密封保存的是( )
A.浓硫酸 B.氯化钠固体 C.浓盐酸 D.烧碱固体
2.盛放在敞口瓶内的下列物质长期暴露在空气中,瓶内物质的质量会减少的是( )
A.盐酸 B. 生石灰
C.浓硫酸 D.烧碱固体
B
A
3.下列气体中,既能用固体NaOH干燥又能用浓H2SO4干燥的是( )
A. CO2 B. HCl C. SO2 D. O2
D
4. 碱溶液中都含有OH-,因此不同碱会表现出一些共同性质,下列有关氢氧化钙的描述中不能体现碱的共同性质的是( )
A. 能使无色酚酞试液变为红色
B. 能与碳酸钠反应生成碳酸钙沉淀
C. 能与氯化铜溶液反应生成氢氧化铜沉淀
D. 能与酸反应生成水
B
5. 下列反应中不属于复分解反应的是( )
A. H2SO4 + Ca(OH)2 === CaSO4 + 2H2O
B. H2SO4 + BaCl2 === BaSO4↓ + 2HCl
C. 2HCl + Fe === FeCl2 + H2 ↑
D. 2HCl + CaCO3 === CaCl2 + CO2 ↑ +H2O
C
6.如图所示,锥形瓶内盛有气体X,滴管内盛有液体Y。若挤压胶头滴管,使液体Y滴入锥形瓶中,充分振荡,观察到小气球膨胀起来。则气体X和液体Y不可能是( )
A.HCl、水
B.SO2、NaOH溶液
C.CO、稀硫酸
D.CO2、KOH溶液
C
7. 同学们为验证氢氧化钙的化学性质,做了以下实验(试管中均盛有氢氧化钙溶液)。
(1)将酚酞试液滴入氢氧化钙溶液中,溶液由无色变成红色,原因是其在水溶液中能解离出________(填离子符号)。
(2)B试管中发生反应的化学方程式为_______________________________。
OH-
Ca(OH) 2+CO2===CaCO3↓+ H2O
(3)C试管中可观察到的现象是______________。
(4)将B、C试管中反应后的物质过滤,将滤液倒入同一个大烧杯中,观察到有蓝色沉淀产生,由此可得出C试管反应后溶液中的溶质为______________(填化学式)。
产生蓝色沉淀
CuCl2、CaCl2
