第7章 应用广泛的酸、碱、盐基础研题(含答案) ---2023-2024学年九年级化学沪教版(全国)下册
文档属性
| 名称 | 第7章 应用广泛的酸、碱、盐基础研题(含答案) ---2023-2024学年九年级化学沪教版(全国)下册 |  | |
| 格式 | docx | ||
| 文件大小 | 169.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-02-20 15:18:21 | ||
图片预览




文档简介
第7章 应用广泛的酸、碱、盐 基础研题(含答案)沪教版(全国)化学九年级下册
一、选择题。
1、下列实验方案中,设计合理的是( )
A.用酒精浸泡牵牛花自制酸碱指示剂
B.用过滤的方法将硬水转化为软水
C.用燃烧木条的方法制备纯净的二氧化碳气体
D.常温下用水区分一氧化碳和氮气
2、用稀盐酸除铁锈的原理是( )
A.FeO+2HCl===FeCl2+H2O B.FeO+2HCl===FeCl3+H2O
C.Fe2O3+6HCl===2FeCl2+3H2O D.Fe2O3+6HCl===2FeCl3+3H2O
3、不可能由两种元素组成的化合物是( )
A.氧化物 B.酸 C.碱 D.盐
4、按如图所示装置,玻璃棒末端固定一团喷有酚酞溶液的脱脂棉Y。先加入物质X,再塞上带玻璃棒的橡胶塞。片刻后,能观察到喷有酚酞溶液的脱脂棉Y变红,则物质X可能是( )
A.浓盐酸 B.浓氨水 C.浓醋酸 D.浓氢氧化钠溶液
5、向一定质量的Na2CO3和Na2SO4混合溶液中先后滴加BaCl2、HCl溶液,反应过程中加入溶液的质量与产生沉淀或气体的质量关系如图所示。下列说法错误的是( )
A. 0-a段溶液的pH始终不变
B. c点有两种沉淀
C. 生成硫酸钡沉淀的质量是2.33g
D. d点对应的溶液中溶质的成分为BaCl2和HCl
6、如图所示是室温下稀硫酸和氢氧化钠反应过程中的pH变化曲线。下列有关说法正确的是( )
A.图中X是氢氧化钠
B.图中a点的阴离子是OH-
C.向图中c点所示溶液中加入铁粉后,溶液中有气泡产生
D.稀硫酸与氢氧化钠溶液反应的化学方程式为:H2SO4+2NaOH═Na2SO4+H2O
7、柠檬酸(C6H8O7)是一种较强的有机酸,在水溶液中可以解离出来H+,从而呈现酸的通性,下列物质不能与柠檬酸反应的是( )
A.Fe2O3 B.CO2 C.CaCO3 D.Zn
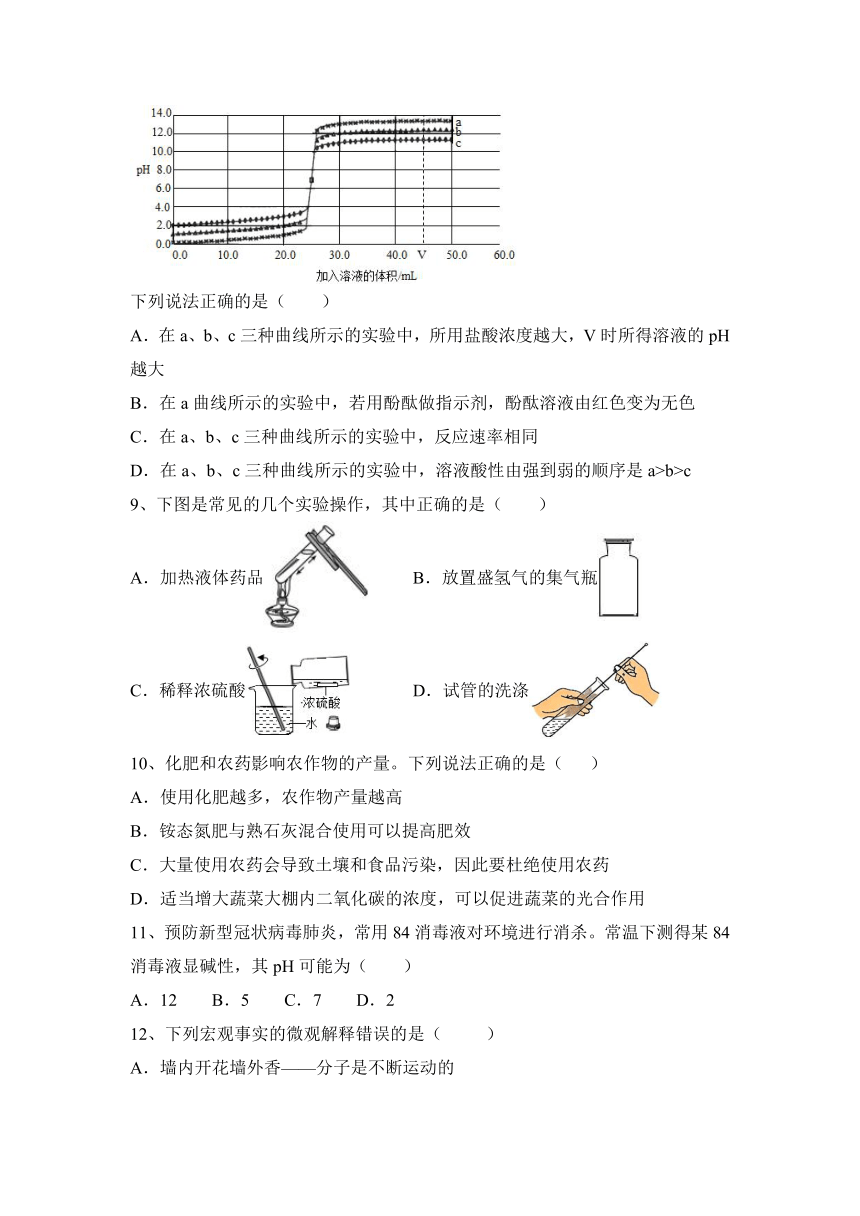
8、下图为三种不同浓度的氢氧化钠溶液与对应浓度的盐酸反应的曲线。
下列说法正确的是( )
A.在a、b、c三种曲线所示的实验中,所用盐酸浓度越大,V时所得溶液的pH越大
B.在a曲线所示的实验中,若用酚酞做指示剂,酚酞溶液由红色变为无色
C.在a、b、c三种曲线所示的实验中,反应速率相同
D.在a、b、c三种曲线所示的实验中,溶液酸性由强到弱的顺序是a>b>c
9、下图是常见的几个实验操作,其中正确的是( )
A.加热液体药品 B.放置盛氢气的集气瓶
C.稀释浓硫酸 D.试管的洗涤
10、化肥和农药影响农作物的产量。下列说法正确的是( )
A.使用化肥越多,农作物产量越高
B.铵态氮肥与熟石灰混合使用可以提高肥效
C.大量使用农药会导致土壤和食品污染,因此要杜绝使用农药
D.适当增大蔬菜大棚内二氧化碳的浓度,可以促进蔬菜的光合作用
11、预防新型冠状病毒肺炎,常用84消毒液对环境进行消杀。常温下测得某84消毒液显碱性,其pH可能为( )
A.12 B.5 C.7 D.2
12、下列宏观事实的微观解释错误的是( )
A.墙内开花墙外香——分子是不断运动的
B.6000升氧气在加压的情况下可装入容积为40升的钢瓶中——分子体积变小
C.硫酸、盐酸有一些相似的性质原因——不同的酸溶液中都含有氢离子
D.一氧化碳能燃烧二氧化碳不能燃烧——分子构成不同
13、一些食物pH 的近似值范围如下:橘子汁3.~4.0;泡菜3.2~3.6;牛奶6.3~6.6;鸡蛋清7.6~8.0.下列说法中,不正确的是( )
A.鸡蛋清显碱性 B.胃酸过多的人应少吃泡菜
C.橘子汁能使紫色石蕊溶液变红 D.牛奶比橘子汁的酸性强
14、某工厂排出的废水pH小于7,并含有较多的Cu2+,对环境污染严重。从环保及回收利用考虑,较切合实际的治理方案是应适量加入( )
A.烧碱和纯碱 B.盐酸和铁粉
C.生石灰和铁粉 D.熟石灰和金属银
15、区分下列各组物质的两种方法均正确的是( )
选项 待区分物质 方法一 方法二
A 蒸馏水和氯化钾溶液 分别蒸干观察 分别加入硫酸铜溶液
B 氧气和二氧化碳 分别伸入燃着的小木条 分别闻气味
C 黄铜和铜 观察颜色 相互刻画比较硬度
D 氢氧化钠和熟石灰 分别溶于水后加入碳酸钾溶液 分别加入硝酸按研磨闻气味
A.A B.B C.C D.D
16、下列常见物质显碱性的是( )
A.食醋 B.食盐水 C.肥皂水 D.柠檬水
二、填空题。
17、某同学将一朵紫色牵牛花泡在石灰水里,牵牛花很快就变成了蓝色,又将牵牛花泡在稀盐酸中,牵牛花又变成了红色,请你根据以上实验现象回答:
(1)该同学将紫色牵牛花泡在肥皂水里,牵牛花很快就变成了蓝色,据此可推断肥皂水显_____(填“酸性”或“碱性”)。
(2)该牵牛花的汁液_____(填“能”或“不能”)用作指示剂。
18、如图所示是稀释浓硫酸实验的示意图。
(1)写出图中a、b两种仪器的名称:a________;b________。
(2)b容器中所盛的试剂是________(填“水”或“浓硫酸”)。
(3)稀释时,若两种试剂添加顺序颠倒,将会发生__________________。
【联系与拓展】据媒体报道,有一村民在家里误将装在酒瓶中的浓硫酸当成白酒喝下,造成食道和胃严重损伤,这是因为浓硫酸具有__________。这一事件警示我们,家中存放或使用药物时应注意______________________________________________________。
19、已知可溶性钡盐有剧毒,透视胃病时,让病人口服BaSO4。如果误服BaCO3就会中毒,中毒的原因请用化学方程式来表示______。若解毒最好吃______等食物,若要解毒服用一种含Mg2+的药物,它的化学式为______。
20、日常使用的洗发剂和护发剂都有一定酸碱度,若使用不当,就会对头发造成损害。
(1)用pH试纸测定某溶液的酸碱度时,正确的操作方法是______
______ ;
(2)小华同学用pH试纸按正确操作测定护发剂和洗发剂的酸碱度,测得护发剂的pH略小于7,则护发剂显______性;测得洗发剂的pH略大于7,则洗发剂显_______性.
(3)弱酸性有益于头发的健康.想一想洗发时应先用_______剂,后用______剂。
21、日前,全球平均气温较工业化前已上升了1.1℃,其主要原因是自然界中的碳平衡被破坏。2020年9月22日,我国政府承诺:中国将力争于2030年前实现CO2排放达到峰值,2060年前实现碳中和,即通过各种方式抵消排放的CO2量,重新实现碳平衡。如图是碳循环和碳中和策略的示意图。
(1)人类进入工业化社会后,化石燃料的大量使用是碳平衡被破坏的主要原因之一,对此可采取的碳中和策略②有 。
(2)要实现我国政府提出的目标,除图中策略外,还可用化学方法人工捕获,如将空气通入氢氧化钾溶液反应生成碳酸钾和水。写出用氢氧化钾捕获CO2的化学方程式 。
(3)2020年12月下句,我国部分地区出现多年未遇的极寒天气,因此有人质疑:今年天气这么冷,地球气温真的在上升吗?对于这样的质疑,你是否认同?并说明理由: 。
三、综合应用题。
22、金属材料在生活中随处可见。某学习小组围绕金属材料展开项目式学习。
【项目一】金属的物理性质
(1)316不锈钢与组成它的纯金属相比,有良好的___________ 。
【项目二】金属的化学性质
(2)组员小王将打磨后的镁条放入硫酸铜溶液中,发生反应的化学方程式为__________ 。
组员小李意外发现镁条表面还有气泡产生,于是学习小组对此展开探究。
(3)小王用拇指堵住试管,收集一会气体之后伸入燃着的木条,发出尖锐的爆鸣声,说明该气体是__________。
【提出问题】为什么会产生该气体呢?
【作出猜想】硫酸铜溶液显酸性,所以放入镁条后会产生该气体。
【实验验证】
(4)用pH试纸测量硫酸铜溶液的pH,实验操作是__________ 。经测定,溶液pH<7,证实猜想正确。
【项目三】冶炼金属
(5)冶炼金属铁的原料有铁矿石、焦炭、__________、热空气。
铁的氧化物有FeO、Fe2O3、Fe3O4。组员小卫称取6.0g铁的氧化物混合样品,采用如图装置模拟炼铁过程(夹持装置省略),完全反应后,测得实验前后装置B增重4.4g。
(6)实验开始时先打开__________,关闭另一止水夹,让CO通一段时间。
(7)根据实验数据进行计算,该固体样品成分可能是 (填字母序号)。
A.FeO、Fe2O3 B.Fe2O3、Fe3O4
C.FeO、Fe3O4 D.FeO、Fe2O3、Fe3O4
23、在实验室里,可用如图装置进行CO还原Fe2O3的实验,并检验该反应的气体生成物。已知由一氧化碳发生装置得到的CO中混有CO2和H2O。
(1)写出装置C处尾气处理的方法______ (写一种即可);A装置中有关反应的化学方程式______ 。(写出一个即可)
(2)检验CO还原Fe2O3反应的气体生成物的现象是什么?
______ 。
(3)实验后取A中固体溶于水,滴加酚酞溶液,溶液变红色,请分析可能的原因:______ 。
(4)某钢铁厂用赤铁矿石炼铁。若该厂每天需消耗6000t含氧化铁80%的赤铁矿石,则理论上可日产含铁96%的生铁的质量是多少?(写出计算过程)
第7章 应用广泛的酸、碱、盐 基础研题(含答案)沪教版(全国)化学九年级下册
一、选择题。
1、下列实验方案中,设计合理的是( )
A.用酒精浸泡牵牛花自制酸碱指示剂
B.用过滤的方法将硬水转化为软水
C.用燃烧木条的方法制备纯净的二氧化碳气体
D.常温下用水区分一氧化碳和氮气
【答案】A
2、用稀盐酸除铁锈的原理是( )
A.FeO+2HCl===FeCl2+H2O B.FeO+2HCl===FeCl3+H2O
C.Fe2O3+6HCl===2FeCl2+3H2O D.Fe2O3+6HCl===2FeCl3+3H2O
【答案】D
3、不可能由两种元素组成的化合物是( )
A.氧化物 B.酸 C.碱 D.盐
【答案】C
4、按如图所示装置,玻璃棒末端固定一团喷有酚酞溶液的脱脂棉Y。先加入物质X,再塞上带玻璃棒的橡胶塞。片刻后,能观察到喷有酚酞溶液的脱脂棉Y变红,则物质X可能是( )
A.浓盐酸 B.浓氨水 C.浓醋酸 D.浓氢氧化钠溶液
【答案】B
5、向一定质量的Na2CO3和Na2SO4混合溶液中先后滴加BaCl2、HCl溶液,反应过程中加入溶液的质量与产生沉淀或气体的质量关系如图所示。下列说法错误的是( )
A. 0-a段溶液的pH始终不变
B. c点有两种沉淀
C. 生成硫酸钡沉淀的质量是2.33g
D. d点对应的溶液中溶质的成分为BaCl2和HCl
【答案】A
6、如图所示是室温下稀硫酸和氢氧化钠反应过程中的pH变化曲线。下列有关说法正确的是( )
A.图中X是氢氧化钠
B.图中a点的阴离子是OH-
C.向图中c点所示溶液中加入铁粉后,溶液中有气泡产生
D.稀硫酸与氢氧化钠溶液反应的化学方程式为:H2SO4+2NaOH═Na2SO4+H2O
【答案】C
7、柠檬酸(C6H8O7)是一种较强的有机酸,在水溶液中可以解离出来H+,从而呈现酸的通性,下列物质不能与柠檬酸反应的是( )
A.Fe2O3 B.CO2 C.CaCO3 D.Zn
【答案】B
8、下图为三种不同浓度的氢氧化钠溶液与对应浓度的盐酸反应的曲线。
下列说法正确的是( )
A.在a、b、c三种曲线所示的实验中,所用盐酸浓度越大,V时所得溶液的pH越大
B.在a曲线所示的实验中,若用酚酞做指示剂,酚酞溶液由红色变为无色
C.在a、b、c三种曲线所示的实验中,反应速率相同
D.在a、b、c三种曲线所示的实验中,溶液酸性由强到弱的顺序是a>b>c
【答案】A
9、下图是常见的几个实验操作,其中正确的是( )
A.加热液体药品 B.放置盛氢气的集气瓶
C.稀释浓硫酸 D.试管的洗涤
【答案】D
10、化肥和农药影响农作物的产量。下列说法正确的是( )
A.使用化肥越多,农作物产量越高
B.铵态氮肥与熟石灰混合使用可以提高肥效
C.大量使用农药会导致土壤和食品污染,因此要杜绝使用农药
D.适当增大蔬菜大棚内二氧化碳的浓度,可以促进蔬菜的光合作用
【答案】D
11、预防新型冠状病毒肺炎,常用84消毒液对环境进行消杀。常温下测得某84消毒液显碱性,其pH可能为( )
A.12 B.5 C.7 D.2
【答案】A
12、下列宏观事实的微观解释错误的是( )
A.墙内开花墙外香——分子是不断运动的
B.6000升氧气在加压的情况下可装入容积为40升的钢瓶中——分子体积变小
C.硫酸、盐酸有一些相似的性质原因——不同的酸溶液中都含有氢离子
D.一氧化碳能燃烧二氧化碳不能燃烧——分子构成不同
【答案】B
13、一些食物pH 的近似值范围如下:橘子汁3.~4.0;泡菜3.2~3.6;牛奶6.3~6.6;鸡蛋清7.6~8.0.下列说法中,不正确的是( )
A.鸡蛋清显碱性 B.胃酸过多的人应少吃泡菜
C.橘子汁能使紫色石蕊溶液变红 D.牛奶比橘子汁的酸性强
【答案】D
14、某工厂排出的废水pH小于7,并含有较多的Cu2+,对环境污染严重。从环保及回收利用考虑,较切合实际的治理方案是应适量加入( )
A.烧碱和纯碱 B.盐酸和铁粉
C.生石灰和铁粉 D.熟石灰和金属银
【答案】C
15、区分下列各组物质的两种方法均正确的是( )
选项 待区分物质 方法一 方法二
A 蒸馏水和氯化钾溶液 分别蒸干观察 分别加入硫酸铜溶液
B 氧气和二氧化碳 分别伸入燃着的小木条 分别闻气味
C 黄铜和铜 观察颜色 相互刻画比较硬度
D 氢氧化钠和熟石灰 分别溶于水后加入碳酸钾溶液 分别加入硝酸按研磨闻气味
A.A B.B C.C D.D
【答案】C
16、下列常见物质显碱性的是( )
A.食醋 B.食盐水 C.肥皂水 D.柠檬水
【答案】C
二、填空题。
17、某同学将一朵紫色牵牛花泡在石灰水里,牵牛花很快就变成了蓝色,又将牵牛花泡在稀盐酸中,牵牛花又变成了红色,请你根据以上实验现象回答:
(1)该同学将紫色牵牛花泡在肥皂水里,牵牛花很快就变成了蓝色,据此可推断肥皂水显_____(填“酸性”或“碱性”)。
(2)该牵牛花的汁液_____(填“能”或“不能”)用作指示剂。
【答案】碱性 能
18、如图所示是稀释浓硫酸实验的示意图。
(1)写出图中a、b两种仪器的名称:a________;b________。
(2)b容器中所盛的试剂是________(填“水”或“浓硫酸”)。
(3)稀释时,若两种试剂添加顺序颠倒,将会发生__________________。
【联系与拓展】据媒体报道,有一村民在家里误将装在酒瓶中的浓硫酸当成白酒喝下,造成食道和胃严重损伤,这是因为浓硫酸具有__________。这一事件警示我们,家中存放或使用药物时应注意______________________________________________________。
【答案】(1)玻璃棒 量筒 (2)浓硫酸 (3)酸液飞溅
【联系与拓展】腐蚀性 存放时要贴好标签,放在安全的地方(或使用时要核对标签)
19、已知可溶性钡盐有剧毒,透视胃病时,让病人口服BaSO4。如果误服BaCO3就会中毒,中毒的原因请用化学方程式来表示______。若解毒最好吃______等食物,若要解毒服用一种含Mg2+的药物,它的化学式为______。
【答案】BaCO3+2HCl=BaCl2+CO2↑+H2O 牛奶 MgSO4
20、日常使用的洗发剂和护发剂都有一定酸碱度,若使用不当,就会对头发造成损害。
(1)用pH试纸测定某溶液的酸碱度时,正确的操作方法是______
______ ;
(2)小华同学用pH试纸按正确操作测定护发剂和洗发剂的酸碱度,测得护发剂的pH略小于7,则护发剂显______性;测得洗发剂的pH略大于7,则洗发剂显_______性.
(3)弱酸性有益于头发的健康.想一想洗发时应先用_______剂,后用______剂。
【答案】(1)在玻璃片或白瓷板上放片pH试纸,用玻璃棒蘸取待测液滴到试纸上,将试纸显示的颜色与标准比色卡对照得溶液的pH
(2) 酸 碱 (3) 洗发 护发
21、日前,全球平均气温较工业化前已上升了1.1℃,其主要原因是自然界中的碳平衡被破坏。2020年9月22日,我国政府承诺:中国将力争于2030年前实现CO2排放达到峰值,2060年前实现碳中和,即通过各种方式抵消排放的CO2量,重新实现碳平衡。如图是碳循环和碳中和策略的示意图。
(1)人类进入工业化社会后,化石燃料的大量使用是碳平衡被破坏的主要原因之一,对此可采取的碳中和策略②有 。
(2)要实现我国政府提出的目标,除图中策略外,还可用化学方法人工捕获,如将空气通入氢氧化钾溶液反应生成碳酸钾和水。写出用氢氧化钾捕获CO2的化学方程式 。
(3)2020年12月下句,我国部分地区出现多年未遇的极寒天气,因此有人质疑:今年天气这么冷,地球气温真的在上升吗?对于这样的质疑,你是否认同?并说明理由: 。
【答案】(1)开发新能源、减少化石燃料的使用;
(2);
(3)不认同,因为全球变暖是全球性的气候变化,是大趋势,极寒天气的出现,可能只是偶然性的天气现象。
三、综合应用题。
22、金属材料在生活中随处可见。某学习小组围绕金属材料展开项目式学习。
【项目一】金属的物理性质
(1)316不锈钢与组成它的纯金属相比,有良好的___________ 。
【项目二】金属的化学性质
(2)组员小王将打磨后的镁条放入硫酸铜溶液中,发生反应的化学方程式为__________ 。
组员小李意外发现镁条表面还有气泡产生,于是学习小组对此展开探究。
(3)小王用拇指堵住试管,收集一会气体之后伸入燃着的木条,发出尖锐的爆鸣声,说明该气体是__________。
【提出问题】为什么会产生该气体呢?
【作出猜想】硫酸铜溶液显酸性,所以放入镁条后会产生该气体。
【实验验证】
(4)用pH试纸测量硫酸铜溶液的pH,实验操作是__________ 。经测定,溶液pH<7,证实猜想正确。
【项目三】冶炼金属
(5)冶炼金属铁的原料有铁矿石、焦炭、__________、热空气。
铁的氧化物有FeO、Fe2O3、Fe3O4。组员小卫称取6.0g铁的氧化物混合样品,采用如图装置模拟炼铁过程(夹持装置省略),完全反应后,测得实验前后装置B增重4.4g。
(6)实验开始时先打开__________,关闭另一止水夹,让CO通一段时间。
(7)根据实验数据进行计算,该固体样品成分可能是 (填字母序号)。
A.FeO、Fe2O3 B.Fe2O3、Fe3O4
C.FeO、Fe3O4 D.FeO、Fe2O3、Fe3O4
【答案】(1)硬度大、熔点低 (2) (3)氢气##
(4)在白瓷板或玻璃片上放一小片pH试纸,用玻璃棒蘸取溶液滴到pH试纸上,把试纸显示的颜色与标准比色卡比较,读出pH。
(5)石灰石 (6)K2 (7)ACD
23、在实验室里,可用如图装置进行CO还原Fe2O3的实验,并检验该反应的气体生成物。已知由一氧化碳发生装置得到的CO中混有CO2和H2O。
(1)写出装置C处尾气处理的方法______ (写一种即可);A装置中有关反应的化学方程式______ 。(写出一个即可)
(2)检验CO还原Fe2O3反应的气体生成物的现象是什么?
______ 。
(3)实验后取A中固体溶于水,滴加酚酞溶液,溶液变红色,请分析可能的原因:______ 。
(4)某钢铁厂用赤铁矿石炼铁。若该厂每天需消耗6000t含氧化铁80%的赤铁矿石,则理论上可日产含铁96%的生铁的质量是多少?(写出计算过程)
【答案】(1) 加一个燃着的酒精灯或绑一个气球
或 或
(2)C处澄清石灰水变浑浊
(3)氢氧化钠、氢氧化钙、碳酸钠溶液均显碱性,均能使无色酚酞试液变色
(4)解:设理论上可日产含铁96%的生铁的质量是x
x=3500t
答:理论上可日产含铁96%的生铁的质量是3500t。
一、选择题。
1、下列实验方案中,设计合理的是( )
A.用酒精浸泡牵牛花自制酸碱指示剂
B.用过滤的方法将硬水转化为软水
C.用燃烧木条的方法制备纯净的二氧化碳气体
D.常温下用水区分一氧化碳和氮气
2、用稀盐酸除铁锈的原理是( )
A.FeO+2HCl===FeCl2+H2O B.FeO+2HCl===FeCl3+H2O
C.Fe2O3+6HCl===2FeCl2+3H2O D.Fe2O3+6HCl===2FeCl3+3H2O
3、不可能由两种元素组成的化合物是( )
A.氧化物 B.酸 C.碱 D.盐
4、按如图所示装置,玻璃棒末端固定一团喷有酚酞溶液的脱脂棉Y。先加入物质X,再塞上带玻璃棒的橡胶塞。片刻后,能观察到喷有酚酞溶液的脱脂棉Y变红,则物质X可能是( )
A.浓盐酸 B.浓氨水 C.浓醋酸 D.浓氢氧化钠溶液
5、向一定质量的Na2CO3和Na2SO4混合溶液中先后滴加BaCl2、HCl溶液,反应过程中加入溶液的质量与产生沉淀或气体的质量关系如图所示。下列说法错误的是( )
A. 0-a段溶液的pH始终不变
B. c点有两种沉淀
C. 生成硫酸钡沉淀的质量是2.33g
D. d点对应的溶液中溶质的成分为BaCl2和HCl
6、如图所示是室温下稀硫酸和氢氧化钠反应过程中的pH变化曲线。下列有关说法正确的是( )
A.图中X是氢氧化钠
B.图中a点的阴离子是OH-
C.向图中c点所示溶液中加入铁粉后,溶液中有气泡产生
D.稀硫酸与氢氧化钠溶液反应的化学方程式为:H2SO4+2NaOH═Na2SO4+H2O
7、柠檬酸(C6H8O7)是一种较强的有机酸,在水溶液中可以解离出来H+,从而呈现酸的通性,下列物质不能与柠檬酸反应的是( )
A.Fe2O3 B.CO2 C.CaCO3 D.Zn
8、下图为三种不同浓度的氢氧化钠溶液与对应浓度的盐酸反应的曲线。
下列说法正确的是( )
A.在a、b、c三种曲线所示的实验中,所用盐酸浓度越大,V时所得溶液的pH越大
B.在a曲线所示的实验中,若用酚酞做指示剂,酚酞溶液由红色变为无色
C.在a、b、c三种曲线所示的实验中,反应速率相同
D.在a、b、c三种曲线所示的实验中,溶液酸性由强到弱的顺序是a>b>c
9、下图是常见的几个实验操作,其中正确的是( )
A.加热液体药品 B.放置盛氢气的集气瓶
C.稀释浓硫酸 D.试管的洗涤
10、化肥和农药影响农作物的产量。下列说法正确的是( )
A.使用化肥越多,农作物产量越高
B.铵态氮肥与熟石灰混合使用可以提高肥效
C.大量使用农药会导致土壤和食品污染,因此要杜绝使用农药
D.适当增大蔬菜大棚内二氧化碳的浓度,可以促进蔬菜的光合作用
11、预防新型冠状病毒肺炎,常用84消毒液对环境进行消杀。常温下测得某84消毒液显碱性,其pH可能为( )
A.12 B.5 C.7 D.2
12、下列宏观事实的微观解释错误的是( )
A.墙内开花墙外香——分子是不断运动的
B.6000升氧气在加压的情况下可装入容积为40升的钢瓶中——分子体积变小
C.硫酸、盐酸有一些相似的性质原因——不同的酸溶液中都含有氢离子
D.一氧化碳能燃烧二氧化碳不能燃烧——分子构成不同
13、一些食物pH 的近似值范围如下:橘子汁3.~4.0;泡菜3.2~3.6;牛奶6.3~6.6;鸡蛋清7.6~8.0.下列说法中,不正确的是( )
A.鸡蛋清显碱性 B.胃酸过多的人应少吃泡菜
C.橘子汁能使紫色石蕊溶液变红 D.牛奶比橘子汁的酸性强
14、某工厂排出的废水pH小于7,并含有较多的Cu2+,对环境污染严重。从环保及回收利用考虑,较切合实际的治理方案是应适量加入( )
A.烧碱和纯碱 B.盐酸和铁粉
C.生石灰和铁粉 D.熟石灰和金属银
15、区分下列各组物质的两种方法均正确的是( )
选项 待区分物质 方法一 方法二
A 蒸馏水和氯化钾溶液 分别蒸干观察 分别加入硫酸铜溶液
B 氧气和二氧化碳 分别伸入燃着的小木条 分别闻气味
C 黄铜和铜 观察颜色 相互刻画比较硬度
D 氢氧化钠和熟石灰 分别溶于水后加入碳酸钾溶液 分别加入硝酸按研磨闻气味
A.A B.B C.C D.D
16、下列常见物质显碱性的是( )
A.食醋 B.食盐水 C.肥皂水 D.柠檬水
二、填空题。
17、某同学将一朵紫色牵牛花泡在石灰水里,牵牛花很快就变成了蓝色,又将牵牛花泡在稀盐酸中,牵牛花又变成了红色,请你根据以上实验现象回答:
(1)该同学将紫色牵牛花泡在肥皂水里,牵牛花很快就变成了蓝色,据此可推断肥皂水显_____(填“酸性”或“碱性”)。
(2)该牵牛花的汁液_____(填“能”或“不能”)用作指示剂。
18、如图所示是稀释浓硫酸实验的示意图。
(1)写出图中a、b两种仪器的名称:a________;b________。
(2)b容器中所盛的试剂是________(填“水”或“浓硫酸”)。
(3)稀释时,若两种试剂添加顺序颠倒,将会发生__________________。
【联系与拓展】据媒体报道,有一村民在家里误将装在酒瓶中的浓硫酸当成白酒喝下,造成食道和胃严重损伤,这是因为浓硫酸具有__________。这一事件警示我们,家中存放或使用药物时应注意______________________________________________________。
19、已知可溶性钡盐有剧毒,透视胃病时,让病人口服BaSO4。如果误服BaCO3就会中毒,中毒的原因请用化学方程式来表示______。若解毒最好吃______等食物,若要解毒服用一种含Mg2+的药物,它的化学式为______。
20、日常使用的洗发剂和护发剂都有一定酸碱度,若使用不当,就会对头发造成损害。
(1)用pH试纸测定某溶液的酸碱度时,正确的操作方法是______
______ ;
(2)小华同学用pH试纸按正确操作测定护发剂和洗发剂的酸碱度,测得护发剂的pH略小于7,则护发剂显______性;测得洗发剂的pH略大于7,则洗发剂显_______性.
(3)弱酸性有益于头发的健康.想一想洗发时应先用_______剂,后用______剂。
21、日前,全球平均气温较工业化前已上升了1.1℃,其主要原因是自然界中的碳平衡被破坏。2020年9月22日,我国政府承诺:中国将力争于2030年前实现CO2排放达到峰值,2060年前实现碳中和,即通过各种方式抵消排放的CO2量,重新实现碳平衡。如图是碳循环和碳中和策略的示意图。
(1)人类进入工业化社会后,化石燃料的大量使用是碳平衡被破坏的主要原因之一,对此可采取的碳中和策略②有 。
(2)要实现我国政府提出的目标,除图中策略外,还可用化学方法人工捕获,如将空气通入氢氧化钾溶液反应生成碳酸钾和水。写出用氢氧化钾捕获CO2的化学方程式 。
(3)2020年12月下句,我国部分地区出现多年未遇的极寒天气,因此有人质疑:今年天气这么冷,地球气温真的在上升吗?对于这样的质疑,你是否认同?并说明理由: 。
三、综合应用题。
22、金属材料在生活中随处可见。某学习小组围绕金属材料展开项目式学习。
【项目一】金属的物理性质
(1)316不锈钢与组成它的纯金属相比,有良好的___________ 。
【项目二】金属的化学性质
(2)组员小王将打磨后的镁条放入硫酸铜溶液中,发生反应的化学方程式为__________ 。
组员小李意外发现镁条表面还有气泡产生,于是学习小组对此展开探究。
(3)小王用拇指堵住试管,收集一会气体之后伸入燃着的木条,发出尖锐的爆鸣声,说明该气体是__________。
【提出问题】为什么会产生该气体呢?
【作出猜想】硫酸铜溶液显酸性,所以放入镁条后会产生该气体。
【实验验证】
(4)用pH试纸测量硫酸铜溶液的pH,实验操作是__________ 。经测定,溶液pH<7,证实猜想正确。
【项目三】冶炼金属
(5)冶炼金属铁的原料有铁矿石、焦炭、__________、热空气。
铁的氧化物有FeO、Fe2O3、Fe3O4。组员小卫称取6.0g铁的氧化物混合样品,采用如图装置模拟炼铁过程(夹持装置省略),完全反应后,测得实验前后装置B增重4.4g。
(6)实验开始时先打开__________,关闭另一止水夹,让CO通一段时间。
(7)根据实验数据进行计算,该固体样品成分可能是 (填字母序号)。
A.FeO、Fe2O3 B.Fe2O3、Fe3O4
C.FeO、Fe3O4 D.FeO、Fe2O3、Fe3O4
23、在实验室里,可用如图装置进行CO还原Fe2O3的实验,并检验该反应的气体生成物。已知由一氧化碳发生装置得到的CO中混有CO2和H2O。
(1)写出装置C处尾气处理的方法______ (写一种即可);A装置中有关反应的化学方程式______ 。(写出一个即可)
(2)检验CO还原Fe2O3反应的气体生成物的现象是什么?
______ 。
(3)实验后取A中固体溶于水,滴加酚酞溶液,溶液变红色,请分析可能的原因:______ 。
(4)某钢铁厂用赤铁矿石炼铁。若该厂每天需消耗6000t含氧化铁80%的赤铁矿石,则理论上可日产含铁96%的生铁的质量是多少?(写出计算过程)
第7章 应用广泛的酸、碱、盐 基础研题(含答案)沪教版(全国)化学九年级下册
一、选择题。
1、下列实验方案中,设计合理的是( )
A.用酒精浸泡牵牛花自制酸碱指示剂
B.用过滤的方法将硬水转化为软水
C.用燃烧木条的方法制备纯净的二氧化碳气体
D.常温下用水区分一氧化碳和氮气
【答案】A
2、用稀盐酸除铁锈的原理是( )
A.FeO+2HCl===FeCl2+H2O B.FeO+2HCl===FeCl3+H2O
C.Fe2O3+6HCl===2FeCl2+3H2O D.Fe2O3+6HCl===2FeCl3+3H2O
【答案】D
3、不可能由两种元素组成的化合物是( )
A.氧化物 B.酸 C.碱 D.盐
【答案】C
4、按如图所示装置,玻璃棒末端固定一团喷有酚酞溶液的脱脂棉Y。先加入物质X,再塞上带玻璃棒的橡胶塞。片刻后,能观察到喷有酚酞溶液的脱脂棉Y变红,则物质X可能是( )
A.浓盐酸 B.浓氨水 C.浓醋酸 D.浓氢氧化钠溶液
【答案】B
5、向一定质量的Na2CO3和Na2SO4混合溶液中先后滴加BaCl2、HCl溶液,反应过程中加入溶液的质量与产生沉淀或气体的质量关系如图所示。下列说法错误的是( )
A. 0-a段溶液的pH始终不变
B. c点有两种沉淀
C. 生成硫酸钡沉淀的质量是2.33g
D. d点对应的溶液中溶质的成分为BaCl2和HCl
【答案】A
6、如图所示是室温下稀硫酸和氢氧化钠反应过程中的pH变化曲线。下列有关说法正确的是( )
A.图中X是氢氧化钠
B.图中a点的阴离子是OH-
C.向图中c点所示溶液中加入铁粉后,溶液中有气泡产生
D.稀硫酸与氢氧化钠溶液反应的化学方程式为:H2SO4+2NaOH═Na2SO4+H2O
【答案】C
7、柠檬酸(C6H8O7)是一种较强的有机酸,在水溶液中可以解离出来H+,从而呈现酸的通性,下列物质不能与柠檬酸反应的是( )
A.Fe2O3 B.CO2 C.CaCO3 D.Zn
【答案】B
8、下图为三种不同浓度的氢氧化钠溶液与对应浓度的盐酸反应的曲线。
下列说法正确的是( )
A.在a、b、c三种曲线所示的实验中,所用盐酸浓度越大,V时所得溶液的pH越大
B.在a曲线所示的实验中,若用酚酞做指示剂,酚酞溶液由红色变为无色
C.在a、b、c三种曲线所示的实验中,反应速率相同
D.在a、b、c三种曲线所示的实验中,溶液酸性由强到弱的顺序是a>b>c
【答案】A
9、下图是常见的几个实验操作,其中正确的是( )
A.加热液体药品 B.放置盛氢气的集气瓶
C.稀释浓硫酸 D.试管的洗涤
【答案】D
10、化肥和农药影响农作物的产量。下列说法正确的是( )
A.使用化肥越多,农作物产量越高
B.铵态氮肥与熟石灰混合使用可以提高肥效
C.大量使用农药会导致土壤和食品污染,因此要杜绝使用农药
D.适当增大蔬菜大棚内二氧化碳的浓度,可以促进蔬菜的光合作用
【答案】D
11、预防新型冠状病毒肺炎,常用84消毒液对环境进行消杀。常温下测得某84消毒液显碱性,其pH可能为( )
A.12 B.5 C.7 D.2
【答案】A
12、下列宏观事实的微观解释错误的是( )
A.墙内开花墙外香——分子是不断运动的
B.6000升氧气在加压的情况下可装入容积为40升的钢瓶中——分子体积变小
C.硫酸、盐酸有一些相似的性质原因——不同的酸溶液中都含有氢离子
D.一氧化碳能燃烧二氧化碳不能燃烧——分子构成不同
【答案】B
13、一些食物pH 的近似值范围如下:橘子汁3.~4.0;泡菜3.2~3.6;牛奶6.3~6.6;鸡蛋清7.6~8.0.下列说法中,不正确的是( )
A.鸡蛋清显碱性 B.胃酸过多的人应少吃泡菜
C.橘子汁能使紫色石蕊溶液变红 D.牛奶比橘子汁的酸性强
【答案】D
14、某工厂排出的废水pH小于7,并含有较多的Cu2+,对环境污染严重。从环保及回收利用考虑,较切合实际的治理方案是应适量加入( )
A.烧碱和纯碱 B.盐酸和铁粉
C.生石灰和铁粉 D.熟石灰和金属银
【答案】C
15、区分下列各组物质的两种方法均正确的是( )
选项 待区分物质 方法一 方法二
A 蒸馏水和氯化钾溶液 分别蒸干观察 分别加入硫酸铜溶液
B 氧气和二氧化碳 分别伸入燃着的小木条 分别闻气味
C 黄铜和铜 观察颜色 相互刻画比较硬度
D 氢氧化钠和熟石灰 分别溶于水后加入碳酸钾溶液 分别加入硝酸按研磨闻气味
A.A B.B C.C D.D
【答案】C
16、下列常见物质显碱性的是( )
A.食醋 B.食盐水 C.肥皂水 D.柠檬水
【答案】C
二、填空题。
17、某同学将一朵紫色牵牛花泡在石灰水里,牵牛花很快就变成了蓝色,又将牵牛花泡在稀盐酸中,牵牛花又变成了红色,请你根据以上实验现象回答:
(1)该同学将紫色牵牛花泡在肥皂水里,牵牛花很快就变成了蓝色,据此可推断肥皂水显_____(填“酸性”或“碱性”)。
(2)该牵牛花的汁液_____(填“能”或“不能”)用作指示剂。
【答案】碱性 能
18、如图所示是稀释浓硫酸实验的示意图。
(1)写出图中a、b两种仪器的名称:a________;b________。
(2)b容器中所盛的试剂是________(填“水”或“浓硫酸”)。
(3)稀释时,若两种试剂添加顺序颠倒,将会发生__________________。
【联系与拓展】据媒体报道,有一村民在家里误将装在酒瓶中的浓硫酸当成白酒喝下,造成食道和胃严重损伤,这是因为浓硫酸具有__________。这一事件警示我们,家中存放或使用药物时应注意______________________________________________________。
【答案】(1)玻璃棒 量筒 (2)浓硫酸 (3)酸液飞溅
【联系与拓展】腐蚀性 存放时要贴好标签,放在安全的地方(或使用时要核对标签)
19、已知可溶性钡盐有剧毒,透视胃病时,让病人口服BaSO4。如果误服BaCO3就会中毒,中毒的原因请用化学方程式来表示______。若解毒最好吃______等食物,若要解毒服用一种含Mg2+的药物,它的化学式为______。
【答案】BaCO3+2HCl=BaCl2+CO2↑+H2O 牛奶 MgSO4
20、日常使用的洗发剂和护发剂都有一定酸碱度,若使用不当,就会对头发造成损害。
(1)用pH试纸测定某溶液的酸碱度时,正确的操作方法是______
______ ;
(2)小华同学用pH试纸按正确操作测定护发剂和洗发剂的酸碱度,测得护发剂的pH略小于7,则护发剂显______性;测得洗发剂的pH略大于7,则洗发剂显_______性.
(3)弱酸性有益于头发的健康.想一想洗发时应先用_______剂,后用______剂。
【答案】(1)在玻璃片或白瓷板上放片pH试纸,用玻璃棒蘸取待测液滴到试纸上,将试纸显示的颜色与标准比色卡对照得溶液的pH
(2) 酸 碱 (3) 洗发 护发
21、日前,全球平均气温较工业化前已上升了1.1℃,其主要原因是自然界中的碳平衡被破坏。2020年9月22日,我国政府承诺:中国将力争于2030年前实现CO2排放达到峰值,2060年前实现碳中和,即通过各种方式抵消排放的CO2量,重新实现碳平衡。如图是碳循环和碳中和策略的示意图。
(1)人类进入工业化社会后,化石燃料的大量使用是碳平衡被破坏的主要原因之一,对此可采取的碳中和策略②有 。
(2)要实现我国政府提出的目标,除图中策略外,还可用化学方法人工捕获,如将空气通入氢氧化钾溶液反应生成碳酸钾和水。写出用氢氧化钾捕获CO2的化学方程式 。
(3)2020年12月下句,我国部分地区出现多年未遇的极寒天气,因此有人质疑:今年天气这么冷,地球气温真的在上升吗?对于这样的质疑,你是否认同?并说明理由: 。
【答案】(1)开发新能源、减少化石燃料的使用;
(2);
(3)不认同,因为全球变暖是全球性的气候变化,是大趋势,极寒天气的出现,可能只是偶然性的天气现象。
三、综合应用题。
22、金属材料在生活中随处可见。某学习小组围绕金属材料展开项目式学习。
【项目一】金属的物理性质
(1)316不锈钢与组成它的纯金属相比,有良好的___________ 。
【项目二】金属的化学性质
(2)组员小王将打磨后的镁条放入硫酸铜溶液中,发生反应的化学方程式为__________ 。
组员小李意外发现镁条表面还有气泡产生,于是学习小组对此展开探究。
(3)小王用拇指堵住试管,收集一会气体之后伸入燃着的木条,发出尖锐的爆鸣声,说明该气体是__________。
【提出问题】为什么会产生该气体呢?
【作出猜想】硫酸铜溶液显酸性,所以放入镁条后会产生该气体。
【实验验证】
(4)用pH试纸测量硫酸铜溶液的pH,实验操作是__________ 。经测定,溶液pH<7,证实猜想正确。
【项目三】冶炼金属
(5)冶炼金属铁的原料有铁矿石、焦炭、__________、热空气。
铁的氧化物有FeO、Fe2O3、Fe3O4。组员小卫称取6.0g铁的氧化物混合样品,采用如图装置模拟炼铁过程(夹持装置省略),完全反应后,测得实验前后装置B增重4.4g。
(6)实验开始时先打开__________,关闭另一止水夹,让CO通一段时间。
(7)根据实验数据进行计算,该固体样品成分可能是 (填字母序号)。
A.FeO、Fe2O3 B.Fe2O3、Fe3O4
C.FeO、Fe3O4 D.FeO、Fe2O3、Fe3O4
【答案】(1)硬度大、熔点低 (2) (3)氢气##
(4)在白瓷板或玻璃片上放一小片pH试纸,用玻璃棒蘸取溶液滴到pH试纸上,把试纸显示的颜色与标准比色卡比较,读出pH。
(5)石灰石 (6)K2 (7)ACD
23、在实验室里,可用如图装置进行CO还原Fe2O3的实验,并检验该反应的气体生成物。已知由一氧化碳发生装置得到的CO中混有CO2和H2O。
(1)写出装置C处尾气处理的方法______ (写一种即可);A装置中有关反应的化学方程式______ 。(写出一个即可)
(2)检验CO还原Fe2O3反应的气体生成物的现象是什么?
______ 。
(3)实验后取A中固体溶于水,滴加酚酞溶液,溶液变红色,请分析可能的原因:______ 。
(4)某钢铁厂用赤铁矿石炼铁。若该厂每天需消耗6000t含氧化铁80%的赤铁矿石,则理论上可日产含铁96%的生铁的质量是多少?(写出计算过程)
【答案】(1) 加一个燃着的酒精灯或绑一个气球
或 或
(2)C处澄清石灰水变浑浊
(3)氢氧化钠、氢氧化钙、碳酸钠溶液均显碱性,均能使无色酚酞试液变色
(4)解:设理论上可日产含铁96%的生铁的质量是x
x=3500t
答:理论上可日产含铁96%的生铁的质量是3500t。
