第7章应用广泛的酸、碱、盐综合练习(含答案)-2023-2024学年九年级化学沪教版下册
文档属性
| 名称 | 第7章应用广泛的酸、碱、盐综合练习(含答案)-2023-2024学年九年级化学沪教版下册 |

|
|
| 格式 | docx | ||
| 文件大小 | 175.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-02-20 00:00:00 | ||
图片预览

文档简介
九年级化学第7章《应用广泛的酸、碱、盐》复习综合练习
一、选择题:
1、下列物质与水充分相混后,能使紫色石蕊试液变蓝色的是( )
A.H2SO4 B.NH3 C.NaCl D.Cu(OH)2
2、把某稀硫酸分为等体积的两份,放入两个烧杯中,分别加入等质量的甲、乙两种金属,反应后金属都没有剩余且生成的化合物中金属元素化合价都为+2,产生H2的质量随时间变化的趋势如图,下列说法正确的是( )
A.金属活动性甲>乙 B.相对原子质量甲>乙
C.反应硫酸的质量甲>乙 D.消耗金属的质量甲>乙
3、某物质可以用来作CO2气体的干燥剂,则该物质( )
A.能与CO2反应 B.是浓硫酸
C.能与水反应 D.能吸收空气中的水份,不与CO2反应
4、下列有关实验现象的描述或实验操作的叙述正确的是( )
A.镁在空气中燃烧,生成了白色的氧化镁
B.向一种无色溶液中加入 BaCl2 溶液发现有白色沉淀产生,再加入稀 HNO3,沉淀不溶解,由此确认该溶液中一定含有 SO42-
C.测定溶液 pH 值时,用玻璃棒蘸上一滴待测溶液到干燥的 pH 试纸上,再跟标准比色卡对照即可
D.打开浓 HCl 瓶盖,可观察到瓶口有白色烟雾
5、下列物质名称与化学式对应关系错误的是( )
A.烧碱—NaOH B.纯碱—Na2CO3
C.小苏打—NaHCO3 D.熟石灰—CaO
6、运用推理、归纳、类比、对比的方法得出下列结论,其中合理的是
A.浓硫酸、氢氧化钠固体都具有吸水性,所以都可以用来干燥氨气
B.单质由同种元素组成,所以由同种元素组成的纯净物一定是单质
C.Na+、Mg2+、C1-的最外层电子数均为8,由此得出离子的最外层电子数均为8
D.MnO2能让氯酸钾在较低的温度下快速产生氧气,说明反应速率加快的方法一定使用了催化剂
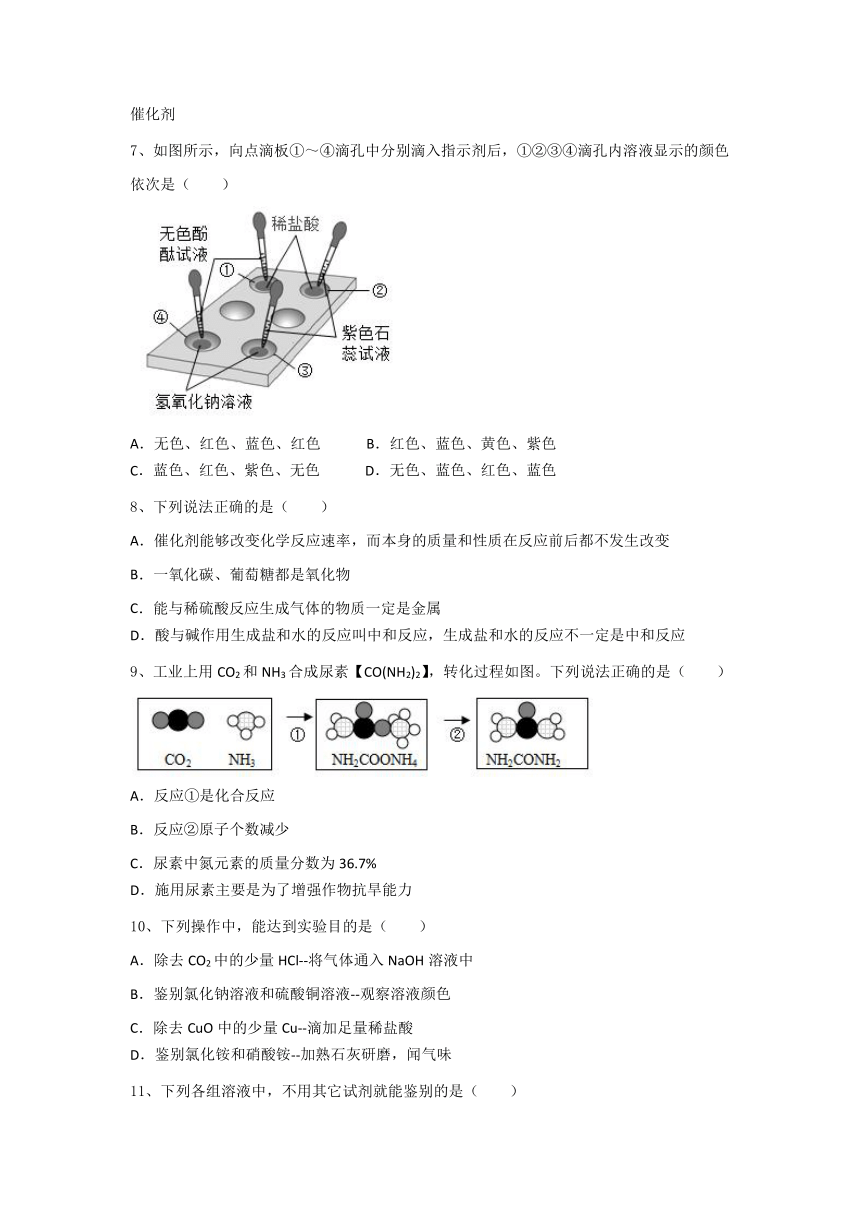
7、如图所示,向点滴板①~④滴孔中分别滴入指示剂后,①②③④滴孔内溶液显示的颜色依次是( )
A.无色、红色、蓝色、红色 B.红色、蓝色、黄色、紫色
C.蓝色、红色、紫色、无色 D.无色、蓝色、红色、蓝色
8、下列说法正确的是( )
A.催化剂能够改变化学反应速率,而本身的质量和性质在反应前后都不发生改变
B.一氧化碳、葡萄糖都是氧化物
C.能与稀硫酸反应生成气体的物质一定是金属
D.酸与碱作用生成盐和水的反应叫中和反应,生成盐和水的反应不一定是中和反应
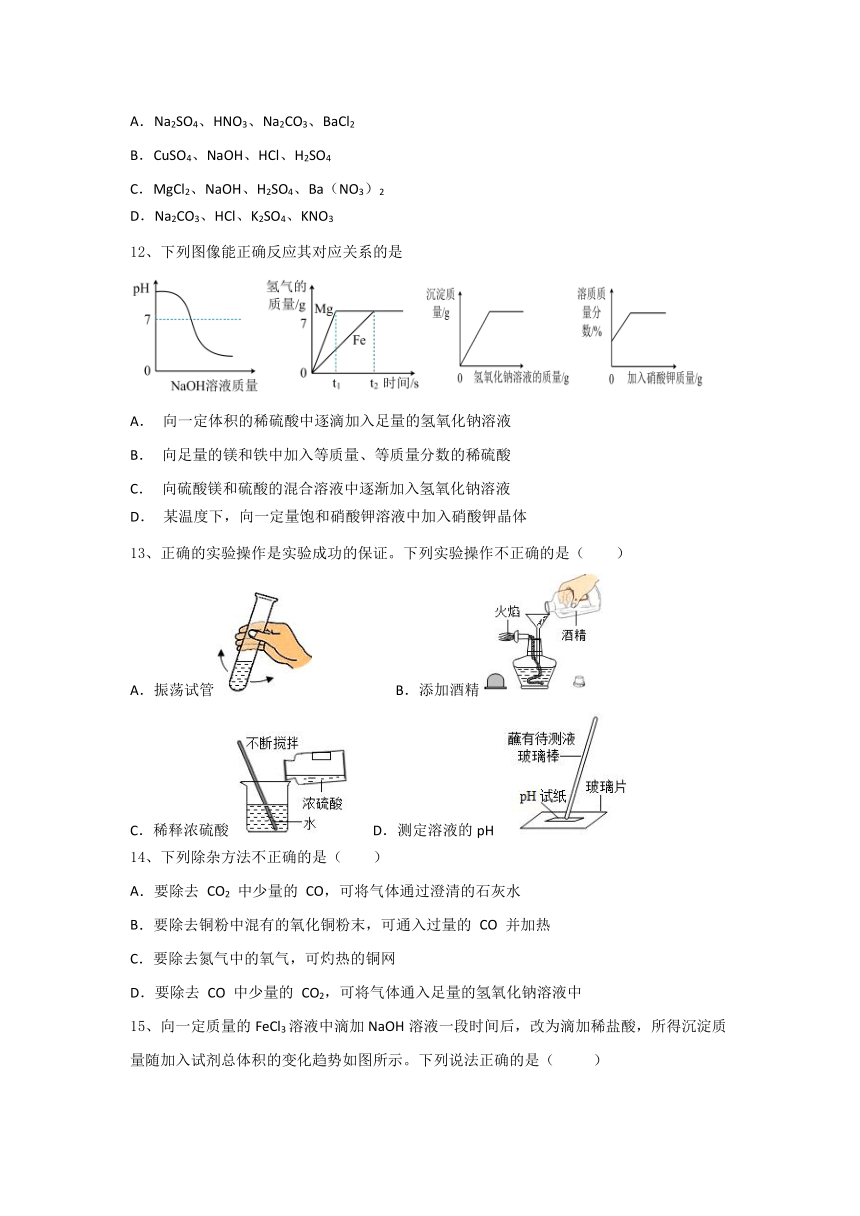
9、工业上用CO2和NH3合成尿素【CO(NH2)2】,转化过程如图。下列说法正确的是( )
A.反应①是化合反应
B.反应②原子个数减少
C.尿素中氮元素的质量分数为36.7%
D.施用尿素主要是为了增强作物抗旱能力
10、下列操作中,能达到实验目的是( )
A.除去CO2中的少量HCl--将气体通入NaOH溶液中
B.鉴别氯化钠溶液和硫酸铜溶液--观察溶液颜色
C.除去CuO中的少量Cu--滴加足量稀盐酸
D.鉴别氯化铵和硝酸铵--加熟石灰研磨,闻气味
11、下列各组溶液中,不用其它试剂就能鉴别的是( )
A.Na2SO4、HNO3、Na2CO3、BaCl2
B.CuSO4、NaOH、HCl、H2SO4
C.MgCl2、NaOH、H2SO4、Ba(NO3)2
D.Na2CO3、HCl、K2SO4、KNO3
12、下列图像能正确反应其对应关系的是
A. 向一定体积的稀硫酸中逐滴加入足量的氢氧化钠溶液
B. 向足量的镁和铁中加入等质量、等质量分数的稀硫酸
C. 向硫酸镁和硫酸的混合溶液中逐渐加入氢氧化钠溶液
D. 某温度下,向一定量饱和硝酸钾溶液中加入硝酸钾晶体
13、正确的实验操作是实验成功的保证。下列实验操作不正确的是( )
A.振荡试管 B.添加酒精
C.稀释浓硫酸 D.测定溶液的pH
14、下列除杂方法不正确的是( )
A.要除去 CO2 中少量的 CO,可将气体通过澄清的石灰水
B.要除去铜粉中混有的氧化铜粉末,可通入过量的 CO 并加热
C.要除去氮气中的氧气,可灼热的铜网
D.要除去 CO 中少量的 CO2,可将气体通入足量的氢氧化钠溶液中
15、向一定质量的FeCl3溶液中滴加NaOH溶液一段时间后,改为滴加稀盐酸,所得沉淀质量随加入试剂总体积的变化趋势如图所示。下列说法正确的是( )
A.a点时溶液中一定存在Fe3+
B.c点时所加试剂是NaOH溶液
C.加入试剂总体积为V1时,溶液中不存在NaOH
D.d点时溶液中的溶质不只是盐
二、非选择题:
16、金属钯是稀有的贵重金属之一,金属钯制成的首饰不仅有迷人的光彩,而且经得住岁月的磨砺。现有银(Ag)、铂(Pt)、钯(Pd)三种金属制成的戒指,某实验小组利用它们来探究三种金属的活动性。
(1)把钯戒指放入稀硫酸溶液中,戒指完好无损,可推测钯在金属活动性顺序表中位于铁之_____(填“前”或“后”)。
(2)如果将钯粉置于盐酸溶液中,边通入氧气边搅拌,钯粉溶解得到二氯化钯(PdCl2)溶液,该反应的化学方程式为 _____________________________。
(3)如上图所示,将银、铂戒指分别放入甲、乙两烧杯中,一段时间后取出,发现只有银戒指表面有明显变化,推测甲烧杯中还可能出现的现象是________________________ ,通过该实验判断,银、铂、钯的金属活动性由强到弱顺序为 __________。
17、A I是初中化学常见的物质,它们之间有如图所示的转化关系,部分反应条件已略去,已知人和动植物的呼吸离不开物质B,反应②是化合反应且G的溶解度随温度升高而降低,F、G、H中滴加酚酞溶液都显红色。
(1)物质B的化学式是 ;
(2)反应④的基本类型应是 ;
(3)写出符合反应③的化学方程式: ;
(4)写出物质G的一种应用实例 。
18、今年3月22日是第二十二届“世界水日”,3月22﹣28日是第二十七届“中国水周”.联合国确定“世界水日”的宣传主题是“水与能源”(Water and Energy).水与人类的生活和生产密切相关。如图为我国《生活饮用水国家标准》的部分内容,请回答下列问题。
(1)测得某地区合格饮用水的pH=6.6,可知略呈_____性(填“酸”或“碱”),通常是因为水中有一种常见弱酸是_____(填化学式)。
(2)生活饮用水中的铝元素以铝离子形式存在,则3个铝离子表示为_____,铁元素以硫酸铁形式存在,硫酸铁的化学式为_____。
(3)天然水中含有许多杂质,可利用吸附、沉淀、过滤和蒸馏等方法净化,其中净化程度最高的方法是_____。
(4)(选做)天然水的硬度较大时,煮沸后饮用是降低硬度的方法之一,其化学原理是Ca(HCO3)2、Mg(HCO3)2加热后发生反应生成了水垢.Ca(HCO3)2加热分解为碳酸钙、二氧化碳和水,请写出化学方程式_____ ,Mg(HCO3)2加热后分解为氢氧化镁和二氧化碳,请写出化学方程式:
_____ ,因而水垢的主要成分有2种,请写出醋酸(用HAc代表醋酸)与水垢中碳酸钙反应的化学方程式_____ 。
(5)1升合格的生活饮用水中,均以CaCO3计算硬度,则钙元素的含量应不超过_____mg。
19、芬兰发明家马蒂·努尔米亚发明了一种中和处理二氧化碳的新方法,是将二氧化碳从火力发电厂的烟气中分离出来,放入含有长石成分的水溶液里进行中和处理。在反应过程中,长石的成分不仅能吸收二氧化碳,同时还会生成一些有用的副产品,这些副产品可用作生产铝的原材料和玻璃制造业。其主要流程可示意如下:
(1)发明家将CO2从火力发电厂的烟气中分离出来,通入含有长石的水溶液里吸收,从环保的角度看,这样做的意义是 ;
(2)长石是地壳中最常见的矿石,含量高达60%。长石主要包括钾长石(KAlSi3O8)、钠长石(NaAlSi3O8)、钙长石(CaAl2Si2O8)。若钙长石吸收CO2的反应方程式为:。
请模仿钙长石,写出钠长石吸收CO2的化学反应方程式 ;
(3)若A的pH小于7,试写出一个符合反应②的化学方程式 ;
(4)溶液M中的溶质为 ,B可用作改良酸性土壤,则B为 ;操作③主要目的为 。
参考答案
一、选择题:
1、 B 2、 C 3、D 4、 C 5、 D
6、B 7、A 8、D 9、A 10、B
11、A 12、B 13、B 14、A 15、C
二、非选择题:
16、(1) 后 2Pd+4HCl+O2=2PdCl2+2H2O
(2)有白色沉淀 (3)银 钯 铂
17、O2 复分解反应 2NaOH+CO2=Na2CO3+H2O 配制农药波尔多液
18、(1)酸;H2CO3 (2)3Al3+;Fe2(SO4)3 (3)蒸馏
(4)Ca(HCO3)2CaCO3↓+CO2↑+H2O;
Mg(HCO3)2Mg(OH)2↓+2CO2↑;
CaCO3+2 HAc=Ca(Ac)2+CO2↑+H2O(5)180
19、(1)减少二氧化碳的排放,减缓温室效应
(2)
(3)
(4) Ca(HCO3)2、NaHCO3、KHCO3 Ca(OH)2 从溶液中提取晶体
一、选择题:
1、下列物质与水充分相混后,能使紫色石蕊试液变蓝色的是( )
A.H2SO4 B.NH3 C.NaCl D.Cu(OH)2
2、把某稀硫酸分为等体积的两份,放入两个烧杯中,分别加入等质量的甲、乙两种金属,反应后金属都没有剩余且生成的化合物中金属元素化合价都为+2,产生H2的质量随时间变化的趋势如图,下列说法正确的是( )
A.金属活动性甲>乙 B.相对原子质量甲>乙
C.反应硫酸的质量甲>乙 D.消耗金属的质量甲>乙
3、某物质可以用来作CO2气体的干燥剂,则该物质( )
A.能与CO2反应 B.是浓硫酸
C.能与水反应 D.能吸收空气中的水份,不与CO2反应
4、下列有关实验现象的描述或实验操作的叙述正确的是( )
A.镁在空气中燃烧,生成了白色的氧化镁
B.向一种无色溶液中加入 BaCl2 溶液发现有白色沉淀产生,再加入稀 HNO3,沉淀不溶解,由此确认该溶液中一定含有 SO42-
C.测定溶液 pH 值时,用玻璃棒蘸上一滴待测溶液到干燥的 pH 试纸上,再跟标准比色卡对照即可
D.打开浓 HCl 瓶盖,可观察到瓶口有白色烟雾
5、下列物质名称与化学式对应关系错误的是( )
A.烧碱—NaOH B.纯碱—Na2CO3
C.小苏打—NaHCO3 D.熟石灰—CaO
6、运用推理、归纳、类比、对比的方法得出下列结论,其中合理的是
A.浓硫酸、氢氧化钠固体都具有吸水性,所以都可以用来干燥氨气
B.单质由同种元素组成,所以由同种元素组成的纯净物一定是单质
C.Na+、Mg2+、C1-的最外层电子数均为8,由此得出离子的最外层电子数均为8
D.MnO2能让氯酸钾在较低的温度下快速产生氧气,说明反应速率加快的方法一定使用了催化剂
7、如图所示,向点滴板①~④滴孔中分别滴入指示剂后,①②③④滴孔内溶液显示的颜色依次是( )
A.无色、红色、蓝色、红色 B.红色、蓝色、黄色、紫色
C.蓝色、红色、紫色、无色 D.无色、蓝色、红色、蓝色
8、下列说法正确的是( )
A.催化剂能够改变化学反应速率,而本身的质量和性质在反应前后都不发生改变
B.一氧化碳、葡萄糖都是氧化物
C.能与稀硫酸反应生成气体的物质一定是金属
D.酸与碱作用生成盐和水的反应叫中和反应,生成盐和水的反应不一定是中和反应
9、工业上用CO2和NH3合成尿素【CO(NH2)2】,转化过程如图。下列说法正确的是( )
A.反应①是化合反应
B.反应②原子个数减少
C.尿素中氮元素的质量分数为36.7%
D.施用尿素主要是为了增强作物抗旱能力
10、下列操作中,能达到实验目的是( )
A.除去CO2中的少量HCl--将气体通入NaOH溶液中
B.鉴别氯化钠溶液和硫酸铜溶液--观察溶液颜色
C.除去CuO中的少量Cu--滴加足量稀盐酸
D.鉴别氯化铵和硝酸铵--加熟石灰研磨,闻气味
11、下列各组溶液中,不用其它试剂就能鉴别的是( )
A.Na2SO4、HNO3、Na2CO3、BaCl2
B.CuSO4、NaOH、HCl、H2SO4
C.MgCl2、NaOH、H2SO4、Ba(NO3)2
D.Na2CO3、HCl、K2SO4、KNO3
12、下列图像能正确反应其对应关系的是
A. 向一定体积的稀硫酸中逐滴加入足量的氢氧化钠溶液
B. 向足量的镁和铁中加入等质量、等质量分数的稀硫酸
C. 向硫酸镁和硫酸的混合溶液中逐渐加入氢氧化钠溶液
D. 某温度下,向一定量饱和硝酸钾溶液中加入硝酸钾晶体
13、正确的实验操作是实验成功的保证。下列实验操作不正确的是( )
A.振荡试管 B.添加酒精
C.稀释浓硫酸 D.测定溶液的pH
14、下列除杂方法不正确的是( )
A.要除去 CO2 中少量的 CO,可将气体通过澄清的石灰水
B.要除去铜粉中混有的氧化铜粉末,可通入过量的 CO 并加热
C.要除去氮气中的氧气,可灼热的铜网
D.要除去 CO 中少量的 CO2,可将气体通入足量的氢氧化钠溶液中
15、向一定质量的FeCl3溶液中滴加NaOH溶液一段时间后,改为滴加稀盐酸,所得沉淀质量随加入试剂总体积的变化趋势如图所示。下列说法正确的是( )
A.a点时溶液中一定存在Fe3+
B.c点时所加试剂是NaOH溶液
C.加入试剂总体积为V1时,溶液中不存在NaOH
D.d点时溶液中的溶质不只是盐
二、非选择题:
16、金属钯是稀有的贵重金属之一,金属钯制成的首饰不仅有迷人的光彩,而且经得住岁月的磨砺。现有银(Ag)、铂(Pt)、钯(Pd)三种金属制成的戒指,某实验小组利用它们来探究三种金属的活动性。
(1)把钯戒指放入稀硫酸溶液中,戒指完好无损,可推测钯在金属活动性顺序表中位于铁之_____(填“前”或“后”)。
(2)如果将钯粉置于盐酸溶液中,边通入氧气边搅拌,钯粉溶解得到二氯化钯(PdCl2)溶液,该反应的化学方程式为 _____________________________。
(3)如上图所示,将银、铂戒指分别放入甲、乙两烧杯中,一段时间后取出,发现只有银戒指表面有明显变化,推测甲烧杯中还可能出现的现象是________________________ ,通过该实验判断,银、铂、钯的金属活动性由强到弱顺序为 __________。
17、A I是初中化学常见的物质,它们之间有如图所示的转化关系,部分反应条件已略去,已知人和动植物的呼吸离不开物质B,反应②是化合反应且G的溶解度随温度升高而降低,F、G、H中滴加酚酞溶液都显红色。
(1)物质B的化学式是 ;
(2)反应④的基本类型应是 ;
(3)写出符合反应③的化学方程式: ;
(4)写出物质G的一种应用实例 。
18、今年3月22日是第二十二届“世界水日”,3月22﹣28日是第二十七届“中国水周”.联合国确定“世界水日”的宣传主题是“水与能源”(Water and Energy).水与人类的生活和生产密切相关。如图为我国《生活饮用水国家标准》的部分内容,请回答下列问题。
(1)测得某地区合格饮用水的pH=6.6,可知略呈_____性(填“酸”或“碱”),通常是因为水中有一种常见弱酸是_____(填化学式)。
(2)生活饮用水中的铝元素以铝离子形式存在,则3个铝离子表示为_____,铁元素以硫酸铁形式存在,硫酸铁的化学式为_____。
(3)天然水中含有许多杂质,可利用吸附、沉淀、过滤和蒸馏等方法净化,其中净化程度最高的方法是_____。
(4)(选做)天然水的硬度较大时,煮沸后饮用是降低硬度的方法之一,其化学原理是Ca(HCO3)2、Mg(HCO3)2加热后发生反应生成了水垢.Ca(HCO3)2加热分解为碳酸钙、二氧化碳和水,请写出化学方程式_____ ,Mg(HCO3)2加热后分解为氢氧化镁和二氧化碳,请写出化学方程式:
_____ ,因而水垢的主要成分有2种,请写出醋酸(用HAc代表醋酸)与水垢中碳酸钙反应的化学方程式_____ 。
(5)1升合格的生活饮用水中,均以CaCO3计算硬度,则钙元素的含量应不超过_____mg。
19、芬兰发明家马蒂·努尔米亚发明了一种中和处理二氧化碳的新方法,是将二氧化碳从火力发电厂的烟气中分离出来,放入含有长石成分的水溶液里进行中和处理。在反应过程中,长石的成分不仅能吸收二氧化碳,同时还会生成一些有用的副产品,这些副产品可用作生产铝的原材料和玻璃制造业。其主要流程可示意如下:
(1)发明家将CO2从火力发电厂的烟气中分离出来,通入含有长石的水溶液里吸收,从环保的角度看,这样做的意义是 ;
(2)长石是地壳中最常见的矿石,含量高达60%。长石主要包括钾长石(KAlSi3O8)、钠长石(NaAlSi3O8)、钙长石(CaAl2Si2O8)。若钙长石吸收CO2的反应方程式为:。
请模仿钙长石,写出钠长石吸收CO2的化学反应方程式 ;
(3)若A的pH小于7,试写出一个符合反应②的化学方程式 ;
(4)溶液M中的溶质为 ,B可用作改良酸性土壤,则B为 ;操作③主要目的为 。
参考答案
一、选择题:
1、 B 2、 C 3、D 4、 C 5、 D
6、B 7、A 8、D 9、A 10、B
11、A 12、B 13、B 14、A 15、C
二、非选择题:
16、(1) 后 2Pd+4HCl+O2=2PdCl2+2H2O
(2)有白色沉淀 (3)银 钯 铂
17、O2 复分解反应 2NaOH+CO2=Na2CO3+H2O 配制农药波尔多液
18、(1)酸;H2CO3 (2)3Al3+;Fe2(SO4)3 (3)蒸馏
(4)Ca(HCO3)2CaCO3↓+CO2↑+H2O;
Mg(HCO3)2Mg(OH)2↓+2CO2↑;
CaCO3+2 HAc=Ca(Ac)2+CO2↑+H2O(5)180
19、(1)减少二氧化碳的排放,减缓温室效应
(2)
(3)
(4) Ca(HCO3)2、NaHCO3、KHCO3 Ca(OH)2 从溶液中提取晶体
