化学沪教版九下课后练习:6.3 物质的溶解性(含答案)
文档属性
| 名称 | 化学沪教版九下课后练习:6.3 物质的溶解性(含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 115.4KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-03-14 00:00:00 | ||
图片预览




文档简介
6.3 物质的溶解性
一、单选题
1.如图所示图象与对应说法相一致的是( )
A.向20℃饱和石灰水中加少量生石灰
B.向一定量的MnO2中加入双氧水
C.向盐酸溶液中不断加水
D.高温加热一定量的碳和氧化铜
2.溶液对人类的生产、生活都有很重要的意义。下列关于溶液的说法正确的是( )
A.溶液组成中一定含有水
B.均一、稳定的液体都是溶液
C.溶质可为固体、液体或气体
D.饱和溶液就是不能再溶解任何物质的溶液
3.一定温度下,向图1烧杯中加入一定量的水,如图Ⅱ所示,所得溶液与原溶液相比,下列判断一定正确的是( )
A.所得溶液是不饱和溶液 B.溶质的质量分数变大
C.溶质的质量增加 D.溶质的溶解度变大
4.如图是A、B两种固体物质的溶解度曲线下列说法中错误的是( )
A.t1℃时A、B的溶解度相等
B.t2℃时,A的饱和溶液中溶质的质量分数为 a 100 ×100%
C.A、B的溶解度都随温度升高而增大
D.将t2℃时B的饱和溶液降温到t1℃时,溶液变稀了
5.25℃时,向一定量接近饱和的硝酸钾溶液中逐渐加入硝酸钾固体,则下列图像能正确表示此过程溶质质量变化规律的是( )
A. B.
C. D.
6.甲和乙两种固体物质的溶解度曲线如图所示。下列叙述正确的是( )
A.甲的溶解度随温度的升高而增大
B.45℃时,加热甲的饱和溶液会析出晶体
C.20℃时,往50g水中加入20g乙物质,充分溶解后,得到70g溶液
D.40℃时,甲、乙两种物质的溶液分别降温到10℃,析出晶体的质量甲一定大于乙
7.甲、乙两种不含结晶水的固体物质的溶解度曲线如图所示。下列说法中错误的是( )
A.在t1℃时,甲、乙两物质溶解度相等
B.将t2℃时甲、乙物质的饱和溶液降温,甲析出的晶体比乙多
C.将t1℃时乙的饱和溶液升温到t2℃时,溶质的质量分数不变
D.将t2℃时甲、乙物质的饱和溶液降温,都会析出晶体
8.如图为KNO3、NaCl两种物质的溶解度曲线,下列说法正确的是( )
A.a1℃时,向100g水中加入20gKNO3,充分溶解后所得溶液是饱和溶液
B.KNO3和NaCl的溶解度相等
C.当KNO3中含有少量NaCl时,可以用蒸发结晶的方法提纯KNO3
D.将a2℃时等质量的NaCl与KNO3的饱和溶液降温到a1℃,所得溶液中溶质质量NaCl大于KNO3
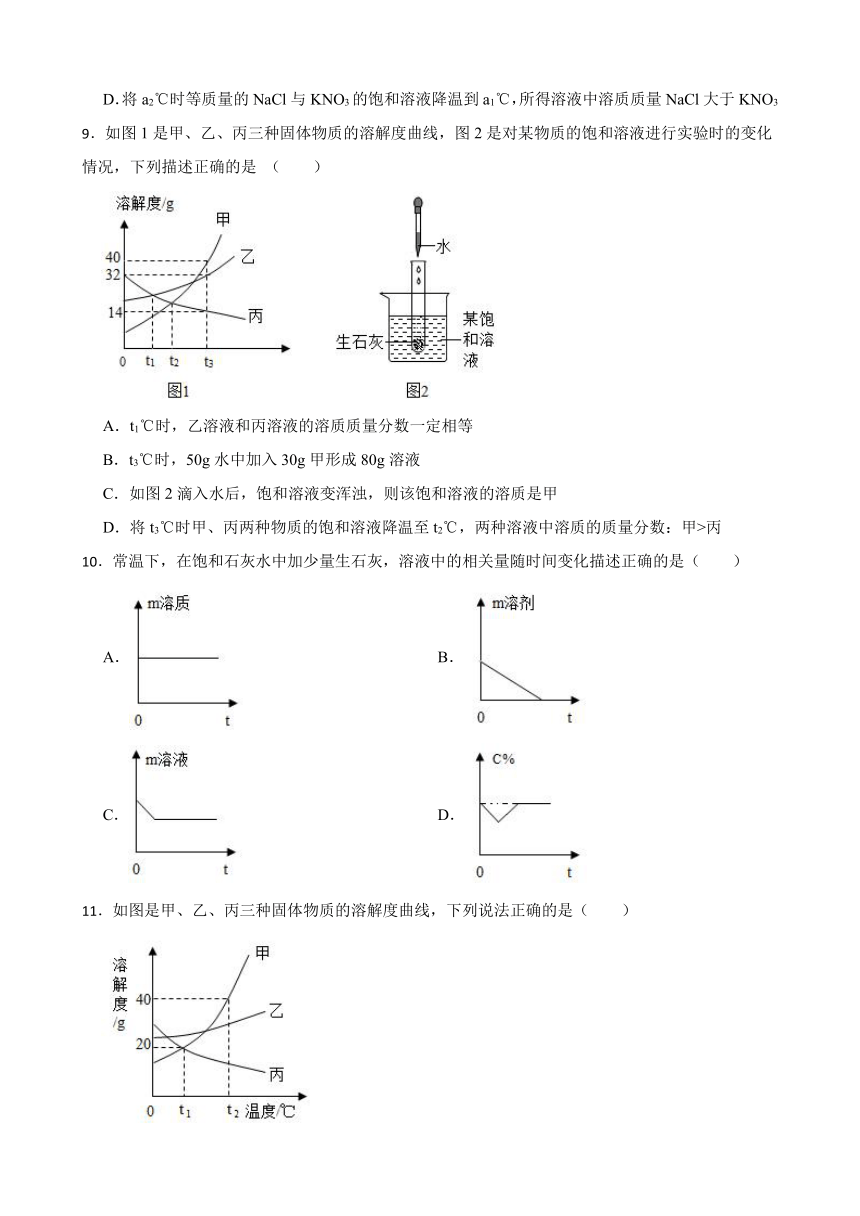
9.如图1是甲、乙、丙三种固体物质的溶解度曲线,图2是对某物质的饱和溶液进行实验时的变化情况,下列描述正确的是 ( )
A.t1℃时,乙溶液和丙溶液的溶质质量分数一定相等
B.t3℃时,50g水中加入30g甲形成80g溶液
C.如图2滴入水后,饱和溶液变浑浊,则该饱和溶液的溶质是甲
D.将t3℃时甲、丙两种物质的饱和溶液降温至t2℃,两种溶液中溶质的质量分数:甲>丙
10.常温下,在饱和石灰水中加少量生石灰,溶液中的相关量随时间变化描述正确的是( )
A. B.
C. D.
11.如图是甲、乙、丙三种固体物质的溶解度曲线,下列说法正确的是( )
A.三种物质的溶解度都随温度升高而增大
B.t1℃时20g丙加入50g水中,充分搅拌得到70g溶液
C.甲的饱和溶液中混有少量乙,可通过降温结晶获得较纯净的甲
D.t2℃时三种物质的饱和溶液降温到t1℃,所得溶液中甲和丙的溶质质量分数相等
12.如图是a、b、c三种物质的溶解度曲线,下列说法正确的是( )
A.a、c物质溶解度相等
B.将t2℃a、b、c的饱和溶液降温至t1℃,析出晶体的质量a>b>c
C.t2℃时,a、b、c的饱和溶液蒸发相同质量的水,析出晶体质量a>b>c
D.通过降温将c的不饱和溶液变为饱和溶液
二、填空题
13.根据给出的KNO3和NaCl两种物质的溶解度表、溶解度曲线,回答问题。
温度(℃) 0 20 40 60 80 100
溶解度 (g/100g水) KNO3 13.3 31.6 64.0 110.0 169.0 246.0
NaCl 35.7 36.0 36.6 37.3 38.4 39.8
(1)在80℃时,NaCl的溶解度为 g;
(2)在35℃时,KNO3和NaCl两种物质中,溶解度较大的是 ;
(3)将80gKNO3、20gNaCl分别放入100g60℃的水中,充分搅拌,再到20℃,下列有关说法中,正确的是_______________。
A.0℃时有部分KNO3与溶液共存
B.降温到20℃时只有KNO3析出
C.降温到20℃时NaCl已经饱和
14.如图是A,B,C 三种物质的溶解度曲线,回答下列问题:
①A、B 两种物质在 ℃时溶解度相同。
②t2℃时,B 物质的溶解度是 。
③t2℃时,等质量的三种饱和溶液中溶剂质量最少的是 。
④t2℃时,将三种物质各 ag 分别加入到 100g 水中,充分溶解后,若只有一种物质能形成饱和溶液,则a的取值范围是 。(用“ > ”、“ < ”、“ ≤”、“ ≥”、“ = ”表示)
⑤A中混有少量 B,要得到较纯净的A,可采取的方法是 。
⑥A的不饱和溶液变成饱和,可采用的方法是 。(写一种)
⑦如图烧杯甲中盛有饱和的C溶液。现向烧杯乙中加入生石灰后,烧杯甲中有晶体析出,可能的原因是 。
⑧t2℃时,将三种物质的饱和溶液各100g,分别加热蒸发10g水后,再恢复到 t2℃,剩余溶液的质量由大到小的顺序是 ,此时A的溶质质量分数是 。(列式即可)
15.甲、乙两种固体的溶解度曲线如图所示。 ℃时,甲、乙的饱和溶液中溶质的质量分数相等;40℃时,将等质量的甲、乙饱和溶液分别蒸发等质量的水,则析出固体的质量甲 乙(填“大于”“小于”或“等于”);40℃时,将60g甲饱和溶液稀释到20%,需要加水的质量为 g。
16.将下列各名词填在与之相对应的空格中(填写序号)
①溶解 ②挥发性 ③酸性 ④碱性 ⑤乳化 ⑥潮解 ⑦结晶 ⑧升华
A.氢氧化钠固体露置在空气中,表面变潮湿是 现象;
B.打开装有浓盐酸的试剂瓶瓶塞,瓶口出现白雾,这是浓盐酸的 造成的;
C.用洗去餐具上的油污时,洗洁精起到了 作用;
D.冷却热的硝酸钾饱和溶液,出现晶体的过程叫做 ;
E.由于熟石灰的 ,所以不能与铵盐混合使用。
17.将NH4Cl与少量NaCl的混合溶液降温,NH4Cl晶体大量析出,而NaCl却仍留在了溶液中.根据下图的溶解度曲线,你认为NH4Cl先结晶的原因可能是什么?
.
18.化学源于生活,生活中蕴含着许多化学知识。
(1)用洗涤剂去除油污,是利用洗涤剂的 作用。
(2)邵阳地区的生活用水多是硬水,生活中常用 的方法降低水的硬度。
(3)打开汽水瓶盖时,汽水会自动喷出来,说明气体在水中的溶解度随 而减小。
(4)医生给胃酸过多的病人所开处方中,常包括含 Al(OH)3 的药物,试用化学方程式表示其治疗原理: 。
三、综合题
19.溶液在日常生活、工农业生产和科学研究中具有广泛的用途。
(1)溶液的溶质可以是固体,也可以是 或气体;生理盐水是医疗上常用的一种溶液,其溶质为 (填化学式)。
(2)下图是利用海水提取粗盐的过程:
上图中①是 池(填“结晶”或“冷却”)。
(3)配制溶质的质量分数为5%的氯化钠溶液。配制步骤:①称量和量取②溶解③计算④装入试剂瓶贴好标签。配制上述溶液的正确顺序是 (填序号)。
(4)如图为甲、乙两种固体物质的溶解度曲线。
①溶解度随温度升高而增大的物质是 (填“甲”或“乙”)。
②将t2℃时的甲、乙两种物质的饱和溶液降温至t1℃,所得溶液中溶质的质量分数甲 乙(填“<”、“=”或“>”)。
③t1℃时,在50g水中加入19g乙固体,充分搅拌后得到 (填“饱和”或“不饱和”)溶液,此时该溶液中溶质的质量分数为 (计算结果精确到0.1%)。
20.一包白色固体,可能含有氯化钠、碳酸钠、硫酸钠、氯化镁、氢氧化钠中的一种或几种,某兴趣小组为了确定其成分,进行了如下所示的实验:
(1)实验一:探究固体的成分
氢氧化钡溶液呈 (选填“酸”“碱”“中”)性。
(2)沉淀甲部分溶解的化学方程式为 。
(3)白色固体中一定含有的物质是 。
(4)实验二:拓展探究
“Y溶液”及“操作Ⅰ”分别是____。
A.稀硝酸、蒸发结晶 B.稀盐酸、蒸发结晶 C.氯化钙溶液、过滤
(5)若将溶液丙和溶液X混合,则下列说法正确的是____。
A.混合后若无沉淀产生,则所得溶液中一定含有氯化钠和氯化镁
B.混合后若产生白色沉淀,则最终所得上层溶液可能呈酸性
C.混合后若只产生气泡(生成的微溶物此处以沉淀形式存在),则所得上层溶液可能呈碱性
21.图1为甲、乙两种物质(均不含结晶水)的溶解度曲线图.请回答下列问题.
(1)在10℃时,甲的溶解度 乙的溶解度.(选填“>”“<”或“=”)
(2)在20℃时,向盛有50g水的烧杯中加入25g甲物质,充分搅拌后溶液质量是 g.
(3)取乙进行如图2实验,属于饱和溶液的是 ,溶质质量分数最大的是 .
22.青海省柴达木盆地的察尔汗盐湖是我国最大的天然内陆咸水湖,当地农民通过“冬天捞碱,夏天晒盐”获得大量湖盐。
(1)“夏天晒盐”中的“盐”其溶解度可用图中 来表示(填“a ”、或“b ”、或“c ”)。
(2)在t1℃时,三种物质的溶解度大小关系是 。
(3)在t2℃时,将40g 的a放入50g 水中充分搅拌,所得溶液质量为 g 。
(4)将t2℃ 时 的饱和溶液降温至 时,溶质的质量分数由大到小的顺序为 。
答案
1.【答案】B
2.【答案】C
3.【答案】C
4.【答案】B
5.【答案】D
6.【答案】B
7.【答案】B
8.【答案】D
9.【答案】D
10.【答案】D
11.【答案】C
12.【答案】C
13.【答案】(1)38.4
(2)KNO3
(3)A;B
14.【答案】t1;40g;A;20g≤a<40g;降温结晶;加溶质、减溶剂、降温;生石灰加入水中与水反应放热,温度升高,C 的溶解度减小,溶质析出;C>B>A; ×100%
15.【答案】20;大于;40
16.【答案】⑥;②;⑤;⑦;④
17.【答案】NH4Cl溶解度受温度影响较大,而NaCl溶解度受温度影响不大
18.【答案】(1)乳化
(2)煮沸
(3)压强减小(或气压减小)
(4)Al(OH)3+3HCl=AlCl3+3H2O
19.【答案】(1)液体;NaCl
(2)结晶
(3)③①②④
(4)甲;>;饱和;16.7%
20.【答案】(1)碱
(2)2HCl+Mg(OH)2=MgCl2+2H2O
(3)硫酸钠、氯化镁
(4)B
(5)A
21.【答案】(1)>
(2)70
(3)AC;B
22.【答案】(1)b
(2)b=c>a
(3)80
(4)b>a>c
一、单选题
1.如图所示图象与对应说法相一致的是( )
A.向20℃饱和石灰水中加少量生石灰
B.向一定量的MnO2中加入双氧水
C.向盐酸溶液中不断加水
D.高温加热一定量的碳和氧化铜
2.溶液对人类的生产、生活都有很重要的意义。下列关于溶液的说法正确的是( )
A.溶液组成中一定含有水
B.均一、稳定的液体都是溶液
C.溶质可为固体、液体或气体
D.饱和溶液就是不能再溶解任何物质的溶液
3.一定温度下,向图1烧杯中加入一定量的水,如图Ⅱ所示,所得溶液与原溶液相比,下列判断一定正确的是( )
A.所得溶液是不饱和溶液 B.溶质的质量分数变大
C.溶质的质量增加 D.溶质的溶解度变大
4.如图是A、B两种固体物质的溶解度曲线下列说法中错误的是( )
A.t1℃时A、B的溶解度相等
B.t2℃时,A的饱和溶液中溶质的质量分数为 a 100 ×100%
C.A、B的溶解度都随温度升高而增大
D.将t2℃时B的饱和溶液降温到t1℃时,溶液变稀了
5.25℃时,向一定量接近饱和的硝酸钾溶液中逐渐加入硝酸钾固体,则下列图像能正确表示此过程溶质质量变化规律的是( )
A. B.
C. D.
6.甲和乙两种固体物质的溶解度曲线如图所示。下列叙述正确的是( )
A.甲的溶解度随温度的升高而增大
B.45℃时,加热甲的饱和溶液会析出晶体
C.20℃时,往50g水中加入20g乙物质,充分溶解后,得到70g溶液
D.40℃时,甲、乙两种物质的溶液分别降温到10℃,析出晶体的质量甲一定大于乙
7.甲、乙两种不含结晶水的固体物质的溶解度曲线如图所示。下列说法中错误的是( )
A.在t1℃时,甲、乙两物质溶解度相等
B.将t2℃时甲、乙物质的饱和溶液降温,甲析出的晶体比乙多
C.将t1℃时乙的饱和溶液升温到t2℃时,溶质的质量分数不变
D.将t2℃时甲、乙物质的饱和溶液降温,都会析出晶体
8.如图为KNO3、NaCl两种物质的溶解度曲线,下列说法正确的是( )
A.a1℃时,向100g水中加入20gKNO3,充分溶解后所得溶液是饱和溶液
B.KNO3和NaCl的溶解度相等
C.当KNO3中含有少量NaCl时,可以用蒸发结晶的方法提纯KNO3
D.将a2℃时等质量的NaCl与KNO3的饱和溶液降温到a1℃,所得溶液中溶质质量NaCl大于KNO3
9.如图1是甲、乙、丙三种固体物质的溶解度曲线,图2是对某物质的饱和溶液进行实验时的变化情况,下列描述正确的是 ( )
A.t1℃时,乙溶液和丙溶液的溶质质量分数一定相等
B.t3℃时,50g水中加入30g甲形成80g溶液
C.如图2滴入水后,饱和溶液变浑浊,则该饱和溶液的溶质是甲
D.将t3℃时甲、丙两种物质的饱和溶液降温至t2℃,两种溶液中溶质的质量分数:甲>丙
10.常温下,在饱和石灰水中加少量生石灰,溶液中的相关量随时间变化描述正确的是( )
A. B.
C. D.
11.如图是甲、乙、丙三种固体物质的溶解度曲线,下列说法正确的是( )
A.三种物质的溶解度都随温度升高而增大
B.t1℃时20g丙加入50g水中,充分搅拌得到70g溶液
C.甲的饱和溶液中混有少量乙,可通过降温结晶获得较纯净的甲
D.t2℃时三种物质的饱和溶液降温到t1℃,所得溶液中甲和丙的溶质质量分数相等
12.如图是a、b、c三种物质的溶解度曲线,下列说法正确的是( )
A.a、c物质溶解度相等
B.将t2℃a、b、c的饱和溶液降温至t1℃,析出晶体的质量a>b>c
C.t2℃时,a、b、c的饱和溶液蒸发相同质量的水,析出晶体质量a>b>c
D.通过降温将c的不饱和溶液变为饱和溶液
二、填空题
13.根据给出的KNO3和NaCl两种物质的溶解度表、溶解度曲线,回答问题。
温度(℃) 0 20 40 60 80 100
溶解度 (g/100g水) KNO3 13.3 31.6 64.0 110.0 169.0 246.0
NaCl 35.7 36.0 36.6 37.3 38.4 39.8
(1)在80℃时,NaCl的溶解度为 g;
(2)在35℃时,KNO3和NaCl两种物质中,溶解度较大的是 ;
(3)将80gKNO3、20gNaCl分别放入100g60℃的水中,充分搅拌,再到20℃,下列有关说法中,正确的是_______________。
A.0℃时有部分KNO3与溶液共存
B.降温到20℃时只有KNO3析出
C.降温到20℃时NaCl已经饱和
14.如图是A,B,C 三种物质的溶解度曲线,回答下列问题:
①A、B 两种物质在 ℃时溶解度相同。
②t2℃时,B 物质的溶解度是 。
③t2℃时,等质量的三种饱和溶液中溶剂质量最少的是 。
④t2℃时,将三种物质各 ag 分别加入到 100g 水中,充分溶解后,若只有一种物质能形成饱和溶液,则a的取值范围是 。(用“ > ”、“ < ”、“ ≤”、“ ≥”、“ = ”表示)
⑤A中混有少量 B,要得到较纯净的A,可采取的方法是 。
⑥A的不饱和溶液变成饱和,可采用的方法是 。(写一种)
⑦如图烧杯甲中盛有饱和的C溶液。现向烧杯乙中加入生石灰后,烧杯甲中有晶体析出,可能的原因是 。
⑧t2℃时,将三种物质的饱和溶液各100g,分别加热蒸发10g水后,再恢复到 t2℃,剩余溶液的质量由大到小的顺序是 ,此时A的溶质质量分数是 。(列式即可)
15.甲、乙两种固体的溶解度曲线如图所示。 ℃时,甲、乙的饱和溶液中溶质的质量分数相等;40℃时,将等质量的甲、乙饱和溶液分别蒸发等质量的水,则析出固体的质量甲 乙(填“大于”“小于”或“等于”);40℃时,将60g甲饱和溶液稀释到20%,需要加水的质量为 g。
16.将下列各名词填在与之相对应的空格中(填写序号)
①溶解 ②挥发性 ③酸性 ④碱性 ⑤乳化 ⑥潮解 ⑦结晶 ⑧升华
A.氢氧化钠固体露置在空气中,表面变潮湿是 现象;
B.打开装有浓盐酸的试剂瓶瓶塞,瓶口出现白雾,这是浓盐酸的 造成的;
C.用洗去餐具上的油污时,洗洁精起到了 作用;
D.冷却热的硝酸钾饱和溶液,出现晶体的过程叫做 ;
E.由于熟石灰的 ,所以不能与铵盐混合使用。
17.将NH4Cl与少量NaCl的混合溶液降温,NH4Cl晶体大量析出,而NaCl却仍留在了溶液中.根据下图的溶解度曲线,你认为NH4Cl先结晶的原因可能是什么?
.
18.化学源于生活,生活中蕴含着许多化学知识。
(1)用洗涤剂去除油污,是利用洗涤剂的 作用。
(2)邵阳地区的生活用水多是硬水,生活中常用 的方法降低水的硬度。
(3)打开汽水瓶盖时,汽水会自动喷出来,说明气体在水中的溶解度随 而减小。
(4)医生给胃酸过多的病人所开处方中,常包括含 Al(OH)3 的药物,试用化学方程式表示其治疗原理: 。
三、综合题
19.溶液在日常生活、工农业生产和科学研究中具有广泛的用途。
(1)溶液的溶质可以是固体,也可以是 或气体;生理盐水是医疗上常用的一种溶液,其溶质为 (填化学式)。
(2)下图是利用海水提取粗盐的过程:
上图中①是 池(填“结晶”或“冷却”)。
(3)配制溶质的质量分数为5%的氯化钠溶液。配制步骤:①称量和量取②溶解③计算④装入试剂瓶贴好标签。配制上述溶液的正确顺序是 (填序号)。
(4)如图为甲、乙两种固体物质的溶解度曲线。
①溶解度随温度升高而增大的物质是 (填“甲”或“乙”)。
②将t2℃时的甲、乙两种物质的饱和溶液降温至t1℃,所得溶液中溶质的质量分数甲 乙(填“<”、“=”或“>”)。
③t1℃时,在50g水中加入19g乙固体,充分搅拌后得到 (填“饱和”或“不饱和”)溶液,此时该溶液中溶质的质量分数为 (计算结果精确到0.1%)。
20.一包白色固体,可能含有氯化钠、碳酸钠、硫酸钠、氯化镁、氢氧化钠中的一种或几种,某兴趣小组为了确定其成分,进行了如下所示的实验:
(1)实验一:探究固体的成分
氢氧化钡溶液呈 (选填“酸”“碱”“中”)性。
(2)沉淀甲部分溶解的化学方程式为 。
(3)白色固体中一定含有的物质是 。
(4)实验二:拓展探究
“Y溶液”及“操作Ⅰ”分别是____。
A.稀硝酸、蒸发结晶 B.稀盐酸、蒸发结晶 C.氯化钙溶液、过滤
(5)若将溶液丙和溶液X混合,则下列说法正确的是____。
A.混合后若无沉淀产生,则所得溶液中一定含有氯化钠和氯化镁
B.混合后若产生白色沉淀,则最终所得上层溶液可能呈酸性
C.混合后若只产生气泡(生成的微溶物此处以沉淀形式存在),则所得上层溶液可能呈碱性
21.图1为甲、乙两种物质(均不含结晶水)的溶解度曲线图.请回答下列问题.
(1)在10℃时,甲的溶解度 乙的溶解度.(选填“>”“<”或“=”)
(2)在20℃时,向盛有50g水的烧杯中加入25g甲物质,充分搅拌后溶液质量是 g.
(3)取乙进行如图2实验,属于饱和溶液的是 ,溶质质量分数最大的是 .
22.青海省柴达木盆地的察尔汗盐湖是我国最大的天然内陆咸水湖,当地农民通过“冬天捞碱,夏天晒盐”获得大量湖盐。
(1)“夏天晒盐”中的“盐”其溶解度可用图中 来表示(填“a ”、或“b ”、或“c ”)。
(2)在t1℃时,三种物质的溶解度大小关系是 。
(3)在t2℃时,将40g 的a放入50g 水中充分搅拌,所得溶液质量为 g 。
(4)将t2℃ 时 的饱和溶液降温至 时,溶质的质量分数由大到小的顺序为 。
答案
1.【答案】B
2.【答案】C
3.【答案】C
4.【答案】B
5.【答案】D
6.【答案】B
7.【答案】B
8.【答案】D
9.【答案】D
10.【答案】D
11.【答案】C
12.【答案】C
13.【答案】(1)38.4
(2)KNO3
(3)A;B
14.【答案】t1;40g;A;20g≤a<40g;降温结晶;加溶质、减溶剂、降温;生石灰加入水中与水反应放热,温度升高,C 的溶解度减小,溶质析出;C>B>A; ×100%
15.【答案】20;大于;40
16.【答案】⑥;②;⑤;⑦;④
17.【答案】NH4Cl溶解度受温度影响较大,而NaCl溶解度受温度影响不大
18.【答案】(1)乳化
(2)煮沸
(3)压强减小(或气压减小)
(4)Al(OH)3+3HCl=AlCl3+3H2O
19.【答案】(1)液体;NaCl
(2)结晶
(3)③①②④
(4)甲;>;饱和;16.7%
20.【答案】(1)碱
(2)2HCl+Mg(OH)2=MgCl2+2H2O
(3)硫酸钠、氯化镁
(4)B
(5)A
21.【答案】(1)>
(2)70
(3)AC;B
22.【答案】(1)b
(2)b=c>a
(3)80
(4)b>a>c
