化学沪教版九下课后练习:7.1 溶液的酸碱性(含答案)
文档属性
| 名称 | 化学沪教版九下课后练习:7.1 溶液的酸碱性(含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 82.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-03-14 00:00:00 | ||
图片预览



文档简介
7.1 溶液的酸碱性
一、单选题
1.常温下,下列说法错误的是( )
A.pH=2的溶液显酸性
B.pH=7的溶液显中性
C.溶液的pH由5变成2,其酸性减弱
D.pH>10的土壤不适于种植农作物,因为碱性太强
2.下列说法中正确的是( )
A.生铁和钢都属于金属材料
B.人呼出的气体中二氧化碳的含量比空气中低
C.酚酞溶液滴入稀盐酸变成红色
D.检查煤气泄漏用明火查看
3.某同学在化学晚会上用毛笔蘸取一种无色液体在一张白纸上书写了“化学魔术”四字,然后再喷上另一种无色液体,白纸上立即出现了红色的“化学魔术”四字.该同学所用的两种无色液体可能是( )
A.NaOH溶液、酚酞溶液
B.CuSO4溶液、NaOH溶液
C.紫色石蕊溶液、酚酞溶液
D.酚酞溶液、“雪碧”饮料
4.分析推理是化学学习中常用的思维方法,下列分析推理说法中,正确的是( )
A.各种酸溶液中都含有H+,所以酸溶液有许多相似的化学性质
B.中和反应生成盐和水,所以生成盐和水的反应一定是中和反应
C.碱溶液的pH大于7,所以pH大于7的溶液一定是碱溶液
D.有机物是指含碳元素的化合物,所以含碳元素的化合物一定都是有机物
5.绣球花的颜色与土壤酸碱度有关,当土壤呈酸性时花朵为蓝色。下列是不同土壤的pH,能让绣球花呈蓝色的是( )
A.pH=5.8 B.pH=9.6 C.pH=7.0 D.pH=12.1
6.根据你的生活经验和所学的化学知识,判断下列做法能达到目的是( )
A.煤炉火上放一盆水,就能防止CO中毒
B.用无色酚酞试液检验溶液是否显酸性
C.用石灰乳与硫酸铜溶液混合配制防治植物病害的波尔多液
D.用燃烧的小木条放入集气瓶中来检验CO2是否集满
7.质量为50g溶质质量分数为20%的氢氧化钾溶液和质量为50g溶质质量分数为20%的稀硫酸混合,所得溶液的pH( )
A.小于7 B.等于7 C.大于7 D.不确定
8.下列“不一定”的说法正确的是( )
①化合物中的某种元素变为单质不一定要通过分解反应
②在一定的条件下二氧化碳与水反应不一定生成碳酸
③能使紫色石蕊试液变蓝色的物质不一定是碱
④物质在燃烧时不一定产生火焰,灭火时不一定要将温度降到着火点以下.
A.①②③④ B.②③④ C.①③④ D.①③
9.下列离子组合能在pH=12的溶液中大量共存的是( )
A.K+、Cu2+、SO42﹣、Cl﹣ B.K+、Na+、NO3﹣、Cl﹣
C.CO32﹣、H+、Na+、Cl﹣ D.Ba2+、Cl﹣、Na+、SO42﹣
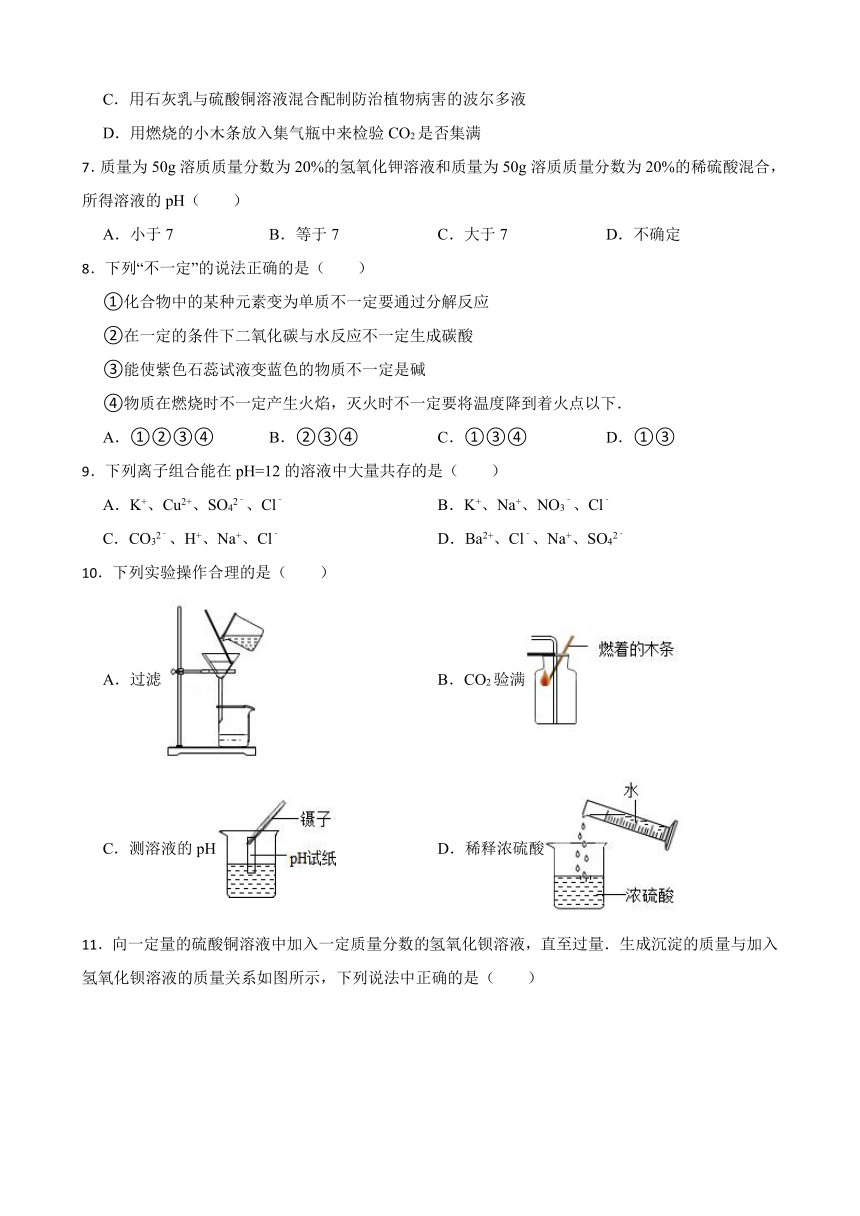
10.下列实验操作合理的是( )
A.过滤 B.CO2验满
C.测溶液的pH D.稀释浓硫酸
11.向一定量的硫酸铜溶液中加入一定质量分数的氢氧化钡溶液,直至过量.生成沉淀的质量与加入氢氧化钡溶液的质量关系如图所示,下列说法中正确的是( )
A.0﹣a段只生成氢氧化铜沉淀
B.室温下,b点溶液的pH>7
C.c点溶液中溶质至少有两种
D.整个过程中,溶液中氢元素的质量一直在增加
12.下表是生活中一些物质的pH,有关它们的说法中正确的是( )
物质种类 厕所清洁剂 桔子汁 牛奶 草木灰水 厨房清洁剂
pH 1 3 6.5 11 12.5
A.草木灰水显酸性 B.厕所清洁剂显碱性
C.桔子汁的酸性比牛奶弱 D.胃酸过多的人不宜多吃桔子
二、填空题
13.如图所示的实验中,A杯溶液逐渐变 色;墙角数枝梅,凌寒独自开,遥知不是雪,为有暗香来。”人在远处就能闻到淡淡的梅花香味的原因是 冬天暴露在空气中的水管冻裂了,这是因为
14.根据下表中的信息填空:
物质 氨水 苹果汁 牛奶 鸡蛋清
pH 8.5﹣10.5 2.9﹣3.3 6.3﹣6.6 7.6﹣8.0
(1)其中酸性最强的是 ;
(2)鸡蛋清是 性;
(3)若向一支盛有氨水的试管中滴稀盐酸,则试管中液体的pH会 (填“变大”“变小”或不变).
15.实验室有A、B两种溶液,A能使紫色石蕊溶液变红色,B能使无色酚酞溶液变红色,则A、B两种溶液的pH大小关系是A B(填“大于”或“小于”).要测定A、B溶液的酸碱度,其做法是 .
16.学习化学需要在宏观物质的性质与其微观结构之间建立联系.1个CO2分子由 构成.在氢氧化钠、氯化钠、硫酸三种物质中,由阴阳离子构成的是 ,常温下,这三种物质的水溶液中pH<7的是 .
17.向盛有氢氧化钠溶液的锥形瓶里滴入几滴酚酞溶液,溶液变成 色,pH 7;逐滴向锥形瓶中滴入盐酸并振荡,至溶液刚刚褪成无色时,pH 7。
18.弱酸性有益于头发的健康.想一想,洗发时应先用 剂,后用 剂.
三、综合题
19.甜瓜珍品﹣江西梨瓜,以“脆、甜、香”而闻名
(1)将鲜梨瓜榨成果汁,该变化属于 (填“物理”或“化学”)变化;
(2)吃江西梨瓜,除补充水分和糖类外,主要补充的营养素还有 ;
(3)梨瓜贮存时常套一个塑料袋,其作用是阻止梨瓜中水分流失,还能隔绝 ,防止腐烂;
(4)梨瓜适宜生长在pH为6.0﹣6.8土壤中,若土壤酸性过强,可用 来进行改良.
20.用如图装置研究Na2CO3的性质。
(1)第一步后,溶液为无色的孔穴有 (填孔穴序号)。
(2)第二步后,孔穴1中发生反应的化学方程式为 。
(3)第二步后,孔穴2、3的溶液均变成红色,说明Na2CO3溶液显 (填“酸”或“碱”)性,此时孔穴2的溶液中含有的溶质是 。
21.阅读下面科普短文,回答下列问题。
我们的胃液呈酸性,是因为胃腺壁细胞能分泌出盐酸。胃酸在人体的消化吸收中发挥着重要作用,如为胃蛋白酶提供适宜的酸性环境,分解食物中的结缔组织和肌纤维使其易于被消化吸收。
你知道吗?深受人们喜欢的早餐食品燕麦中常添加颗粒极小的铁粉,它既可以作为双吸剂(起到干燥和减缓食品变质的作用),还可以作为人体补铁剂。要把铁粉变为人体需要的、能吸收的营养元素,就离不开胃酸的帮助。
健康人胃液的pH在0.9~1.5,胃液的pH不仅影响人的消化吸收功能,还对伴随食物进入胃内的各类病菌的繁殖有影响。某医院对99位胃溃疡和十二指肠溃疡等患者胃液的pH及胃液中的病菌进行了检测,结果如下表:
分组 胃液的pH 受检患者人数 胃液中检出病菌的人数及比例
A ≤2.0 7 0
B 2.0~4.0 13 3(23.1%)
C 4.0~6.0 26 17(65.4%)
D >6.0 53 45(84.9%)
胃酸过多会对胃黏膜具有侵蚀作用,并使人感觉反酸或烧心。治疗胃酸过多的药主要有两大类:一是抑酸药,能抑制胃酸分泌,但本身不能和胃酸反应;二是抗酸药,能直接与胃酸反应,常见的抗酸药有:碳酸氢钠、氢氧化铝、氧化镁、氢氧化镁和碳酸钙等。
胃溃疡患者若服用不合适的抗酸药,会因胃内气体压力增大而引起胃穿孔。患者如长期使用抗酸药,很可能刺激胃酸分泌过多。因此,应遵医嘱合理使用抗酸类和抑酸类药物。
依据文章内容,回答下列问题。
(1)燕麦中的铁粉遇胃酸发生的反应方程式为: 。
(2)铁粉可以在食品包装袋内作双吸剂,是因为铁可以和 反应。
(3)常见的抗酸药中,胃溃疡患者不宜服用的抗酸药是 。(只写一个)
(4)关于文中提到的几种抗酸药,属于氧化物的有 (填写化学式)。
(5)根据文章,下列说法正确的是____(填字母序号)。
A.适量使用碳酸钙可治疗胃酸过多,同时还可为人体补充微量元素钙
B.在使用抗酸药时不是用量越多越好
C.胃酸能帮助人体消化吸收食物,所以胃液pH越小越利于人体健康
D.胃液pH越大越有利于病菌生存
E.胃酸过多会对胃黏膜具有侵蚀作用,所以胃液pH越大越利于人体健康
22.根据要求回答问题:
(1)二氯异氰脲酸钠(C3O3N3Cl2Na)是一种预防H7N9禽流感的有效消毒剂.如图为某工厂生产的二氯异氰脲酸钠产品的标签.
①21%的二氯异氰脲酸钠溶液呈 性(填“酸”或“碱”).
②25℃时,饱和二氯异氰脲酸钠溶液的溶质质量分数为 .(写出计算过程)
(2)自来水厂常用电解饱和食盐水制备消毒剂Cl2,反应的化学方程式为:2NaCl+2H2O 2NaOH+Cl2↑+H2↑.现需要71t氯气用于自来水消毒,理论上需要含杂质10%的粗盐多少吨?
答案
1.【答案】C
2.【答案】A
3.【答案】A
4.【答案】A
5.【答案】A
6.【答案】C
7.【答案】A
8.【答案】A
9.【答案】B
10.【答案】A
11.【答案】D
12.【答案】D
13.【答案】红;分子不断地运动;分子间隔增大
14.【答案】苹果汁;碱;变小
15.【答案】小于;用干净的玻璃棒蘸取待测溶液并滴在pH试纸上,把试纸显示的颜色与标准比色卡对照,读出相同颜色的pH值
16.【答案】一个碳原子和两个氧原子;氢氧化钠、氯化钠;硫酸
17.【答案】红;>;=
18.【答案】洗发;护发
19.【答案】(1)物理
(2)维生素
(3)氧气
(4)熟石灰
20.【答案】(1)2、3
(2)Ca(OH)2+Na2CO3=CaCO3↓+2NaOH
(3)碱;氯化钠、碳酸钠
21.【答案】(1)Fe+2HCl=FeCl2+H2↑
(2)氧气、水
(3)碳酸氢钠(合理即可)
(4)MgO
(5)B;D
22.【答案】(1)酸;205%;25℃时,饱和二氯异氰脲酸钠溶液的溶质质量分数为: 25 g 100 g + 25 g ×100%=20%
(2)解:设理论上需要含杂质10%的粗盐质量为x,
2NaCl+2H2O2NaOH+H2↑+ Cl2↑
117 71
x×(1-10%) 71t
= ,x=130t,
答:现需要71t氯气用于自来水消毒理论上需要含杂质10%的粗盐130t.
一、单选题
1.常温下,下列说法错误的是( )
A.pH=2的溶液显酸性
B.pH=7的溶液显中性
C.溶液的pH由5变成2,其酸性减弱
D.pH>10的土壤不适于种植农作物,因为碱性太强
2.下列说法中正确的是( )
A.生铁和钢都属于金属材料
B.人呼出的气体中二氧化碳的含量比空气中低
C.酚酞溶液滴入稀盐酸变成红色
D.检查煤气泄漏用明火查看
3.某同学在化学晚会上用毛笔蘸取一种无色液体在一张白纸上书写了“化学魔术”四字,然后再喷上另一种无色液体,白纸上立即出现了红色的“化学魔术”四字.该同学所用的两种无色液体可能是( )
A.NaOH溶液、酚酞溶液
B.CuSO4溶液、NaOH溶液
C.紫色石蕊溶液、酚酞溶液
D.酚酞溶液、“雪碧”饮料
4.分析推理是化学学习中常用的思维方法,下列分析推理说法中,正确的是( )
A.各种酸溶液中都含有H+,所以酸溶液有许多相似的化学性质
B.中和反应生成盐和水,所以生成盐和水的反应一定是中和反应
C.碱溶液的pH大于7,所以pH大于7的溶液一定是碱溶液
D.有机物是指含碳元素的化合物,所以含碳元素的化合物一定都是有机物
5.绣球花的颜色与土壤酸碱度有关,当土壤呈酸性时花朵为蓝色。下列是不同土壤的pH,能让绣球花呈蓝色的是( )
A.pH=5.8 B.pH=9.6 C.pH=7.0 D.pH=12.1
6.根据你的生活经验和所学的化学知识,判断下列做法能达到目的是( )
A.煤炉火上放一盆水,就能防止CO中毒
B.用无色酚酞试液检验溶液是否显酸性
C.用石灰乳与硫酸铜溶液混合配制防治植物病害的波尔多液
D.用燃烧的小木条放入集气瓶中来检验CO2是否集满
7.质量为50g溶质质量分数为20%的氢氧化钾溶液和质量为50g溶质质量分数为20%的稀硫酸混合,所得溶液的pH( )
A.小于7 B.等于7 C.大于7 D.不确定
8.下列“不一定”的说法正确的是( )
①化合物中的某种元素变为单质不一定要通过分解反应
②在一定的条件下二氧化碳与水反应不一定生成碳酸
③能使紫色石蕊试液变蓝色的物质不一定是碱
④物质在燃烧时不一定产生火焰,灭火时不一定要将温度降到着火点以下.
A.①②③④ B.②③④ C.①③④ D.①③
9.下列离子组合能在pH=12的溶液中大量共存的是( )
A.K+、Cu2+、SO42﹣、Cl﹣ B.K+、Na+、NO3﹣、Cl﹣
C.CO32﹣、H+、Na+、Cl﹣ D.Ba2+、Cl﹣、Na+、SO42﹣
10.下列实验操作合理的是( )
A.过滤 B.CO2验满
C.测溶液的pH D.稀释浓硫酸
11.向一定量的硫酸铜溶液中加入一定质量分数的氢氧化钡溶液,直至过量.生成沉淀的质量与加入氢氧化钡溶液的质量关系如图所示,下列说法中正确的是( )
A.0﹣a段只生成氢氧化铜沉淀
B.室温下,b点溶液的pH>7
C.c点溶液中溶质至少有两种
D.整个过程中,溶液中氢元素的质量一直在增加
12.下表是生活中一些物质的pH,有关它们的说法中正确的是( )
物质种类 厕所清洁剂 桔子汁 牛奶 草木灰水 厨房清洁剂
pH 1 3 6.5 11 12.5
A.草木灰水显酸性 B.厕所清洁剂显碱性
C.桔子汁的酸性比牛奶弱 D.胃酸过多的人不宜多吃桔子
二、填空题
13.如图所示的实验中,A杯溶液逐渐变 色;墙角数枝梅,凌寒独自开,遥知不是雪,为有暗香来。”人在远处就能闻到淡淡的梅花香味的原因是 冬天暴露在空气中的水管冻裂了,这是因为
14.根据下表中的信息填空:
物质 氨水 苹果汁 牛奶 鸡蛋清
pH 8.5﹣10.5 2.9﹣3.3 6.3﹣6.6 7.6﹣8.0
(1)其中酸性最强的是 ;
(2)鸡蛋清是 性;
(3)若向一支盛有氨水的试管中滴稀盐酸,则试管中液体的pH会 (填“变大”“变小”或不变).
15.实验室有A、B两种溶液,A能使紫色石蕊溶液变红色,B能使无色酚酞溶液变红色,则A、B两种溶液的pH大小关系是A B(填“大于”或“小于”).要测定A、B溶液的酸碱度,其做法是 .
16.学习化学需要在宏观物质的性质与其微观结构之间建立联系.1个CO2分子由 构成.在氢氧化钠、氯化钠、硫酸三种物质中,由阴阳离子构成的是 ,常温下,这三种物质的水溶液中pH<7的是 .
17.向盛有氢氧化钠溶液的锥形瓶里滴入几滴酚酞溶液,溶液变成 色,pH 7;逐滴向锥形瓶中滴入盐酸并振荡,至溶液刚刚褪成无色时,pH 7。
18.弱酸性有益于头发的健康.想一想,洗发时应先用 剂,后用 剂.
三、综合题
19.甜瓜珍品﹣江西梨瓜,以“脆、甜、香”而闻名
(1)将鲜梨瓜榨成果汁,该变化属于 (填“物理”或“化学”)变化;
(2)吃江西梨瓜,除补充水分和糖类外,主要补充的营养素还有 ;
(3)梨瓜贮存时常套一个塑料袋,其作用是阻止梨瓜中水分流失,还能隔绝 ,防止腐烂;
(4)梨瓜适宜生长在pH为6.0﹣6.8土壤中,若土壤酸性过强,可用 来进行改良.
20.用如图装置研究Na2CO3的性质。
(1)第一步后,溶液为无色的孔穴有 (填孔穴序号)。
(2)第二步后,孔穴1中发生反应的化学方程式为 。
(3)第二步后,孔穴2、3的溶液均变成红色,说明Na2CO3溶液显 (填“酸”或“碱”)性,此时孔穴2的溶液中含有的溶质是 。
21.阅读下面科普短文,回答下列问题。
我们的胃液呈酸性,是因为胃腺壁细胞能分泌出盐酸。胃酸在人体的消化吸收中发挥着重要作用,如为胃蛋白酶提供适宜的酸性环境,分解食物中的结缔组织和肌纤维使其易于被消化吸收。
你知道吗?深受人们喜欢的早餐食品燕麦中常添加颗粒极小的铁粉,它既可以作为双吸剂(起到干燥和减缓食品变质的作用),还可以作为人体补铁剂。要把铁粉变为人体需要的、能吸收的营养元素,就离不开胃酸的帮助。
健康人胃液的pH在0.9~1.5,胃液的pH不仅影响人的消化吸收功能,还对伴随食物进入胃内的各类病菌的繁殖有影响。某医院对99位胃溃疡和十二指肠溃疡等患者胃液的pH及胃液中的病菌进行了检测,结果如下表:
分组 胃液的pH 受检患者人数 胃液中检出病菌的人数及比例
A ≤2.0 7 0
B 2.0~4.0 13 3(23.1%)
C 4.0~6.0 26 17(65.4%)
D >6.0 53 45(84.9%)
胃酸过多会对胃黏膜具有侵蚀作用,并使人感觉反酸或烧心。治疗胃酸过多的药主要有两大类:一是抑酸药,能抑制胃酸分泌,但本身不能和胃酸反应;二是抗酸药,能直接与胃酸反应,常见的抗酸药有:碳酸氢钠、氢氧化铝、氧化镁、氢氧化镁和碳酸钙等。
胃溃疡患者若服用不合适的抗酸药,会因胃内气体压力增大而引起胃穿孔。患者如长期使用抗酸药,很可能刺激胃酸分泌过多。因此,应遵医嘱合理使用抗酸类和抑酸类药物。
依据文章内容,回答下列问题。
(1)燕麦中的铁粉遇胃酸发生的反应方程式为: 。
(2)铁粉可以在食品包装袋内作双吸剂,是因为铁可以和 反应。
(3)常见的抗酸药中,胃溃疡患者不宜服用的抗酸药是 。(只写一个)
(4)关于文中提到的几种抗酸药,属于氧化物的有 (填写化学式)。
(5)根据文章,下列说法正确的是____(填字母序号)。
A.适量使用碳酸钙可治疗胃酸过多,同时还可为人体补充微量元素钙
B.在使用抗酸药时不是用量越多越好
C.胃酸能帮助人体消化吸收食物,所以胃液pH越小越利于人体健康
D.胃液pH越大越有利于病菌生存
E.胃酸过多会对胃黏膜具有侵蚀作用,所以胃液pH越大越利于人体健康
22.根据要求回答问题:
(1)二氯异氰脲酸钠(C3O3N3Cl2Na)是一种预防H7N9禽流感的有效消毒剂.如图为某工厂生产的二氯异氰脲酸钠产品的标签.
①21%的二氯异氰脲酸钠溶液呈 性(填“酸”或“碱”).
②25℃时,饱和二氯异氰脲酸钠溶液的溶质质量分数为 .(写出计算过程)
(2)自来水厂常用电解饱和食盐水制备消毒剂Cl2,反应的化学方程式为:2NaCl+2H2O 2NaOH+Cl2↑+H2↑.现需要71t氯气用于自来水消毒,理论上需要含杂质10%的粗盐多少吨?
答案
1.【答案】C
2.【答案】A
3.【答案】A
4.【答案】A
5.【答案】A
6.【答案】C
7.【答案】A
8.【答案】A
9.【答案】B
10.【答案】A
11.【答案】D
12.【答案】D
13.【答案】红;分子不断地运动;分子间隔增大
14.【答案】苹果汁;碱;变小
15.【答案】小于;用干净的玻璃棒蘸取待测溶液并滴在pH试纸上,把试纸显示的颜色与标准比色卡对照,读出相同颜色的pH值
16.【答案】一个碳原子和两个氧原子;氢氧化钠、氯化钠;硫酸
17.【答案】红;>;=
18.【答案】洗发;护发
19.【答案】(1)物理
(2)维生素
(3)氧气
(4)熟石灰
20.【答案】(1)2、3
(2)Ca(OH)2+Na2CO3=CaCO3↓+2NaOH
(3)碱;氯化钠、碳酸钠
21.【答案】(1)Fe+2HCl=FeCl2+H2↑
(2)氧气、水
(3)碳酸氢钠(合理即可)
(4)MgO
(5)B;D
22.【答案】(1)酸;205%;25℃时,饱和二氯异氰脲酸钠溶液的溶质质量分数为: 25 g 100 g + 25 g ×100%=20%
(2)解:设理论上需要含杂质10%的粗盐质量为x,
2NaCl+2H2O2NaOH+H2↑+ Cl2↑
117 71
x×(1-10%) 71t
= ,x=130t,
答:现需要71t氯气用于自来水消毒理论上需要含杂质10%的粗盐130t.
