第7章应用广泛的酸、碱、盐检测题(含解析)2023-2024学年九年级化学沪教版(全国)下册
文档属性
| 名称 | 第7章应用广泛的酸、碱、盐检测题(含解析)2023-2024学年九年级化学沪教版(全国)下册 |

|
|
| 格式 | docx | ||
| 文件大小 | 637.3KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-03-19 00:00:00 | ||
图片预览




文档简介
第7章应用广泛的酸、碱、盐 检测题
一、选择题
1.等质量的碳素钢、生铁放入两支试管中各加入过量的稀盐酸,充分反应后产生氢气的情况是
A.一样多 B.钢产生得多 C.生铁产生得多 D.无法比较
2.下列除去物质中所含少量杂质的方法中,错误的是
选项 物质 杂质 除去杂质的方法
A CO2气体 CO气体 通入氧气,点燃
B Na2SO4溶液 Na2CO3溶液 滴入适量稀硫酸至无气泡产生
C C粉 CuO粉 加入足量盐酸充分反应后过滤
D Fe(NO3)2溶液 AgNO3溶液 加足量铁粉充分反应后过滤
A.A B.B C.C D.D
3.除去下列物质中的少量杂质。所选用的试剂、方法能达到目的的是( )
选项 物质 杂质(少量) 试剂 操作方法
A CO2 CO NaOH溶液、浓硫酸 洗气、干燥
B NaCl固体 KNO3固体 水 配成热饱和溶液,降温结晶、过滤、洗涤、干燥
C CaCl2溶液 盐酸 过量碳酸钙固体 充分反应后过滤
D CaO CaCO3 水 过滤,烘干
A.A B.B C.C D.D
4.除去下列各组物质中的杂质,所用试剂和方法均正确的是
物质 杂质 除杂所用的试剂和方法
A CO2气体 HCl气体 先通过NaOH溶液,再通过浓硫酸
B KCl晶体 K2CO3溶液 加入稍过量的稀盐酸,蒸发结晶
C CO2气体 CO气体 点燃
D 铁粉 铜粉 加入足量的稀硫酸,过滤
A.A B.B C.C D.D
5.氢氧化钙可用于改良酸性土壤,其俗称是
A.纯碱 B.烧碱 C.生石灰 D.熟石灰
6.下列有关KNO3的说法正确的是。
A.是一种复合肥料 B.氮元素的质量分数为20.3%
C.由3个氧原子构成 D.由5种元素组成
7.小明同学取镁、铝、锌三种金属,分别放入盛有质量和质量分数都相等的稀盐酸的锥形瓶中,实验装置如图1,采集数据,得到如图2所示的气压变化曲线。下列说法不正确的是
A.镁、铝、锌与稀盐酸反应产生的相同气体是H2
B.铝对应的曲线是B,反应速率先慢后快,其主要原因是酸与铝的表面的氧化铝先反应
C.金属镁对应的气压变化曲线是A
D.M点时参加反应的镁锌质量相等
8.分类法是学习化学的常用方法下列物质的分类完全正确的是
A.氧化物:干冰、可燃冰
B.混合物:生石灰、稀盐酸
C.合金:氧化铁、不锈钢
D.盐:纯碱、氯化钠
9.除去下列各物质中少量杂质方法,不可行的是( )
物质 所含杂质 除杂质的方法
A CO2 CO 通过足量的灼热氧化铜粉末
B CuO粉末 炭粉 在氧气流中灼烧
C FeCl2溶液 CuCl2 加足量的铁粉,过滤
D H2 O2 用燃着的木条,点燃
A.A B.B C.C D.D
10.下列关于实验现象的描述正确的是
A.红磷在空气中燃烧,产生大量白色烟雾
B.向滴有石蕊的稀盐酸中滴加氢氧化钠溶液至过量,溶液由蓝色变紫色再变红色
C.铁丝在空气中剧烈燃烧,火星四射,生成黑色固体
D.向一定量的饱和石灰水中加入少量氧化钙,溶液变浑浊
11.某同学的实验报告中,有以下实验数据,其中合理的是( )
A.用托盘天平称得11.7g食盐 B.用pH试纸测得雨水的pH约为5.6
C.用量筒量取到5.26mL盐酸 D.某溶液中溶质的质量分数为100%
12.下列实验操作叙述正确的是
A.过滤时,漏斗中液面低于滤纸的边缘
B.加热蒸发过程中,当溶液蒸干时停止加热
C.用pH试纸测定溶液的酸碱度时,将pH试纸放入待测液中蘸取
D.倾倒液体时,试剂瓶口紧挨着试管口快速倒入
13.微观示意图可以帮助我们更好地认识化学反应。下列相关认识中,错误的是
A.图1表示中和反应的实质是H+和OH-结合成水分子
B.图2表示化学方程式是Mg + CuSO4=MgSO4 + Cu,说明镁的活动性比铜强
C.图3表示的反应若在通电的条件下能发生,说明电能可以转化为化学能
D.图3说明化学变化中分子可分,也说明水是由氢气和氧气组成的
二、填空与简答
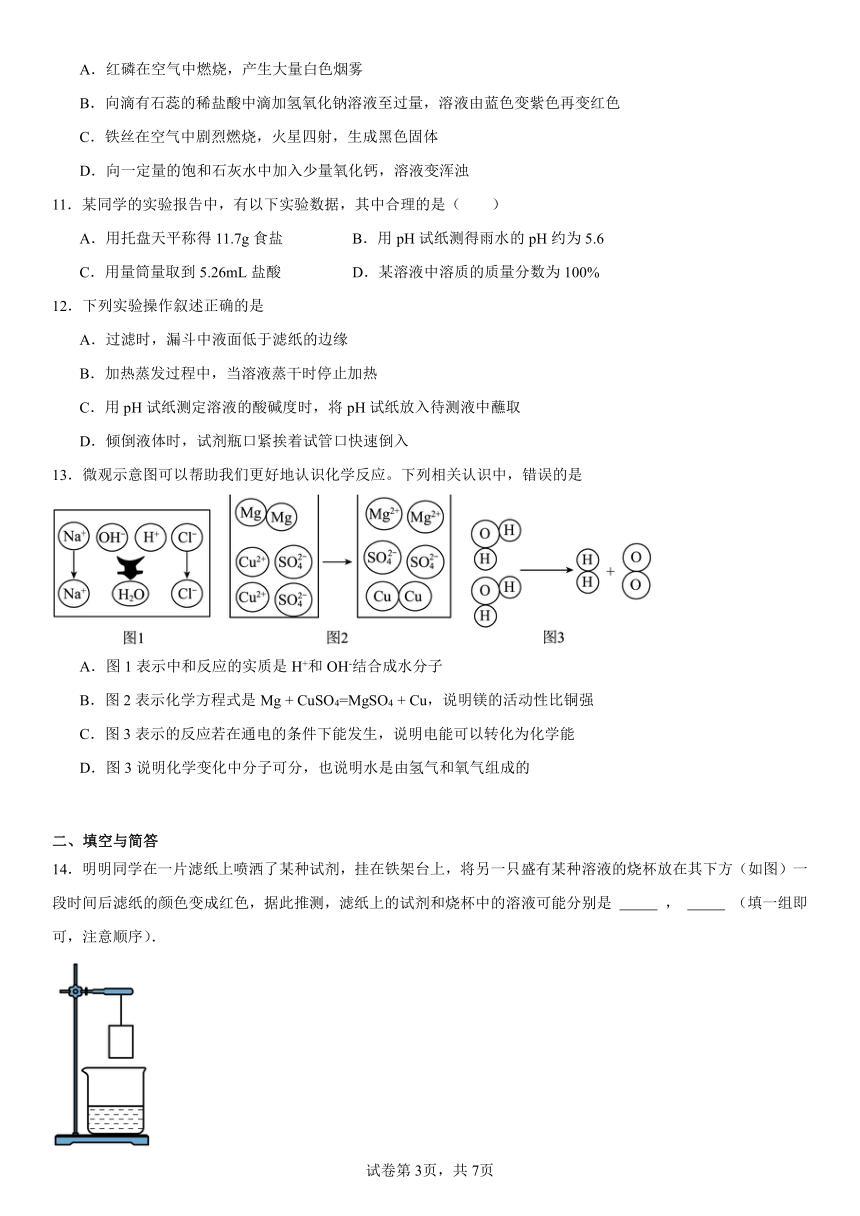
14.明明同学在一片滤纸上喷洒了某种试剂,挂在铁架台上,将另一只盛有某种溶液的烧杯放在其下方(如图)一段时间后滤纸的颜色变成红色,据此推测,滤纸上的试剂和烧杯中的溶液可能分别是 , (填一组即可,注意顺序).
15.智能手机的各项功能令人眼花缭乱,几乎无所不能,下图1为某品牌手机拆解图。
(1)金属钛(Ti)的硬度大、熔点高,常温下耐酸碱。
①选择钛合金作为螺丝材料,是因为合金的硬度比组成它的纯金属的硬度更 (填“大”或“小”)。
②工业上可通过下面两种方法制金属钛:
方法一: TiCl4在高温下与过量的Mg反应可制取金属钛,同时生成氯化镁。除去所得金属钛中混有的少量金属镁可用的试剂是 。
方法二: 高温条件下电解熔融TiO2来制取金属钛,该反应的化学方程式为 ;电解过程中需定期更换石墨电极,原因是 。
(2)手机所用电池为锂电池,具有质量轻、充电时间短、放电时间长等优点。
①某锂电池放电时的反应为:4Li + 2SOCl2= 4LiCl + S + ,请在空格处完善该反应的化学方程式,放电过程中化学能转化为 。
②电池的电压与电池内部所发生的化学反应速率有关。上图2是某电池手机在不同温度下的电压与待机时间的关系变化图像。当电压低于3.6V,手机会自动关机。请分析手机电池在冬天不耐用的原因是 。
16.根据下图可以总结出稀硫酸的五个化学性质。
(1)请在编号①填入一种物质是 。
(2)请分别写出符合编号②、③、④的化学方程式:
② ;
③ ;
④ 。
17.如图是某矿泉水标签的部分内容,根据标签回答下列问题:
(1)该矿泉水是 (选填“纯净物”或“混合物”);
(2)标签中镁元素的化合价为 ;
(3)标签上共列举了 种金属阳离子;
(4)该矿泉水呈 (选填“酸性”、“碱性”或“中性”)。
18.按要求写出下列各反应的化学方程式。
(1)将铁钉投入硫酸铜溶液中,发生反应的化学方程式为 ;
(2)实验室用氯酸钾和二氧化锰制取氧气,该反应的化学方程式为 。
19.A、B、C、D、E、F六种物质均为初中常见的化学物质。其中C可用作炉具清洁剂,E为一种紫红色固体,D→E的反应属于非基本反应类型。它们存在如图所示的转化关系,“→”表示可以向箭头所指方向一步转化.“一”表示两种物质之间可以发生反应(反应条件与其他物质均已略去)。请回答下列问题:
(1)写出F的化学式: 。
(2)写出D→E的化学方程式: 。
20.我国古代将炉甘石(),赤铜(Cu2O)和木炭粉混合加热到约800°C,得到黄铜(锌和铜的合金)。以下是模拟该过程的工艺流程图。
已知:。
(1)流程中体现了木炭的 (填“可燃性”或“还原性”)。
(2)“磨细,混匀”的目的是 。
(3)气体A中一定含有CO2,可能含有 ;为检验气体A的成分,请你设计实验验证: (写出验证方法、现象、结论)。
(4)往黄铜中加入稀硫酸,固体部分消失,写出该反应的化学方程式: 。
三、科学探究题
21.2020年年初至今新冠病毒肆虐全球,广泛使用“84”消毒液进行消毒杀菌。小明同学看电视报道说“84”消毒液不能与洁厕灵混用,否则会产生使人中毒的气体。于是他与化学兴趣小组的同学一起对洁厕灵的成分进行探究。
【提出问题】洁厕灵的主要成分是什么?
【查阅资料】(1)洁厕灵是酸性洗涤剂。
(2)洁厕灵中所含的阴离子主要是氯离子。
(3)“84”消毒液的主要成分是次氯酸钠( NaCIO)。
【猜想与假设】猜想1:洁厕灵的主要成分为NaCl。
猜想2:洁厕灵的主要成分为稀盐酸。
【讨论交流1】同学们认为猜想1不合理,因为 。
【设计并完成实验】
实验操作 实验现象 实验结论
取少量洁厕灵于试管中,加适量水振荡,放入一片打磨过的镁条 猜想2成立
写出该反应的化学方程式 。
【讨论交流2】
(1)请你设计一个不同于以上的实验方案检验洁厕灵的成分;实验步骤 。实验现象 。实验结论 。
(2)洁厕灵与“84”消毒液混用时发生如下化学反应请完成反应方程式2HCl+NaClO=NaCl+ +H2O。
四、计算题
22.小明年前在迎春花市挑了盆叶色浓绿,郁郁葱葱的盆景摆放在自己的房间,可是最近发现叶子发黄,他根据所学化肥知识对此进行研究。
(1)该盆景缺 肥。
(2)小明查到网上售卖的磷酸氢二铵是一种白色的晶体,化学式为(NH4)2HPO4,是一种常用的复合肥。于是他进行了一系列计算后决定购买它,请你完成:
①磷酸氢二铵的相对分子质量是 ,其中氮元素和磷元素的质量比为 。
②买66g的磷酸氢二铵,可给他的盆景补充氮元素 g。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.B
【详解】生铁是含碳量为2%~4.3%的铁合金,钢是含碳量为0.03%~2%的铁合金,生铁的含碳量比钢的含碳量要高,则同质量的生铁含铁量低于钢,置换出来的氢气也较少。故选B。
2.A
【详解】A、二氧化碳气体中混有少量的一氧化碳不能被点燃,错误;
B、碳酸钠和硫酸反应生成硫酸钠、水和二氧化碳,至无气泡产生说明碳酸钠和硫酸恰好完全反应,不会引入新杂质,正确;
C、氧化铜和盐酸反应生成氯化铜和水,过滤除去氯化铜溶液,得到C粉,正确;
D、铁和硝酸银反应生成硝酸亚铁和银,过滤除去铁和银得到硝酸亚铁溶液,正确;
故选A。
3.C
【详解】A、CO不能与NaOH溶液反应,将混合气体通过NaOH溶液、浓硫酸,不能除去一氧化碳,此选项错误;
B、NaCl的溶解度受温度影响不大,KNO3的溶解度受温度影响较大,将固体混合物溶于水,配成热饱和溶液,降温结晶、过滤,得到的晶体主要是KNO3,此选项错误;
C、盐酸能与碳酸钙反应生成氯化钙、水、二氧化碳,向混合溶液中加入过量碳酸钙固体,充分反应后过滤,滤出剩余的碳酸钙,得到氯化钙溶液,此选项正确;
D、CaO能与水反应生成氢氧化钙,最终得不到CaO,此选项错误。
故选C。
【点睛】根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂,是指除去杂质,同时被提纯物质不得改变,除杂题至少要满足两个条件:一是加入的试剂只能与杂质反应,二是反应后不能引入新的杂质。
4.B
【详解】A、氢氧化钠与氯化氢和二氧化碳均反应,分别生成氯化钠和碳酸钠,浓硫酸具有吸水性,故A错误;B、碳酸钾与稀盐酸反应生成氯化钾,水和二氧化碳,通过蒸发结晶,可得氯化钾晶体,故B正确;C、一氧化碳含量很少,很难通过点燃除去,故C错误;D、铁与稀硫酸反应生成硫酸亚铁,铜与稀硫酸不反应,故D错误。
点睛∶除杂原则⑴杂质尽量除净,⑵在除去一种杂质的同时不应增添新的杂质,⑶在除去杂质的同时,非杂物质不应过多消耗,但质量可以增加。
5.D
【详解】纯碱是碳酸钠,烧碱是氢氧化钠,生石灰是氧化钙,氢氧化钙俗称熟石灰或消石灰,故选:D。
6.A
【分析】本题考查化肥。
【详解】A、硝酸钾中含有钾元素和氮元素,是复合肥料,故A符合题意;
B、氮元素的质量分数为:,故B不符合题意;
C、硝酸钾是由钾离子和硝酸根离子构成的,故C不符合题意;
D、硝酸钾由钾、氮、氧三种元素组成,故D不符合题意;
故选A。
【点睛】本题难度不大,根据化学式的基本概念进行辨识即可。
7.D
【详解】A、镁、铝、锌与稀盐酸反应都能生成氢气,故A正确;
B、铝的表面有一层致密的氧化铝薄膜,氧化铝先与稀盐酸反应生成氯化铝和水,氧化铝反应完,铝再与稀盐酸反应生成氯化铝和氢气,所以铝对应的曲线是B,反应速率先慢后快,故B正确;
C、镁、铝、锌三种金属中镁的金属活动性最强,反应速率最快,所以金属镁对应的气压变化曲线是A,故C正确;
D、M点时AC曲线对应的气压相等,生成氢气的质量相等,根据反应关系、可知,生成等质量的氢气,消耗的锌的质量多,则M点时参加反应的镁锌质量不相等,故D错误。
故选D。
8.D
【详解】A、干冰即固态的二氧化碳,是氧化物;可燃冰主要成分为甲烷,是混合物,不是氧化物,故A选不完全正确。
B、生石灰为氧化钙的俗称,是纯净物;稀盐酸是氯化氢气体的水溶液,是混合物,故B 选项不完全正确。
C、合金是混合物,氧化铁是纯净物,不是合金;不锈钢是合金,故C选项不完全正确。
D、纯碱是碳酸钠的俗称,碳酸钠和氯化钠都是钠盐,故D选项完全正确。
故选D。
9.D
【详解】A、CO通过足量的灼热氧化铜粉末生成铜和二氧化碳,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确。
B、炭粉在氧气流中灼烧生成二氧化碳气体,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确。
C、足量的铁粉能与CuCl2溶液反应生成氯化亚铁溶液和铜,再过滤,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确。
D、氢气具有可燃性,除去氢气中的氧气,不能用燃着的木条点燃的方法,否则反而会把原物质除去;且氢气与氧气的混合气体在点燃时易发生爆炸,不符合除杂原则,故选项所采取的方法错误。
故选:D。
【点睛】除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质。
10.D
【详解】A、红磷在空气中燃烧,产生大量白烟,而不是白色烟雾,此选项错误;
B、滴有石蕊的稀盐酸显红色,向滴有石蕊的稀盐酸中滴加氢氧化钠溶液至过量,稀盐酸与氢氧化钠反应生成氯化钠和水,至恰好完全反应,溶液显紫色,滴加氢氧化钠溶液至过量,溶液显碱性,溶液变蓝色,此选项错误;
C、铁丝在氧气中剧烈燃烧,火星四射,生成黑色固体,此选项错误;
D、向一定量的饱和石灰水中加入少量氧化钙,这时溶液已经达到饱和,无法在继续溶解,溶液变浑浊,此选项正确。
故选D。
11.A
【详解】A. 托盘天平用于粗略称量药品的质量,能准确到,可用托盘天平称取食盐,故A符合题意;
B. 由于标准比色卡上的数字只有整数,用广范pH试纸测得溶液的pH不可能精确为,故B不符合题意;
C. 10mL量筒的精确度为,不能用10mL量筒量盐酸,故C不符合题意;
D. 溶液是混合物,溶质的质量分数不能达到,故D不符合题意;
故选A。
【点睛】本题难度不大,考查各种仪器的使用方法及使用注意事项,特别是天平、量筒在中考中出现频度较高,其读数方法和误差的分析更是重中之重。
12.A
【详解】 A.过滤时,漏斗中液面低于滤纸的边缘,选项正确;
B.蒸发滤液时,等出现大量固体就停止加热,利用余热将剩余十分蒸干,不能待蒸发皿中的滤液蒸干后再停止加热,那样会使晶体蹦溅,选项错误;
C.用pH试纸测定溶液的酸碱度时,要用玻璃棒蘸取待测溶液滴到pH试纸上,不能将pH试纸放入待测液中蘸取,那样会污染试剂,选项错误;
D.倾倒液体时,试剂瓶口紧挨着试管口,应缓慢倒入,选项错误;故选A。
考点:基本操作
13.D
【详解】A、图1表示中和反应的实质是H+和OH-结合成水分子:H++OH-=H2O;故选项正确,但不符合题意。
B、图2表示化学方程式是Mg + CuSO4=MgSO4 + Cu,说明镁的活动性比铜强;故选项正确,但不符合题意。
C、图3表示的反应若在通电的条件下能发生,2H2O2H2↑+O2↑,说明电能可以转化为化学能;故选项正确,但不符合题意。
D、图3说明化学变化中分子可分,也说明水是由氢元素和氧元素组成的;故选项错误,但符合题意。
故选D。
14. 酚酞试液 浓氨水
【详解】从滤纸变成红色可推断滤纸上喷洒的物质不是石蕊,而是酚酞试液;浓氨水有挥发性,挥发出的氨气体遇到试剂中的水形成氨水,氨水呈碱性,无色的酚酞溶液遇碱性溶液变红色.
故答案为:酚酞试液;浓氨水;
15.(1) 大
稀盐酸
石墨能和氧气反应生成二氧化碳,使石墨减少
(2) SO2↑ 电能 温度越低,电压下降越快,使用时间越短
【详解】(1)①选择钛合金作为螺丝材料,是因为合金的硬度比组成金属的硬度大;
②除去所得金属钛中混有的少量金属镁可用的试剂是稀盐酸,是因为稀盐酸能和镁反应生成氯化镁和氢气,不能和钛反应;
二氧化钛高温和通电的条件下反应生成钛和氧气,反应的化学方程式为:,电解过程中需定期更换石墨电极,原因是石墨能和氧气反应生成二氧化碳,使石墨减少;
(2)①根据质量守恒定律可知,反应前后原子的数目不变,反应前4个锂原子、2个硫原子、2个氧原子、4个氯原子,反应后有4个锂原子、4个氯原子、1个硫原子,有一个硫原子和2个氧原子没有参加反应,空白处数二氧化硫气体,有气体符号,故填:SO2↑,能量转化形式为化学能转化成电能;
②根据图2 分析可知,温度越低,电压下降越快,使用时间越短,所以手机电池在冬天不耐用。
16.(1)紫色石蕊试液
(2) 或
【详解】(1)稀硫酸是酸溶液,显酸性,根据加入指示剂显红色,故所加指示剂是紫色石蕊试液;
(2)②、稀硫酸和单质反应生成浅绿色溶液,根据亚铁离子的颜色是浅绿色,故所加的单质是铁,则铁和稀硫酸反应生成硫酸亚铁和氢气,化学方程式为:;
③、根据反应后是蓝色溶液即含铜离子的溶液,分析为稀硫酸与氧化铜反应生成硫酸铜和水,化学方程式为:;
④根据与稀硫酸反应生成白色沉淀,判断为硫酸钡沉淀,则加入的碱或是盐为含钡离子的物质,故为氢氧化钡与稀硫酸反应硫酸钡沉淀和水,化学方程式为:或氯化钡与稀硫酸反应生成硫酸钡沉淀和盐酸,化学方程式为:。
17.(1)混合物
(2)+2价/+2
(3)4/四
(4)碱性
【详解】(1)该矿泉水中含有多种物质,属于混合物;
(2)标签中镁离子带两个单位正电荷,故在化合物中镁元素显+2价,故填:+2价或+2;
(3)标签上共列举了钾离子、钠离子、钙离子和镁离子四种金属阳离子,故填:4或四;
(4)该矿泉水的pH大于7,故呈碱性。
18.(1)Fe+CuSO4=FeSO4+Cu
(2)2KClO32KCl+3O2↑
【详解】(1)铁与硫酸铜反应生成硫酸亚铁和铜,化学方程式为。
(2)氯酸钾在二氧化锰催化、加热的条件下生成氯化钾和氧气,化学方程式为。
19. Cu(NO3)2
【分析】A、B、C、D、E、F六种物质均为初中常见的化学物质,E为一种紫红色固体,可推出E为铜,D→E的反应属于非基本反应类型,故D→E可能为一氧化碳还原氧化铜生成铜和二氧化碳,C可用作炉具清洁剂,可推出C为氢氧化钠,铜可与F互相转化,F可与氢氧化钠反应,可推出F为Cu(NO3)2,一氧化碳可以转化为二氧化碳,二氧化碳可以与氢氧化钠反应,则B为二氧化碳,二氧化碳、氢氧化钠均可以与碳酸钠相互转化,A可以是碳酸钠;经过验证,符合题意。
【详解】(1)F为硝酸铜,化学式为:Cu(NO3)2;
(2)D→E可能为一氧化碳还原氧化铜生成铜和二氧化碳,该反应的化学方程式为:。
20.(1)还原性
(2)增大反应物之间的接触面积,使反应更快更充分
(3) 一氧化碳/CO 将气体A通入澄清石灰水中,澄清石灰水变浑浊,说明含二氧化碳,接着通过足量的氢氧化钠溶液和浓硫酸,除去二氧化碳,并干燥气体,然后将气体通入灼烧的氧化铜,并将生成气体通入澄清石灰水,黑色固体逐渐变红,澄清石灰水变浑浊,说明含一氧化碳,否则不含一氧化碳
(4)
【详解】(1)该流程中木炭得到氧,属于还原剂,体现了木炭的还原性;
(2)“磨细,混匀”的目的是:增大反应物之间的接触面积,使反应更快更充分;
(3)气体A中一定含有CO2,二氧化碳能与木炭在高温下反应生成一氧化碳,故可能含有一氧化碳;
二氧化碳能与氢氧化钙反应生成碳酸钙和水,能使澄清石灰水变浑浊,可用澄清石灰水检验二氧化碳,一氧化碳能与氧化铜在加热的条件下反应生成铜和二氧化碳,故可用灼烧的氧化铜检验一氧化碳;可将气体A通入澄清石灰水中,澄清石灰水变浑浊,说明含二氧化碳,接着通过足量的氢氧化钠溶液和浓硫酸,除去二氧化碳,并干燥气体,然后将气体通入灼烧的氧化铜,并将生成气体通入澄清石灰水,黑色固体逐渐变红,澄清石灰水变浑浊,说明含一氧化碳,否则不含一氧化碳;
(4)黄铜是铜锌合金,往黄铜中加入稀硫酸,铜和稀硫酸不反应,锌和稀硫酸反应生成硫酸锌和氢气,该反应的化学方程式为:。
21. 氯化钠溶液呈中性 有气泡产生,镁条溶解 取少量洁厕灵于试管中,加适量的水振荡,放入几粒大理石(合理即可) 试管有气泡产生 洁厕灵的成分为稀盐酸 Cl2
【详解】讨论交流1:
因为NaCl溶液呈中性,而洁厕灵是酸性洗涤剂,故猜想1不合理;
设计并完成实验:
镁是活泼金属能与酸反应生成可溶的氯化镁和氢气,所以取少量洁厕灵于试管中,加适量水振荡,放入一片打磨过的镁条,有大量气泡产生,镁条溶解,说明洁厕灵的主要成分为稀盐酸,故猜想2合理;反应的化学方程式Mg+2HCl=MgCl2+H2↑;
讨论交流2:
(1)酸能与碳酸盐反应生成二氧化碳气体。故取少量洁厕灵于试管中,加适量水振荡,放入一块大理石,试管有气泡产生,则洁厕灵的成分为稀盐酸;
(2)由质量守恒定律可知,反应前后氢原子都是2个,钠原子都是1个,氧原子都是1个,反应前氯原子是3个,反应后应该是3个,其中2个包含在未知物质中,因此未知物质化学式为Cl2。
22. 氮 132 28:31 14
【分析】(1)氮肥能使农作物枝叶繁茂、叶色浓绿、提高产量,进行分析解答。(2)①根据相对分子质量为构成分子的各原子的相对原子质量之和,化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答。②根据化合物中某元素的质量=该化合物的质量×该元素的质量分数,进行分析解答。
【详解】(1)氮肥能使农作物枝叶繁茂、叶色浓绿、提高产量,郁郁葱葱的盆景摆放在自己的房间,可是最近发现叶子发黄,说明该盆景缺氮肥。
(2)①磷酸氢二铵的相对分子质量为(14+1×4)×2+1+31+(16×4)=132;磷酸氢二铵中氮元素与磷元素的质量比为(14×2)︰31=28︰31;
②66g的磷酸氢二铵,所含氮元素的质量为66g××100%=14g。
答案第1页,共2页
答案第1页,共2页
一、选择题
1.等质量的碳素钢、生铁放入两支试管中各加入过量的稀盐酸,充分反应后产生氢气的情况是
A.一样多 B.钢产生得多 C.生铁产生得多 D.无法比较
2.下列除去物质中所含少量杂质的方法中,错误的是
选项 物质 杂质 除去杂质的方法
A CO2气体 CO气体 通入氧气,点燃
B Na2SO4溶液 Na2CO3溶液 滴入适量稀硫酸至无气泡产生
C C粉 CuO粉 加入足量盐酸充分反应后过滤
D Fe(NO3)2溶液 AgNO3溶液 加足量铁粉充分反应后过滤
A.A B.B C.C D.D
3.除去下列物质中的少量杂质。所选用的试剂、方法能达到目的的是( )
选项 物质 杂质(少量) 试剂 操作方法
A CO2 CO NaOH溶液、浓硫酸 洗气、干燥
B NaCl固体 KNO3固体 水 配成热饱和溶液,降温结晶、过滤、洗涤、干燥
C CaCl2溶液 盐酸 过量碳酸钙固体 充分反应后过滤
D CaO CaCO3 水 过滤,烘干
A.A B.B C.C D.D
4.除去下列各组物质中的杂质,所用试剂和方法均正确的是
物质 杂质 除杂所用的试剂和方法
A CO2气体 HCl气体 先通过NaOH溶液,再通过浓硫酸
B KCl晶体 K2CO3溶液 加入稍过量的稀盐酸,蒸发结晶
C CO2气体 CO气体 点燃
D 铁粉 铜粉 加入足量的稀硫酸,过滤
A.A B.B C.C D.D
5.氢氧化钙可用于改良酸性土壤,其俗称是
A.纯碱 B.烧碱 C.生石灰 D.熟石灰
6.下列有关KNO3的说法正确的是。
A.是一种复合肥料 B.氮元素的质量分数为20.3%
C.由3个氧原子构成 D.由5种元素组成
7.小明同学取镁、铝、锌三种金属,分别放入盛有质量和质量分数都相等的稀盐酸的锥形瓶中,实验装置如图1,采集数据,得到如图2所示的气压变化曲线。下列说法不正确的是
A.镁、铝、锌与稀盐酸反应产生的相同气体是H2
B.铝对应的曲线是B,反应速率先慢后快,其主要原因是酸与铝的表面的氧化铝先反应
C.金属镁对应的气压变化曲线是A
D.M点时参加反应的镁锌质量相等
8.分类法是学习化学的常用方法下列物质的分类完全正确的是
A.氧化物:干冰、可燃冰
B.混合物:生石灰、稀盐酸
C.合金:氧化铁、不锈钢
D.盐:纯碱、氯化钠
9.除去下列各物质中少量杂质方法,不可行的是( )
物质 所含杂质 除杂质的方法
A CO2 CO 通过足量的灼热氧化铜粉末
B CuO粉末 炭粉 在氧气流中灼烧
C FeCl2溶液 CuCl2 加足量的铁粉,过滤
D H2 O2 用燃着的木条,点燃
A.A B.B C.C D.D
10.下列关于实验现象的描述正确的是
A.红磷在空气中燃烧,产生大量白色烟雾
B.向滴有石蕊的稀盐酸中滴加氢氧化钠溶液至过量,溶液由蓝色变紫色再变红色
C.铁丝在空气中剧烈燃烧,火星四射,生成黑色固体
D.向一定量的饱和石灰水中加入少量氧化钙,溶液变浑浊
11.某同学的实验报告中,有以下实验数据,其中合理的是( )
A.用托盘天平称得11.7g食盐 B.用pH试纸测得雨水的pH约为5.6
C.用量筒量取到5.26mL盐酸 D.某溶液中溶质的质量分数为100%
12.下列实验操作叙述正确的是
A.过滤时,漏斗中液面低于滤纸的边缘
B.加热蒸发过程中,当溶液蒸干时停止加热
C.用pH试纸测定溶液的酸碱度时,将pH试纸放入待测液中蘸取
D.倾倒液体时,试剂瓶口紧挨着试管口快速倒入
13.微观示意图可以帮助我们更好地认识化学反应。下列相关认识中,错误的是
A.图1表示中和反应的实质是H+和OH-结合成水分子
B.图2表示化学方程式是Mg + CuSO4=MgSO4 + Cu,说明镁的活动性比铜强
C.图3表示的反应若在通电的条件下能发生,说明电能可以转化为化学能
D.图3说明化学变化中分子可分,也说明水是由氢气和氧气组成的
二、填空与简答
14.明明同学在一片滤纸上喷洒了某种试剂,挂在铁架台上,将另一只盛有某种溶液的烧杯放在其下方(如图)一段时间后滤纸的颜色变成红色,据此推测,滤纸上的试剂和烧杯中的溶液可能分别是 , (填一组即可,注意顺序).
15.智能手机的各项功能令人眼花缭乱,几乎无所不能,下图1为某品牌手机拆解图。
(1)金属钛(Ti)的硬度大、熔点高,常温下耐酸碱。
①选择钛合金作为螺丝材料,是因为合金的硬度比组成它的纯金属的硬度更 (填“大”或“小”)。
②工业上可通过下面两种方法制金属钛:
方法一: TiCl4在高温下与过量的Mg反应可制取金属钛,同时生成氯化镁。除去所得金属钛中混有的少量金属镁可用的试剂是 。
方法二: 高温条件下电解熔融TiO2来制取金属钛,该反应的化学方程式为 ;电解过程中需定期更换石墨电极,原因是 。
(2)手机所用电池为锂电池,具有质量轻、充电时间短、放电时间长等优点。
①某锂电池放电时的反应为:4Li + 2SOCl2= 4LiCl + S + ,请在空格处完善该反应的化学方程式,放电过程中化学能转化为 。
②电池的电压与电池内部所发生的化学反应速率有关。上图2是某电池手机在不同温度下的电压与待机时间的关系变化图像。当电压低于3.6V,手机会自动关机。请分析手机电池在冬天不耐用的原因是 。
16.根据下图可以总结出稀硫酸的五个化学性质。
(1)请在编号①填入一种物质是 。
(2)请分别写出符合编号②、③、④的化学方程式:
② ;
③ ;
④ 。
17.如图是某矿泉水标签的部分内容,根据标签回答下列问题:
(1)该矿泉水是 (选填“纯净物”或“混合物”);
(2)标签中镁元素的化合价为 ;
(3)标签上共列举了 种金属阳离子;
(4)该矿泉水呈 (选填“酸性”、“碱性”或“中性”)。
18.按要求写出下列各反应的化学方程式。
(1)将铁钉投入硫酸铜溶液中,发生反应的化学方程式为 ;
(2)实验室用氯酸钾和二氧化锰制取氧气,该反应的化学方程式为 。
19.A、B、C、D、E、F六种物质均为初中常见的化学物质。其中C可用作炉具清洁剂,E为一种紫红色固体,D→E的反应属于非基本反应类型。它们存在如图所示的转化关系,“→”表示可以向箭头所指方向一步转化.“一”表示两种物质之间可以发生反应(反应条件与其他物质均已略去)。请回答下列问题:
(1)写出F的化学式: 。
(2)写出D→E的化学方程式: 。
20.我国古代将炉甘石(),赤铜(Cu2O)和木炭粉混合加热到约800°C,得到黄铜(锌和铜的合金)。以下是模拟该过程的工艺流程图。
已知:。
(1)流程中体现了木炭的 (填“可燃性”或“还原性”)。
(2)“磨细,混匀”的目的是 。
(3)气体A中一定含有CO2,可能含有 ;为检验气体A的成分,请你设计实验验证: (写出验证方法、现象、结论)。
(4)往黄铜中加入稀硫酸,固体部分消失,写出该反应的化学方程式: 。
三、科学探究题
21.2020年年初至今新冠病毒肆虐全球,广泛使用“84”消毒液进行消毒杀菌。小明同学看电视报道说“84”消毒液不能与洁厕灵混用,否则会产生使人中毒的气体。于是他与化学兴趣小组的同学一起对洁厕灵的成分进行探究。
【提出问题】洁厕灵的主要成分是什么?
【查阅资料】(1)洁厕灵是酸性洗涤剂。
(2)洁厕灵中所含的阴离子主要是氯离子。
(3)“84”消毒液的主要成分是次氯酸钠( NaCIO)。
【猜想与假设】猜想1:洁厕灵的主要成分为NaCl。
猜想2:洁厕灵的主要成分为稀盐酸。
【讨论交流1】同学们认为猜想1不合理,因为 。
【设计并完成实验】
实验操作 实验现象 实验结论
取少量洁厕灵于试管中,加适量水振荡,放入一片打磨过的镁条 猜想2成立
写出该反应的化学方程式 。
【讨论交流2】
(1)请你设计一个不同于以上的实验方案检验洁厕灵的成分;实验步骤 。实验现象 。实验结论 。
(2)洁厕灵与“84”消毒液混用时发生如下化学反应请完成反应方程式2HCl+NaClO=NaCl+ +H2O。
四、计算题
22.小明年前在迎春花市挑了盆叶色浓绿,郁郁葱葱的盆景摆放在自己的房间,可是最近发现叶子发黄,他根据所学化肥知识对此进行研究。
(1)该盆景缺 肥。
(2)小明查到网上售卖的磷酸氢二铵是一种白色的晶体,化学式为(NH4)2HPO4,是一种常用的复合肥。于是他进行了一系列计算后决定购买它,请你完成:
①磷酸氢二铵的相对分子质量是 ,其中氮元素和磷元素的质量比为 。
②买66g的磷酸氢二铵,可给他的盆景补充氮元素 g。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.B
【详解】生铁是含碳量为2%~4.3%的铁合金,钢是含碳量为0.03%~2%的铁合金,生铁的含碳量比钢的含碳量要高,则同质量的生铁含铁量低于钢,置换出来的氢气也较少。故选B。
2.A
【详解】A、二氧化碳气体中混有少量的一氧化碳不能被点燃,错误;
B、碳酸钠和硫酸反应生成硫酸钠、水和二氧化碳,至无气泡产生说明碳酸钠和硫酸恰好完全反应,不会引入新杂质,正确;
C、氧化铜和盐酸反应生成氯化铜和水,过滤除去氯化铜溶液,得到C粉,正确;
D、铁和硝酸银反应生成硝酸亚铁和银,过滤除去铁和银得到硝酸亚铁溶液,正确;
故选A。
3.C
【详解】A、CO不能与NaOH溶液反应,将混合气体通过NaOH溶液、浓硫酸,不能除去一氧化碳,此选项错误;
B、NaCl的溶解度受温度影响不大,KNO3的溶解度受温度影响较大,将固体混合物溶于水,配成热饱和溶液,降温结晶、过滤,得到的晶体主要是KNO3,此选项错误;
C、盐酸能与碳酸钙反应生成氯化钙、水、二氧化碳,向混合溶液中加入过量碳酸钙固体,充分反应后过滤,滤出剩余的碳酸钙,得到氯化钙溶液,此选项正确;
D、CaO能与水反应生成氢氧化钙,最终得不到CaO,此选项错误。
故选C。
【点睛】根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂,是指除去杂质,同时被提纯物质不得改变,除杂题至少要满足两个条件:一是加入的试剂只能与杂质反应,二是反应后不能引入新的杂质。
4.B
【详解】A、氢氧化钠与氯化氢和二氧化碳均反应,分别生成氯化钠和碳酸钠,浓硫酸具有吸水性,故A错误;B、碳酸钾与稀盐酸反应生成氯化钾,水和二氧化碳,通过蒸发结晶,可得氯化钾晶体,故B正确;C、一氧化碳含量很少,很难通过点燃除去,故C错误;D、铁与稀硫酸反应生成硫酸亚铁,铜与稀硫酸不反应,故D错误。
点睛∶除杂原则⑴杂质尽量除净,⑵在除去一种杂质的同时不应增添新的杂质,⑶在除去杂质的同时,非杂物质不应过多消耗,但质量可以增加。
5.D
【详解】纯碱是碳酸钠,烧碱是氢氧化钠,生石灰是氧化钙,氢氧化钙俗称熟石灰或消石灰,故选:D。
6.A
【分析】本题考查化肥。
【详解】A、硝酸钾中含有钾元素和氮元素,是复合肥料,故A符合题意;
B、氮元素的质量分数为:,故B不符合题意;
C、硝酸钾是由钾离子和硝酸根离子构成的,故C不符合题意;
D、硝酸钾由钾、氮、氧三种元素组成,故D不符合题意;
故选A。
【点睛】本题难度不大,根据化学式的基本概念进行辨识即可。
7.D
【详解】A、镁、铝、锌与稀盐酸反应都能生成氢气,故A正确;
B、铝的表面有一层致密的氧化铝薄膜,氧化铝先与稀盐酸反应生成氯化铝和水,氧化铝反应完,铝再与稀盐酸反应生成氯化铝和氢气,所以铝对应的曲线是B,反应速率先慢后快,故B正确;
C、镁、铝、锌三种金属中镁的金属活动性最强,反应速率最快,所以金属镁对应的气压变化曲线是A,故C正确;
D、M点时AC曲线对应的气压相等,生成氢气的质量相等,根据反应关系、可知,生成等质量的氢气,消耗的锌的质量多,则M点时参加反应的镁锌质量不相等,故D错误。
故选D。
8.D
【详解】A、干冰即固态的二氧化碳,是氧化物;可燃冰主要成分为甲烷,是混合物,不是氧化物,故A选不完全正确。
B、生石灰为氧化钙的俗称,是纯净物;稀盐酸是氯化氢气体的水溶液,是混合物,故B 选项不完全正确。
C、合金是混合物,氧化铁是纯净物,不是合金;不锈钢是合金,故C选项不完全正确。
D、纯碱是碳酸钠的俗称,碳酸钠和氯化钠都是钠盐,故D选项完全正确。
故选D。
9.D
【详解】A、CO通过足量的灼热氧化铜粉末生成铜和二氧化碳,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确。
B、炭粉在氧气流中灼烧生成二氧化碳气体,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确。
C、足量的铁粉能与CuCl2溶液反应生成氯化亚铁溶液和铜,再过滤,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确。
D、氢气具有可燃性,除去氢气中的氧气,不能用燃着的木条点燃的方法,否则反而会把原物质除去;且氢气与氧气的混合气体在点燃时易发生爆炸,不符合除杂原则,故选项所采取的方法错误。
故选:D。
【点睛】除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质。
10.D
【详解】A、红磷在空气中燃烧,产生大量白烟,而不是白色烟雾,此选项错误;
B、滴有石蕊的稀盐酸显红色,向滴有石蕊的稀盐酸中滴加氢氧化钠溶液至过量,稀盐酸与氢氧化钠反应生成氯化钠和水,至恰好完全反应,溶液显紫色,滴加氢氧化钠溶液至过量,溶液显碱性,溶液变蓝色,此选项错误;
C、铁丝在氧气中剧烈燃烧,火星四射,生成黑色固体,此选项错误;
D、向一定量的饱和石灰水中加入少量氧化钙,这时溶液已经达到饱和,无法在继续溶解,溶液变浑浊,此选项正确。
故选D。
11.A
【详解】A. 托盘天平用于粗略称量药品的质量,能准确到,可用托盘天平称取食盐,故A符合题意;
B. 由于标准比色卡上的数字只有整数,用广范pH试纸测得溶液的pH不可能精确为,故B不符合题意;
C. 10mL量筒的精确度为,不能用10mL量筒量盐酸,故C不符合题意;
D. 溶液是混合物,溶质的质量分数不能达到,故D不符合题意;
故选A。
【点睛】本题难度不大,考查各种仪器的使用方法及使用注意事项,特别是天平、量筒在中考中出现频度较高,其读数方法和误差的分析更是重中之重。
12.A
【详解】 A.过滤时,漏斗中液面低于滤纸的边缘,选项正确;
B.蒸发滤液时,等出现大量固体就停止加热,利用余热将剩余十分蒸干,不能待蒸发皿中的滤液蒸干后再停止加热,那样会使晶体蹦溅,选项错误;
C.用pH试纸测定溶液的酸碱度时,要用玻璃棒蘸取待测溶液滴到pH试纸上,不能将pH试纸放入待测液中蘸取,那样会污染试剂,选项错误;
D.倾倒液体时,试剂瓶口紧挨着试管口,应缓慢倒入,选项错误;故选A。
考点:基本操作
13.D
【详解】A、图1表示中和反应的实质是H+和OH-结合成水分子:H++OH-=H2O;故选项正确,但不符合题意。
B、图2表示化学方程式是Mg + CuSO4=MgSO4 + Cu,说明镁的活动性比铜强;故选项正确,但不符合题意。
C、图3表示的反应若在通电的条件下能发生,2H2O2H2↑+O2↑,说明电能可以转化为化学能;故选项正确,但不符合题意。
D、图3说明化学变化中分子可分,也说明水是由氢元素和氧元素组成的;故选项错误,但符合题意。
故选D。
14. 酚酞试液 浓氨水
【详解】从滤纸变成红色可推断滤纸上喷洒的物质不是石蕊,而是酚酞试液;浓氨水有挥发性,挥发出的氨气体遇到试剂中的水形成氨水,氨水呈碱性,无色的酚酞溶液遇碱性溶液变红色.
故答案为:酚酞试液;浓氨水;
15.(1) 大
稀盐酸
石墨能和氧气反应生成二氧化碳,使石墨减少
(2) SO2↑ 电能 温度越低,电压下降越快,使用时间越短
【详解】(1)①选择钛合金作为螺丝材料,是因为合金的硬度比组成金属的硬度大;
②除去所得金属钛中混有的少量金属镁可用的试剂是稀盐酸,是因为稀盐酸能和镁反应生成氯化镁和氢气,不能和钛反应;
二氧化钛高温和通电的条件下反应生成钛和氧气,反应的化学方程式为:,电解过程中需定期更换石墨电极,原因是石墨能和氧气反应生成二氧化碳,使石墨减少;
(2)①根据质量守恒定律可知,反应前后原子的数目不变,反应前4个锂原子、2个硫原子、2个氧原子、4个氯原子,反应后有4个锂原子、4个氯原子、1个硫原子,有一个硫原子和2个氧原子没有参加反应,空白处数二氧化硫气体,有气体符号,故填:SO2↑,能量转化形式为化学能转化成电能;
②根据图2 分析可知,温度越低,电压下降越快,使用时间越短,所以手机电池在冬天不耐用。
16.(1)紫色石蕊试液
(2) 或
【详解】(1)稀硫酸是酸溶液,显酸性,根据加入指示剂显红色,故所加指示剂是紫色石蕊试液;
(2)②、稀硫酸和单质反应生成浅绿色溶液,根据亚铁离子的颜色是浅绿色,故所加的单质是铁,则铁和稀硫酸反应生成硫酸亚铁和氢气,化学方程式为:;
③、根据反应后是蓝色溶液即含铜离子的溶液,分析为稀硫酸与氧化铜反应生成硫酸铜和水,化学方程式为:;
④根据与稀硫酸反应生成白色沉淀,判断为硫酸钡沉淀,则加入的碱或是盐为含钡离子的物质,故为氢氧化钡与稀硫酸反应硫酸钡沉淀和水,化学方程式为:或氯化钡与稀硫酸反应生成硫酸钡沉淀和盐酸,化学方程式为:。
17.(1)混合物
(2)+2价/+2
(3)4/四
(4)碱性
【详解】(1)该矿泉水中含有多种物质,属于混合物;
(2)标签中镁离子带两个单位正电荷,故在化合物中镁元素显+2价,故填:+2价或+2;
(3)标签上共列举了钾离子、钠离子、钙离子和镁离子四种金属阳离子,故填:4或四;
(4)该矿泉水的pH大于7,故呈碱性。
18.(1)Fe+CuSO4=FeSO4+Cu
(2)2KClO32KCl+3O2↑
【详解】(1)铁与硫酸铜反应生成硫酸亚铁和铜,化学方程式为。
(2)氯酸钾在二氧化锰催化、加热的条件下生成氯化钾和氧气,化学方程式为。
19. Cu(NO3)2
【分析】A、B、C、D、E、F六种物质均为初中常见的化学物质,E为一种紫红色固体,可推出E为铜,D→E的反应属于非基本反应类型,故D→E可能为一氧化碳还原氧化铜生成铜和二氧化碳,C可用作炉具清洁剂,可推出C为氢氧化钠,铜可与F互相转化,F可与氢氧化钠反应,可推出F为Cu(NO3)2,一氧化碳可以转化为二氧化碳,二氧化碳可以与氢氧化钠反应,则B为二氧化碳,二氧化碳、氢氧化钠均可以与碳酸钠相互转化,A可以是碳酸钠;经过验证,符合题意。
【详解】(1)F为硝酸铜,化学式为:Cu(NO3)2;
(2)D→E可能为一氧化碳还原氧化铜生成铜和二氧化碳,该反应的化学方程式为:。
20.(1)还原性
(2)增大反应物之间的接触面积,使反应更快更充分
(3) 一氧化碳/CO 将气体A通入澄清石灰水中,澄清石灰水变浑浊,说明含二氧化碳,接着通过足量的氢氧化钠溶液和浓硫酸,除去二氧化碳,并干燥气体,然后将气体通入灼烧的氧化铜,并将生成气体通入澄清石灰水,黑色固体逐渐变红,澄清石灰水变浑浊,说明含一氧化碳,否则不含一氧化碳
(4)
【详解】(1)该流程中木炭得到氧,属于还原剂,体现了木炭的还原性;
(2)“磨细,混匀”的目的是:增大反应物之间的接触面积,使反应更快更充分;
(3)气体A中一定含有CO2,二氧化碳能与木炭在高温下反应生成一氧化碳,故可能含有一氧化碳;
二氧化碳能与氢氧化钙反应生成碳酸钙和水,能使澄清石灰水变浑浊,可用澄清石灰水检验二氧化碳,一氧化碳能与氧化铜在加热的条件下反应生成铜和二氧化碳,故可用灼烧的氧化铜检验一氧化碳;可将气体A通入澄清石灰水中,澄清石灰水变浑浊,说明含二氧化碳,接着通过足量的氢氧化钠溶液和浓硫酸,除去二氧化碳,并干燥气体,然后将气体通入灼烧的氧化铜,并将生成气体通入澄清石灰水,黑色固体逐渐变红,澄清石灰水变浑浊,说明含一氧化碳,否则不含一氧化碳;
(4)黄铜是铜锌合金,往黄铜中加入稀硫酸,铜和稀硫酸不反应,锌和稀硫酸反应生成硫酸锌和氢气,该反应的化学方程式为:。
21. 氯化钠溶液呈中性 有气泡产生,镁条溶解 取少量洁厕灵于试管中,加适量的水振荡,放入几粒大理石(合理即可) 试管有气泡产生 洁厕灵的成分为稀盐酸 Cl2
【详解】讨论交流1:
因为NaCl溶液呈中性,而洁厕灵是酸性洗涤剂,故猜想1不合理;
设计并完成实验:
镁是活泼金属能与酸反应生成可溶的氯化镁和氢气,所以取少量洁厕灵于试管中,加适量水振荡,放入一片打磨过的镁条,有大量气泡产生,镁条溶解,说明洁厕灵的主要成分为稀盐酸,故猜想2合理;反应的化学方程式Mg+2HCl=MgCl2+H2↑;
讨论交流2:
(1)酸能与碳酸盐反应生成二氧化碳气体。故取少量洁厕灵于试管中,加适量水振荡,放入一块大理石,试管有气泡产生,则洁厕灵的成分为稀盐酸;
(2)由质量守恒定律可知,反应前后氢原子都是2个,钠原子都是1个,氧原子都是1个,反应前氯原子是3个,反应后应该是3个,其中2个包含在未知物质中,因此未知物质化学式为Cl2。
22. 氮 132 28:31 14
【分析】(1)氮肥能使农作物枝叶繁茂、叶色浓绿、提高产量,进行分析解答。(2)①根据相对分子质量为构成分子的各原子的相对原子质量之和,化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答。②根据化合物中某元素的质量=该化合物的质量×该元素的质量分数,进行分析解答。
【详解】(1)氮肥能使农作物枝叶繁茂、叶色浓绿、提高产量,郁郁葱葱的盆景摆放在自己的房间,可是最近发现叶子发黄,说明该盆景缺氮肥。
(2)①磷酸氢二铵的相对分子质量为(14+1×4)×2+1+31+(16×4)=132;磷酸氢二铵中氮元素与磷元素的质量比为(14×2)︰31=28︰31;
②66g的磷酸氢二铵,所含氮元素的质量为66g××100%=14g。
答案第1页,共2页
答案第1页,共2页
