第7章应用广泛的酸、碱、盐基础复习题(含解析)2023-2024学年九年级化学沪教版(全国)下册
文档属性
| 名称 | 第7章应用广泛的酸、碱、盐基础复习题(含解析)2023-2024学年九年级化学沪教版(全国)下册 |

|
|
| 格式 | docx | ||
| 文件大小 | 367.4KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-03-19 00:00:00 | ||
图片预览




文档简介
第7章应用广泛的酸、碱、盐 基础复习题
一、选择题
1.自来水加入氯气消毒的过程中会发生如下反应,下列说法中不正确的是
A.参加反应的微观粒子个数比为1:1 B.该反应为复分解反应
C.该反应中氯元素的化合价有三种 D.在化学变化中,分子可分,原子不可分
2.下列说法正确的是
A.在滴有石蕊试液的水中通入CO2后溶液变红,说明CO2气体能使石蕊试液变红色
B.铁桶能用来盛氢氧化钠溶液,也能用来盛放稀盐酸
C.熟石灰涂在墙壁表面后变硬,原因是熟石灰与CO2反应生成了坚硬的碳酸钙
D.浓硫酸具有吸水性,因此能用浓硫酸干燥所有气体
3.比较推理是化学学习中常用的思维方法,下列有关物质的比较推理中正确的是
A.铁在潮湿的空气中易腐蚀,故铝在潮湿的空气中也易腐蚀
B.钢比纯铁硬,故黄铜比纯铜硬
C.氢氧化铝可治疗胃酸过多,故氢氧化钠也可治疗胃酸过多
D.厨房洗涤剂对油污有乳化作用,故汽油对油污也有乳化作用
4.下列课外实验中,不能达到实验目的的是
A.用紫甘蓝和酒精溶液自制酸碱指示剂
B.用食醋可除去热水壶内壁的水垢
C.用10%的氯化钠溶液浸泡新鲜的树叶,制作叶脉书签
D.用报纸和保鲜膜分别蒙住盛等体积水的两只相同的烧杯,比较报纸和保鲜膜的透气性
5.下列关于酸、碱、盐的说法正确的是
A.碱溶液一定显碱性,显碱性的也一定是碱溶液
B.酸碱中和反应生成盐和水,所以生成盐和水的也一定是中和反应
C.施铵态氮肥时不可以配合呈碱性的草木灰一起使用
D.大量浓硫酸溅到皮肤上,最好先用干布擦拭,再用水冲,最后涂氢氧化钠溶液
6.下列物质的用途与其化学性质有关的是
A.用干冰人工降雨 B.用石墨做电极
C.用稀盐酸除水垢 D.用氦气充探空气球
7.下列知识整理的内容不完全正确的一组是( )
A 食品保鲜的办法 B 灭火实例与原理
填充氮气——防止变质 放入生石灰——防止受潮 放入细铁粉———防止受潮和变质 油锅着火时用锅盖盖灭——隔绝空气 住宅失火时用水灭火——降低着火点 扑灭森林火灾时设置隔离带——隔离可燃物
C 日常物质的区别 D 化学中常见的“三”
硬水和软水——加肥皂水并搅拌 区别氢氧化钠溶液和石灰水——通入二氧化碳 氯化铵和磷矿粉——观察颜色 三种可燃性气体——H2、CO、CH4 三种可加热仪器——试管、烧杯、蒸发皿 三种构成物质的粒子——分子、原子、离子
A.A B.B C.C D.D
8.作为生命之源的水同时也是最重要的化学物质之一、下列关于水的说法正确的是
A.水在直流电的作用下分解,在电源的正负极上分别产生氢气和氧气
B.在日常生活中常用煮沸的方法将软水变成硬水
C.许多化学反应需要在水作溶剂的溶液中进行
D.纯水的pH为0
9.构建化学基本观念是学好化学的基础,下列有关化学基本观念的认识正确的是
A.微粒观:稀盐酸和稀硫酸中都有氢离子,所有化学性质完全相同
B.元素观:元素组成完全相同的物质,其化学性质也一定相同
C.变化观:化学反应后有氧气生成的物质中,一定含有氧元素
D.守恒观:10g氢气与10g氧气充分反应后,一定生成20g水
10.下列各组物质的化学式书写都正确的是
A.银Ag、水银Hg B.苏打NaCO3、小苏打NaHCO3
C.生石灰CaO、熟石灰CaOH D.氧化铁FeO、四氧化三铁Fe3O4
11.以下对某一主题知识进行的归纳,正确的一组是
A.性质与用途 B.安全常识
石墨能导电——作电极 活性炭有吸附性——作冰箱除臭剂 不明洞穴探险——先做灯火实验 家中石油气泄漏——立即打开排气扇
C.健康常识 D.物质分类
人体缺铁——易患贫血病 人体缺锌——易患佝偻病 常见的碱——熟石灰、烧碱、纯碱 常见的干燥剂——浓硫酸、生石灰、碱石灰
A.A B.B C.C D.D
12.化学知识在生产和生活中有着重要的应用,下列说法中不正确的是
A.鱼骨粉的主要成分是碳酸钙,可用于补钙
B.明矾可使水中悬浮小颗粒快速沉降,也可用于自来水的消毒杀菌
C.发酵粉中含有较多的NaHCO3、,能使焙制出的糕点疏松多孔
D.纯碱也叫苏打,可用于清洗厨房用具的油污
二、填空与简答
13.在抗击“新冠肺炎病毒”期间,消毒剂在公共场所进行卫生防疫时发挥着重要的作用,其中84消毒液[有效成分为次氯酸钠(NaClO)]和二氧化氯(ClO2)是常用消毒剂。
(1)“84消毒液”的有效成分为NaClO,其中氯元素的化合价为 ;使用“84 消毒液” 消毒时,常用水稀释,稀释后测得消毒液的pH=9,该溶液呈 性。
(2)ClO2是一种环保型杀菌消毒剂,生活中常用ClO2消毒饮用水,ClO2是属于 (填序号)。
A混合物 B化合物 C氧化物
14.下列是一些与人类的生产、生活密切相关的物质。
a.75%的酒精溶液;b.铝;c.一氧化碳;d.氢氧化钙;e.氯化钠;f.碳酸氢钠
请选择适当的物质,用其字母序号填空。
(1) 可用作食品调味;
(2) 可用于工业冶炼铁:
(3) 可用于制作炊具;
(4) 可用于改良酸性土壤;
(5)医院常用 消毒杀菌。
(6)制作馒头过程中加入 使蒸好的馒头疏松多孔。
15.常用的农药绝大多数都是用 方法配制或合成的。例如波尔多液就是用 、 和 混合制得的,是一种天蓝色、黏稠的悬浊液,它是一种广泛使用的 剂。
16.中和反应是重要的化学反应。图1是氢氧化钠溶液和稀硫酸反应的示意图。图2是向氢氧化钠溶液中滴加硫酸时电导率的变化情况。查阅资料:①单位体积溶液中某离子的个数越多,则该离子的浓度越大,溶液的导电能力越强。②溶液的导电能力越强,溶液的电导率越大。
(1)观察图1,该反应中未发生变化的离子是 (写离子符号)。
(2)图2中N点溶液中的溶质有哪些? (写化学式)。
17.生产生活中,化学无处不在。从A.石墨;B.二氧化硫;C.熟石灰;D.氢气;E.稀有气体等物质中,选择与下列叙述相应的物质并用字母编号填空:
(1)可用作建筑材料的是 。
(2)形成酸雨的主要气体是 。
(3)可用于制造干电池电极的是 。
(4)可用于填充霓虹灯的是 。
(5)可作为清洁绿色能源是 。
18.如图,物质王国中的A~F及X种物质玩“独木桥”游戏,其中A~F分别是稀盐酸,氢气,氧化铜,氢氧化钙溶液,碳酸钠溶液,二氧化碳六种物质中的一种
(1)搭桥
游戏规则:A~F搭桥后相邻的物质之间能发生化学反应(所涉及反应均为初中常见化学反应)。已知E的俗名叫澄清石灰水,请回答下列问题:
①F的化学式是 ;
②A与B反应的实验现象 ;
③C与D反应的化学方程式是 。
(2)过桥:
游戏规则:若A~F每种物质分别通过一步反应都能直接转化为X,则X就可以成功过桥,请推测物质X的化学式是 。
19.工业上粗盐(含MgCl2、CaCl2、Na2SO4等杂质),精制的工艺流程如下:
(1)X中含有的阳离子是 ;沉淀C的化学式是 。
(2)写出生成沉淀D的一个化学方程式 。
(3)溶液E中加过量稀盐酸的作用是 。
三、科学探究题
20.学习小组尝试从反应物消耗和新物质生成两个不同的角度,验证 CO2与 NaOH溶液发生了反应。
【查阅资料】
Ⅰ.常温下,NaOH易溶于水也易溶于酒精,Na2CO3易溶于水但难溶于酒精。
Ⅱ.BaCl2溶液呈中性,CO2不溶于酒精也与酒精不反应。
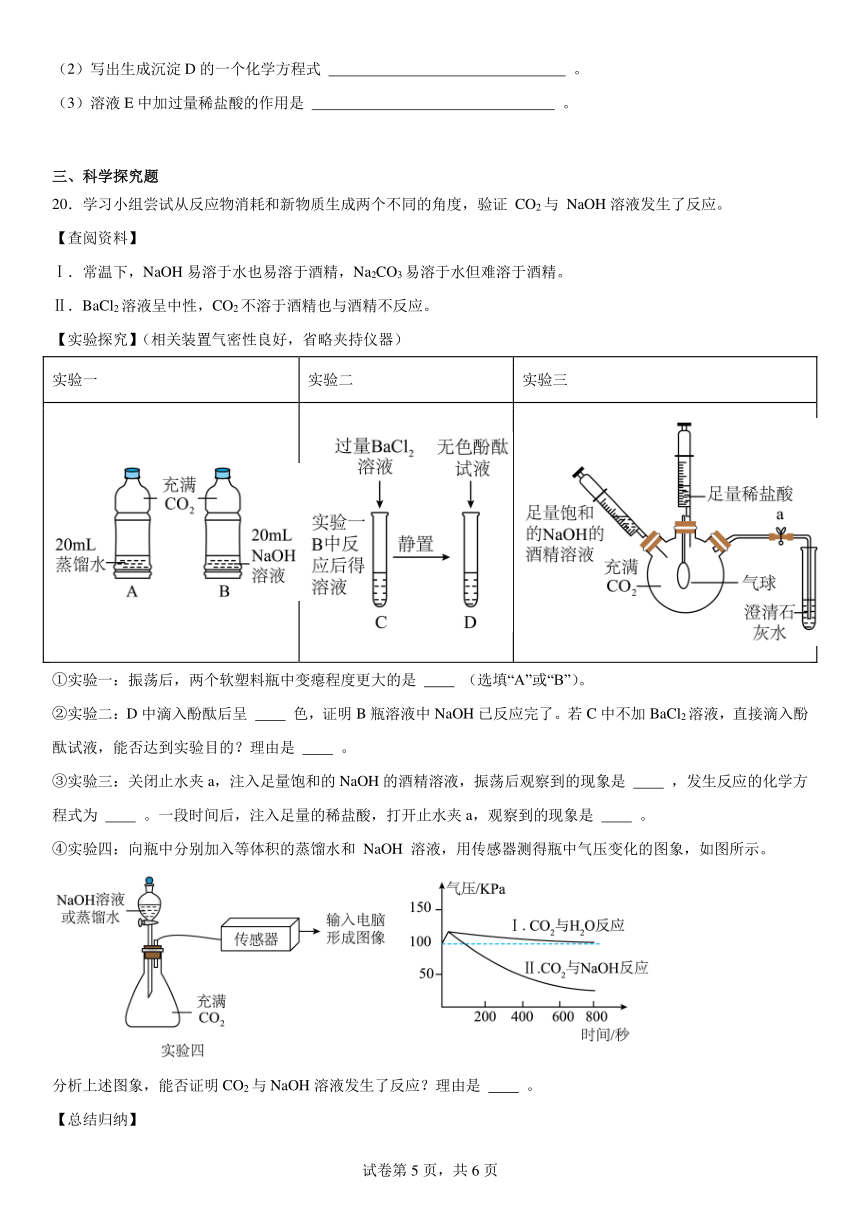
【实验探究】(相关装置气密性良好,省略夹持仪器)
实验一 实验二 实验三
①实验一:振荡后,两个软塑料瓶中变瘪程度更大的是 (选填“A”或“B”)。
②实验二:D中滴入酚酞后呈 色,证明B瓶溶液中NaOH已反应完了。若C中不加BaCl2溶液,直接滴入酚酞试液,能否达到实验目的?理由是 。
③实验三:关闭止水夹a,注入足量饱和的NaOH的酒精溶液,振荡后观察到的现象是 ,发生反应的化学方程式为 。一段时间后,注入足量的稀盐酸,打开止水夹a,观察到的现象是 。
④实验四:向瓶中分别加入等体积的蒸馏水和 NaOH 溶液,用传感器测得瓶中气压变化的图象,如图所示。
分析上述图象,能否证明CO2与NaOH溶液发生了反应?理由是 。
【总结归纳】
以上四个实验中,既从反应物消耗角度,又从新物质生成角度,证明NaOH与CO2发生了反应的实验是 (选填“一”、“二”、“三”或“四”)。
四、计算题
21.欲测定一瓶标签破损的盐酸中溶质的质量分数,现将50g该盐酸样品与80g溶质的质量分数为10%的氢氧化钠溶液混合,恰好完全反应。
(1)80g该氢氧化钠溶液中所含溶质的质量为 。
(2)计算该盐酸中溶质的质量分数 。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.B
【分析】由微观示意图分析可知,该反应为。
【详解】A.参加反应的微观粒子个数比为1:1,选项说法正确。
B.该反应由单质和化合物反应生成另外两种化合物,不属于复分解反应,选项说法错误。
C.该反应中氯元素的化合价有三种:Cl2中为0价,HCl中为-1价,HClO中为+1价,选项说法正确。
D.在化学变化中,分子可分,原子不可分,选项说法正确。
故选:B。
2.C
【详解】A、在滴有石蕊试液的水中通入CO2后溶液变红,是因为CO2气体和水反应生成的碳酸,碳酸呈酸性,能使石蕊试液变红色,故选项说法错误;
B、Fe不能与NaOH反应,则铁桶能用来盛氢氧化钠溶液;Fe金属活动性大于H,能与稀盐酸反应生成氢气,则铁桶不能用来盛放稀盐酸,故选项说法错误;
C、熟石灰是氢氧化钙的俗称,熟石灰涂在墙壁表面后变硬,原因是氢氧化钙与CO2反应生成了坚硬的碳酸钙,故选项说法正确;
D、浓硫酸具有吸水性,但是不能用浓硫酸干燥所有气体,例如氨气,因为氨气能与硫酸发生反应生成硫酸铵,故选项说法错误。
故选C。
3.B
【详解】A、铁与空气中的氧气和水接触,会生锈,故铁在潮湿的空气中易腐蚀,而铝能与空气中的氧气反应生成一层致密的氧化铝薄膜,从而阻止铝进一步被氧化,故铝在潮湿的空气中不易腐蚀,不符合题意;
B、合金比组成它的纯金属硬度大,钢是铁的合金,故钢比纯铁硬,黄铜是铜锌合金,故黄铜比纯铜硬,符合题意;
C、氢氧化铝能与盐酸反应生成氯化铝和水,可用于治疗胃酸过多,但是氢氧化钠腐蚀性较强,不能用于治疗胃酸过多,不符合题意;
D、洗涤剂具有乳化作用,能将油污乳化为细小油滴,随水冲走,故可用于去油污,而汽油能去油污,是因为汽油能溶解油污,不符合题意。
故选B。
4.C
【详解】A、某些植物的花瓣的汁液可作酸碱指示剂,可用酒精浸泡得到溶液,可用紫甘蓝和酒精溶液自制酸碱指示剂,故选项课外实验能达到实验目的。
B、水垢的主要成分是碳酸钙,能与食醋中的醋酸反应生成易溶于水的醋酸钙,可除去热水壶内的水垢,故选项课外实验能达到实验目的。
C、氯化钠溶液不具有腐蚀性,不能制作叶脉书签,应使用氢氧化钠溶液,故选项课外实验不能达到实验目的。
D、用报纸和保鲜膜分别蒙住盛等体积水的两只相同的烧杯,可以比较报纸和保鲜膜的透气性,故选项课外实验能达到实验目的。
故选C。
5.C
【详解】A、碱性溶液不一定都是碱,如碳酸钠的溶液呈碱性但碳酸钠是盐不是碱,故选项说法错误;B、酸碱中和反应生成盐和水,但生成盐和水的反应不一定是中和反应,如CO2+2NaOH═Na2CO3+H2O,故选项说法错误;C、铵态氮肥与草木灰混合使用,会产生氨气,降低肥效,故选项说法正确;D、浓硫酸具有较强的腐蚀性,不慎沾到皮肤上,先用干布拭干,然后用大量清水冲洗,后涂上3%~5%的碳酸氢钠溶液,故选项说法错误。故选C。
6.C
【详解】A、用干冰人工降雨是利用干冰升华吸热使周围温度降低,利用的是物质的物理性质,错误;
B、用石墨做电极利用石墨的导电性,属于物理性质,错误;
C、用稀盐酸除水垢是利用盐酸能与水垢的主要成分碳酸钙、氢氧化镁反应,属于物质的化学性质,正确;
D、用氦气充探空气球利用氦气的密度比空气小,属于物质的物理性质,错误;
故选C。
7.B
【详解】A、氮气性质稳定,填充氮气可以防止变质;生石灰和水反应生成氢氧化钙,放入生石灰可以防止受潮;铁和水、氧气生成氧化铁,放入细铁粉可以防止受潮和变质,内容完全正确;
B、油锅着火时用锅盖盖灭是隔绝空气;住宅失火时用水灭火是降低温度至可燃物着火点以下;扑灭森林火灾时设置隔离带是隔离可燃物,内容不完全正确;
C、硬水和软水中加肥皂水并搅拌,产生泡沫较多的是软水,产生泡沫较少的是硬水;二氧化碳和氢氧化钙反应是碳酸钙沉淀,二氧化碳和氢氧化钠反应不生成沉淀,区别氢氧化钠溶液和石灰水通入二氧化碳,产生沉淀的是石灰水,不产生沉淀的是氢氧化钠溶液;氯化铵是白色固体,磷矿粉是灰色固体,氯化铵和磷矿粉观察颜色可以区别,内容完全正确;
D、H2、CO、CH4均是可燃性气体;试管、烧杯、蒸发皿均是可加热仪器;分子、原子、离子均是构成物质的粒子,内容完全正确。
故选B。
8.C
【详解】A、电解水实验中,正氧负氢,在电源的正、负极上分别产生氧气和氢气,选项说法不正确;
B、加热煮沸时,水中的钙离子、镁离子能够以碳酸钙沉淀、氢氧化镁沉淀的形式从水中析出从而降低水的硬度,因此煮沸能降低水硬度,变成软水,选项说法不正确;
C、两种物质相互接触的面积越大,反应的速率越快,由于溶液是均一稳定的混合物,在溶液中两种物质接触面积大,化学反应的速率快,选项说法正确;
D、纯水的pH为7,选项说法不正确。
故选C。
9.C
【详解】A、稀盐酸和稀硫酸中都有氢离子,所以它们具有一些共同的化学性质,但是它们的化学性质并不是完全相同 的,因为解离出的酸根离子不同,故A认识错误;
B、元素组成完全相同的物质,其化学性质不一定相同,例如一氧化碳和二氧化碳都是由碳元素和氧元素组成的化合物,但是二者的分子构成不同,所以二者的化学性质不同,故B认识错误;
C、根据质量守恒定律,化学反应前后元素种类不变,所以化学反应后有氧气生成的物质中,一定含有氧元素,故C认识正确;
D、氢气与氧气点燃生成水,即,有反应方程式可知,参加反应的氢气、氧气与生成的水的质量比为4:32:36=1:8:9,所以当10g氢气与10g氧气充分反应后,氢气有剩余,根据质量守恒定律,所以生成水的质量<20g,故D认识错误;
故选C。
10.A
【详解】A、由原子直接构成的物质,直接用元素符号来表示,若元素中含有两个字母,第一个字母要大写,第二个字母要小写,银的化学式为Ag、水银是汞的俗称,化学式为Hg,故A正确;
B、苏打是碳酸钠的俗称,碳酸钠中钠元素显+1价,碳酸根离子显-2价,其化学式为Na2CO3,小苏打是碳酸氢钠的俗称,碳酸氢钠由钠离子和碳酸氢根离子构成,钠离子显+1价,碳酸氢根离子显-1价,化学式为NaHCO3,故B错误;
C、生石灰是氧化钙的俗称,化学式为CaO,熟石灰是氢氧化钙的俗称,氢氧化钙中钙元素显+2价,氢氧根显-1价,其化学式为Ca(OH)2,故C错误;
D、氧化铁中铁元素显+3价,氧元素显-2价,其化学式为Fe2O3,根据“先读后写”,四氧化三铁的化学式为Fe3O4,故D错误。
故选A。
11.A
【详解】A、石墨具有良好的导电性,可作电极;活性炭有很强的吸附性,能除去异味和色素,可作冰箱除臭剂,此选项正确;
B、不明洞穴探险,先做灯火实验,以检查洞穴内二氧化碳的含量;家中石油气泄漏,立即关闭活塞,不能打开排气扇,以防发生爆炸,此选项不完全正确,不符合题意;
C、人体缺铁,易患贫血病;人体缺钙,易患佝偻病,此选项不完全正确,不符合题意;
D、熟石灰是氢氧化钙的俗称,烧碱是氢氧化钠的俗称,它们是常见的碱,纯碱是碳酸钠,碳酸钠属于盐;浓硫酸、生石灰、碱石灰是常见的干燥剂,此选项不完全正确,不符合题意。
故选A。
12.B
【详解】A、鱼骨粉的主要成分是碳酸钙,可用于补钙,正确;B、明矾中的铝离子水解得到的氢氧化铝能净水,但是不具有杀菌作用,错误;C、NaHCO3与面粉中产生的氢离子反应生成二氧化碳,使焙制出的糕点疏松多孔,正确;D、碳酸钠俗称苏打或纯碱,纯碱溶液显碱性,油污在碱性条件下可水解,且水解为不可逆过程,则使用纯碱清洗厨房用具的油污,正确。故选B。
13. +1 碱 C
【详解】(1)根据化合物中元素正负化合价的代数和为零可知,NaClO中钠元素为+1价,氧元素为-2价,所以氯元素为+1价,故填写:+1;
根据pH与溶液酸碱性的关系:pH<7,显酸性,pH=7,显中性,pH>7,显碱性可知,稀释后测得消毒液的pH=9>7,显碱性,故填写:碱;
(2)根据氧化物是由两种元素组成,其中一种为氧元素的化合物可知,ClO2是属于氧化物,故填写:C。
14. e c b d a f
【详解】(1)氯化钠可作作调味品,故填:e;
(2)一氧化碳具有还原性,可用于工业冶炼铁,故填:c;
(3)铝具有良好的导热性,可用于制作炊具,故填:b;
(4)氢氧化钙呈碱性,常用于改良酸性土壤,故填:d;
(5)体积分数为75%的酒精溶液常用于灭菌消毒,此浓度杀菌力最强.在75%的酒精作用下,乙醇能渗入细胞内,使蛋白质凝固变性,从而起到杀菌的作用,故填:a;
(6)制作馒头过程中加入碳酸氢钠,碳酸氢钠受热时会产生二氧化碳气体,且能与酸性物质反应生成二氧化碳,使蒸好的馒头疏松多孔,故填:f。
15. 化学 胆矾/ 生石灰/CaO 水/H2O 杀菌
【详解】大多数农药需要通过其他物质合成,该过程有新物质生成,属于化学变化,故填化学;
波尔多液是用水与生石灰混合,得到石灰乳,并将剩余的水与硫酸铜混合得到硫酸铜溶液,最后使用时将硫酸铜溶液慢慢倒入石灰乳中,并不断搅拌,即可得到蓝色胶状悬浊液,是常用的杀菌剂。故填胆矾;生石灰;水;杀菌;
16.(1)、
(2)Na2SO4、H2SO4
【详解】(1)由图1可知,氢离子与氢氧根离子结合成了水分子,钠离子和硫酸根离子没有发生改变,离子符号分别为:、;
(2)氢氧化钠和稀硫酸反应生成硫酸钠和水,溶液离子浓度减小,直至将氢氧化钠消耗完全时,溶液中离子浓度最小,导电率最低,即M点,继续滴加硫酸溶液,离子浓度逐渐变大,电导率变大,所以N点所示溶液中的溶质硫酸钠、硫酸,化学式为:Na2SO4、H2SO4;
17. C B A E D
【详解】(1)熟石灰为氢氧化钙,将熟石灰加水做成石灰浆,用于抹墙,在吸收二氧化碳后变为坚硬的碳酸钙,是很好建筑材料,所以熟石灰可以用作建筑材料;
(2)二氧化硫溶于水生成亚硫酸,亚硫酸被氧化可以生成硫酸,另外二氧化硫也可以被氧化生成三氧化硫,三氧化硫溶于水生成硫酸,最终都可生成硫酸,形成酸雨;
(3)石墨具有良好的导电性,所以常用作干电池的电极;
(4)稀有气体可以通过或吸收不同波长的光,所以常用于填充霓虹灯,作为电光源使用;
(5)氢气燃烧后只生成水,无其他物质生成,放出热量较高,被称为清洁绿色能源。
18. 黑色固体变红色
【分析】A~F分别是盐酸,氢气,氧化铜,氢氧化钙,碳酸钠,二氧化碳六中物质中的一种,搭桥:规则是A~F搭桥后相邻的物质之间能发生化学反应,E的俗名叫熟石灰,氢氧化钙会与碳酸钠、盐酸反应,氢气只会与氧化铜反应,A或F可能是氢气,当F是氢气时,不会与氢氧化钙反应,当A是氢气,B是氧化铜,氧化铜会与稀盐酸反应,C是稀盐酸,D是碳酸钠,F是二氧化碳;过桥:若A~F分别通过一步反应能直接转化为X,则X可成功过桥,氢气和氧化铜反应生成水,氧化铜和盐酸反应生成水,盐酸和碳酸钠反应生成水,碳酸钠和氢氧化钙反应生成水,氢氧化钙和二氧化碳反应生成水,X是水。
【详解】(1)①E的俗名叫熟石灰,氢氧化钙会与碳酸钠、盐酸反应,氢气只会与氧化铜反应,A或F是氢气,当F是氢气时,不会与氢氧化钙反应,当A是氢气,B是氧化铜,氧化铜会与稀盐酸反应,C是稀盐酸,D是碳酸钠,F是二氧化碳,故F的化学式是。
②A与B反应是氢气和氧化铜在加热的条件下生成铜和二氧化碳,故实验现象是黑色固体变红色。
③C与D反应是碳酸钠和盐酸反应生成氯化钠、水和二氧化碳,反应的化学方程式为。
(2)A~F分别通过一步反应能直接转化为X,则X可成功过桥,氢气和氧化铜反应生成水,氧化铜和盐酸反应生成水,盐酸和碳酸钠反应生成水,碳酸钠和氢氧化钙反应生成水,氢氧化钙和二氧化碳反应生成水,X是水,故X的化学式是。
【点睛】E的俗名叫熟石灰,E是氢氧化钙,氢气和氧化铜在加热的条件下生成铜和二氧化碳,碳酸钠和盐酸反应生成氯化钠、水和二氧化碳,氧化铜和盐酸反应生成氯化铜和水。
19. Ba2+ Mg(OH)2 CaCl2+Na2CO3=CaCO3↓+2NaCl或BaCl2+Na2CO3=BaCO3↓+2NaCl 除尽过量的Na2CO3和NaOH
【分析】工业上粗盐(含MgCl2、CaCl2、Na2SO4等杂质)的精制实际上是除去镁离子、钙离子、硫酸根离子的过程。
【详解】(1)粗盐中含有MgCl2、CaCl2、Na2SO4等杂质,所以X中含有的阳离子是Ba2+,X是氯化钡溶液,加入过量的X生成了硫酸钡沉淀;溶液A中含有镁离子,氢氧根离子和镁离子会生成氢氧化镁沉淀,所以沉淀C的化学式是Mg(OH)2;
(2)碳酸根离子和钙离子、钡离子会生成碳酸钙沉淀、碳酸钡沉淀,所以生成沉淀D的化学方程式是:CaCl2+Na2CO3=CaCO3↓+2NaCl或BaCl2+Na2CO3=BaCO3↓+2NaCl;
(3)加入的过量的碳酸钠和氢氧化钠对于氯化钠也是杂质,所以溶液E中加过量稀盐酸的作用是:除尽过量的碳酸钠和氢氧化钠。
20. B 无 不能;碳酸钠溶液和氢氧化钠溶液都呈碱性,无法验证CO2和NaOH溶液发生了反应 气球变大,瓶内产生白色固体 2NaOH+CO2=Na2CO3+H2O 试管内澄清石灰水变浑浊 对比分析曲线Ⅱ和Ⅰ,CO2和NaOH溶液反应后,容器内气压下降得更低 二、三
【详解】①由于二氧化碳能溶于水,二氧化碳与氢氧化钠反应生成了碳酸钠和水,所以两个塑料瓶中共同的现象都会变瘪,其中二氧化碳与氢氧化钠的反应消耗二氧化碳的量大,B瓶变化程度更大;
②氢氧化钠溶液能使无色酚酞试液变红色,D中滴入酚酞后呈无色,证明B瓶溶液中NaOH已反应完了;碳酸钠溶液和氢氧化钠溶液都呈碱性,无法验证 CO2和 NaOH溶液发生了反应;
③二氧化碳和氢氧化钠反应生成碳酸钠,瓶内气体压强减少,在外界大气压的作用下,气球变大;由于碳酸钠难溶于酒精,形成沉淀析出;发生反应的化学方程式为:2NaOH+CO2=Na2CO3+H2O;碳酸钠和盐酸反应生成二氧化碳,打开止水夹a,观察到试管内澄清石灰水变浑浊;
④根据上述图象,能证明CO2与NaOH溶液发生了反应,理由是对比分析曲线Ⅱ和Ⅰ,CO2和 NaOH 溶液反应后,容器内气压下降得更低;
[总结归纳]通过对以上实验进行分析可知,以上四个实验中,既从反应物消耗角度,又从新物质生成角度,证明NaOH与CO2发生了反应的实验是二、三。。
21.(1)8g
(2)解:设该盐酸中溶质的质量分数为x
x=14.6%
答:该盐酸中溶质的质量分数为14.6%。
【分析】(1)
溶质的质量为:80g×10%=8g
(2)
见答案。
答案第1页,共2页
答案第1页,共2页
一、选择题
1.自来水加入氯气消毒的过程中会发生如下反应,下列说法中不正确的是
A.参加反应的微观粒子个数比为1:1 B.该反应为复分解反应
C.该反应中氯元素的化合价有三种 D.在化学变化中,分子可分,原子不可分
2.下列说法正确的是
A.在滴有石蕊试液的水中通入CO2后溶液变红,说明CO2气体能使石蕊试液变红色
B.铁桶能用来盛氢氧化钠溶液,也能用来盛放稀盐酸
C.熟石灰涂在墙壁表面后变硬,原因是熟石灰与CO2反应生成了坚硬的碳酸钙
D.浓硫酸具有吸水性,因此能用浓硫酸干燥所有气体
3.比较推理是化学学习中常用的思维方法,下列有关物质的比较推理中正确的是
A.铁在潮湿的空气中易腐蚀,故铝在潮湿的空气中也易腐蚀
B.钢比纯铁硬,故黄铜比纯铜硬
C.氢氧化铝可治疗胃酸过多,故氢氧化钠也可治疗胃酸过多
D.厨房洗涤剂对油污有乳化作用,故汽油对油污也有乳化作用
4.下列课外实验中,不能达到实验目的的是
A.用紫甘蓝和酒精溶液自制酸碱指示剂
B.用食醋可除去热水壶内壁的水垢
C.用10%的氯化钠溶液浸泡新鲜的树叶,制作叶脉书签
D.用报纸和保鲜膜分别蒙住盛等体积水的两只相同的烧杯,比较报纸和保鲜膜的透气性
5.下列关于酸、碱、盐的说法正确的是
A.碱溶液一定显碱性,显碱性的也一定是碱溶液
B.酸碱中和反应生成盐和水,所以生成盐和水的也一定是中和反应
C.施铵态氮肥时不可以配合呈碱性的草木灰一起使用
D.大量浓硫酸溅到皮肤上,最好先用干布擦拭,再用水冲,最后涂氢氧化钠溶液
6.下列物质的用途与其化学性质有关的是
A.用干冰人工降雨 B.用石墨做电极
C.用稀盐酸除水垢 D.用氦气充探空气球
7.下列知识整理的内容不完全正确的一组是( )
A 食品保鲜的办法 B 灭火实例与原理
填充氮气——防止变质 放入生石灰——防止受潮 放入细铁粉———防止受潮和变质 油锅着火时用锅盖盖灭——隔绝空气 住宅失火时用水灭火——降低着火点 扑灭森林火灾时设置隔离带——隔离可燃物
C 日常物质的区别 D 化学中常见的“三”
硬水和软水——加肥皂水并搅拌 区别氢氧化钠溶液和石灰水——通入二氧化碳 氯化铵和磷矿粉——观察颜色 三种可燃性气体——H2、CO、CH4 三种可加热仪器——试管、烧杯、蒸发皿 三种构成物质的粒子——分子、原子、离子
A.A B.B C.C D.D
8.作为生命之源的水同时也是最重要的化学物质之一、下列关于水的说法正确的是
A.水在直流电的作用下分解,在电源的正负极上分别产生氢气和氧气
B.在日常生活中常用煮沸的方法将软水变成硬水
C.许多化学反应需要在水作溶剂的溶液中进行
D.纯水的pH为0
9.构建化学基本观念是学好化学的基础,下列有关化学基本观念的认识正确的是
A.微粒观:稀盐酸和稀硫酸中都有氢离子,所有化学性质完全相同
B.元素观:元素组成完全相同的物质,其化学性质也一定相同
C.变化观:化学反应后有氧气生成的物质中,一定含有氧元素
D.守恒观:10g氢气与10g氧气充分反应后,一定生成20g水
10.下列各组物质的化学式书写都正确的是
A.银Ag、水银Hg B.苏打NaCO3、小苏打NaHCO3
C.生石灰CaO、熟石灰CaOH D.氧化铁FeO、四氧化三铁Fe3O4
11.以下对某一主题知识进行的归纳,正确的一组是
A.性质与用途 B.安全常识
石墨能导电——作电极 活性炭有吸附性——作冰箱除臭剂 不明洞穴探险——先做灯火实验 家中石油气泄漏——立即打开排气扇
C.健康常识 D.物质分类
人体缺铁——易患贫血病 人体缺锌——易患佝偻病 常见的碱——熟石灰、烧碱、纯碱 常见的干燥剂——浓硫酸、生石灰、碱石灰
A.A B.B C.C D.D
12.化学知识在生产和生活中有着重要的应用,下列说法中不正确的是
A.鱼骨粉的主要成分是碳酸钙,可用于补钙
B.明矾可使水中悬浮小颗粒快速沉降,也可用于自来水的消毒杀菌
C.发酵粉中含有较多的NaHCO3、,能使焙制出的糕点疏松多孔
D.纯碱也叫苏打,可用于清洗厨房用具的油污
二、填空与简答
13.在抗击“新冠肺炎病毒”期间,消毒剂在公共场所进行卫生防疫时发挥着重要的作用,其中84消毒液[有效成分为次氯酸钠(NaClO)]和二氧化氯(ClO2)是常用消毒剂。
(1)“84消毒液”的有效成分为NaClO,其中氯元素的化合价为 ;使用“84 消毒液” 消毒时,常用水稀释,稀释后测得消毒液的pH=9,该溶液呈 性。
(2)ClO2是一种环保型杀菌消毒剂,生活中常用ClO2消毒饮用水,ClO2是属于 (填序号)。
A混合物 B化合物 C氧化物
14.下列是一些与人类的生产、生活密切相关的物质。
a.75%的酒精溶液;b.铝;c.一氧化碳;d.氢氧化钙;e.氯化钠;f.碳酸氢钠
请选择适当的物质,用其字母序号填空。
(1) 可用作食品调味;
(2) 可用于工业冶炼铁:
(3) 可用于制作炊具;
(4) 可用于改良酸性土壤;
(5)医院常用 消毒杀菌。
(6)制作馒头过程中加入 使蒸好的馒头疏松多孔。
15.常用的农药绝大多数都是用 方法配制或合成的。例如波尔多液就是用 、 和 混合制得的,是一种天蓝色、黏稠的悬浊液,它是一种广泛使用的 剂。
16.中和反应是重要的化学反应。图1是氢氧化钠溶液和稀硫酸反应的示意图。图2是向氢氧化钠溶液中滴加硫酸时电导率的变化情况。查阅资料:①单位体积溶液中某离子的个数越多,则该离子的浓度越大,溶液的导电能力越强。②溶液的导电能力越强,溶液的电导率越大。
(1)观察图1,该反应中未发生变化的离子是 (写离子符号)。
(2)图2中N点溶液中的溶质有哪些? (写化学式)。
17.生产生活中,化学无处不在。从A.石墨;B.二氧化硫;C.熟石灰;D.氢气;E.稀有气体等物质中,选择与下列叙述相应的物质并用字母编号填空:
(1)可用作建筑材料的是 。
(2)形成酸雨的主要气体是 。
(3)可用于制造干电池电极的是 。
(4)可用于填充霓虹灯的是 。
(5)可作为清洁绿色能源是 。
18.如图,物质王国中的A~F及X种物质玩“独木桥”游戏,其中A~F分别是稀盐酸,氢气,氧化铜,氢氧化钙溶液,碳酸钠溶液,二氧化碳六种物质中的一种
(1)搭桥
游戏规则:A~F搭桥后相邻的物质之间能发生化学反应(所涉及反应均为初中常见化学反应)。已知E的俗名叫澄清石灰水,请回答下列问题:
①F的化学式是 ;
②A与B反应的实验现象 ;
③C与D反应的化学方程式是 。
(2)过桥:
游戏规则:若A~F每种物质分别通过一步反应都能直接转化为X,则X就可以成功过桥,请推测物质X的化学式是 。
19.工业上粗盐(含MgCl2、CaCl2、Na2SO4等杂质),精制的工艺流程如下:
(1)X中含有的阳离子是 ;沉淀C的化学式是 。
(2)写出生成沉淀D的一个化学方程式 。
(3)溶液E中加过量稀盐酸的作用是 。
三、科学探究题
20.学习小组尝试从反应物消耗和新物质生成两个不同的角度,验证 CO2与 NaOH溶液发生了反应。
【查阅资料】
Ⅰ.常温下,NaOH易溶于水也易溶于酒精,Na2CO3易溶于水但难溶于酒精。
Ⅱ.BaCl2溶液呈中性,CO2不溶于酒精也与酒精不反应。
【实验探究】(相关装置气密性良好,省略夹持仪器)
实验一 实验二 实验三
①实验一:振荡后,两个软塑料瓶中变瘪程度更大的是 (选填“A”或“B”)。
②实验二:D中滴入酚酞后呈 色,证明B瓶溶液中NaOH已反应完了。若C中不加BaCl2溶液,直接滴入酚酞试液,能否达到实验目的?理由是 。
③实验三:关闭止水夹a,注入足量饱和的NaOH的酒精溶液,振荡后观察到的现象是 ,发生反应的化学方程式为 。一段时间后,注入足量的稀盐酸,打开止水夹a,观察到的现象是 。
④实验四:向瓶中分别加入等体积的蒸馏水和 NaOH 溶液,用传感器测得瓶中气压变化的图象,如图所示。
分析上述图象,能否证明CO2与NaOH溶液发生了反应?理由是 。
【总结归纳】
以上四个实验中,既从反应物消耗角度,又从新物质生成角度,证明NaOH与CO2发生了反应的实验是 (选填“一”、“二”、“三”或“四”)。
四、计算题
21.欲测定一瓶标签破损的盐酸中溶质的质量分数,现将50g该盐酸样品与80g溶质的质量分数为10%的氢氧化钠溶液混合,恰好完全反应。
(1)80g该氢氧化钠溶液中所含溶质的质量为 。
(2)计算该盐酸中溶质的质量分数 。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.B
【分析】由微观示意图分析可知,该反应为。
【详解】A.参加反应的微观粒子个数比为1:1,选项说法正确。
B.该反应由单质和化合物反应生成另外两种化合物,不属于复分解反应,选项说法错误。
C.该反应中氯元素的化合价有三种:Cl2中为0价,HCl中为-1价,HClO中为+1价,选项说法正确。
D.在化学变化中,分子可分,原子不可分,选项说法正确。
故选:B。
2.C
【详解】A、在滴有石蕊试液的水中通入CO2后溶液变红,是因为CO2气体和水反应生成的碳酸,碳酸呈酸性,能使石蕊试液变红色,故选项说法错误;
B、Fe不能与NaOH反应,则铁桶能用来盛氢氧化钠溶液;Fe金属活动性大于H,能与稀盐酸反应生成氢气,则铁桶不能用来盛放稀盐酸,故选项说法错误;
C、熟石灰是氢氧化钙的俗称,熟石灰涂在墙壁表面后变硬,原因是氢氧化钙与CO2反应生成了坚硬的碳酸钙,故选项说法正确;
D、浓硫酸具有吸水性,但是不能用浓硫酸干燥所有气体,例如氨气,因为氨气能与硫酸发生反应生成硫酸铵,故选项说法错误。
故选C。
3.B
【详解】A、铁与空气中的氧气和水接触,会生锈,故铁在潮湿的空气中易腐蚀,而铝能与空气中的氧气反应生成一层致密的氧化铝薄膜,从而阻止铝进一步被氧化,故铝在潮湿的空气中不易腐蚀,不符合题意;
B、合金比组成它的纯金属硬度大,钢是铁的合金,故钢比纯铁硬,黄铜是铜锌合金,故黄铜比纯铜硬,符合题意;
C、氢氧化铝能与盐酸反应生成氯化铝和水,可用于治疗胃酸过多,但是氢氧化钠腐蚀性较强,不能用于治疗胃酸过多,不符合题意;
D、洗涤剂具有乳化作用,能将油污乳化为细小油滴,随水冲走,故可用于去油污,而汽油能去油污,是因为汽油能溶解油污,不符合题意。
故选B。
4.C
【详解】A、某些植物的花瓣的汁液可作酸碱指示剂,可用酒精浸泡得到溶液,可用紫甘蓝和酒精溶液自制酸碱指示剂,故选项课外实验能达到实验目的。
B、水垢的主要成分是碳酸钙,能与食醋中的醋酸反应生成易溶于水的醋酸钙,可除去热水壶内的水垢,故选项课外实验能达到实验目的。
C、氯化钠溶液不具有腐蚀性,不能制作叶脉书签,应使用氢氧化钠溶液,故选项课外实验不能达到实验目的。
D、用报纸和保鲜膜分别蒙住盛等体积水的两只相同的烧杯,可以比较报纸和保鲜膜的透气性,故选项课外实验能达到实验目的。
故选C。
5.C
【详解】A、碱性溶液不一定都是碱,如碳酸钠的溶液呈碱性但碳酸钠是盐不是碱,故选项说法错误;B、酸碱中和反应生成盐和水,但生成盐和水的反应不一定是中和反应,如CO2+2NaOH═Na2CO3+H2O,故选项说法错误;C、铵态氮肥与草木灰混合使用,会产生氨气,降低肥效,故选项说法正确;D、浓硫酸具有较强的腐蚀性,不慎沾到皮肤上,先用干布拭干,然后用大量清水冲洗,后涂上3%~5%的碳酸氢钠溶液,故选项说法错误。故选C。
6.C
【详解】A、用干冰人工降雨是利用干冰升华吸热使周围温度降低,利用的是物质的物理性质,错误;
B、用石墨做电极利用石墨的导电性,属于物理性质,错误;
C、用稀盐酸除水垢是利用盐酸能与水垢的主要成分碳酸钙、氢氧化镁反应,属于物质的化学性质,正确;
D、用氦气充探空气球利用氦气的密度比空气小,属于物质的物理性质,错误;
故选C。
7.B
【详解】A、氮气性质稳定,填充氮气可以防止变质;生石灰和水反应生成氢氧化钙,放入生石灰可以防止受潮;铁和水、氧气生成氧化铁,放入细铁粉可以防止受潮和变质,内容完全正确;
B、油锅着火时用锅盖盖灭是隔绝空气;住宅失火时用水灭火是降低温度至可燃物着火点以下;扑灭森林火灾时设置隔离带是隔离可燃物,内容不完全正确;
C、硬水和软水中加肥皂水并搅拌,产生泡沫较多的是软水,产生泡沫较少的是硬水;二氧化碳和氢氧化钙反应是碳酸钙沉淀,二氧化碳和氢氧化钠反应不生成沉淀,区别氢氧化钠溶液和石灰水通入二氧化碳,产生沉淀的是石灰水,不产生沉淀的是氢氧化钠溶液;氯化铵是白色固体,磷矿粉是灰色固体,氯化铵和磷矿粉观察颜色可以区别,内容完全正确;
D、H2、CO、CH4均是可燃性气体;试管、烧杯、蒸发皿均是可加热仪器;分子、原子、离子均是构成物质的粒子,内容完全正确。
故选B。
8.C
【详解】A、电解水实验中,正氧负氢,在电源的正、负极上分别产生氧气和氢气,选项说法不正确;
B、加热煮沸时,水中的钙离子、镁离子能够以碳酸钙沉淀、氢氧化镁沉淀的形式从水中析出从而降低水的硬度,因此煮沸能降低水硬度,变成软水,选项说法不正确;
C、两种物质相互接触的面积越大,反应的速率越快,由于溶液是均一稳定的混合物,在溶液中两种物质接触面积大,化学反应的速率快,选项说法正确;
D、纯水的pH为7,选项说法不正确。
故选C。
9.C
【详解】A、稀盐酸和稀硫酸中都有氢离子,所以它们具有一些共同的化学性质,但是它们的化学性质并不是完全相同 的,因为解离出的酸根离子不同,故A认识错误;
B、元素组成完全相同的物质,其化学性质不一定相同,例如一氧化碳和二氧化碳都是由碳元素和氧元素组成的化合物,但是二者的分子构成不同,所以二者的化学性质不同,故B认识错误;
C、根据质量守恒定律,化学反应前后元素种类不变,所以化学反应后有氧气生成的物质中,一定含有氧元素,故C认识正确;
D、氢气与氧气点燃生成水,即,有反应方程式可知,参加反应的氢气、氧气与生成的水的质量比为4:32:36=1:8:9,所以当10g氢气与10g氧气充分反应后,氢气有剩余,根据质量守恒定律,所以生成水的质量<20g,故D认识错误;
故选C。
10.A
【详解】A、由原子直接构成的物质,直接用元素符号来表示,若元素中含有两个字母,第一个字母要大写,第二个字母要小写,银的化学式为Ag、水银是汞的俗称,化学式为Hg,故A正确;
B、苏打是碳酸钠的俗称,碳酸钠中钠元素显+1价,碳酸根离子显-2价,其化学式为Na2CO3,小苏打是碳酸氢钠的俗称,碳酸氢钠由钠离子和碳酸氢根离子构成,钠离子显+1价,碳酸氢根离子显-1价,化学式为NaHCO3,故B错误;
C、生石灰是氧化钙的俗称,化学式为CaO,熟石灰是氢氧化钙的俗称,氢氧化钙中钙元素显+2价,氢氧根显-1价,其化学式为Ca(OH)2,故C错误;
D、氧化铁中铁元素显+3价,氧元素显-2价,其化学式为Fe2O3,根据“先读后写”,四氧化三铁的化学式为Fe3O4,故D错误。
故选A。
11.A
【详解】A、石墨具有良好的导电性,可作电极;活性炭有很强的吸附性,能除去异味和色素,可作冰箱除臭剂,此选项正确;
B、不明洞穴探险,先做灯火实验,以检查洞穴内二氧化碳的含量;家中石油气泄漏,立即关闭活塞,不能打开排气扇,以防发生爆炸,此选项不完全正确,不符合题意;
C、人体缺铁,易患贫血病;人体缺钙,易患佝偻病,此选项不完全正确,不符合题意;
D、熟石灰是氢氧化钙的俗称,烧碱是氢氧化钠的俗称,它们是常见的碱,纯碱是碳酸钠,碳酸钠属于盐;浓硫酸、生石灰、碱石灰是常见的干燥剂,此选项不完全正确,不符合题意。
故选A。
12.B
【详解】A、鱼骨粉的主要成分是碳酸钙,可用于补钙,正确;B、明矾中的铝离子水解得到的氢氧化铝能净水,但是不具有杀菌作用,错误;C、NaHCO3与面粉中产生的氢离子反应生成二氧化碳,使焙制出的糕点疏松多孔,正确;D、碳酸钠俗称苏打或纯碱,纯碱溶液显碱性,油污在碱性条件下可水解,且水解为不可逆过程,则使用纯碱清洗厨房用具的油污,正确。故选B。
13. +1 碱 C
【详解】(1)根据化合物中元素正负化合价的代数和为零可知,NaClO中钠元素为+1价,氧元素为-2价,所以氯元素为+1价,故填写:+1;
根据pH与溶液酸碱性的关系:pH<7,显酸性,pH=7,显中性,pH>7,显碱性可知,稀释后测得消毒液的pH=9>7,显碱性,故填写:碱;
(2)根据氧化物是由两种元素组成,其中一种为氧元素的化合物可知,ClO2是属于氧化物,故填写:C。
14. e c b d a f
【详解】(1)氯化钠可作作调味品,故填:e;
(2)一氧化碳具有还原性,可用于工业冶炼铁,故填:c;
(3)铝具有良好的导热性,可用于制作炊具,故填:b;
(4)氢氧化钙呈碱性,常用于改良酸性土壤,故填:d;
(5)体积分数为75%的酒精溶液常用于灭菌消毒,此浓度杀菌力最强.在75%的酒精作用下,乙醇能渗入细胞内,使蛋白质凝固变性,从而起到杀菌的作用,故填:a;
(6)制作馒头过程中加入碳酸氢钠,碳酸氢钠受热时会产生二氧化碳气体,且能与酸性物质反应生成二氧化碳,使蒸好的馒头疏松多孔,故填:f。
15. 化学 胆矾/ 生石灰/CaO 水/H2O 杀菌
【详解】大多数农药需要通过其他物质合成,该过程有新物质生成,属于化学变化,故填化学;
波尔多液是用水与生石灰混合,得到石灰乳,并将剩余的水与硫酸铜混合得到硫酸铜溶液,最后使用时将硫酸铜溶液慢慢倒入石灰乳中,并不断搅拌,即可得到蓝色胶状悬浊液,是常用的杀菌剂。故填胆矾;生石灰;水;杀菌;
16.(1)、
(2)Na2SO4、H2SO4
【详解】(1)由图1可知,氢离子与氢氧根离子结合成了水分子,钠离子和硫酸根离子没有发生改变,离子符号分别为:、;
(2)氢氧化钠和稀硫酸反应生成硫酸钠和水,溶液离子浓度减小,直至将氢氧化钠消耗完全时,溶液中离子浓度最小,导电率最低,即M点,继续滴加硫酸溶液,离子浓度逐渐变大,电导率变大,所以N点所示溶液中的溶质硫酸钠、硫酸,化学式为:Na2SO4、H2SO4;
17. C B A E D
【详解】(1)熟石灰为氢氧化钙,将熟石灰加水做成石灰浆,用于抹墙,在吸收二氧化碳后变为坚硬的碳酸钙,是很好建筑材料,所以熟石灰可以用作建筑材料;
(2)二氧化硫溶于水生成亚硫酸,亚硫酸被氧化可以生成硫酸,另外二氧化硫也可以被氧化生成三氧化硫,三氧化硫溶于水生成硫酸,最终都可生成硫酸,形成酸雨;
(3)石墨具有良好的导电性,所以常用作干电池的电极;
(4)稀有气体可以通过或吸收不同波长的光,所以常用于填充霓虹灯,作为电光源使用;
(5)氢气燃烧后只生成水,无其他物质生成,放出热量较高,被称为清洁绿色能源。
18. 黑色固体变红色
【分析】A~F分别是盐酸,氢气,氧化铜,氢氧化钙,碳酸钠,二氧化碳六中物质中的一种,搭桥:规则是A~F搭桥后相邻的物质之间能发生化学反应,E的俗名叫熟石灰,氢氧化钙会与碳酸钠、盐酸反应,氢气只会与氧化铜反应,A或F可能是氢气,当F是氢气时,不会与氢氧化钙反应,当A是氢气,B是氧化铜,氧化铜会与稀盐酸反应,C是稀盐酸,D是碳酸钠,F是二氧化碳;过桥:若A~F分别通过一步反应能直接转化为X,则X可成功过桥,氢气和氧化铜反应生成水,氧化铜和盐酸反应生成水,盐酸和碳酸钠反应生成水,碳酸钠和氢氧化钙反应生成水,氢氧化钙和二氧化碳反应生成水,X是水。
【详解】(1)①E的俗名叫熟石灰,氢氧化钙会与碳酸钠、盐酸反应,氢气只会与氧化铜反应,A或F是氢气,当F是氢气时,不会与氢氧化钙反应,当A是氢气,B是氧化铜,氧化铜会与稀盐酸反应,C是稀盐酸,D是碳酸钠,F是二氧化碳,故F的化学式是。
②A与B反应是氢气和氧化铜在加热的条件下生成铜和二氧化碳,故实验现象是黑色固体变红色。
③C与D反应是碳酸钠和盐酸反应生成氯化钠、水和二氧化碳,反应的化学方程式为。
(2)A~F分别通过一步反应能直接转化为X,则X可成功过桥,氢气和氧化铜反应生成水,氧化铜和盐酸反应生成水,盐酸和碳酸钠反应生成水,碳酸钠和氢氧化钙反应生成水,氢氧化钙和二氧化碳反应生成水,X是水,故X的化学式是。
【点睛】E的俗名叫熟石灰,E是氢氧化钙,氢气和氧化铜在加热的条件下生成铜和二氧化碳,碳酸钠和盐酸反应生成氯化钠、水和二氧化碳,氧化铜和盐酸反应生成氯化铜和水。
19. Ba2+ Mg(OH)2 CaCl2+Na2CO3=CaCO3↓+2NaCl或BaCl2+Na2CO3=BaCO3↓+2NaCl 除尽过量的Na2CO3和NaOH
【分析】工业上粗盐(含MgCl2、CaCl2、Na2SO4等杂质)的精制实际上是除去镁离子、钙离子、硫酸根离子的过程。
【详解】(1)粗盐中含有MgCl2、CaCl2、Na2SO4等杂质,所以X中含有的阳离子是Ba2+,X是氯化钡溶液,加入过量的X生成了硫酸钡沉淀;溶液A中含有镁离子,氢氧根离子和镁离子会生成氢氧化镁沉淀,所以沉淀C的化学式是Mg(OH)2;
(2)碳酸根离子和钙离子、钡离子会生成碳酸钙沉淀、碳酸钡沉淀,所以生成沉淀D的化学方程式是:CaCl2+Na2CO3=CaCO3↓+2NaCl或BaCl2+Na2CO3=BaCO3↓+2NaCl;
(3)加入的过量的碳酸钠和氢氧化钠对于氯化钠也是杂质,所以溶液E中加过量稀盐酸的作用是:除尽过量的碳酸钠和氢氧化钠。
20. B 无 不能;碳酸钠溶液和氢氧化钠溶液都呈碱性,无法验证CO2和NaOH溶液发生了反应 气球变大,瓶内产生白色固体 2NaOH+CO2=Na2CO3+H2O 试管内澄清石灰水变浑浊 对比分析曲线Ⅱ和Ⅰ,CO2和NaOH溶液反应后,容器内气压下降得更低 二、三
【详解】①由于二氧化碳能溶于水,二氧化碳与氢氧化钠反应生成了碳酸钠和水,所以两个塑料瓶中共同的现象都会变瘪,其中二氧化碳与氢氧化钠的反应消耗二氧化碳的量大,B瓶变化程度更大;
②氢氧化钠溶液能使无色酚酞试液变红色,D中滴入酚酞后呈无色,证明B瓶溶液中NaOH已反应完了;碳酸钠溶液和氢氧化钠溶液都呈碱性,无法验证 CO2和 NaOH溶液发生了反应;
③二氧化碳和氢氧化钠反应生成碳酸钠,瓶内气体压强减少,在外界大气压的作用下,气球变大;由于碳酸钠难溶于酒精,形成沉淀析出;发生反应的化学方程式为:2NaOH+CO2=Na2CO3+H2O;碳酸钠和盐酸反应生成二氧化碳,打开止水夹a,观察到试管内澄清石灰水变浑浊;
④根据上述图象,能证明CO2与NaOH溶液发生了反应,理由是对比分析曲线Ⅱ和Ⅰ,CO2和 NaOH 溶液反应后,容器内气压下降得更低;
[总结归纳]通过对以上实验进行分析可知,以上四个实验中,既从反应物消耗角度,又从新物质生成角度,证明NaOH与CO2发生了反应的实验是二、三。。
21.(1)8g
(2)解:设该盐酸中溶质的质量分数为x
x=14.6%
答:该盐酸中溶质的质量分数为14.6%。
【分析】(1)
溶质的质量为:80g×10%=8g
(2)
见答案。
答案第1页,共2页
答案第1页,共2页
