【浙教版】2024年春初二科学讲义5表示元素和物质的符号-答案附后
文档属性
| 名称 | 【浙教版】2024年春初二科学讲义5表示元素和物质的符号-答案附后 |
|
|
| 格式 | docx | ||
| 文件大小 | 1.5MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2024-03-29 00:00:00 | ||
图片预览



文档简介
中小学教育资源及组卷应用平台
5 表示元素和物质的符号
一、组成物质的元素
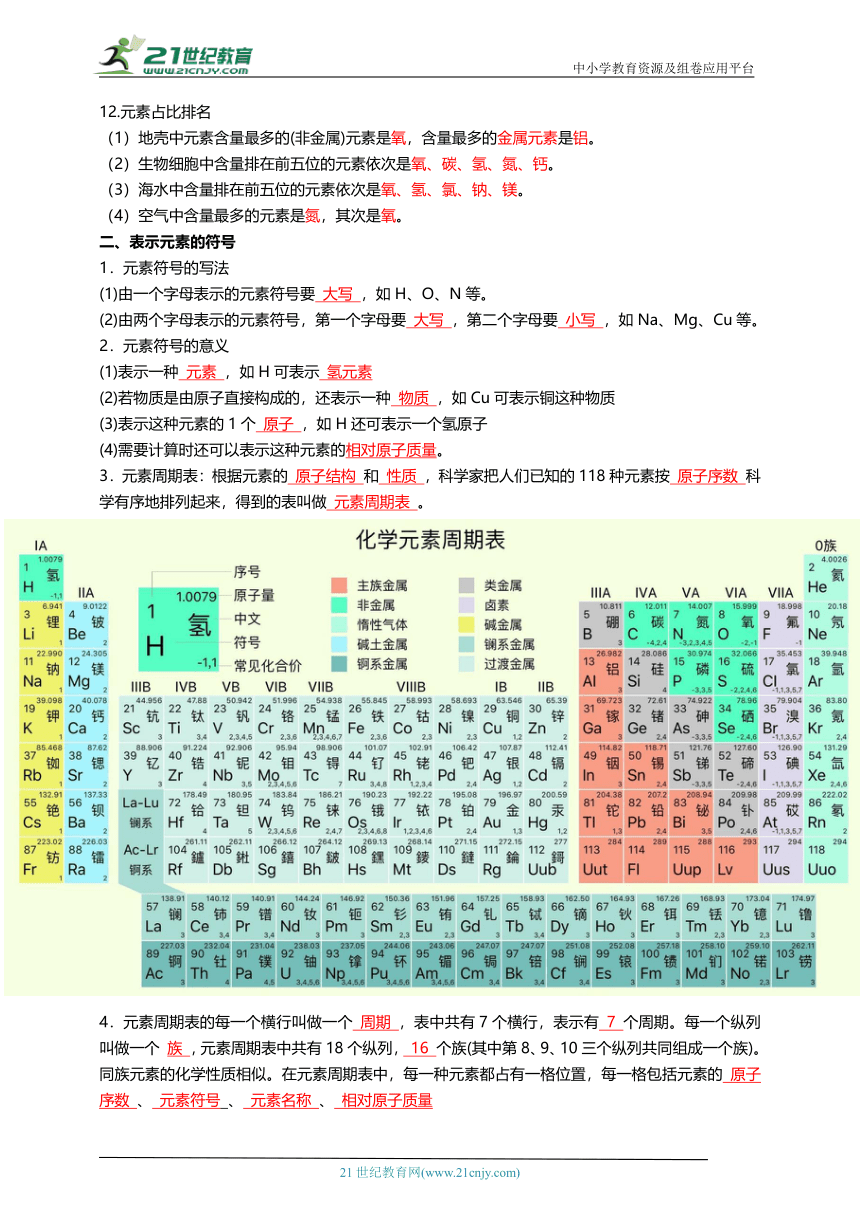
1.目前人类已知的元素有118种,其中有些是人造元素。世界上大部分物质只是由几十种常见元素组成的,其中仅碳 、 氢 、 氧 三种元素就能组成许许多多种物质。
2.人们通常把元素分为 金属 元素和 非金属 元素(包括 稀有气体元素 ,如氩元素)。在118种元素中, 金属 元素占大多数。金属元素的名称一般都以“钅”作偏旁(汞除外);非金属元素的名称一般都以“石”“氵”“气”作偏旁,其中以“石”为偏旁的一般为固态非金属元素,以“氵”为偏旁的一般为液态非金属元素,以“气”为偏旁的一般为气态非金属元素
3.单质和化合物的比较
单质 化合物
概念 由 同种 元素组成的 纯净物 由 不同种 元素组成的 纯净物
宏观组成 一种元素 至少两种元素
微观构成 同种原子或同种原子构成的同种分子 不同种原子构成的同种分子或不同种离子
举例 铁Fe、氧气O2 二氧化碳CO2、氯化钠NaCl
相同点 都是纯净物
4.由同种元素组成的物质不一定是纯净物,也可能是混合物。如氧气(O2)和臭氧(O3)的混合物只由氧元素组成
5.元素是宏观概念,可以讲种类,但不能讲个数。如描述二氧化碳的元素组成时,只能说“二氧化碳是由氧元素和碳元素组成的”,而不能说“二氧化碳是由一个碳元素和两个氧元素组成的”。
6.物质、元素、分子、原子间的关系
7.地壳主要由 氧 、硅 、铝 、铁 、钙、钠、钾、镁、氢等元素组成,其中含量最高的是 氧 ,其次是 硅 。金属元素中含量最高的是 铝 ,其次是 铁 。
8.人体中的元素及作用
(1)人体内大约含有30多种元素,其中11种(C、H、O、N、S、P、Cl、Ca、Mg、Na、K)为大量元素,约占99.95%,其余为 微量 元素。它们中有些是必需元素,每一种必需元素在体内都有一个适量范围, 过多 或 过少 都不利于人体健康。另外,人体内也含有一些有害元素,如镉、汞、铅等。
(2)人体含量最高的元素是 氧 元素,含量最高的金属元素是 钙 元素。
(3) 钙 元素能促进儿童骨骼生长; 铁 元素能预防贫血; 碘 元素能预防甲状腺肿大; 氟 元素能预防龋齿; 锌 元素能增进食欲,促进儿童的生长发育; 硒 元素能预防癌症。
9.海水中,除了水由氢、氧两种元素组成以外,含量较高的是 氯 元素、 钠 元素和 镁 元素,还有一些贵重金属,如金等
10.有机化合物中大都含有 碳 、 氢 、 氧 三种元素。
11.人造元素是通过核反应制得的,其中有些人造元素和天然元素具有 放射性 。放射性元素对人体有害,但利用放射性可以检查和治疗一些疾病、灭菌和消毒。
12.元素占比排名
(1)地壳中元素含量最多的(非金属)元素是氧,含量最多的金属元素是铝。
(2)生物细胞中含量排在前五位的元素依次是氧、碳、氢、氮、钙。
(3)海水中含量排在前五位的元素依次是氧、氢、氯、钠、镁。
(4)空气中含量最多的元素是氮,其次是氧。
二、表示元素的符号
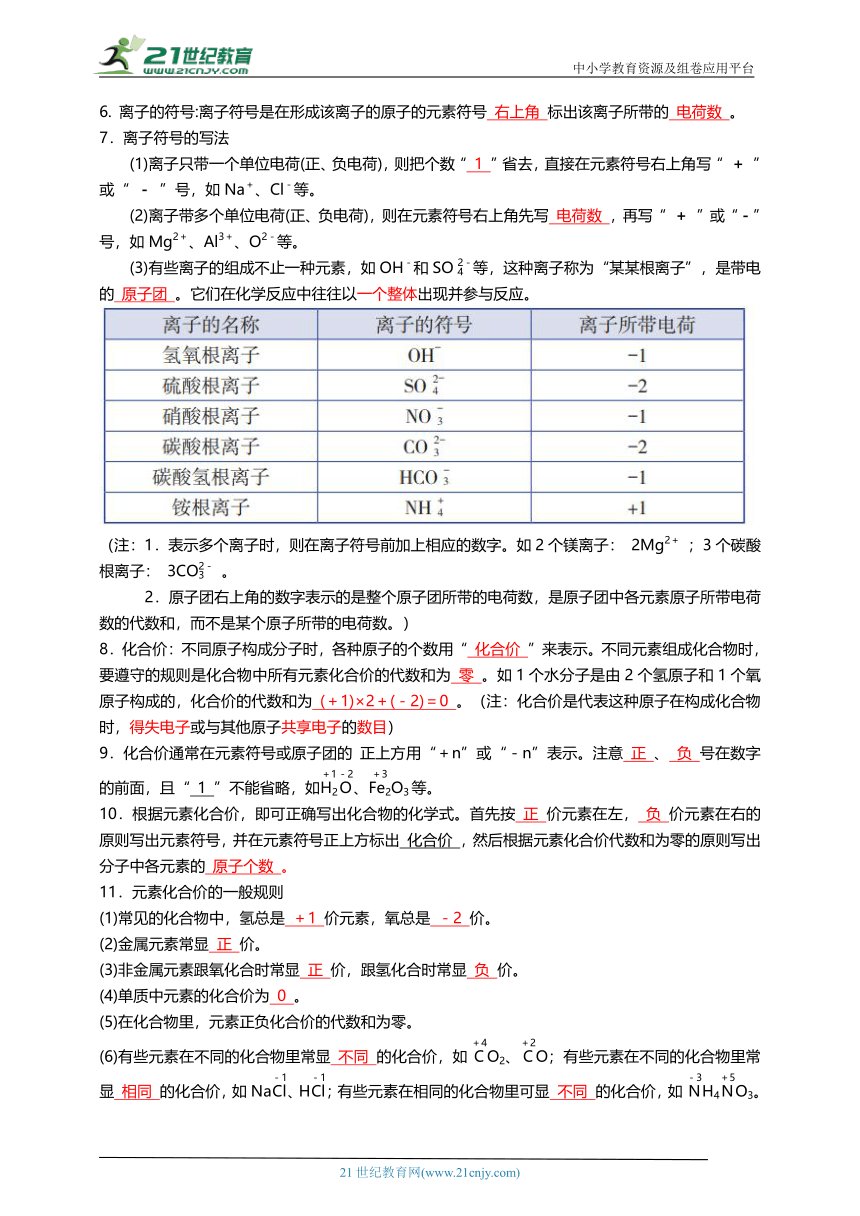
1.元素符号的写法
(1)由一个字母表示的元素符号要 大写 ,如H、O、N等。
(2)由两个字母表示的元素符号,第一个字母要 大写 ,第二个字母要 小写 ,如Na、Mg、Cu等。
2.元素符号的意义
(1)表示一种 元素 ,如H可表示 氢元素
(2)若物质是由原子直接构成的,还表示一种 物质 ,如Cu可表示铜这种物质
(3)表示这种元素的1个 原子 ,如H还可表示一个氢原子
(4)需要计算时还可以表示这种元素的相对原子质量。
3.元素周期表:根据元素的 原子结构 和 性质 ,科学家把人们已知的118种元素按 原子序数 科学有序地排列起来,得到的表叫做 元素周期表 。
4.元素周期表的每一个横行叫做一个 周期 ,表中共有7个横行,表示有 7 个周期。每一个纵列叫做一个 族 ,元素周期表中共有18个纵列, 16 个族(其中第8、9、10三个纵列共同组成一个族)。同族元素的化学性质相似。在元素周期表中,每一种元素都占有一格位置,每一格包括元素的 原子序数 、 元素符号 、 元素名称 、 相对原子质量
三、表示物质的符号
1.化学式定义:用 元素符号 来表示物质组成的式子叫做化学式。如二氧化碳分子可表示成“ CO2 ”。
2.单质化学式的写法
(1)稀有气体是由原子直接构成的,通常就用 元素符号 来表示它们的化学式。金属单质和固态非金属单质的结构比较复杂,习惯上也用 元素符号 来表示它们的化学式。如氩气、铝、磷分别用 Ar 、 Al 、 P 来表示。
(2)对于多原子分子构成的单质,先写出组成单质的 元素符号 ,再在元素符号右下角写上构成这个单质分子的 原子数目 。如氧气、氢气、溴水、碘、臭氧分别用 O2 、H2 、Br2 、I2 、O3 来表示。
3.化合物化学式的写法(正价在左、负价在右)
(1)按一定顺序写出组成化合物的所有元素符号:①氧元素与另一元素组成的化合物,一般要把氧元素符号写在 右 边;②氢元素与另一元素组成的化合物,一般要把氢元素符号写在 左 边;(记住两个特例:NH3 CH4)③金属元素、氢元素与非金属元素组成的化合物,一般要把 非金属 元素符号写在右边。
(2)在每种元素符号的右下角用数字写出每个化合物分子中该元素的 原子个数 。直接由离子构成的化合物,其化学式常用其离子 最简单整数比 表示。
4.化学式的读法,一般是从右向左叫做“某化某”,如“CuO”读作“ 氧化铜 ”。当1个分子中原子个数不止1个时,还要指出1个分子里元素的原子个数,如“P2O5”读作“ 五氧化二磷 ”。
5.化学式的意义
化学式的意义 以CO2为例
宏 观 表示一种物质 表示 二氧化碳 这种物质
表示该物质的元素组成 表示二氧化碳是由 碳 元素和 氧 元素组成的
微 观 表示构成物质的基本微粒 表示二氧化碳是由 二氧化碳分子 构成的
由分子构成的物质的化学式可表示该物质的一个分子 表示 一个二氧化碳分子
表示物质的分子构成 表示一个二氧化碳分子是由一个 碳原子 和两个 氧原子 构成的
如果在化学式前面加上系数,就表示某物质的几个分子如2个氧气分子可用 2O2 表示。
(注:1.化学式不能凭空想象,而应由实验确定,一种物质只有一个化学式。
2.对于任何一种纯净物而言,其组成是固定的,也就是说,一种物质是由哪些元素组成的和这些元素的原子个数比都是一定的,所以每一种纯净物都可以用化学式表示。而混合物的组成是不固定的,因此混合物没有化学式。)
6. 离子的符号:离子符号是在形成该离子的原子的元素符号 右上角 标出该离子所带的 电荷数 。
7.离子符号的写法
(1)离子只带一个单位电荷(正、负电荷),则把个数“ 1 ”省去,直接在元素符号右上角写“ + ”或“ - ”号,如Na+、Cl-等。
(2)离子带多个单位电荷(正、负电荷),则在元素符号右上角先写 电荷数 ,再写“ + ”或“-”号,如Mg2+、Al3+、O2-等。
(3)有些离子的组成不止一种元素,如OH-和SO等,这种离子称为“某某根离子”,是带电的 原子团 。它们在化学反应中往往以一个整体出现并参与反应。
(注:1.表示多个离子时,则在离子符号前加上相应的数字。如2个镁离子: 2Mg2+ ;3个碳酸根离子: 3CO 。
2.原子团右上角的数字表示的是整个原子团所带的电荷数,是原子团中各元素原子所带电荷数的代数和,而不是某个原子所带的电荷数。)
8.化合价:不同原子构成分子时,各种原子的个数用“ 化合价 ”来表示。不同元素组成化合物时,要遵守的规则是化合物中所有元素化合价的代数和为 零 。如1个水分子是由2个氢原子和1个氧原子构成的,化合价的代数和为 (+1)×2+(-2)=0 。(注:化合价是代表这种原子在构成化合物时,得失电子或与其他原子共享电子的数目)
9.化合价通常在元素符号或原子团的 正上方用“+n”或“-n”表示。注意 正 、 负 号在数字的前面,且“ 1 ”不能省略,如、O3等。
10.根据元素化合价,即可正确写出化合物的化学式。首先按 正 价元素在左, 负 价元素在右的原则写出元素符号,并在元素符号正上方标出 化合价 ,然后根据元素化合价代数和为零的原则写出分子中各元素的 原子个数 。
11.元素化合价的一般规则
(1)常见的化合物中,氢总是 +1 价元素,氧总是 -2 价。
(2)金属元素常显 正 价。
(3)非金属元素跟氧化合时常显 正 价,跟氢化合时常显 负 价。
(4)单质中元素的化合价为 0 。
(5)在化合物里,元素正负化合价的代数和为零。
(6)有些元素在不同的化合物里常显 不同 的化合价,如O2、O;有些元素在不同的化合物里常显 相同 的化合价,如Na、H;有些元素在相同的化合物里可显 不同 的化合价,如H4O3。
12.化合价和离子符号的区别与联系如下表所示:
化合价 离子符号
表示 方法 用+1、+2、-1、-2……表示,标在元素符号(或原子团)的正上方(“1”不省略) 用+、2+、-、2-……表示,标在元素符号(或原子团)的右上角(“1”省略)
实例 、 、24 H+、Cl-、Mg2+、S2-、Na+、SO
联系 同种元素(或原子团)的化合价和离子所带的电荷,通常数值相等,正负一致
(注:1.常见元素的化合价口诀:
钾钠氯银正一价,钙钡镁锌正二价;三铝四硅五价磷, 二三铁、二四碳;
二四六硫三五氮,铜汞二价最常见;一五七氯都齐全,单质零价永不变。
2.某些金属元素在不同化合物中常显不同的化合价,如铁元素可显+2、+3两种化合价,命名时习惯上将显较低化合价的铁元素读作“亚铁”,如FeO读作“氧化亚铁”,而Fe2O3读作“氧化铁“。
3.根据化合价写化学式时,物质应是客观存在的,不能根据化合价臆造实际上不存在的物质。)
四、典型例题
(一)考点:组成物质的元素
【例1】(2022上城期中)世界上各种物质都是由一些最基本的元素组成的。下列说法不正确的是( )
A.元素在地壳中的分布是不均匀的,地壳中最多的金属元素是铝
B.海水中有大量的氯化钠,因此含量最高的是氯元素
C.放射性元素对人体有害,但利用放射性可以检查和治疗一些疾病
D.人体内也含有一些有害元素,如镉、汞、铅等,这与食物、水体及大气的污染相关
【例2】(2023建功单元)有关下右图所示的五种物质的说法正确的是( )
A.五种物质都是混合物 B.①②④有相似之处,都盛放了不同状态的同种物质
C.③④属于化合物 D.②和⑤有相似之处:元素种类相同,但分子构成不同
【例3】(2023杭州期中)下列说法正确的是( )
①地壳中最多的金属元素是铝,也就是金属铝
②地壳中非金属元素的总含量大于金属元素,种类少于金属元素
③人体中只含有非金属元素,没有金属元素
④人体中氢、氧元素含量很高,这与水占人体质量的70%以上有关
A.①③④ B.②③④ C.①② D.②④
【例4】(2023临平期中)C60发现使人类了解到一个全新的碳世界,根据图回答下列问题:
①C60属于 (填“单质”或“化合物”)。
②C60这种物质是由 (填“分子”或“原子”)构成。
③C60与金刚石、石墨具有相似的 (填“化学”或“物理”)性质。
(二)考点:表示元素的符号
【例1】(2023上城期中)下列常见元素中,属于金属元素的是( )
A.C B.Cu C.Si D.O
【例2】(2023建功单元)如图为元素周期表的一部分,A~E代表五种不同元素。下列说法不正确的是( )
A原子半径C>D B.核内质子数:E>D
C.B、C同周期且电子层数相同 D.A、D同族且化学性质相似
【例3】(2023乐清期中)天宫课堂中,航天员王亚平用视频展示了在无容器材料实验柜中进行的“锆金属熔化与凝固”实验,锆原子核外电子数为40,中子数为51,相对原子质量为91,元素符号为Zr,请模仿图甲,将该元素对应信息编写到图乙中相应位置,“①”处应填( )
A.91 B.51 C.40 D.11
【例4】(2023柯桥期中)2021年3月,三星堆的再次发掘引人关注,如图的青铜面具就是之前出土的典型文物,三星堆青铜主要成分是铜、铅、锡等,锡的元素符号是“Sn”,下列关于“Sn”表述错误的是( )
A.表示锡这种物质 B.表示一个锡原子
C.表示锡元素 D.表示一个锡分子
(三)考点:表示物质的符号
【例1】(2023建功单元)下列化学式书写都正确的一组是( )
A.硝酸HNO 硫酸H SO 盐酸HCl
B.氧化钙CaO 五氧化二磷P O 二氧化硫SO
C.氢氧化钠NaOH 氢氧化钾KOH 氢氧化钙CaOH
D.氯化钡BaCl 氯化锌ZnCl 硫酸铜CuSO
【例2】(2023玉环期中)在研究空气成分的历史上,许多科学家做了大量的研究。下列是普里斯特利在研究中收集到的各种气体及当时的名称,这些气体中氮元素化合价最低的是( )
A.“亚硝蒸气”(NO2) B.“亚硝空气”(NO)
C.“减缩的亚硝空气”(N2O) D.“燃素化空气”(N2)
【例3】(2023建功单元)在化学王国里,数字被赋予了丰富的内涵.对下列化学用语中数字“2”的说法正确的是( )
①2H ②2NH ③SO ④O ⑤Mg ⑥2OH ⑦H O
A.表示离子个数的是⑤⑥ B.表示离子所带电荷数的是④⑤
C.表示分子中原子个数的是③⑦ D.表示分子个数的是①②
【例4】(2023永嘉期中)2022年11月,比亚迪新能源动力电池生产基地项目落地浙江省温州市水嘉县桥头镇,动力电池领域对氧氧化锂(化学式LiOH)的需求量很大,兴趣小组同学对氧氧化锂及相关的化学用语进行了研究。氢氧化锂(LiOH)化学式表示的意义的理解,不正确的是( )
A.表示氢氧化锂中锂离子和氢氧根离子个数比是1:1
B.表示氢氧化锂由锂元素、氢元素、氧元素组成
C.表示氢氧化锂由1个锂原子、1个氧原子、1个氢原子构成
D.表示氢氧化锂这种物质
【例5】我国科学家发现,亚硒酸钠能消除加速人体衰老的活性氧,亚硒酸钠中硒元素(Se)为+4价,氧元素为﹣2价,则亚硒酸钠的化学式为( )
A.Na2SeO3 B.Na2SeO4 C.NaSeO3 D.Na2SeO2
【例6】(2023建功单元)(1)以下内容请你用最合适的化学符号填空: 地壳中含量最多的金属元素与最多的非金属元素组成的化合物______________, 3个铁离子______________,能保持二氧化硫化学性质的微粒______________,调味品食盐的阳离子______________,相对分子质量最小的物质______________;温度计中填充的液态金属______________; -2价的硫元素______________; 3个氨气分子______________.3个碳酸根离子______________, FeSO 读作______________
硝酸铝______________氖气______________溴水______________
(2)写出“3O42-”中数字的含义:“4”________________________________________
“+6”________________________________________
“2-”________________________________________
“3”________________________________________
五、学力训练
A组 夯实基础
1.(2023建功单元)原子失去或得到电子后,一定不会引起改变的是( )
①电子总数②质子数③化学性质④质量数⑤微粒的电性⑥电子层数
A.③④ B.②③⑥ C.②④ D.②④⑥
2.(2023建功单元)某元素的阳离子A 的核外有10个电子,核内有14个中子,则该元素原子的核电荷数和质量数分别为( )
A .10 24 B.13 24 C.10 27 D.13 27
3.(2023杭州期中)下列元素分类正确的是( )
A.金属元素:Ca Mg Fe Cu
B.非金属元素:P Si Ag C
C.稀有气体元素:He Ne Ar Cl
D.固体非金属元素:O S P Si
4.(2023上城期末)下列有关元素的说法正确的是( )
①地壳中最多的金属元素是铝,也就是金属铝
②对人体而言,钙是微量元素
③元素既可以天然存在也可以人工合成
④人体中H、O元素含量高跟水占人体质量的以上有关
A.①④ B.②③ C.②④ D.③④
5.(2022西湖期中)下列元素符号表示正确的是( )
A.银Hg B.氯Al C.氟Fu D.钙Ca
B组 强化提高
1.(2023鹿城期中)世界是由元素组成的。图中能正确表示地壳中元素含量分布的是( )
A.B.C.D.
2.(2023杭州期中)下列说法正确的是( )
①地壳中最多的金属元素是铝,也就是金属铝
②地壳中非金属元素的总含量大于金属元素,种类少于金属元素
③人体中只含有非金属元素,没有金属元素
④人体中氢、氧元素含量很高,这与水占人体质量的70%以上有关
A.①③④ B.②③④ C.①② D.②④
3.(2022乐清期中)永嘉乌牛早茶味醇气香,茶叶中含有茶氨酸(C7H14O3N2),根据物质的分类,茶氨酸属于( )
A.单质 B.氧化物 C.混合物 D.化合物
4.(2023鹿城期中)钋是一种能够在黑暗中发光的金属,由居里夫人和其丈夫发现。为了纪念居里夫人的祖国波兰,两人将该金属命名为Polonium。则钋的元素符号是( )
A.P B.po C.p D.Po
5.(2023上城期中)下列化学用语与含义相符的是( )
A.O﹣2——氧离子 B.3H2——6个氢原子
C.NaMo2O4——Mo元素的化合价为+6 D.2N2——2个氮分子
6.(2023金东期中)某化合物在水中能完全电离,将该化合物配制成甲、乙、丙三种不同浓度的水溶液,对溶液中所含阴、阳离子数目进行测定,结果如图所示。由图可判断该化合物可能是( )
A.HNO3 B.Fe2(SO4)3 C.Ca(OH)2 D.H2SO4
7.(2023鹿城期中)天宫二号是我国首个空间实验室。在太空舱里常借助铁酸镍 (NiFe2O4 )将宇航员呼出的二氧化碳转化为氧气。已知镍(Ni)元素化合价为+2价,则中铁元素的化合价为( )
A.+2 B.+3 C.+6 D.0
8.(2022绍兴期中)如图是教材中元素周期表的一部分,除标出的元素外,表中的数字编号①~③各表示一种元素。请回答问题。
(1)①表示的元素是 。
(2)1个铝原子的核外电子有 个。
(3)元素硅比第2周期、第ⅥA族的元素在地壳中的含量 (选填“高”或“低”)。
9.(2023永嘉期中)2022北京冬奥会将“科技奥运”显现得淋漓尽致!
(1)国家速滑馆又称“冰丝带”,采用当前冬季运动场馆最环保的制冰技术之一——二氧化碳跨临界直接制冰技术,通过压力变化使二氧化碳汽化实现制冷,二氧化碳跨临界直接制冰技术利用了二氧化碳的 。(填“物理性质”或“化学性质”)
(2)北京冬奥会火种灯的火种燃料为丙烷,如图是丙烷分子微观示意图,则丙烷的化学式为 。
(3)颁奖服内胆使用了第二代石墨烯(由碳元素组成)发热材料,石墨烯属于 (填“单质”或“化合物”)。
10.(2023温州期中)(1)用符号表示下列物质或微粒:
2个亚铁离子 ;5个甲烷分子 ;3个氖原子 ;保持氧气化学性质的最小粒子 。
(2)判断下列化学符号中“2”的意义,并将其序号写在相应位置。
①CO2 ② ③ ④2NH3
表示化合物中元素的化合价 ;表示分子中原子的个数 。
(3)现有铁屑、硫粉、硫化亚铁、氧化汞和海水五种物质,为了区分它们,小希参照二歧分类检索表制作了一个物质检索表,如表所示,请分析乙是 。已知铁屑和硫粉在一定条件下形成硫化亚铁,这属于 变化。
C组 瞄准中考
1.(2023建功单元)化合物MX6。分子呈正八面体结构(正八面体是指由八个全等的正三角形围成的如图所示的几何体)。由于六个X 原子与M的连接完全对称,因此将任意一个X用Y原子替换,均只能得到一种结构的MX5Y 分子,按此思路,若其中任意两个X 原子用Y原子替换,则得到的化学式为MX4Y 的分子( )
A.只有1种结构 B.存在2种不同结构
C.存在3种不同结构 D.存在4种不同结构
2.(2023新昌期末)氕、氘、氚三种不同原子在元素周期表中( )
A.同占一个位置 B.占三个不同的位置 C.不占位置 D.只有氕占位置
3.(2023上城期中)苏打水即碳酸氢钠的水溶液,为人工合成的碳酸饮料,是在经过纯化的饮用水中压入二氧化碳,并添加甜味剂和香料的饮料,含有弱碱性。下列有关苏打水中各成分化学式书写错误的是( )
A.碳酸氢钠(NaHCO3) B.水(H2O) C.二氧化碳(CO2) D.碳酸钠(NaCO3)
4.(2022乐清期末)根据相对原子质量来研究元素,始于19世纪初。
1829年,德国化学家德贝纳提出了锂钠钾、钙锶钡、磷砷锑、氯溴碘等15种元素,他把这些元素称为“三种元素组”。
1864年,德国化学家迈耶,按相对原子质量递增顺序制定了一个“六元素表”。
1865年,英国化学家纽兰兹按相对原子质量递增顺序,将已知元素作了排列。他发现第八个元素就与第一个元素性质相似(元素的排列每逢八就出现周期性)。这好像音乐上的八个音阶一样重复出现,于是提出“八音律”的理论(下表是“八音律表”的前部分)。
H Li G Bo C N O
F Na Mg Al Si P S
1869年,俄罗斯化学家门捷列夫对当时已知的63种元素的相对原子质量和物理性质(熔点、密度等)进行了比较,直到19世纪末才制成了第一张元素周期表。事实上,在1869年,德国的迈耶和俄国的门捷列夫几乎同时发现了元素周期律。
(1)写出德贝纳提出的“三种元素组”中,氯元素的元素符号: 。
(2)根据纽兰兹“八音律表”,与Na性质相似的元素是 。
(3)分析上述科学史料,判断下列观点正确的有 (可多选)。
A.研究复杂的现象往往需要寻找规律。
B.科学家在研究元素周期规律时,不需要借助技术手段。
C.如果门捷列夫没有发现元素周期表,也会有其他科学家发现。
D.随着科学的进步,我们现在所学的元素周期表已包含所有元素。
E.纽兰兹的“八音律表”中没有稀有元素,说明他的理论是错误,没有作用的。
5.(2023长兴期中)通过对已学知识的对比和归纳,我们往往可以得出一些十分有趣的规律,这些规律可以帮助我们掌握学习科学的方法。请仔细阅读下表中的内容,并回答相应的问题:
常见的几种离子 H+、Na+、Mg2+、OH﹣、Cl﹣、
对应元素及原子团在化合物中的化合价 、、、、、
所能形成化合物的化学式 酸 碱 盐
HCl、H2SO4 NaOH、Mg(OH)2 MgCl2、Na2SO4
(1)由前两行内容对照可得出的规律是:元素或原子团的化合价数值往往与相应离子所带的 数相等。
(2)由后两行内容对照可得出的规律是:通过元素或原子团的 可以确定相应化合物的化学式。
(3)根据硫酸亚铁的化学式FeSO4,可推出该物质所含阳离子的符号为 。
参考答案
四、典型例题
(一)考点:组成物质的元素
【例1】(2022上城期中)世界上各种物质都是由一些最基本的元素组成的。下列说法不正确的是( )
A.元素在地壳中的分布是不均匀的,地壳中最多的金属元素是铝
B.海水中有大量的氯化钠,因此含量最高的是氯元素
C.放射性元素对人体有害,但利用放射性可以检查和治疗一些疾病
D.人体内也含有一些有害元素,如镉、汞、铅等,这与食物、水体及大气的污染相关
【答案】B
【例2】(2023建功单元)有关下右图所示的五种物质的说法正确的是( )
A.五种物质都是混合物 B.①②④有相似之处,都盛放了不同状态的同种物质
C.③④属于化合物 D.②和⑤有相似之处:元素种类相同,但分子构成不同
【答案】D
【例3】(2023杭州期中)下列说法正确的是( )
①地壳中最多的金属元素是铝,也就是金属铝
②地壳中非金属元素的总含量大于金属元素,种类少于金属元素
③人体中只含有非金属元素,没有金属元素
④人体中氢、氧元素含量很高,这与水占人体质量的70%以上有关
A.①③④ B.②③④ C.①② D.②④
【答案】D
【例4】(2023临平期中)C60发现使人类了解到一个全新的碳世界,根据图回答下列问题:
①C60属于 (填“单质”或“化合物”)。
②C60这种物质是由 (填“分子”或“原子”)构成。
③C60与金刚石、石墨具有相似的 (填“化学”或“物理”)性质。
【答案】单质;分子;化学
(二)考点:表示元素的符号
【例1】(2023上城期中)下列常见元素中,属于金属元素的是( )
A.C B.Cu C.Si D.O
【答案】B
【例2】(2023建功单元)如图为元素周期表的一部分,A~E代表五种不同元素。下列说法不正确的是( )
A原子半径C>D B.核内质子数:E>D
C.B、C同周期且电子层数相同 D.A、D同族且化学性质相似
【答案】A
【例3】(2023乐清期中)天宫课堂中,航天员王亚平用视频展示了在无容器材料实验柜中进行的“锆金属熔化与凝固”实验,锆原子核外电子数为40,中子数为51,相对原子质量为91,元素符号为Zr,请模仿图甲,将该元素对应信息编写到图乙中相应位置,“①”处应填( )
A.91 B.51 C.40 D.11
【答案】C
【例4】(2023柯桥期中)2021年3月,三星堆的再次发掘引人关注,如图的青铜面具就是之前出土的典型文物,三星堆青铜主要成分是铜、铅、锡等,锡的元素符号是“Sn”,下列关于“Sn”表述错误的是( )
A.表示锡这种物质 B.表示一个锡原子
C.表示锡元素 D.表示一个锡分子
【答案】D
(三)考点:表示物质的符号
【例1】(2023建功单元)下列化学式书写都正确的一组是( )
A.硝酸HNO 硫酸H SO 盐酸HCl
B.氧化钙CaO 五氧化二磷P O 二氧化硫SO
C.氢氧化钠NaOH 氢氧化钾KOH 氢氧化钙CaOH
D.氯化钡BaCl 氯化锌ZnCl 硫酸铜CuSO
【答案】D
【例2】(2023玉环期中)在研究空气成分的历史上,许多科学家做了大量的研究。下列是普里斯特利在研究中收集到的各种气体及当时的名称,这些气体中氮元素化合价最低的是( )
A.“亚硝蒸气”(NO2) B.“亚硝空气”(NO)
C.“减缩的亚硝空气”(N2O) D.“燃素化空气”(N2)
【答案】D
【例3】(2023建功单元)在化学王国里,数字被赋予了丰富的内涵.对下列化学用语中数字“2”的说法正确的是( )
①2H ②2NH ③SO ④O ⑤Mg ⑥2OH ⑦H O
A.表示离子个数的是⑤⑥ B.表示离子所带电荷数的是④⑤
C.表示分子中原子个数的是③⑦ D.表示分子个数的是①②
【答案】C
【例4】(2023永嘉期中)2022年11月,比亚迪新能源动力电池生产基地项目落地浙江省温州市水嘉县桥头镇,动力电池领域对氧氧化锂(化学式LiOH)的需求量很大,兴趣小组同学对氧氧化锂及相关的化学用语进行了研究。氢氧化锂(LiOH)化学式表示的意义的理解,不正确的是( )
A.表示氢氧化锂中锂离子和氢氧根离子个数比是1:1
B.表示氢氧化锂由锂元素、氢元素、氧元素组成
C.表示氢氧化锂由1个锂原子、1个氧原子、1个氢原子构成
D.表示氢氧化锂这种物质
【答案】C
【例5】我国科学家发现,亚硒酸钠能消除加速人体衰老的活性氧,亚硒酸钠中硒元素(Se)为+4价,氧元素为﹣2价,则亚硒酸钠的化学式为( )
A.Na2SeO3 B.Na2SeO4 C.NaSeO3 D.Na2SeO2
【答案】A
【例6】(2023建功单元)(1)以下内容请你用最合适的化学符号填空: 地壳中含量最多的金属元素与最多的非金属元素组成的化合物______________, 3个铁离子______________,能保持二氧化硫化学性质的微粒______________,调味品食盐的阳离子______________,相对分子质量最小的物质______________;温度计中填充的液态金属______________; -2价的硫元素______________; 3个氨气分子______________.3个碳酸根离子______________, FeSO 读作______________
硝酸铝______________氖气______________溴水______________
(2)写出“3O42-”中数字的含义:“4”________________________________________
“+6”________________________________________
“2-”________________________________________
“3”________________________________________
【答案】Al2O3 3Fe3+ SO2 Na+ H2 Hg 3NH3 3CO32- 硫酸亚铁 Al(NO3)3 Ne Br2
一个硫酸根离子中含有四个氧原子
硫酸根离子中硫元素的化合价为正六价
一个硫酸根离子带两个单位负电荷
三个硫酸根离子
五、学力训练
A组 夯实基础
1.(2023建功单元)原子失去或得到电子后,一定不会引起改变的是( )
①电子总数②质子数③化学性质④质量数⑤微粒的电性⑥电子层数
A.③④ B.②③⑥ C.②④ D.②④⑥
【答案】C
2.(2023建功单元)某元素的阳离子A 的核外有10个电子,核内有14个中子,则该元素原子的核电荷数和质量数分别为( )
A .10 24 B.13 24 C.10 27 D.13 27
【答案】D
3.(2023杭州期中)下列元素分类正确的是( )
A.金属元素:Ca Mg Fe Cu
B.非金属元素:P Si Ag C
C.稀有气体元素:He Ne Ar Cl
D.固体非金属元素:O S P Si
【答案】A
4.(2023上城期末)下列有关元素的说法正确的是( )
①地壳中最多的金属元素是铝,也就是金属铝
②对人体而言,钙是微量元素
③元素既可以天然存在也可以人工合成
④人体中H、O元素含量高跟水占人体质量的以上有关
A.①④ B.②③ C.②④ D.③④
【答案】D
5.(2022西湖期中)下列元素符号表示正确的是( )
A.银Hg B.氯Al C.氟Fu D.钙Ca
【答案】D
B组 强化提高
1.(2023春 鹿城区校级期中)世界是由元素组成的。图中能正确表示地壳中元素含量分布的是( )
A.B.C.D.
【答案】B
2.(2023春 杭州期中)下列说法正确的是( )
①地壳中最多的金属元素是铝,也就是金属铝
②地壳中非金属元素的总含量大于金属元素,种类少于金属元素
③人体中只含有非金属元素,没有金属元素
④人体中氢、氧元素含量很高,这与水占人体质量的70%以上有关
A.①③④ B.②③④ C.①② D.②④
【答案】D
3.(2022乐清期中)永嘉乌牛早茶味醇气香,茶叶中含有茶氨酸(C7H14O3N2),根据物质的分类,茶氨酸属于( )
A.单质 B.氧化物 C.混合物 D.化合物
【答案】D
4.(2023鹿城期中)钋是一种能够在黑暗中发光的金属,由居里夫人和其丈夫发现。为了纪念居里夫人的祖国波兰,两人将该金属命名为Polonium。则钋的元素符号是( )
A.P B.po C.p D.Po
【答案】D
5.(2023上城期中)下列化学用语与含义相符的是( )
A.O﹣2——氧离子 B.3H2——6个氢原子
C.NaMo2O4——Mo元素的化合价为+6 D.2N2——2个氮分子
【答案】D
6.(2023金东期中)某化合物在水中能完全电离,将该化合物配制成甲、乙、丙三种不同浓度的水溶液,对溶液中所含阴、阳离子数目进行测定,结果如图所示。由图可判断该化合物可能是( )
A.HNO3 B.Fe2(SO4)3 C.Ca(OH)2 D.H2SO4
【答案】A
7.(2023鹿城期中)天宫二号是我国首个空间实验室。在太空舱里常借助铁酸镍 (NiFe2O4 )将宇航员呼出的二氧化碳转化为氧气。已知镍(Ni)元素化合价为+2价,则中铁元素的化合价为( )
A.+2 B.+3 C.+6 D.0
【答案】B
8.(2022绍兴期中)如图是教材中元素周期表的一部分,除标出的元素外,表中的数字编号①~③各表示一种元素。请回答问题。
(1)①表示的元素是 。
(2)1个铝原子的核外电子有 个。
(3)元素硅比第2周期、第ⅥA族的元素在地壳中的含量 (选填“高”或“低”)。
【答案】氢 13 低
9.(2023永嘉期中)2022北京冬奥会将“科技奥运”显现得淋漓尽致!
(1)国家速滑馆又称“冰丝带”,采用当前冬季运动场馆最环保的制冰技术之一——二氧化碳跨临界直接制冰技术,通过压力变化使二氧化碳汽化实现制冷,二氧化碳跨临界直接制冰技术利用了二氧化碳的 。(填“物理性质”或“化学性质”)
(2)北京冬奥会火种灯的火种燃料为丙烷,如图是丙烷分子微观示意图,则丙烷的化学式为 。
(3)颁奖服内胆使用了第二代石墨烯(由碳元素组成)发热材料,石墨烯属于 (填“单质”或“化合物”)。
【答案】物理性质 C3H8 单质
10.(2023温州期中)(1)用符号表示下列物质或微粒:
2个亚铁离子 ;5个甲烷分子 ;3个氖原子 ;保持氧气化学性质的最小粒子 。
(2)判断下列化学符号中“2”的意义,并将其序号写在相应位置。
①CO2 ② ③ ④2NH3
表示化合物中元素的化合价 ;表示分子中原子的个数 。
(3)现有铁屑、硫粉、硫化亚铁、氧化汞和海水五种物质,为了区分它们,小希参照二歧分类检索表制作了一个物质检索表,如表所示,请分析乙是 。已知铁屑和硫粉在一定条件下形成硫化亚铁,这属于 变化。
【答案】2Fe2+ 5CH4 3Ne O2 ② ① 铁屑 化学
C组 瞄准中考
1.(2023建功单元)化合物MX6。分子呈正八面体结构(正八面体是指由八个全等的正三角形围成的如图所示的几何体)。由于六个X 原子与M的连接完全对称,因此将任意一个X用Y原子替换,均只能得到一种结构的MX5Y 分子,按此思路,若其中任意两个X 原子用Y原子替换,则得到的化学式为MX4Y 的分子( )
A.只有1种结构 B.存在2种不同结构
C.存在3种不同结构 D.存在4种不同结构
【答案】B
2.(2023新昌期末)氕、氘、氚三种不同原子在元素周期表中( )
A.同占一个位置 B.占三个不同的位置 C.不占位置 D.只有氕占位置
【答案】A
3.(2023上城期中)苏打水即碳酸氢钠的水溶液,为人工合成的碳酸饮料,是在经过纯化的饮用水中压入二氧化碳,并添加甜味剂和香料的饮料,含有弱碱性。下列有关苏打水中各成分化学式书写错误的是( )
A.碳酸氢钠(NaHCO3) B.水(H2O) C.二氧化碳(CO2) D.碳酸钠(NaCO3)
【答案】D
4.(2022乐清期末)根据相对原子质量来研究元素,始于19世纪初。
1829年,德国化学家德贝纳提出了锂钠钾、钙锶钡、磷砷锑、氯溴碘等15种元素,他把这些元素称为“三种元素组”。
1864年,德国化学家迈耶,按相对原子质量递增顺序制定了一个“六元素表”。
1865年,英国化学家纽兰兹按相对原子质量递增顺序,将已知元素作了排列。他发现第八个元素就与第一个元素性质相似(元素的排列每逢八就出现周期性)。这好像音乐上的八个音阶一样重复出现,于是提出“八音律”的理论(下表是“八音律表”的前部分)。
H Li G Bo C N O
F Na Mg Al Si P S
1869年,俄罗斯化学家门捷列夫对当时已知的63种元素的相对原子质量和物理性质(熔点、密度等)进行了比较,直到19世纪末才制成了第一张元素周期表。事实上,在1869年,德国的迈耶和俄国的门捷列夫几乎同时发现了元素周期律。
(1)写出德贝纳提出的“三种元素组”中,氯元素的元素符号: 。
(2)根据纽兰兹“八音律表”,与Na性质相似的元素是 。
(3)分析上述科学史料,判断下列观点正确的有 (可多选)。
A.研究复杂的现象往往需要寻找规律。
B.科学家在研究元素周期规律时,不需要借助技术手段。
C.如果门捷列夫没有发现元素周期表,也会有其他科学家发现。
D.随着科学的进步,我们现在所学的元素周期表已包含所有元素。
E.纽兰兹的“八音律表”中没有稀有元素,说明他的理论是错误,没有作用的。
【答案】Cl Li AC
5.(2023长兴期中)通过对已学知识的对比和归纳,我们往往可以得出一些十分有趣的规律,这些规律可以帮助我们掌握学习科学的方法。请仔细阅读下表中的内容,并回答相应的问题:
常见的几种离子 H+、Na+、Mg2+、OH﹣、Cl﹣、
对应元素及原子团在化合物中的化合价 、、、、、
所能形成化合物的化学式 酸 碱 盐
HCl、H2SO4 NaOH、Mg(OH)2 MgCl2、Na2SO4
(1)由前两行内容对照可得出的规律是:元素或原子团的化合价数值往往与相应离子所带的 数相等。
(2)由后两行内容对照可得出的规律是:通过元素或原子团的 可以确定相应化合物的化学式。
(3)根据硫酸亚铁的化学式FeSO4,可推出该物质所含阳离子的符号为 。
【答案】电荷 化合价 Fe2+
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网(www.21cnjy.com)
5 表示元素和物质的符号
一、组成物质的元素
1.目前人类已知的元素有118种,其中有些是人造元素。世界上大部分物质只是由几十种常见元素组成的,其中仅碳 、 氢 、 氧 三种元素就能组成许许多多种物质。
2.人们通常把元素分为 金属 元素和 非金属 元素(包括 稀有气体元素 ,如氩元素)。在118种元素中, 金属 元素占大多数。金属元素的名称一般都以“钅”作偏旁(汞除外);非金属元素的名称一般都以“石”“氵”“气”作偏旁,其中以“石”为偏旁的一般为固态非金属元素,以“氵”为偏旁的一般为液态非金属元素,以“气”为偏旁的一般为气态非金属元素
3.单质和化合物的比较
单质 化合物
概念 由 同种 元素组成的 纯净物 由 不同种 元素组成的 纯净物
宏观组成 一种元素 至少两种元素
微观构成 同种原子或同种原子构成的同种分子 不同种原子构成的同种分子或不同种离子
举例 铁Fe、氧气O2 二氧化碳CO2、氯化钠NaCl
相同点 都是纯净物
4.由同种元素组成的物质不一定是纯净物,也可能是混合物。如氧气(O2)和臭氧(O3)的混合物只由氧元素组成
5.元素是宏观概念,可以讲种类,但不能讲个数。如描述二氧化碳的元素组成时,只能说“二氧化碳是由氧元素和碳元素组成的”,而不能说“二氧化碳是由一个碳元素和两个氧元素组成的”。
6.物质、元素、分子、原子间的关系
7.地壳主要由 氧 、硅 、铝 、铁 、钙、钠、钾、镁、氢等元素组成,其中含量最高的是 氧 ,其次是 硅 。金属元素中含量最高的是 铝 ,其次是 铁 。
8.人体中的元素及作用
(1)人体内大约含有30多种元素,其中11种(C、H、O、N、S、P、Cl、Ca、Mg、Na、K)为大量元素,约占99.95%,其余为 微量 元素。它们中有些是必需元素,每一种必需元素在体内都有一个适量范围, 过多 或 过少 都不利于人体健康。另外,人体内也含有一些有害元素,如镉、汞、铅等。
(2)人体含量最高的元素是 氧 元素,含量最高的金属元素是 钙 元素。
(3) 钙 元素能促进儿童骨骼生长; 铁 元素能预防贫血; 碘 元素能预防甲状腺肿大; 氟 元素能预防龋齿; 锌 元素能增进食欲,促进儿童的生长发育; 硒 元素能预防癌症。
9.海水中,除了水由氢、氧两种元素组成以外,含量较高的是 氯 元素、 钠 元素和 镁 元素,还有一些贵重金属,如金等
10.有机化合物中大都含有 碳 、 氢 、 氧 三种元素。
11.人造元素是通过核反应制得的,其中有些人造元素和天然元素具有 放射性 。放射性元素对人体有害,但利用放射性可以检查和治疗一些疾病、灭菌和消毒。
12.元素占比排名
(1)地壳中元素含量最多的(非金属)元素是氧,含量最多的金属元素是铝。
(2)生物细胞中含量排在前五位的元素依次是氧、碳、氢、氮、钙。
(3)海水中含量排在前五位的元素依次是氧、氢、氯、钠、镁。
(4)空气中含量最多的元素是氮,其次是氧。
二、表示元素的符号
1.元素符号的写法
(1)由一个字母表示的元素符号要 大写 ,如H、O、N等。
(2)由两个字母表示的元素符号,第一个字母要 大写 ,第二个字母要 小写 ,如Na、Mg、Cu等。
2.元素符号的意义
(1)表示一种 元素 ,如H可表示 氢元素
(2)若物质是由原子直接构成的,还表示一种 物质 ,如Cu可表示铜这种物质
(3)表示这种元素的1个 原子 ,如H还可表示一个氢原子
(4)需要计算时还可以表示这种元素的相对原子质量。
3.元素周期表:根据元素的 原子结构 和 性质 ,科学家把人们已知的118种元素按 原子序数 科学有序地排列起来,得到的表叫做 元素周期表 。
4.元素周期表的每一个横行叫做一个 周期 ,表中共有7个横行,表示有 7 个周期。每一个纵列叫做一个 族 ,元素周期表中共有18个纵列, 16 个族(其中第8、9、10三个纵列共同组成一个族)。同族元素的化学性质相似。在元素周期表中,每一种元素都占有一格位置,每一格包括元素的 原子序数 、 元素符号 、 元素名称 、 相对原子质量
三、表示物质的符号
1.化学式定义:用 元素符号 来表示物质组成的式子叫做化学式。如二氧化碳分子可表示成“ CO2 ”。
2.单质化学式的写法
(1)稀有气体是由原子直接构成的,通常就用 元素符号 来表示它们的化学式。金属单质和固态非金属单质的结构比较复杂,习惯上也用 元素符号 来表示它们的化学式。如氩气、铝、磷分别用 Ar 、 Al 、 P 来表示。
(2)对于多原子分子构成的单质,先写出组成单质的 元素符号 ,再在元素符号右下角写上构成这个单质分子的 原子数目 。如氧气、氢气、溴水、碘、臭氧分别用 O2 、H2 、Br2 、I2 、O3 来表示。
3.化合物化学式的写法(正价在左、负价在右)
(1)按一定顺序写出组成化合物的所有元素符号:①氧元素与另一元素组成的化合物,一般要把氧元素符号写在 右 边;②氢元素与另一元素组成的化合物,一般要把氢元素符号写在 左 边;(记住两个特例:NH3 CH4)③金属元素、氢元素与非金属元素组成的化合物,一般要把 非金属 元素符号写在右边。
(2)在每种元素符号的右下角用数字写出每个化合物分子中该元素的 原子个数 。直接由离子构成的化合物,其化学式常用其离子 最简单整数比 表示。
4.化学式的读法,一般是从右向左叫做“某化某”,如“CuO”读作“ 氧化铜 ”。当1个分子中原子个数不止1个时,还要指出1个分子里元素的原子个数,如“P2O5”读作“ 五氧化二磷 ”。
5.化学式的意义
化学式的意义 以CO2为例
宏 观 表示一种物质 表示 二氧化碳 这种物质
表示该物质的元素组成 表示二氧化碳是由 碳 元素和 氧 元素组成的
微 观 表示构成物质的基本微粒 表示二氧化碳是由 二氧化碳分子 构成的
由分子构成的物质的化学式可表示该物质的一个分子 表示 一个二氧化碳分子
表示物质的分子构成 表示一个二氧化碳分子是由一个 碳原子 和两个 氧原子 构成的
如果在化学式前面加上系数,就表示某物质的几个分子如2个氧气分子可用 2O2 表示。
(注:1.化学式不能凭空想象,而应由实验确定,一种物质只有一个化学式。
2.对于任何一种纯净物而言,其组成是固定的,也就是说,一种物质是由哪些元素组成的和这些元素的原子个数比都是一定的,所以每一种纯净物都可以用化学式表示。而混合物的组成是不固定的,因此混合物没有化学式。)
6. 离子的符号:离子符号是在形成该离子的原子的元素符号 右上角 标出该离子所带的 电荷数 。
7.离子符号的写法
(1)离子只带一个单位电荷(正、负电荷),则把个数“ 1 ”省去,直接在元素符号右上角写“ + ”或“ - ”号,如Na+、Cl-等。
(2)离子带多个单位电荷(正、负电荷),则在元素符号右上角先写 电荷数 ,再写“ + ”或“-”号,如Mg2+、Al3+、O2-等。
(3)有些离子的组成不止一种元素,如OH-和SO等,这种离子称为“某某根离子”,是带电的 原子团 。它们在化学反应中往往以一个整体出现并参与反应。
(注:1.表示多个离子时,则在离子符号前加上相应的数字。如2个镁离子: 2Mg2+ ;3个碳酸根离子: 3CO 。
2.原子团右上角的数字表示的是整个原子团所带的电荷数,是原子团中各元素原子所带电荷数的代数和,而不是某个原子所带的电荷数。)
8.化合价:不同原子构成分子时,各种原子的个数用“ 化合价 ”来表示。不同元素组成化合物时,要遵守的规则是化合物中所有元素化合价的代数和为 零 。如1个水分子是由2个氢原子和1个氧原子构成的,化合价的代数和为 (+1)×2+(-2)=0 。(注:化合价是代表这种原子在构成化合物时,得失电子或与其他原子共享电子的数目)
9.化合价通常在元素符号或原子团的 正上方用“+n”或“-n”表示。注意 正 、 负 号在数字的前面,且“ 1 ”不能省略,如、O3等。
10.根据元素化合价,即可正确写出化合物的化学式。首先按 正 价元素在左, 负 价元素在右的原则写出元素符号,并在元素符号正上方标出 化合价 ,然后根据元素化合价代数和为零的原则写出分子中各元素的 原子个数 。
11.元素化合价的一般规则
(1)常见的化合物中,氢总是 +1 价元素,氧总是 -2 价。
(2)金属元素常显 正 价。
(3)非金属元素跟氧化合时常显 正 价,跟氢化合时常显 负 价。
(4)单质中元素的化合价为 0 。
(5)在化合物里,元素正负化合价的代数和为零。
(6)有些元素在不同的化合物里常显 不同 的化合价,如O2、O;有些元素在不同的化合物里常显 相同 的化合价,如Na、H;有些元素在相同的化合物里可显 不同 的化合价,如H4O3。
12.化合价和离子符号的区别与联系如下表所示:
化合价 离子符号
表示 方法 用+1、+2、-1、-2……表示,标在元素符号(或原子团)的正上方(“1”不省略) 用+、2+、-、2-……表示,标在元素符号(或原子团)的右上角(“1”省略)
实例 、 、24 H+、Cl-、Mg2+、S2-、Na+、SO
联系 同种元素(或原子团)的化合价和离子所带的电荷,通常数值相等,正负一致
(注:1.常见元素的化合价口诀:
钾钠氯银正一价,钙钡镁锌正二价;三铝四硅五价磷, 二三铁、二四碳;
二四六硫三五氮,铜汞二价最常见;一五七氯都齐全,单质零价永不变。
2.某些金属元素在不同化合物中常显不同的化合价,如铁元素可显+2、+3两种化合价,命名时习惯上将显较低化合价的铁元素读作“亚铁”,如FeO读作“氧化亚铁”,而Fe2O3读作“氧化铁“。
3.根据化合价写化学式时,物质应是客观存在的,不能根据化合价臆造实际上不存在的物质。)
四、典型例题
(一)考点:组成物质的元素
【例1】(2022上城期中)世界上各种物质都是由一些最基本的元素组成的。下列说法不正确的是( )
A.元素在地壳中的分布是不均匀的,地壳中最多的金属元素是铝
B.海水中有大量的氯化钠,因此含量最高的是氯元素
C.放射性元素对人体有害,但利用放射性可以检查和治疗一些疾病
D.人体内也含有一些有害元素,如镉、汞、铅等,这与食物、水体及大气的污染相关
【例2】(2023建功单元)有关下右图所示的五种物质的说法正确的是( )
A.五种物质都是混合物 B.①②④有相似之处,都盛放了不同状态的同种物质
C.③④属于化合物 D.②和⑤有相似之处:元素种类相同,但分子构成不同
【例3】(2023杭州期中)下列说法正确的是( )
①地壳中最多的金属元素是铝,也就是金属铝
②地壳中非金属元素的总含量大于金属元素,种类少于金属元素
③人体中只含有非金属元素,没有金属元素
④人体中氢、氧元素含量很高,这与水占人体质量的70%以上有关
A.①③④ B.②③④ C.①② D.②④
【例4】(2023临平期中)C60发现使人类了解到一个全新的碳世界,根据图回答下列问题:
①C60属于 (填“单质”或“化合物”)。
②C60这种物质是由 (填“分子”或“原子”)构成。
③C60与金刚石、石墨具有相似的 (填“化学”或“物理”)性质。
(二)考点:表示元素的符号
【例1】(2023上城期中)下列常见元素中,属于金属元素的是( )
A.C B.Cu C.Si D.O
【例2】(2023建功单元)如图为元素周期表的一部分,A~E代表五种不同元素。下列说法不正确的是( )
A原子半径C>D B.核内质子数:E>D
C.B、C同周期且电子层数相同 D.A、D同族且化学性质相似
【例3】(2023乐清期中)天宫课堂中,航天员王亚平用视频展示了在无容器材料实验柜中进行的“锆金属熔化与凝固”实验,锆原子核外电子数为40,中子数为51,相对原子质量为91,元素符号为Zr,请模仿图甲,将该元素对应信息编写到图乙中相应位置,“①”处应填( )
A.91 B.51 C.40 D.11
【例4】(2023柯桥期中)2021年3月,三星堆的再次发掘引人关注,如图的青铜面具就是之前出土的典型文物,三星堆青铜主要成分是铜、铅、锡等,锡的元素符号是“Sn”,下列关于“Sn”表述错误的是( )
A.表示锡这种物质 B.表示一个锡原子
C.表示锡元素 D.表示一个锡分子
(三)考点:表示物质的符号
【例1】(2023建功单元)下列化学式书写都正确的一组是( )
A.硝酸HNO 硫酸H SO 盐酸HCl
B.氧化钙CaO 五氧化二磷P O 二氧化硫SO
C.氢氧化钠NaOH 氢氧化钾KOH 氢氧化钙CaOH
D.氯化钡BaCl 氯化锌ZnCl 硫酸铜CuSO
【例2】(2023玉环期中)在研究空气成分的历史上,许多科学家做了大量的研究。下列是普里斯特利在研究中收集到的各种气体及当时的名称,这些气体中氮元素化合价最低的是( )
A.“亚硝蒸气”(NO2) B.“亚硝空气”(NO)
C.“减缩的亚硝空气”(N2O) D.“燃素化空气”(N2)
【例3】(2023建功单元)在化学王国里,数字被赋予了丰富的内涵.对下列化学用语中数字“2”的说法正确的是( )
①2H ②2NH ③SO ④O ⑤Mg ⑥2OH ⑦H O
A.表示离子个数的是⑤⑥ B.表示离子所带电荷数的是④⑤
C.表示分子中原子个数的是③⑦ D.表示分子个数的是①②
【例4】(2023永嘉期中)2022年11月,比亚迪新能源动力电池生产基地项目落地浙江省温州市水嘉县桥头镇,动力电池领域对氧氧化锂(化学式LiOH)的需求量很大,兴趣小组同学对氧氧化锂及相关的化学用语进行了研究。氢氧化锂(LiOH)化学式表示的意义的理解,不正确的是( )
A.表示氢氧化锂中锂离子和氢氧根离子个数比是1:1
B.表示氢氧化锂由锂元素、氢元素、氧元素组成
C.表示氢氧化锂由1个锂原子、1个氧原子、1个氢原子构成
D.表示氢氧化锂这种物质
【例5】我国科学家发现,亚硒酸钠能消除加速人体衰老的活性氧,亚硒酸钠中硒元素(Se)为+4价,氧元素为﹣2价,则亚硒酸钠的化学式为( )
A.Na2SeO3 B.Na2SeO4 C.NaSeO3 D.Na2SeO2
【例6】(2023建功单元)(1)以下内容请你用最合适的化学符号填空: 地壳中含量最多的金属元素与最多的非金属元素组成的化合物______________, 3个铁离子______________,能保持二氧化硫化学性质的微粒______________,调味品食盐的阳离子______________,相对分子质量最小的物质______________;温度计中填充的液态金属______________; -2价的硫元素______________; 3个氨气分子______________.3个碳酸根离子______________, FeSO 读作______________
硝酸铝______________氖气______________溴水______________
(2)写出“3O42-”中数字的含义:“4”________________________________________
“+6”________________________________________
“2-”________________________________________
“3”________________________________________
五、学力训练
A组 夯实基础
1.(2023建功单元)原子失去或得到电子后,一定不会引起改变的是( )
①电子总数②质子数③化学性质④质量数⑤微粒的电性⑥电子层数
A.③④ B.②③⑥ C.②④ D.②④⑥
2.(2023建功单元)某元素的阳离子A 的核外有10个电子,核内有14个中子,则该元素原子的核电荷数和质量数分别为( )
A .10 24 B.13 24 C.10 27 D.13 27
3.(2023杭州期中)下列元素分类正确的是( )
A.金属元素:Ca Mg Fe Cu
B.非金属元素:P Si Ag C
C.稀有气体元素:He Ne Ar Cl
D.固体非金属元素:O S P Si
4.(2023上城期末)下列有关元素的说法正确的是( )
①地壳中最多的金属元素是铝,也就是金属铝
②对人体而言,钙是微量元素
③元素既可以天然存在也可以人工合成
④人体中H、O元素含量高跟水占人体质量的以上有关
A.①④ B.②③ C.②④ D.③④
5.(2022西湖期中)下列元素符号表示正确的是( )
A.银Hg B.氯Al C.氟Fu D.钙Ca
B组 强化提高
1.(2023鹿城期中)世界是由元素组成的。图中能正确表示地壳中元素含量分布的是( )
A.B.C.D.
2.(2023杭州期中)下列说法正确的是( )
①地壳中最多的金属元素是铝,也就是金属铝
②地壳中非金属元素的总含量大于金属元素,种类少于金属元素
③人体中只含有非金属元素,没有金属元素
④人体中氢、氧元素含量很高,这与水占人体质量的70%以上有关
A.①③④ B.②③④ C.①② D.②④
3.(2022乐清期中)永嘉乌牛早茶味醇气香,茶叶中含有茶氨酸(C7H14O3N2),根据物质的分类,茶氨酸属于( )
A.单质 B.氧化物 C.混合物 D.化合物
4.(2023鹿城期中)钋是一种能够在黑暗中发光的金属,由居里夫人和其丈夫发现。为了纪念居里夫人的祖国波兰,两人将该金属命名为Polonium。则钋的元素符号是( )
A.P B.po C.p D.Po
5.(2023上城期中)下列化学用语与含义相符的是( )
A.O﹣2——氧离子 B.3H2——6个氢原子
C.NaMo2O4——Mo元素的化合价为+6 D.2N2——2个氮分子
6.(2023金东期中)某化合物在水中能完全电离,将该化合物配制成甲、乙、丙三种不同浓度的水溶液,对溶液中所含阴、阳离子数目进行测定,结果如图所示。由图可判断该化合物可能是( )
A.HNO3 B.Fe2(SO4)3 C.Ca(OH)2 D.H2SO4
7.(2023鹿城期中)天宫二号是我国首个空间实验室。在太空舱里常借助铁酸镍 (NiFe2O4 )将宇航员呼出的二氧化碳转化为氧气。已知镍(Ni)元素化合价为+2价,则中铁元素的化合价为( )
A.+2 B.+3 C.+6 D.0
8.(2022绍兴期中)如图是教材中元素周期表的一部分,除标出的元素外,表中的数字编号①~③各表示一种元素。请回答问题。
(1)①表示的元素是 。
(2)1个铝原子的核外电子有 个。
(3)元素硅比第2周期、第ⅥA族的元素在地壳中的含量 (选填“高”或“低”)。
9.(2023永嘉期中)2022北京冬奥会将“科技奥运”显现得淋漓尽致!
(1)国家速滑馆又称“冰丝带”,采用当前冬季运动场馆最环保的制冰技术之一——二氧化碳跨临界直接制冰技术,通过压力变化使二氧化碳汽化实现制冷,二氧化碳跨临界直接制冰技术利用了二氧化碳的 。(填“物理性质”或“化学性质”)
(2)北京冬奥会火种灯的火种燃料为丙烷,如图是丙烷分子微观示意图,则丙烷的化学式为 。
(3)颁奖服内胆使用了第二代石墨烯(由碳元素组成)发热材料,石墨烯属于 (填“单质”或“化合物”)。
10.(2023温州期中)(1)用符号表示下列物质或微粒:
2个亚铁离子 ;5个甲烷分子 ;3个氖原子 ;保持氧气化学性质的最小粒子 。
(2)判断下列化学符号中“2”的意义,并将其序号写在相应位置。
①CO2 ② ③ ④2NH3
表示化合物中元素的化合价 ;表示分子中原子的个数 。
(3)现有铁屑、硫粉、硫化亚铁、氧化汞和海水五种物质,为了区分它们,小希参照二歧分类检索表制作了一个物质检索表,如表所示,请分析乙是 。已知铁屑和硫粉在一定条件下形成硫化亚铁,这属于 变化。
C组 瞄准中考
1.(2023建功单元)化合物MX6。分子呈正八面体结构(正八面体是指由八个全等的正三角形围成的如图所示的几何体)。由于六个X 原子与M的连接完全对称,因此将任意一个X用Y原子替换,均只能得到一种结构的MX5Y 分子,按此思路,若其中任意两个X 原子用Y原子替换,则得到的化学式为MX4Y 的分子( )
A.只有1种结构 B.存在2种不同结构
C.存在3种不同结构 D.存在4种不同结构
2.(2023新昌期末)氕、氘、氚三种不同原子在元素周期表中( )
A.同占一个位置 B.占三个不同的位置 C.不占位置 D.只有氕占位置
3.(2023上城期中)苏打水即碳酸氢钠的水溶液,为人工合成的碳酸饮料,是在经过纯化的饮用水中压入二氧化碳,并添加甜味剂和香料的饮料,含有弱碱性。下列有关苏打水中各成分化学式书写错误的是( )
A.碳酸氢钠(NaHCO3) B.水(H2O) C.二氧化碳(CO2) D.碳酸钠(NaCO3)
4.(2022乐清期末)根据相对原子质量来研究元素,始于19世纪初。
1829年,德国化学家德贝纳提出了锂钠钾、钙锶钡、磷砷锑、氯溴碘等15种元素,他把这些元素称为“三种元素组”。
1864年,德国化学家迈耶,按相对原子质量递增顺序制定了一个“六元素表”。
1865年,英国化学家纽兰兹按相对原子质量递增顺序,将已知元素作了排列。他发现第八个元素就与第一个元素性质相似(元素的排列每逢八就出现周期性)。这好像音乐上的八个音阶一样重复出现,于是提出“八音律”的理论(下表是“八音律表”的前部分)。
H Li G Bo C N O
F Na Mg Al Si P S
1869年,俄罗斯化学家门捷列夫对当时已知的63种元素的相对原子质量和物理性质(熔点、密度等)进行了比较,直到19世纪末才制成了第一张元素周期表。事实上,在1869年,德国的迈耶和俄国的门捷列夫几乎同时发现了元素周期律。
(1)写出德贝纳提出的“三种元素组”中,氯元素的元素符号: 。
(2)根据纽兰兹“八音律表”,与Na性质相似的元素是 。
(3)分析上述科学史料,判断下列观点正确的有 (可多选)。
A.研究复杂的现象往往需要寻找规律。
B.科学家在研究元素周期规律时,不需要借助技术手段。
C.如果门捷列夫没有发现元素周期表,也会有其他科学家发现。
D.随着科学的进步,我们现在所学的元素周期表已包含所有元素。
E.纽兰兹的“八音律表”中没有稀有元素,说明他的理论是错误,没有作用的。
5.(2023长兴期中)通过对已学知识的对比和归纳,我们往往可以得出一些十分有趣的规律,这些规律可以帮助我们掌握学习科学的方法。请仔细阅读下表中的内容,并回答相应的问题:
常见的几种离子 H+、Na+、Mg2+、OH﹣、Cl﹣、
对应元素及原子团在化合物中的化合价 、、、、、
所能形成化合物的化学式 酸 碱 盐
HCl、H2SO4 NaOH、Mg(OH)2 MgCl2、Na2SO4
(1)由前两行内容对照可得出的规律是:元素或原子团的化合价数值往往与相应离子所带的 数相等。
(2)由后两行内容对照可得出的规律是:通过元素或原子团的 可以确定相应化合物的化学式。
(3)根据硫酸亚铁的化学式FeSO4,可推出该物质所含阳离子的符号为 。
参考答案
四、典型例题
(一)考点:组成物质的元素
【例1】(2022上城期中)世界上各种物质都是由一些最基本的元素组成的。下列说法不正确的是( )
A.元素在地壳中的分布是不均匀的,地壳中最多的金属元素是铝
B.海水中有大量的氯化钠,因此含量最高的是氯元素
C.放射性元素对人体有害,但利用放射性可以检查和治疗一些疾病
D.人体内也含有一些有害元素,如镉、汞、铅等,这与食物、水体及大气的污染相关
【答案】B
【例2】(2023建功单元)有关下右图所示的五种物质的说法正确的是( )
A.五种物质都是混合物 B.①②④有相似之处,都盛放了不同状态的同种物质
C.③④属于化合物 D.②和⑤有相似之处:元素种类相同,但分子构成不同
【答案】D
【例3】(2023杭州期中)下列说法正确的是( )
①地壳中最多的金属元素是铝,也就是金属铝
②地壳中非金属元素的总含量大于金属元素,种类少于金属元素
③人体中只含有非金属元素,没有金属元素
④人体中氢、氧元素含量很高,这与水占人体质量的70%以上有关
A.①③④ B.②③④ C.①② D.②④
【答案】D
【例4】(2023临平期中)C60发现使人类了解到一个全新的碳世界,根据图回答下列问题:
①C60属于 (填“单质”或“化合物”)。
②C60这种物质是由 (填“分子”或“原子”)构成。
③C60与金刚石、石墨具有相似的 (填“化学”或“物理”)性质。
【答案】单质;分子;化学
(二)考点:表示元素的符号
【例1】(2023上城期中)下列常见元素中,属于金属元素的是( )
A.C B.Cu C.Si D.O
【答案】B
【例2】(2023建功单元)如图为元素周期表的一部分,A~E代表五种不同元素。下列说法不正确的是( )
A原子半径C>D B.核内质子数:E>D
C.B、C同周期且电子层数相同 D.A、D同族且化学性质相似
【答案】A
【例3】(2023乐清期中)天宫课堂中,航天员王亚平用视频展示了在无容器材料实验柜中进行的“锆金属熔化与凝固”实验,锆原子核外电子数为40,中子数为51,相对原子质量为91,元素符号为Zr,请模仿图甲,将该元素对应信息编写到图乙中相应位置,“①”处应填( )
A.91 B.51 C.40 D.11
【答案】C
【例4】(2023柯桥期中)2021年3月,三星堆的再次发掘引人关注,如图的青铜面具就是之前出土的典型文物,三星堆青铜主要成分是铜、铅、锡等,锡的元素符号是“Sn”,下列关于“Sn”表述错误的是( )
A.表示锡这种物质 B.表示一个锡原子
C.表示锡元素 D.表示一个锡分子
【答案】D
(三)考点:表示物质的符号
【例1】(2023建功单元)下列化学式书写都正确的一组是( )
A.硝酸HNO 硫酸H SO 盐酸HCl
B.氧化钙CaO 五氧化二磷P O 二氧化硫SO
C.氢氧化钠NaOH 氢氧化钾KOH 氢氧化钙CaOH
D.氯化钡BaCl 氯化锌ZnCl 硫酸铜CuSO
【答案】D
【例2】(2023玉环期中)在研究空气成分的历史上,许多科学家做了大量的研究。下列是普里斯特利在研究中收集到的各种气体及当时的名称,这些气体中氮元素化合价最低的是( )
A.“亚硝蒸气”(NO2) B.“亚硝空气”(NO)
C.“减缩的亚硝空气”(N2O) D.“燃素化空气”(N2)
【答案】D
【例3】(2023建功单元)在化学王国里,数字被赋予了丰富的内涵.对下列化学用语中数字“2”的说法正确的是( )
①2H ②2NH ③SO ④O ⑤Mg ⑥2OH ⑦H O
A.表示离子个数的是⑤⑥ B.表示离子所带电荷数的是④⑤
C.表示分子中原子个数的是③⑦ D.表示分子个数的是①②
【答案】C
【例4】(2023永嘉期中)2022年11月,比亚迪新能源动力电池生产基地项目落地浙江省温州市水嘉县桥头镇,动力电池领域对氧氧化锂(化学式LiOH)的需求量很大,兴趣小组同学对氧氧化锂及相关的化学用语进行了研究。氢氧化锂(LiOH)化学式表示的意义的理解,不正确的是( )
A.表示氢氧化锂中锂离子和氢氧根离子个数比是1:1
B.表示氢氧化锂由锂元素、氢元素、氧元素组成
C.表示氢氧化锂由1个锂原子、1个氧原子、1个氢原子构成
D.表示氢氧化锂这种物质
【答案】C
【例5】我国科学家发现,亚硒酸钠能消除加速人体衰老的活性氧,亚硒酸钠中硒元素(Se)为+4价,氧元素为﹣2价,则亚硒酸钠的化学式为( )
A.Na2SeO3 B.Na2SeO4 C.NaSeO3 D.Na2SeO2
【答案】A
【例6】(2023建功单元)(1)以下内容请你用最合适的化学符号填空: 地壳中含量最多的金属元素与最多的非金属元素组成的化合物______________, 3个铁离子______________,能保持二氧化硫化学性质的微粒______________,调味品食盐的阳离子______________,相对分子质量最小的物质______________;温度计中填充的液态金属______________; -2价的硫元素______________; 3个氨气分子______________.3个碳酸根离子______________, FeSO 读作______________
硝酸铝______________氖气______________溴水______________
(2)写出“3O42-”中数字的含义:“4”________________________________________
“+6”________________________________________
“2-”________________________________________
“3”________________________________________
【答案】Al2O3 3Fe3+ SO2 Na+ H2 Hg 3NH3 3CO32- 硫酸亚铁 Al(NO3)3 Ne Br2
一个硫酸根离子中含有四个氧原子
硫酸根离子中硫元素的化合价为正六价
一个硫酸根离子带两个单位负电荷
三个硫酸根离子
五、学力训练
A组 夯实基础
1.(2023建功单元)原子失去或得到电子后,一定不会引起改变的是( )
①电子总数②质子数③化学性质④质量数⑤微粒的电性⑥电子层数
A.③④ B.②③⑥ C.②④ D.②④⑥
【答案】C
2.(2023建功单元)某元素的阳离子A 的核外有10个电子,核内有14个中子,则该元素原子的核电荷数和质量数分别为( )
A .10 24 B.13 24 C.10 27 D.13 27
【答案】D
3.(2023杭州期中)下列元素分类正确的是( )
A.金属元素:Ca Mg Fe Cu
B.非金属元素:P Si Ag C
C.稀有气体元素:He Ne Ar Cl
D.固体非金属元素:O S P Si
【答案】A
4.(2023上城期末)下列有关元素的说法正确的是( )
①地壳中最多的金属元素是铝,也就是金属铝
②对人体而言,钙是微量元素
③元素既可以天然存在也可以人工合成
④人体中H、O元素含量高跟水占人体质量的以上有关
A.①④ B.②③ C.②④ D.③④
【答案】D
5.(2022西湖期中)下列元素符号表示正确的是( )
A.银Hg B.氯Al C.氟Fu D.钙Ca
【答案】D
B组 强化提高
1.(2023春 鹿城区校级期中)世界是由元素组成的。图中能正确表示地壳中元素含量分布的是( )
A.B.C.D.
【答案】B
2.(2023春 杭州期中)下列说法正确的是( )
①地壳中最多的金属元素是铝,也就是金属铝
②地壳中非金属元素的总含量大于金属元素,种类少于金属元素
③人体中只含有非金属元素,没有金属元素
④人体中氢、氧元素含量很高,这与水占人体质量的70%以上有关
A.①③④ B.②③④ C.①② D.②④
【答案】D
3.(2022乐清期中)永嘉乌牛早茶味醇气香,茶叶中含有茶氨酸(C7H14O3N2),根据物质的分类,茶氨酸属于( )
A.单质 B.氧化物 C.混合物 D.化合物
【答案】D
4.(2023鹿城期中)钋是一种能够在黑暗中发光的金属,由居里夫人和其丈夫发现。为了纪念居里夫人的祖国波兰,两人将该金属命名为Polonium。则钋的元素符号是( )
A.P B.po C.p D.Po
【答案】D
5.(2023上城期中)下列化学用语与含义相符的是( )
A.O﹣2——氧离子 B.3H2——6个氢原子
C.NaMo2O4——Mo元素的化合价为+6 D.2N2——2个氮分子
【答案】D
6.(2023金东期中)某化合物在水中能完全电离,将该化合物配制成甲、乙、丙三种不同浓度的水溶液,对溶液中所含阴、阳离子数目进行测定,结果如图所示。由图可判断该化合物可能是( )
A.HNO3 B.Fe2(SO4)3 C.Ca(OH)2 D.H2SO4
【答案】A
7.(2023鹿城期中)天宫二号是我国首个空间实验室。在太空舱里常借助铁酸镍 (NiFe2O4 )将宇航员呼出的二氧化碳转化为氧气。已知镍(Ni)元素化合价为+2价,则中铁元素的化合价为( )
A.+2 B.+3 C.+6 D.0
【答案】B
8.(2022绍兴期中)如图是教材中元素周期表的一部分,除标出的元素外,表中的数字编号①~③各表示一种元素。请回答问题。
(1)①表示的元素是 。
(2)1个铝原子的核外电子有 个。
(3)元素硅比第2周期、第ⅥA族的元素在地壳中的含量 (选填“高”或“低”)。
【答案】氢 13 低
9.(2023永嘉期中)2022北京冬奥会将“科技奥运”显现得淋漓尽致!
(1)国家速滑馆又称“冰丝带”,采用当前冬季运动场馆最环保的制冰技术之一——二氧化碳跨临界直接制冰技术,通过压力变化使二氧化碳汽化实现制冷,二氧化碳跨临界直接制冰技术利用了二氧化碳的 。(填“物理性质”或“化学性质”)
(2)北京冬奥会火种灯的火种燃料为丙烷,如图是丙烷分子微观示意图,则丙烷的化学式为 。
(3)颁奖服内胆使用了第二代石墨烯(由碳元素组成)发热材料,石墨烯属于 (填“单质”或“化合物”)。
【答案】物理性质 C3H8 单质
10.(2023温州期中)(1)用符号表示下列物质或微粒:
2个亚铁离子 ;5个甲烷分子 ;3个氖原子 ;保持氧气化学性质的最小粒子 。
(2)判断下列化学符号中“2”的意义,并将其序号写在相应位置。
①CO2 ② ③ ④2NH3
表示化合物中元素的化合价 ;表示分子中原子的个数 。
(3)现有铁屑、硫粉、硫化亚铁、氧化汞和海水五种物质,为了区分它们,小希参照二歧分类检索表制作了一个物质检索表,如表所示,请分析乙是 。已知铁屑和硫粉在一定条件下形成硫化亚铁,这属于 变化。
【答案】2Fe2+ 5CH4 3Ne O2 ② ① 铁屑 化学
C组 瞄准中考
1.(2023建功单元)化合物MX6。分子呈正八面体结构(正八面体是指由八个全等的正三角形围成的如图所示的几何体)。由于六个X 原子与M的连接完全对称,因此将任意一个X用Y原子替换,均只能得到一种结构的MX5Y 分子,按此思路,若其中任意两个X 原子用Y原子替换,则得到的化学式为MX4Y 的分子( )
A.只有1种结构 B.存在2种不同结构
C.存在3种不同结构 D.存在4种不同结构
【答案】B
2.(2023新昌期末)氕、氘、氚三种不同原子在元素周期表中( )
A.同占一个位置 B.占三个不同的位置 C.不占位置 D.只有氕占位置
【答案】A
3.(2023上城期中)苏打水即碳酸氢钠的水溶液,为人工合成的碳酸饮料,是在经过纯化的饮用水中压入二氧化碳,并添加甜味剂和香料的饮料,含有弱碱性。下列有关苏打水中各成分化学式书写错误的是( )
A.碳酸氢钠(NaHCO3) B.水(H2O) C.二氧化碳(CO2) D.碳酸钠(NaCO3)
【答案】D
4.(2022乐清期末)根据相对原子质量来研究元素,始于19世纪初。
1829年,德国化学家德贝纳提出了锂钠钾、钙锶钡、磷砷锑、氯溴碘等15种元素,他把这些元素称为“三种元素组”。
1864年,德国化学家迈耶,按相对原子质量递增顺序制定了一个“六元素表”。
1865年,英国化学家纽兰兹按相对原子质量递增顺序,将已知元素作了排列。他发现第八个元素就与第一个元素性质相似(元素的排列每逢八就出现周期性)。这好像音乐上的八个音阶一样重复出现,于是提出“八音律”的理论(下表是“八音律表”的前部分)。
H Li G Bo C N O
F Na Mg Al Si P S
1869年,俄罗斯化学家门捷列夫对当时已知的63种元素的相对原子质量和物理性质(熔点、密度等)进行了比较,直到19世纪末才制成了第一张元素周期表。事实上,在1869年,德国的迈耶和俄国的门捷列夫几乎同时发现了元素周期律。
(1)写出德贝纳提出的“三种元素组”中,氯元素的元素符号: 。
(2)根据纽兰兹“八音律表”,与Na性质相似的元素是 。
(3)分析上述科学史料,判断下列观点正确的有 (可多选)。
A.研究复杂的现象往往需要寻找规律。
B.科学家在研究元素周期规律时,不需要借助技术手段。
C.如果门捷列夫没有发现元素周期表,也会有其他科学家发现。
D.随着科学的进步,我们现在所学的元素周期表已包含所有元素。
E.纽兰兹的“八音律表”中没有稀有元素,说明他的理论是错误,没有作用的。
【答案】Cl Li AC
5.(2023长兴期中)通过对已学知识的对比和归纳,我们往往可以得出一些十分有趣的规律,这些规律可以帮助我们掌握学习科学的方法。请仔细阅读下表中的内容,并回答相应的问题:
常见的几种离子 H+、Na+、Mg2+、OH﹣、Cl﹣、
对应元素及原子团在化合物中的化合价 、、、、、
所能形成化合物的化学式 酸 碱 盐
HCl、H2SO4 NaOH、Mg(OH)2 MgCl2、Na2SO4
(1)由前两行内容对照可得出的规律是:元素或原子团的化合价数值往往与相应离子所带的 数相等。
(2)由后两行内容对照可得出的规律是:通过元素或原子团的 可以确定相应化合物的化学式。
(3)根据硫酸亚铁的化学式FeSO4,可推出该物质所含阳离子的符号为 。
【答案】电荷 化合价 Fe2+
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网(www.21cnjy.com)
同课章节目录
- 第1章 电与磁
- 第1节 指南针为什么能指方向
- 第2节 电生磁
- 第3节 电磁铁的应用
- 第4节 电动机
- 第5节 磁生电
- 第6节 家庭用电
- 第7节 电的安全使用
- 第2章 微粒的模型与符号
- 第1节 模型、符号的建立与作用
- 第2节 物质的微观粒子模型
- 第3节 原子结构的模型
- 第4节 组成物质的元素
- 第5节 表示元素的符号
- 第6节 表示物质的符号
- 第7节 元素符号表示的量
- 第3章 空气与生命
- 第1节 空气与氧气
- 第2节 氧化和燃烧
- 第3节 化学方程式
- 第4节 二氧化碳
- 第5节 生物的呼吸和呼吸作用
- 第6节 光合作用
- 第7节 自然界中的氧循环和碳循环
- 第8节 空气污染与保护
- 第4章 植物与土壤
- 第1节 土壤的成分
- 第2节 各种各样的土壤
- 第3节 植物的根与物质吸收
- 第4节 植物的茎与物质运输
- 第5节 植物的叶与蒸腾作用
- 第6节 保护土壤
- 研究性学习课题
- 一 设计简单的电磁控制电路
- 二 化学反应中质量守恒的研究
- 三 研究植物的呼吸
- 四 当地水土状况调查
