2023—2024学年沪教版(全国)化学九年级下册第7章 应用广泛的酸、碱、盐 复习练习(含答案)
文档属性
| 名称 | 2023—2024学年沪教版(全国)化学九年级下册第7章 应用广泛的酸、碱、盐 复习练习(含答案) |
|
|
| 格式 | doc | ||
| 文件大小 | 568.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-04-04 00:00:00 | ||
图片预览





文档简介
2023—2024学年沪教版(全国)化学九年级下册第7章 应用广泛的酸、碱、盐 复习练习附答案
一、选择题。
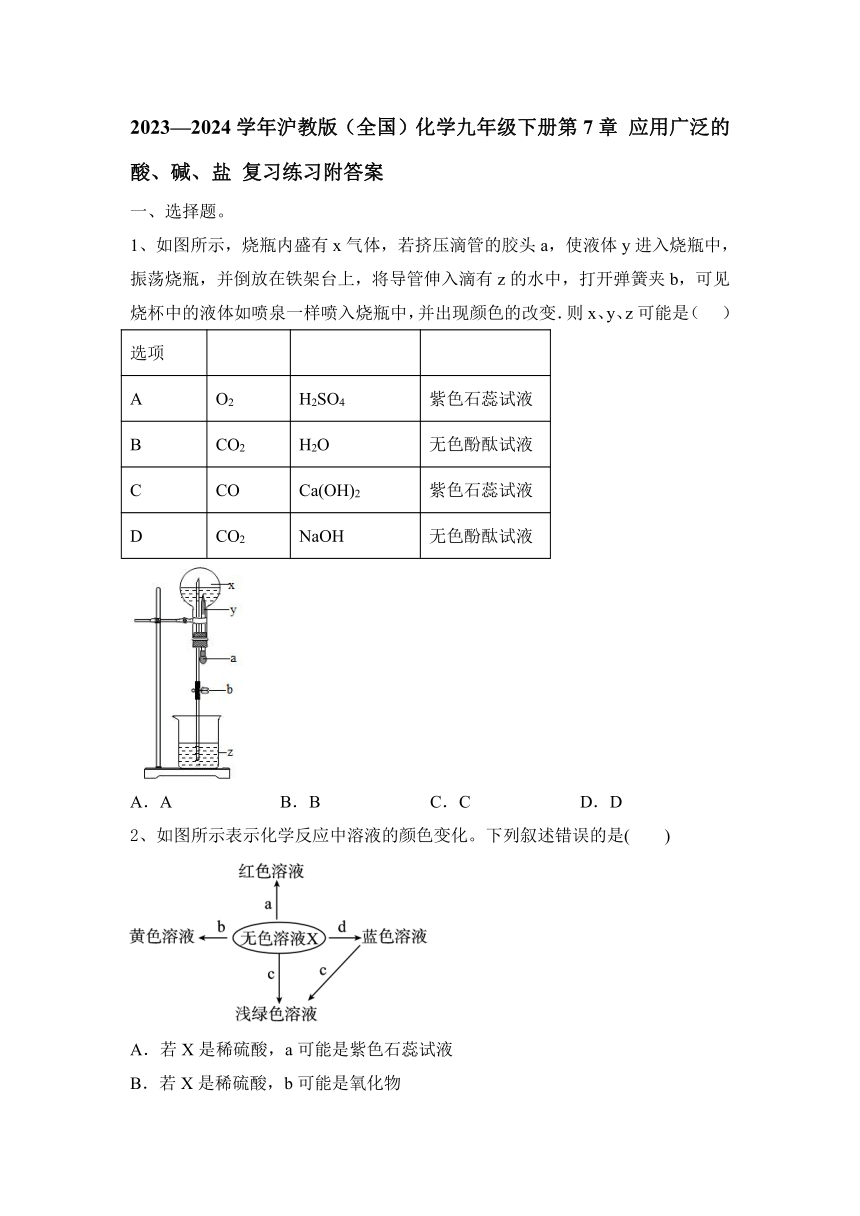
1、如图所示,烧瓶内盛有x气体,若挤压滴管的胶头a,使液体y进入烧瓶中,振荡烧瓶,并倒放在铁架台上,将导管伸入滴有z的水中,打开弹簧夹b,可见烧杯中的液体如喷泉一样喷入烧瓶中,并出现颜色的改变.则x、y、z可能是( )
选项
A O2 H2SO4 紫色石蕊试液
B CO2 H2O 无色酚酞试液
C CO Ca(OH)2 紫色石蕊试液
D CO2 NaOH 无色酚酞试液
A.A B.B C.C D.D
2、如图所示表示化学反应中溶液的颜色变化。下列叙述错误的是( )
A.若X是稀硫酸,a可能是紫色石蕊试液
B.若X是稀硫酸,b可能是氧化物
C.若X是稀盐酸,c不可能是单质
D.若X是稀盐酸,d不可能是单质
3、下列名称与符号相符的是( )
A.熟石灰CaCO3 B.n个硫酸分子nSO4
C.食盐HCl D.亚硫酸钾K2SO3
4、某同学想用实验证明FeCl3溶液显黄色不是Cl﹣离子造成的,下列实验无意义的是( )
A.观察KCl溶液没有颜色
B.加水稀释后FeCl3溶液黄色变浅
C.FeCl3溶液中滴加适量无色硝酸银溶液,振荡后静置,溶液黄色未消失
D.向FeCl3溶液中滴加适量氢氧化钠溶液,振荡后静置,溶液黄色消失
5、下列各组物质的溶液,不用其他试剂,仅通过观察和用组内溶液相互混合的方法,不能将其逐一鉴别出来的是( )
A. NaOH Ca(OH)2 HCl Na2CO3
B. KCl Ba(NO3)2 CuSO4 NaOH
C. AgNO3 HCl Na2CO3 CaCl2
D. Ba(OH)2 KCl Na2SO4 Na2CO3
6、如图是X、Y、Z三种液体的对应近似pH,下列判断不正确的是( )
A.X显酸性 B.Y可能是水
C.Z可能是某种盐溶液 D.Z可使紫色石蕊试液变红
7、下列物质间不能发生反应的是( )
A.稀盐酸和镁条 B.稀盐酸和铜丝
C.稀盐酸和氢氧化镁 D.稀盐酸和氢氧化铜
8、逻辑推理是一种重要的化学思维方法。以下推理正确的是( )
A.氧化物中含有氧元素,含氧元素的化合物一定是氧化物
B.单质中只含有一种元素,只含有一种元素的物质一定是单质
C.碱性溶液能使无色酚酞溶液变红,能使无色酚酞溶液变红的一定是碱性溶液
D.可燃物燃烧时温度需要达到着火点,温度达到着火点时可燃物一定能燃烧
9、工业用反应来制备纯碱,该反应属于( )
A.分解反应 B.化合反应 C.置换反应 D.复分解反应
10、某同学想一次鉴别碳酸钠、氯化铵、氯化钾溶液,他应该加入适量的( )
A. 氢氧化钠溶液 B. 氢氧化钙溶液 C. 硝酸银溶液 D. 稀盐酸
11、下图是生活中常见洗涤用品的 pH, 混用会降低去污效果的组合是( )
A.洁厕灵和消毒液 B.肥皂水和炉具清洁剂
C.消毒液和肥皂水 D.消毒液和炉具清洁剂
12、醋酸(CH3COOH是食醋的成分之一,其水溶液中存在H+和CH3COO-。下列说法正确的是( )
A.醋酸属于氧化物 B.醋酸不能用于除铁锈
C.醋酸能与镁反应产生氢气 D.醋酸中碳元素的质量分数最大
13、小李在学习酸碱指示剂与常见酸、碱溶液作用时,归纳成如图所示的关系.图 中 A、B、C、D 是两圆相交的部分,分别表示指示剂与酸、碱溶液作用时所显示 出的颜色,则其中表示 A 处颜色的是( )
A.紫色 B.蓝色 C.红色 D.无色
14、有甲、乙、丙三种金属,如果将甲、乙、丙分别投入到CuSO4溶液中,一段时间后,甲、丙表面出现红色物质,乙没有明显现象;再将大小相同的甲、丙分别放到相同的盐酸中,甲、丙均产生气泡,但甲产生气泡的速度明显快于丙,则甲、乙、丙三种金属的活动性顺序是( )
A.甲>丙>乙 B.丙>乙>甲 C.甲>乙>丙 D.丙>甲>乙
15、有一溶液是由盐酸、硫酸、硫酸铜、氯化铜几种溶液中的两种混合而成,向该混合液中滴加Ba(OH)2溶液的体积与生成沉淀质量的关系如图所示,则该混合液是( )
A. 盐酸、硫酸 B. 硫酸、氯化铜
C. 盐酸、氯化铜 D. 硫酸、硫酸铜
16、生活中一些物质的pH如下:
物质 白醋 橘子汁 料酒 炉具清洁剂
pH 2~3 3~4 6~7 12~13
其中能使无色酚酞溶液变红的是( )
A.白醋 B.橘子汁 C.料酒 D.炉具清洁剂
二、填空题。
17、小红通过查阅资料得知:红色、蓝色、紫色的花里含有的色素叫花青素。花青素遇酸性溶液就变红,遇碱性溶液就变蓝,于是她选做了如下实验:用一朵紫色的喇叭花浸泡在肥皂水里,喇叭花很快变蓝,她又将另一朵喇叭花浸泡在家庭厨房里的某种调味品中,喇叭花变成了红色,根据上述现象回答:
(1)肥皂水的pH____7(填“>”“=”“<”)测定溶液的pH最简便的方法是使用___________。
(2)小红选用的调味品可能是________________。
(3)如果小红将纯碱溶液滴在喇叭花上则喇叭花应显_________色。
(4)喇叭花汁液的性质与化学实验室中常用的___________性质相似。
18、如图所示是稀释浓硫酸实验的示意图。
(1)写出图中a、b两种仪器的名称:a________;b________。
(2)b容器中所盛的试剂是________(填“水”或“浓硫酸”)。
(3)稀释时,若两种试剂添加顺序颠倒,将会发生__________________。
【联系与拓展】据媒体报道,有一村民在家里误将装在酒瓶中的浓硫酸当成白酒喝下,造成食道和胃严重损伤,这是因为浓硫酸具有__________。这一事件警示我们,家中存放或使用药物时应注意___________________________________。
19、利用海水提取粗盐的过程如下图所示,回答有关问题
(1)一定质量的海水,通过贮水池引入到蒸发池中,在没有引入结晶池之前的蒸发过程中,蒸发池中氯化 钠的质量会__________(填“增大”、“不变”或“减小”)。
(2)粗盐中含有的难溶性杂质,在实验室里可以通过溶解、过滤、蒸发等操作将其去除,这些操作中都会用到玻璃棒,其中在过滤操作中玻璃棒的作用是________(填“引流”或“加快溶解”)。
(3)用氯化钠固体配制100g质量分数为6%的氯化钠溶液。
①配制时,涉及以下实验步骤:
A.称量及量取 B.计算 C.溶解 D.装瓶贴标签。
其正确的实验步骤顺序是______________(填字母)
②将已配好的100g质量分数为6%的氯化钠溶液变成质量分数为16%的氯化钠溶液,需要再加NaCl的质量是______________g(计算结果精确到0.1)
20、某年苏州市初中化学实验操作考查内容为“溶液酸碱性的检验”,请根据实验回答下列问题。
(1)测得碳酸饮料的pH 7(填“<”或“=”或“>”)。
(2)下列使用pH试纸的方法中,正确的是 (填序号)。
A.将pH试纸剪成几段使用
B.将pH试纸直接插入待测液中
C.将pH试纸放在表面皿上,用干净的玻璃棒蘸取待测液滴在pH试纸上
D.将pH试纸湿润后放在表面皿上,用干净的玻璃棒蘸取待测液滴在pH试纸上
E.读数时,在30秒内将pH试纸呈现的颜色与标准比色卡对照
(3)本次实验中滴管使用出现了如图1~图4所示的四种常见错误操作。请你从这四幅图中任意选择一幅(请写明所选图的序号),具体说明改正错误的方法 。
(4)使用白色点滴板完成实验有显色明显、便于对比、 (填一项)等优点。
21、某同学在实验探究中发现了一些物质之间发生化学反应的颜色变化,如图所示。
(1)编号①反应的指示剂是_____________;编号②反应的金属单质是_____________。
(2)根据如图可以总结出稀盐酸的化学性质,其中编号②反应的基本反应类型是_____________反应。
(3)请你写出符合编号③反应的化学方程式__________________。
(4)假设编号④反应的盐是AgNO3,则编号④对应方框中的现象是_____________。
三、实验题。
22、某同学设计了以下三种实验方案,请回答有关问题。
【实验方案一】如图1。
(1)观察到的实验现象是 。
(2)该方案的不足之处是 。(说出一点即可)
【实验方案二】如图2、图3。
图中无色透明塑料瓶的材质、大小、形状完全相同,瓶内用细线固定有用滤纸折叠成的大小和形状相同的小纸花,小纸花上都均匀喷有酚酞溶液,按照图4的操作方式分别用注射器向图2和图3的塑料瓶中同时注入5滴浓氨水,然后将针孔处密封,再将两个塑料瓶分别同时放入等体积的冷水和40℃的热水中。
(3)观察到的现象是:
。
(4)图2、图3采用对照实验的方法,变量只有一个,被控制的量有多个,请说出4个被控制的量:
。
(5)若图4中的小纸花上喷有 ,而注射器向瓶中注入的是浓盐酸,可以观察到小纸花的颜色从下至上变为红色。
【实验方案三】如图5。
用长柄V形玻璃管进行实验,向左、右两端的V形玻璃管口分别同时滴入等量的浓氨水和浓盐酸,塞紧橡皮塞。
(6)过一会儿后,图5中观察到有白烟产生,生成白烟的反应为化合反应,生成一种盐,其化学方程式为 。
(7)从图5中观察到白烟位置偏右,说明 。
四、计算题。
23、黔东南州石灰石资源丰富,某课外小组同学为了测定石灰石中碳酸钙的质量分数,取某地石灰石样品9.0 g于烧杯中,将50 g稀盐酸分5次加入烧杯中,充分反应后(杂质不与稀盐酸反应),测得剩余固体的质量如下表:
次数 1 2 3 4 5
加入稀盐酸质量/g 10 10 10 10 10
剩余固体质量/g 7.0 5.0 3.0 1.5 x
请计算:
(1)x的值为________。
(2)该石灰石样品中碳酸钙的质量分数为________。
(3)所用稀盐酸中溶质的质量分数。(写出计算过程)
2023—2024学年沪教版(全国)化学九年级下册第7章 应用广泛的酸、碱、盐 复习练习附答案
一、选择题。
1、如图所示,烧瓶内盛有x气体,若挤压滴管的胶头a,使液体y进入烧瓶中,振荡烧瓶,并倒放在铁架台上,将导管伸入滴有z的水中,打开弹簧夹b,可见烧杯中的液体如喷泉一样喷入烧瓶中,并出现颜色的改变.则x、y、z可能是( )
选项
A O2 H2SO4 紫色石蕊试液
B CO2 H2O 无色酚酞试液
C CO Ca(OH)2 紫色石蕊试液
D CO2 NaOH 无色酚酞试液
A.A B.B C.C D.D
【答案】D
2、如图所示表示化学反应中溶液的颜色变化。下列叙述错误的是( )
A.若X是稀硫酸,a可能是紫色石蕊试液
B.若X是稀硫酸,b可能是氧化物
C.若X是稀盐酸,c不可能是单质
D.若X是稀盐酸,d不可能是单质
【答案】C
3、下列名称与符号相符的是( )
A.熟石灰CaCO3 B.n个硫酸分子nSO4
C.食盐HCl D.亚硫酸钾K2SO3
【答案】D
4、某同学想用实验证明FeCl3溶液显黄色不是Cl﹣离子造成的,下列实验无意义的是( )
A.观察KCl溶液没有颜色
B.加水稀释后FeCl3溶液黄色变浅
C.FeCl3溶液中滴加适量无色硝酸银溶液,振荡后静置,溶液黄色未消失
D.向FeCl3溶液中滴加适量氢氧化钠溶液,振荡后静置,溶液黄色消失
【答案】B
5、下列各组物质的溶液,不用其他试剂,仅通过观察和用组内溶液相互混合的方法,不能将其逐一鉴别出来的是( )
A. NaOH Ca(OH)2 HCl Na2CO3
B. KCl Ba(NO3)2 CuSO4 NaOH
C. AgNO3 HCl Na2CO3 CaCl2
D. Ba(OH)2 KCl Na2SO4 Na2CO3
【答案】D
6、如图是X、Y、Z三种液体的对应近似pH,下列判断不正确的是( )
A.X显酸性 B.Y可能是水
C.Z可能是某种盐溶液 D.Z可使紫色石蕊试液变红
【答案】D
7、下列物质间不能发生反应的是( )
A.稀盐酸和镁条 B.稀盐酸和铜丝
C.稀盐酸和氢氧化镁 D.稀盐酸和氢氧化铜
【答案】B
8、逻辑推理是一种重要的化学思维方法。以下推理正确的是( )
A.氧化物中含有氧元素,含氧元素的化合物一定是氧化物
B.单质中只含有一种元素,只含有一种元素的物质一定是单质
C.碱性溶液能使无色酚酞溶液变红,能使无色酚酞溶液变红的一定是碱性溶液
D.可燃物燃烧时温度需要达到着火点,温度达到着火点时可燃物一定能燃烧
【答案】C
9、工业用反应来制备纯碱,该反应属于( )
A.分解反应 B.化合反应 C.置换反应 D.复分解反应
【答案】A
10、某同学想一次鉴别碳酸钠、氯化铵、氯化钾溶液,他应该加入适量的( )
A. 氢氧化钠溶液 B. 氢氧化钙溶液 C. 硝酸银溶液 D. 稀盐酸
【答案】B
11、下图是生活中常见洗涤用品的 pH, 混用会降低去污效果的组合是( )
A.洁厕灵和消毒液 B.肥皂水和炉具清洁剂
C.消毒液和肥皂水 D.消毒液和炉具清洁剂
【答案】A
12、醋酸(CH3COOH是食醋的成分之一,其水溶液中存在H+和CH3COO-。下列说法正确的是( )
A.醋酸属于氧化物 B.醋酸不能用于除铁锈
C.醋酸能与镁反应产生氢气 D.醋酸中碳元素的质量分数最大
【答案】C
13、小李在学习酸碱指示剂与常见酸、碱溶液作用时,归纳成如图所示的关系.图 中 A、B、C、D 是两圆相交的部分,分别表示指示剂与酸、碱溶液作用时所显示 出的颜色,则其中表示 A 处颜色的是( )
A.紫色 B.蓝色 C.红色 D.无色
【答案】C
14、有甲、乙、丙三种金属,如果将甲、乙、丙分别投入到CuSO4溶液中,一段时间后,甲、丙表面出现红色物质,乙没有明显现象;再将大小相同的甲、丙分别放到相同的盐酸中,甲、丙均产生气泡,但甲产生气泡的速度明显快于丙,则甲、乙、丙三种金属的活动性顺序是( )
A.甲>丙>乙 B.丙>乙>甲 C.甲>乙>丙 D.丙>甲>乙
【答案】A
15、有一溶液是由盐酸、硫酸、硫酸铜、氯化铜几种溶液中的两种混合而成,向该混合液中滴加Ba(OH)2溶液的体积与生成沉淀质量的关系如图所示,则该混合液是( )
B. 盐酸、硫酸 B. 硫酸、氯化铜
C. 盐酸、氯化铜 D. 硫酸、硫酸铜
【答案】C
16、生活中一些物质的pH如下:
物质 白醋 橘子汁 料酒 炉具清洁剂
pH 2~3 3~4 6~7 12~13
其中能使无色酚酞溶液变红的是( )
A.白醋 B.橘子汁 C.料酒 D.炉具清洁剂
【答案】D
二、填空题。
17、小红通过查阅资料得知:红色、蓝色、紫色的花里含有的色素叫花青素。花青素遇酸性溶液就变红,遇碱性溶液就变蓝,于是她选做了如下实验:用一朵紫色的喇叭花浸泡在肥皂水里,喇叭花很快变蓝,她又将另一朵喇叭花浸泡在家庭厨房里的某种调味品中,喇叭花变成了红色,根据上述现象回答:
(1)肥皂水的pH____7(填“>”“=”“<”)测定溶液的pH最简便的方法是使用___________。
(2)小红选用的调味品可能是________________。
(3)如果小红将纯碱溶液滴在喇叭花上则喇叭花应显_________色。
(4)喇叭花汁液的性质与化学实验室中常用的___________性质相似。
【答案】(1)> pH试纸测定 (2)食醋 (3)蓝 (4)紫色石蕊试液
18、如图所示是稀释浓硫酸实验的示意图。
(1)写出图中a、b两种仪器的名称:a________;b________。
(2)b容器中所盛的试剂是________(填“水”或“浓硫酸”)。
(3)稀释时,若两种试剂添加顺序颠倒,将会发生__________________。
【联系与拓展】据媒体报道,有一村民在家里误将装在酒瓶中的浓硫酸当成白酒喝下,造成食道和胃严重损伤,这是因为浓硫酸具有__________。这一事件警示我们,家中存放或使用药物时应注意___________________________________。
【答案】(1)玻璃棒 量筒 (2)浓硫酸 (3)酸液飞溅
【联系与拓展】腐蚀性 存放时要贴好标签,放在安全的地方(或使用时要核对标签)
19、利用海水提取粗盐的过程如下图所示,回答有关问题
(1)一定质量的海水,通过贮水池引入到蒸发池中,在没有引入结晶池之前的蒸发过程中,蒸发池中氯化 钠的质量会__________(填“增大”、“不变”或“减小”)。
(2)粗盐中含有的难溶性杂质,在实验室里可以通过溶解、过滤、蒸发等操作将其去除,这些操作中都会用到玻璃棒,其中在过滤操作中玻璃棒的作用是________(填“引流”或“加快溶解”)。
(3)用氯化钠固体配制100g质量分数为6%的氯化钠溶液。
①配制时,涉及以下实验步骤:
A.称量及量取 B.计算 C.溶解 D.装瓶贴标签。
其正确的实验步骤顺序是______________(填字母)
②将已配好的100g质量分数为6%的氯化钠溶液变成质量分数为16%的氯化钠溶液,需要再加NaCl的质量是______________g(计算结果精确到0.1)
【答案】不变 引流 BACD 11.9
20、某年苏州市初中化学实验操作考查内容为“溶液酸碱性的检验”,请根据实验回答下列问题。
(1)测得碳酸饮料的pH 7(填“<”或“=”或“>”)。
(2)下列使用pH试纸的方法中,正确的是 (填序号)。
A.将pH试纸剪成几段使用
B.将pH试纸直接插入待测液中
C.将pH试纸放在表面皿上,用干净的玻璃棒蘸取待测液滴在pH试纸上
D.将pH试纸湿润后放在表面皿上,用干净的玻璃棒蘸取待测液滴在pH试纸上
E.读数时,在30秒内将pH试纸呈现的颜色与标准比色卡对照
(3)本次实验中滴管使用出现了如图1~图4所示的四种常见错误操作。请你从这四幅图中任意选择一幅(请写明所选图的序号),具体说明改正错误的方法 。
(4)使用白色点滴板完成实验有显色明显、便于对比、 (填一项)等优点。
【答案】(1)< (2)ACE
(3)图3滴瓶上的滴管不用清洗直接放回原瓶(合理即可)
(4)节约药品
21、某同学在实验探究中发现了一些物质之间发生化学反应的颜色变化,如图所示。
(1)编号①反应的指示剂是_____________;编号②反应的金属单质是_____________。
(2)根据如图可以总结出稀盐酸的化学性质,其中编号②反应的基本反应类型是_____________反应。
(3)请你写出符合编号③反应的化学方程式__________________。
(4)假设编号④反应的盐是AgNO3,则编号④对应方框中的现象是_____________。
【答案】石蕊试剂 Fe 置换反应
产生白色沉淀
三、实验题。
22、某同学设计了以下三种实验方案,请回答有关问题。
【实验方案一】如图1。
(1)观察到的实验现象是 。
(2)该方案的不足之处是 。(说出一点即可)
【实验方案二】如图2、图3。
图中无色透明塑料瓶的材质、大小、形状完全相同,瓶内用细线固定有用滤纸折叠成的大小和形状相同的小纸花,小纸花上都均匀喷有酚酞溶液,按照图4的操作方式分别用注射器向图2和图3的塑料瓶中同时注入5滴浓氨水,然后将针孔处密封,再将两个塑料瓶分别同时放入等体积的冷水和40℃的热水中。
(3)观察到的现象是:
。
(4)图2、图3采用对照实验的方法,变量只有一个,被控制的量有多个,请说出4个被控制的量:
。
(5)若图4中的小纸花上喷有 ,而注射器向瓶中注入的是浓盐酸,可以观察到小纸花的颜色从下至上变为红色。
【实验方案三】如图5。
用长柄V形玻璃管进行实验,向左、右两端的V形玻璃管口分别同时滴入等量的浓氨水和浓盐酸,塞紧橡皮塞。
(6)过一会儿后,图5中观察到有白烟产生,生成白烟的反应为化合反应,生成一种盐,其化学方程式为 。
(7)从图5中观察到白烟位置偏右,说明 。
【答案】(1)酚酞溶液变红
(2)浪费药品或污染空气等
(3)小纸花从下到上逐渐变红,在热水中塑料瓶内的纸花变红的比冷水中塑料瓶内的纸花快
(4)使用的塑料瓶材质、大小、形状完全相同,小纸花的大小和形状相同,塑料瓶中注入的氨水的滴数相同,烧杯内的水的体积相同等
(5)紫色石蕊试液
(6)
(7) 不同分子的运动速度不同 氨气比氯化氢在空气中运动得快
四、计算题。
23、黔东南州石灰石资源丰富,某课外小组同学为了测定石灰石中碳酸钙的质量分数,取某地石灰石样品9.0 g于烧杯中,将50 g稀盐酸分5次加入烧杯中,充分反应后(杂质不与稀盐酸反应),测得剩余固体的质量如下表:
次数 1 2 3 4 5
加入稀盐酸质量/g 10 10 10 10 10
剩余固体质量/g 7.0 5.0 3.0 1.5 x
请计算:
(1)x的值为________。
(2)该石灰石样品中碳酸钙的质量分数为________。
(3)所用稀盐酸中溶质的质量分数。(写出计算过程)
【答案】(1)1.5 (2)83.3% (3)所用稀盐酸中溶质的质量分数为14.6%。
【详解】(3)设10 g稀盐酸中HCl的质量为y。
CaCO3+2HCl===CaCl2+H2O+CO2↑100 73 2 g y
= y=1.46 g
所用稀盐酸中溶质的质量分数为:
×100%=14.6%。
答:所用稀盐酸中溶质的质量分数为14.6%。
一、选择题。
1、如图所示,烧瓶内盛有x气体,若挤压滴管的胶头a,使液体y进入烧瓶中,振荡烧瓶,并倒放在铁架台上,将导管伸入滴有z的水中,打开弹簧夹b,可见烧杯中的液体如喷泉一样喷入烧瓶中,并出现颜色的改变.则x、y、z可能是( )
选项
A O2 H2SO4 紫色石蕊试液
B CO2 H2O 无色酚酞试液
C CO Ca(OH)2 紫色石蕊试液
D CO2 NaOH 无色酚酞试液
A.A B.B C.C D.D
2、如图所示表示化学反应中溶液的颜色变化。下列叙述错误的是( )
A.若X是稀硫酸,a可能是紫色石蕊试液
B.若X是稀硫酸,b可能是氧化物
C.若X是稀盐酸,c不可能是单质
D.若X是稀盐酸,d不可能是单质
3、下列名称与符号相符的是( )
A.熟石灰CaCO3 B.n个硫酸分子nSO4
C.食盐HCl D.亚硫酸钾K2SO3
4、某同学想用实验证明FeCl3溶液显黄色不是Cl﹣离子造成的,下列实验无意义的是( )
A.观察KCl溶液没有颜色
B.加水稀释后FeCl3溶液黄色变浅
C.FeCl3溶液中滴加适量无色硝酸银溶液,振荡后静置,溶液黄色未消失
D.向FeCl3溶液中滴加适量氢氧化钠溶液,振荡后静置,溶液黄色消失
5、下列各组物质的溶液,不用其他试剂,仅通过观察和用组内溶液相互混合的方法,不能将其逐一鉴别出来的是( )
A. NaOH Ca(OH)2 HCl Na2CO3
B. KCl Ba(NO3)2 CuSO4 NaOH
C. AgNO3 HCl Na2CO3 CaCl2
D. Ba(OH)2 KCl Na2SO4 Na2CO3
6、如图是X、Y、Z三种液体的对应近似pH,下列判断不正确的是( )
A.X显酸性 B.Y可能是水
C.Z可能是某种盐溶液 D.Z可使紫色石蕊试液变红
7、下列物质间不能发生反应的是( )
A.稀盐酸和镁条 B.稀盐酸和铜丝
C.稀盐酸和氢氧化镁 D.稀盐酸和氢氧化铜
8、逻辑推理是一种重要的化学思维方法。以下推理正确的是( )
A.氧化物中含有氧元素,含氧元素的化合物一定是氧化物
B.单质中只含有一种元素,只含有一种元素的物质一定是单质
C.碱性溶液能使无色酚酞溶液变红,能使无色酚酞溶液变红的一定是碱性溶液
D.可燃物燃烧时温度需要达到着火点,温度达到着火点时可燃物一定能燃烧
9、工业用反应来制备纯碱,该反应属于( )
A.分解反应 B.化合反应 C.置换反应 D.复分解反应
10、某同学想一次鉴别碳酸钠、氯化铵、氯化钾溶液,他应该加入适量的( )
A. 氢氧化钠溶液 B. 氢氧化钙溶液 C. 硝酸银溶液 D. 稀盐酸
11、下图是生活中常见洗涤用品的 pH, 混用会降低去污效果的组合是( )
A.洁厕灵和消毒液 B.肥皂水和炉具清洁剂
C.消毒液和肥皂水 D.消毒液和炉具清洁剂
12、醋酸(CH3COOH是食醋的成分之一,其水溶液中存在H+和CH3COO-。下列说法正确的是( )
A.醋酸属于氧化物 B.醋酸不能用于除铁锈
C.醋酸能与镁反应产生氢气 D.醋酸中碳元素的质量分数最大
13、小李在学习酸碱指示剂与常见酸、碱溶液作用时,归纳成如图所示的关系.图 中 A、B、C、D 是两圆相交的部分,分别表示指示剂与酸、碱溶液作用时所显示 出的颜色,则其中表示 A 处颜色的是( )
A.紫色 B.蓝色 C.红色 D.无色
14、有甲、乙、丙三种金属,如果将甲、乙、丙分别投入到CuSO4溶液中,一段时间后,甲、丙表面出现红色物质,乙没有明显现象;再将大小相同的甲、丙分别放到相同的盐酸中,甲、丙均产生气泡,但甲产生气泡的速度明显快于丙,则甲、乙、丙三种金属的活动性顺序是( )
A.甲>丙>乙 B.丙>乙>甲 C.甲>乙>丙 D.丙>甲>乙
15、有一溶液是由盐酸、硫酸、硫酸铜、氯化铜几种溶液中的两种混合而成,向该混合液中滴加Ba(OH)2溶液的体积与生成沉淀质量的关系如图所示,则该混合液是( )
A. 盐酸、硫酸 B. 硫酸、氯化铜
C. 盐酸、氯化铜 D. 硫酸、硫酸铜
16、生活中一些物质的pH如下:
物质 白醋 橘子汁 料酒 炉具清洁剂
pH 2~3 3~4 6~7 12~13
其中能使无色酚酞溶液变红的是( )
A.白醋 B.橘子汁 C.料酒 D.炉具清洁剂
二、填空题。
17、小红通过查阅资料得知:红色、蓝色、紫色的花里含有的色素叫花青素。花青素遇酸性溶液就变红,遇碱性溶液就变蓝,于是她选做了如下实验:用一朵紫色的喇叭花浸泡在肥皂水里,喇叭花很快变蓝,她又将另一朵喇叭花浸泡在家庭厨房里的某种调味品中,喇叭花变成了红色,根据上述现象回答:
(1)肥皂水的pH____7(填“>”“=”“<”)测定溶液的pH最简便的方法是使用___________。
(2)小红选用的调味品可能是________________。
(3)如果小红将纯碱溶液滴在喇叭花上则喇叭花应显_________色。
(4)喇叭花汁液的性质与化学实验室中常用的___________性质相似。
18、如图所示是稀释浓硫酸实验的示意图。
(1)写出图中a、b两种仪器的名称:a________;b________。
(2)b容器中所盛的试剂是________(填“水”或“浓硫酸”)。
(3)稀释时,若两种试剂添加顺序颠倒,将会发生__________________。
【联系与拓展】据媒体报道,有一村民在家里误将装在酒瓶中的浓硫酸当成白酒喝下,造成食道和胃严重损伤,这是因为浓硫酸具有__________。这一事件警示我们,家中存放或使用药物时应注意___________________________________。
19、利用海水提取粗盐的过程如下图所示,回答有关问题
(1)一定质量的海水,通过贮水池引入到蒸发池中,在没有引入结晶池之前的蒸发过程中,蒸发池中氯化 钠的质量会__________(填“增大”、“不变”或“减小”)。
(2)粗盐中含有的难溶性杂质,在实验室里可以通过溶解、过滤、蒸发等操作将其去除,这些操作中都会用到玻璃棒,其中在过滤操作中玻璃棒的作用是________(填“引流”或“加快溶解”)。
(3)用氯化钠固体配制100g质量分数为6%的氯化钠溶液。
①配制时,涉及以下实验步骤:
A.称量及量取 B.计算 C.溶解 D.装瓶贴标签。
其正确的实验步骤顺序是______________(填字母)
②将已配好的100g质量分数为6%的氯化钠溶液变成质量分数为16%的氯化钠溶液,需要再加NaCl的质量是______________g(计算结果精确到0.1)
20、某年苏州市初中化学实验操作考查内容为“溶液酸碱性的检验”,请根据实验回答下列问题。
(1)测得碳酸饮料的pH 7(填“<”或“=”或“>”)。
(2)下列使用pH试纸的方法中,正确的是 (填序号)。
A.将pH试纸剪成几段使用
B.将pH试纸直接插入待测液中
C.将pH试纸放在表面皿上,用干净的玻璃棒蘸取待测液滴在pH试纸上
D.将pH试纸湿润后放在表面皿上,用干净的玻璃棒蘸取待测液滴在pH试纸上
E.读数时,在30秒内将pH试纸呈现的颜色与标准比色卡对照
(3)本次实验中滴管使用出现了如图1~图4所示的四种常见错误操作。请你从这四幅图中任意选择一幅(请写明所选图的序号),具体说明改正错误的方法 。
(4)使用白色点滴板完成实验有显色明显、便于对比、 (填一项)等优点。
21、某同学在实验探究中发现了一些物质之间发生化学反应的颜色变化,如图所示。
(1)编号①反应的指示剂是_____________;编号②反应的金属单质是_____________。
(2)根据如图可以总结出稀盐酸的化学性质,其中编号②反应的基本反应类型是_____________反应。
(3)请你写出符合编号③反应的化学方程式__________________。
(4)假设编号④反应的盐是AgNO3,则编号④对应方框中的现象是_____________。
三、实验题。
22、某同学设计了以下三种实验方案,请回答有关问题。
【实验方案一】如图1。
(1)观察到的实验现象是 。
(2)该方案的不足之处是 。(说出一点即可)
【实验方案二】如图2、图3。
图中无色透明塑料瓶的材质、大小、形状完全相同,瓶内用细线固定有用滤纸折叠成的大小和形状相同的小纸花,小纸花上都均匀喷有酚酞溶液,按照图4的操作方式分别用注射器向图2和图3的塑料瓶中同时注入5滴浓氨水,然后将针孔处密封,再将两个塑料瓶分别同时放入等体积的冷水和40℃的热水中。
(3)观察到的现象是:
。
(4)图2、图3采用对照实验的方法,变量只有一个,被控制的量有多个,请说出4个被控制的量:
。
(5)若图4中的小纸花上喷有 ,而注射器向瓶中注入的是浓盐酸,可以观察到小纸花的颜色从下至上变为红色。
【实验方案三】如图5。
用长柄V形玻璃管进行实验,向左、右两端的V形玻璃管口分别同时滴入等量的浓氨水和浓盐酸,塞紧橡皮塞。
(6)过一会儿后,图5中观察到有白烟产生,生成白烟的反应为化合反应,生成一种盐,其化学方程式为 。
(7)从图5中观察到白烟位置偏右,说明 。
四、计算题。
23、黔东南州石灰石资源丰富,某课外小组同学为了测定石灰石中碳酸钙的质量分数,取某地石灰石样品9.0 g于烧杯中,将50 g稀盐酸分5次加入烧杯中,充分反应后(杂质不与稀盐酸反应),测得剩余固体的质量如下表:
次数 1 2 3 4 5
加入稀盐酸质量/g 10 10 10 10 10
剩余固体质量/g 7.0 5.0 3.0 1.5 x
请计算:
(1)x的值为________。
(2)该石灰石样品中碳酸钙的质量分数为________。
(3)所用稀盐酸中溶质的质量分数。(写出计算过程)
2023—2024学年沪教版(全国)化学九年级下册第7章 应用广泛的酸、碱、盐 复习练习附答案
一、选择题。
1、如图所示,烧瓶内盛有x气体,若挤压滴管的胶头a,使液体y进入烧瓶中,振荡烧瓶,并倒放在铁架台上,将导管伸入滴有z的水中,打开弹簧夹b,可见烧杯中的液体如喷泉一样喷入烧瓶中,并出现颜色的改变.则x、y、z可能是( )
选项
A O2 H2SO4 紫色石蕊试液
B CO2 H2O 无色酚酞试液
C CO Ca(OH)2 紫色石蕊试液
D CO2 NaOH 无色酚酞试液
A.A B.B C.C D.D
【答案】D
2、如图所示表示化学反应中溶液的颜色变化。下列叙述错误的是( )
A.若X是稀硫酸,a可能是紫色石蕊试液
B.若X是稀硫酸,b可能是氧化物
C.若X是稀盐酸,c不可能是单质
D.若X是稀盐酸,d不可能是单质
【答案】C
3、下列名称与符号相符的是( )
A.熟石灰CaCO3 B.n个硫酸分子nSO4
C.食盐HCl D.亚硫酸钾K2SO3
【答案】D
4、某同学想用实验证明FeCl3溶液显黄色不是Cl﹣离子造成的,下列实验无意义的是( )
A.观察KCl溶液没有颜色
B.加水稀释后FeCl3溶液黄色变浅
C.FeCl3溶液中滴加适量无色硝酸银溶液,振荡后静置,溶液黄色未消失
D.向FeCl3溶液中滴加适量氢氧化钠溶液,振荡后静置,溶液黄色消失
【答案】B
5、下列各组物质的溶液,不用其他试剂,仅通过观察和用组内溶液相互混合的方法,不能将其逐一鉴别出来的是( )
A. NaOH Ca(OH)2 HCl Na2CO3
B. KCl Ba(NO3)2 CuSO4 NaOH
C. AgNO3 HCl Na2CO3 CaCl2
D. Ba(OH)2 KCl Na2SO4 Na2CO3
【答案】D
6、如图是X、Y、Z三种液体的对应近似pH,下列判断不正确的是( )
A.X显酸性 B.Y可能是水
C.Z可能是某种盐溶液 D.Z可使紫色石蕊试液变红
【答案】D
7、下列物质间不能发生反应的是( )
A.稀盐酸和镁条 B.稀盐酸和铜丝
C.稀盐酸和氢氧化镁 D.稀盐酸和氢氧化铜
【答案】B
8、逻辑推理是一种重要的化学思维方法。以下推理正确的是( )
A.氧化物中含有氧元素,含氧元素的化合物一定是氧化物
B.单质中只含有一种元素,只含有一种元素的物质一定是单质
C.碱性溶液能使无色酚酞溶液变红,能使无色酚酞溶液变红的一定是碱性溶液
D.可燃物燃烧时温度需要达到着火点,温度达到着火点时可燃物一定能燃烧
【答案】C
9、工业用反应来制备纯碱,该反应属于( )
A.分解反应 B.化合反应 C.置换反应 D.复分解反应
【答案】A
10、某同学想一次鉴别碳酸钠、氯化铵、氯化钾溶液,他应该加入适量的( )
A. 氢氧化钠溶液 B. 氢氧化钙溶液 C. 硝酸银溶液 D. 稀盐酸
【答案】B
11、下图是生活中常见洗涤用品的 pH, 混用会降低去污效果的组合是( )
A.洁厕灵和消毒液 B.肥皂水和炉具清洁剂
C.消毒液和肥皂水 D.消毒液和炉具清洁剂
【答案】A
12、醋酸(CH3COOH是食醋的成分之一,其水溶液中存在H+和CH3COO-。下列说法正确的是( )
A.醋酸属于氧化物 B.醋酸不能用于除铁锈
C.醋酸能与镁反应产生氢气 D.醋酸中碳元素的质量分数最大
【答案】C
13、小李在学习酸碱指示剂与常见酸、碱溶液作用时,归纳成如图所示的关系.图 中 A、B、C、D 是两圆相交的部分,分别表示指示剂与酸、碱溶液作用时所显示 出的颜色,则其中表示 A 处颜色的是( )
A.紫色 B.蓝色 C.红色 D.无色
【答案】C
14、有甲、乙、丙三种金属,如果将甲、乙、丙分别投入到CuSO4溶液中,一段时间后,甲、丙表面出现红色物质,乙没有明显现象;再将大小相同的甲、丙分别放到相同的盐酸中,甲、丙均产生气泡,但甲产生气泡的速度明显快于丙,则甲、乙、丙三种金属的活动性顺序是( )
A.甲>丙>乙 B.丙>乙>甲 C.甲>乙>丙 D.丙>甲>乙
【答案】A
15、有一溶液是由盐酸、硫酸、硫酸铜、氯化铜几种溶液中的两种混合而成,向该混合液中滴加Ba(OH)2溶液的体积与生成沉淀质量的关系如图所示,则该混合液是( )
B. 盐酸、硫酸 B. 硫酸、氯化铜
C. 盐酸、氯化铜 D. 硫酸、硫酸铜
【答案】C
16、生活中一些物质的pH如下:
物质 白醋 橘子汁 料酒 炉具清洁剂
pH 2~3 3~4 6~7 12~13
其中能使无色酚酞溶液变红的是( )
A.白醋 B.橘子汁 C.料酒 D.炉具清洁剂
【答案】D
二、填空题。
17、小红通过查阅资料得知:红色、蓝色、紫色的花里含有的色素叫花青素。花青素遇酸性溶液就变红,遇碱性溶液就变蓝,于是她选做了如下实验:用一朵紫色的喇叭花浸泡在肥皂水里,喇叭花很快变蓝,她又将另一朵喇叭花浸泡在家庭厨房里的某种调味品中,喇叭花变成了红色,根据上述现象回答:
(1)肥皂水的pH____7(填“>”“=”“<”)测定溶液的pH最简便的方法是使用___________。
(2)小红选用的调味品可能是________________。
(3)如果小红将纯碱溶液滴在喇叭花上则喇叭花应显_________色。
(4)喇叭花汁液的性质与化学实验室中常用的___________性质相似。
【答案】(1)> pH试纸测定 (2)食醋 (3)蓝 (4)紫色石蕊试液
18、如图所示是稀释浓硫酸实验的示意图。
(1)写出图中a、b两种仪器的名称:a________;b________。
(2)b容器中所盛的试剂是________(填“水”或“浓硫酸”)。
(3)稀释时,若两种试剂添加顺序颠倒,将会发生__________________。
【联系与拓展】据媒体报道,有一村民在家里误将装在酒瓶中的浓硫酸当成白酒喝下,造成食道和胃严重损伤,这是因为浓硫酸具有__________。这一事件警示我们,家中存放或使用药物时应注意___________________________________。
【答案】(1)玻璃棒 量筒 (2)浓硫酸 (3)酸液飞溅
【联系与拓展】腐蚀性 存放时要贴好标签,放在安全的地方(或使用时要核对标签)
19、利用海水提取粗盐的过程如下图所示,回答有关问题
(1)一定质量的海水,通过贮水池引入到蒸发池中,在没有引入结晶池之前的蒸发过程中,蒸发池中氯化 钠的质量会__________(填“增大”、“不变”或“减小”)。
(2)粗盐中含有的难溶性杂质,在实验室里可以通过溶解、过滤、蒸发等操作将其去除,这些操作中都会用到玻璃棒,其中在过滤操作中玻璃棒的作用是________(填“引流”或“加快溶解”)。
(3)用氯化钠固体配制100g质量分数为6%的氯化钠溶液。
①配制时,涉及以下实验步骤:
A.称量及量取 B.计算 C.溶解 D.装瓶贴标签。
其正确的实验步骤顺序是______________(填字母)
②将已配好的100g质量分数为6%的氯化钠溶液变成质量分数为16%的氯化钠溶液,需要再加NaCl的质量是______________g(计算结果精确到0.1)
【答案】不变 引流 BACD 11.9
20、某年苏州市初中化学实验操作考查内容为“溶液酸碱性的检验”,请根据实验回答下列问题。
(1)测得碳酸饮料的pH 7(填“<”或“=”或“>”)。
(2)下列使用pH试纸的方法中,正确的是 (填序号)。
A.将pH试纸剪成几段使用
B.将pH试纸直接插入待测液中
C.将pH试纸放在表面皿上,用干净的玻璃棒蘸取待测液滴在pH试纸上
D.将pH试纸湿润后放在表面皿上,用干净的玻璃棒蘸取待测液滴在pH试纸上
E.读数时,在30秒内将pH试纸呈现的颜色与标准比色卡对照
(3)本次实验中滴管使用出现了如图1~图4所示的四种常见错误操作。请你从这四幅图中任意选择一幅(请写明所选图的序号),具体说明改正错误的方法 。
(4)使用白色点滴板完成实验有显色明显、便于对比、 (填一项)等优点。
【答案】(1)< (2)ACE
(3)图3滴瓶上的滴管不用清洗直接放回原瓶(合理即可)
(4)节约药品
21、某同学在实验探究中发现了一些物质之间发生化学反应的颜色变化,如图所示。
(1)编号①反应的指示剂是_____________;编号②反应的金属单质是_____________。
(2)根据如图可以总结出稀盐酸的化学性质,其中编号②反应的基本反应类型是_____________反应。
(3)请你写出符合编号③反应的化学方程式__________________。
(4)假设编号④反应的盐是AgNO3,则编号④对应方框中的现象是_____________。
【答案】石蕊试剂 Fe 置换反应
产生白色沉淀
三、实验题。
22、某同学设计了以下三种实验方案,请回答有关问题。
【实验方案一】如图1。
(1)观察到的实验现象是 。
(2)该方案的不足之处是 。(说出一点即可)
【实验方案二】如图2、图3。
图中无色透明塑料瓶的材质、大小、形状完全相同,瓶内用细线固定有用滤纸折叠成的大小和形状相同的小纸花,小纸花上都均匀喷有酚酞溶液,按照图4的操作方式分别用注射器向图2和图3的塑料瓶中同时注入5滴浓氨水,然后将针孔处密封,再将两个塑料瓶分别同时放入等体积的冷水和40℃的热水中。
(3)观察到的现象是:
。
(4)图2、图3采用对照实验的方法,变量只有一个,被控制的量有多个,请说出4个被控制的量:
。
(5)若图4中的小纸花上喷有 ,而注射器向瓶中注入的是浓盐酸,可以观察到小纸花的颜色从下至上变为红色。
【实验方案三】如图5。
用长柄V形玻璃管进行实验,向左、右两端的V形玻璃管口分别同时滴入等量的浓氨水和浓盐酸,塞紧橡皮塞。
(6)过一会儿后,图5中观察到有白烟产生,生成白烟的反应为化合反应,生成一种盐,其化学方程式为 。
(7)从图5中观察到白烟位置偏右,说明 。
【答案】(1)酚酞溶液变红
(2)浪费药品或污染空气等
(3)小纸花从下到上逐渐变红,在热水中塑料瓶内的纸花变红的比冷水中塑料瓶内的纸花快
(4)使用的塑料瓶材质、大小、形状完全相同,小纸花的大小和形状相同,塑料瓶中注入的氨水的滴数相同,烧杯内的水的体积相同等
(5)紫色石蕊试液
(6)
(7) 不同分子的运动速度不同 氨气比氯化氢在空气中运动得快
四、计算题。
23、黔东南州石灰石资源丰富,某课外小组同学为了测定石灰石中碳酸钙的质量分数,取某地石灰石样品9.0 g于烧杯中,将50 g稀盐酸分5次加入烧杯中,充分反应后(杂质不与稀盐酸反应),测得剩余固体的质量如下表:
次数 1 2 3 4 5
加入稀盐酸质量/g 10 10 10 10 10
剩余固体质量/g 7.0 5.0 3.0 1.5 x
请计算:
(1)x的值为________。
(2)该石灰石样品中碳酸钙的质量分数为________。
(3)所用稀盐酸中溶质的质量分数。(写出计算过程)
【答案】(1)1.5 (2)83.3% (3)所用稀盐酸中溶质的质量分数为14.6%。
【详解】(3)设10 g稀盐酸中HCl的质量为y。
CaCO3+2HCl===CaCl2+H2O+CO2↑100 73 2 g y
= y=1.46 g
所用稀盐酸中溶质的质量分数为:
×100%=14.6%。
答:所用稀盐酸中溶质的质量分数为14.6%。
