第1节 空气与氧气 第3课时(课件 16张PPT)
文档属性
| 名称 | 第1节 空气与氧气 第3课时(课件 16张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 110.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2024-04-09 00:00:00 | ||
图片预览




文档简介
(共16张PPT)
内容要求
①知道空气主要成分的体积分数,认识空气对人类的重要作用。②认识氧气的主要性质,学会氧气的实验室制法。认识化学反应催化剂的重要作用。
③知道常见的化合反应、分解反应。
学业要求
①能完成氧气的实验室制取,认识实验室制取气体的一般思路和方法。②能辨析常见的化合、分解反应。
实验
氧气的制取和性质研究
第1节 空气与氧气(3)
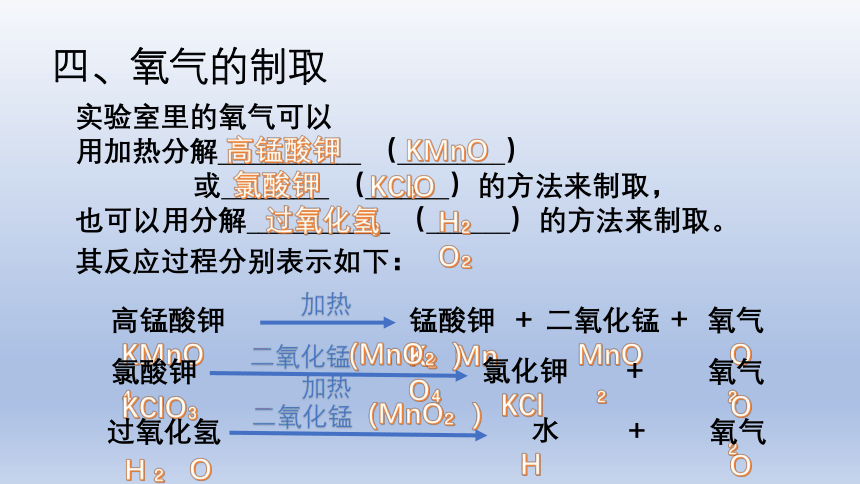
实验室里的氧气可以
用加热分解____________ (_________)
或_________ (_______)的方法来制取,
也可以用分解____________ (_______)的方法来制取。
KMnO
四、氧气的制取
KClO
H O
高锰酸钾
氯酸钾
过氧化氢
其反应过程分别表示如下:
MnO
O
高锰酸钾
锰酸钾
加热
二氧化锰
氧气
+
+
KMnO
K MnO
(MnO )
O
氯酸钾
氯化钾
二氧化锰
氧气
+
KClO
KCl
加热
(MnO )
O
过氧化氢
水
二氧化锰
氧气
+
H O
H O
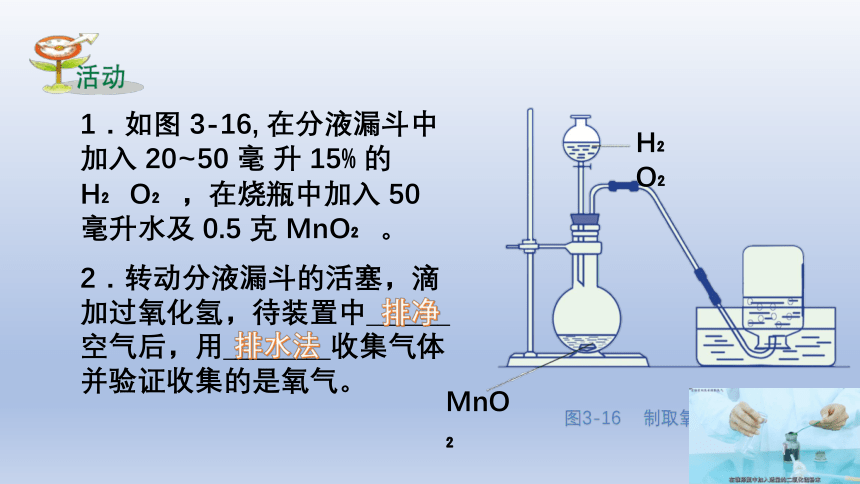
1.如图 3-16, 在分液漏斗中加入 20~50 毫 升 15% 的 H O ,在烧瓶中加入 50 毫升水及 0.5 克 MnO 。
2.转动分液漏斗的活塞,滴加过氧化氢,待装置中_______空气后,用_________收集气体并验证收集的是氧气。
图3-16 制取氧气的装置
H O
MnO
排净
排水法
①
②
③
在以上的反应中,_____________(MnO )只起__________( _______ )反应_______的作用,本身的__________和___________在反应前后都__________。这种物质叫做_________(catalyst),工业上又叫做______ , 它在反应中起______作用。
二氧化锰
改变
加速
速度
质量
化学性质
没有改变
催化剂
催化剂
触媒
催化
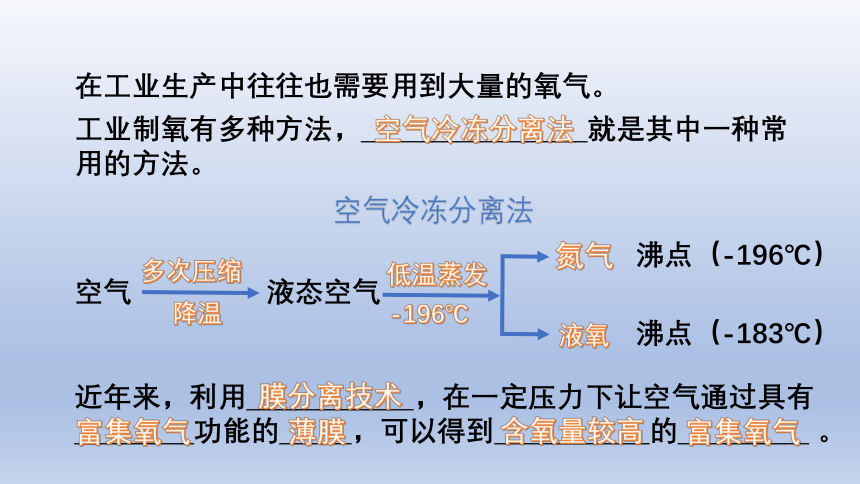
工业制氧有多种方法,___________________就是其中一种常用的方法。
在工业生产中往往也需要用到大量的氧气。
空气冷冻分离法
空气冷冻分离法
空气
多次压缩
降温
液态空气
低温蒸发
-196℃
沸点(-196℃)
沸点(-183℃)
氮气
液氧
近年来,利用______________,在一定压力下让空气通过具有__________功能的______,可以得到_____________的___________ 。
膜分离技术
富集氧气
薄膜
富集氧气
含氧量较高
氧气的发现
1774年,英国科学家普利斯特利(Joseph
Priestley)加热氧化汞(HgO),得到一种使
人感到特别舒适、轻松的气体,并且发现物质
在这种气体里燃烧时比在空气中更强烈。 在这
期间, 瑞典科学家舍勒(Karl Wilhelm Scheele)在把软锰矿与浓硫酸一起加热时,也得到了一种使红热木炭火花四溅、光耀夺目的无色气体。
普利斯特利和舍勒实际上已经发现了氧气,并研究了它的性质。但由于墨守陈旧的燃素学说,他们不知道自己找到了什么。
1774年 10月,法国化学家拉瓦锡重做了普利斯特利的实验,并进行了定量分析,确认由 HgO 分解出来的气体是一种新元素。1777年,他将这种气体正式命名为“氧气”,并提出了他的燃烧学说,建立了科学的氧化学说。
在研究氧气的化学性质及制取氧气的过程中,我们接触了许多化学反应,你是否注意过这些化学反应有什么不同呢?
下列四个化学反应的反应物和生成物的种类有什么相同和不同之处
①S在O 里燃烧生成 SO ;
②铁丝在O 里燃烧生成 Fe O ;
③用KMnO 制取 O ;
④用H O 制取 O 。
有些化学反应中,______反应的物质有______或___________ , ______的物质只有______ ;
分析了大量的化学反应后,可以发现
参加
我们把这种由______或___________的物质______ ______物质的反应叫做___________ ,如
由______物质______ ______或___________的物质的反应叫做___________ ,如
有些化学反应中,______反应的物质只有______,生成的物质却有______或___________ 。
两种
两种以上
生成
一种
参加
一种
两种
两种以上
五、化合反应
两种
两种以上
生成
一种
化合反应
硫和氧气反应生成二氧化硫。
一种
生成
两种
两种以上
过氧化氢分解产生水和氧气。
分解反应
和 分解反应
小结:
四、氧气的制取
高锰酸钾
锰酸钾
加热
二氧化锰
氧气
+
+
氯酸钾
氯化钾
二氧化锰
氧气
+
加热
过氧化氢
水
二氧化锰
氧气
+
在以上的反应中,_____________(MnO )只起__________( _______ )反应_______的作用,本身的__________和___________在反应前后都__________。这种物质叫做_________,工业上又叫做______ , 它在反应中起______作用。
二氧化锰
改变
加速
速度
质量
化学性质
没有改变
催化剂
催化剂
触媒
催化
工业制氧有多种方法,___________________就是其中一种常用的方法。
空气冷冻分离法
近年来,利用______________,在一定压力下让空气通过具有__________功能的______,可以得到_____________的___________ 。
膜分离技术
富集氧气
薄膜
富集氧气
含氧量较高
实验室
工业
五、化合反应和 分解反应
我们把这种由______或___________的物质______ ______物质的反应叫做___________ ,
由______物质______ ______或___________的物质的反应叫做___________ ,
两种
两种以上
生成
一种
化合反应
一种
生成
两种
两种以上
分解反应
1、列实验操作图示正确的是( )
C
2、在利用一定质量的双氧水和二氧化锰制取氧气的实验过程中,相关量的变化与时间的对应关系如图所示,则纵坐标可能表示( )
A.水的质量 B.氧气的质量
C.双氧水的质量 D.二氧化锰的质量
D
3、二氧化钛”是一种能降解甲醛、一氧化氮等有害气体的光触媒。在降解过程中“二氧化钛”不挥发,不消耗,具有长效性。
(1)根据题意,在降解过程中“二氧化钛”的作用是____________________。
(2)一氧化氮在空气中易与氧气反应,反应方程式为2NO+O =2NO ,该反应属于_______(选填“化合”或“分解”)反应。
催化(催化剂)
化合
4、小明同学在探究“氧化铁是否可以作过氧化氢分解反应的催化剂”中进行了如下实验。
实验I:在装有10毫升5%的过氧化氢溶液的试管中,加入一生锈的铁钉(铁锈的成分是氧化铁),观察到试管中很快出现了大量气泡。
实验II:取10毫升5%的过氧化氢溶液于另一支试管中,加入铁,没有观察到明显现象。
(1)实验I中小明要检验试管中出现的气泡是氧气的操作是:____________________________________________________________________。
(2)小明通过设置实验II的目的是_________________________。
(3)小明得出氧化铁可以作过氧化氢分解反应的催化剂的结论。小红认为这样不恰当,还需要继续实验,需验证氧化铁的_________________________在反应前后保持不变。
用一根带火星的木条伸入试管,若带火星的木条复燃,则证明生成了氧气
设置对照组,排除铁能加快过氧化氢的分解
质量和化学性质
内容要求
①知道空气主要成分的体积分数,认识空气对人类的重要作用。②认识氧气的主要性质,学会氧气的实验室制法。认识化学反应催化剂的重要作用。
③知道常见的化合反应、分解反应。
学业要求
①能完成氧气的实验室制取,认识实验室制取气体的一般思路和方法。②能辨析常见的化合、分解反应。
实验
氧气的制取和性质研究
第1节 空气与氧气(3)
实验室里的氧气可以
用加热分解____________ (_________)
或_________ (_______)的方法来制取,
也可以用分解____________ (_______)的方法来制取。
KMnO
四、氧气的制取
KClO
H O
高锰酸钾
氯酸钾
过氧化氢
其反应过程分别表示如下:
MnO
O
高锰酸钾
锰酸钾
加热
二氧化锰
氧气
+
+
KMnO
K MnO
(MnO )
O
氯酸钾
氯化钾
二氧化锰
氧气
+
KClO
KCl
加热
(MnO )
O
过氧化氢
水
二氧化锰
氧气
+
H O
H O
1.如图 3-16, 在分液漏斗中加入 20~50 毫 升 15% 的 H O ,在烧瓶中加入 50 毫升水及 0.5 克 MnO 。
2.转动分液漏斗的活塞,滴加过氧化氢,待装置中_______空气后,用_________收集气体并验证收集的是氧气。
图3-16 制取氧气的装置
H O
MnO
排净
排水法
①
②
③
在以上的反应中,_____________(MnO )只起__________( _______ )反应_______的作用,本身的__________和___________在反应前后都__________。这种物质叫做_________(catalyst),工业上又叫做______ , 它在反应中起______作用。
二氧化锰
改变
加速
速度
质量
化学性质
没有改变
催化剂
催化剂
触媒
催化
工业制氧有多种方法,___________________就是其中一种常用的方法。
在工业生产中往往也需要用到大量的氧气。
空气冷冻分离法
空气冷冻分离法
空气
多次压缩
降温
液态空气
低温蒸发
-196℃
沸点(-196℃)
沸点(-183℃)
氮气
液氧
近年来,利用______________,在一定压力下让空气通过具有__________功能的______,可以得到_____________的___________ 。
膜分离技术
富集氧气
薄膜
富集氧气
含氧量较高
氧气的发现
1774年,英国科学家普利斯特利(Joseph
Priestley)加热氧化汞(HgO),得到一种使
人感到特别舒适、轻松的气体,并且发现物质
在这种气体里燃烧时比在空气中更强烈。 在这
期间, 瑞典科学家舍勒(Karl Wilhelm Scheele)在把软锰矿与浓硫酸一起加热时,也得到了一种使红热木炭火花四溅、光耀夺目的无色气体。
普利斯特利和舍勒实际上已经发现了氧气,并研究了它的性质。但由于墨守陈旧的燃素学说,他们不知道自己找到了什么。
1774年 10月,法国化学家拉瓦锡重做了普利斯特利的实验,并进行了定量分析,确认由 HgO 分解出来的气体是一种新元素。1777年,他将这种气体正式命名为“氧气”,并提出了他的燃烧学说,建立了科学的氧化学说。
在研究氧气的化学性质及制取氧气的过程中,我们接触了许多化学反应,你是否注意过这些化学反应有什么不同呢?
下列四个化学反应的反应物和生成物的种类有什么相同和不同之处
①S在O 里燃烧生成 SO ;
②铁丝在O 里燃烧生成 Fe O ;
③用KMnO 制取 O ;
④用H O 制取 O 。
有些化学反应中,______反应的物质有______或___________ , ______的物质只有______ ;
分析了大量的化学反应后,可以发现
参加
我们把这种由______或___________的物质______ ______物质的反应叫做___________ ,如
由______物质______ ______或___________的物质的反应叫做___________ ,如
有些化学反应中,______反应的物质只有______,生成的物质却有______或___________ 。
两种
两种以上
生成
一种
参加
一种
两种
两种以上
五、化合反应
两种
两种以上
生成
一种
化合反应
硫和氧气反应生成二氧化硫。
一种
生成
两种
两种以上
过氧化氢分解产生水和氧气。
分解反应
和 分解反应
小结:
四、氧气的制取
高锰酸钾
锰酸钾
加热
二氧化锰
氧气
+
+
氯酸钾
氯化钾
二氧化锰
氧气
+
加热
过氧化氢
水
二氧化锰
氧气
+
在以上的反应中,_____________(MnO )只起__________( _______ )反应_______的作用,本身的__________和___________在反应前后都__________。这种物质叫做_________,工业上又叫做______ , 它在反应中起______作用。
二氧化锰
改变
加速
速度
质量
化学性质
没有改变
催化剂
催化剂
触媒
催化
工业制氧有多种方法,___________________就是其中一种常用的方法。
空气冷冻分离法
近年来,利用______________,在一定压力下让空气通过具有__________功能的______,可以得到_____________的___________ 。
膜分离技术
富集氧气
薄膜
富集氧气
含氧量较高
实验室
工业
五、化合反应和 分解反应
我们把这种由______或___________的物质______ ______物质的反应叫做___________ ,
由______物质______ ______或___________的物质的反应叫做___________ ,
两种
两种以上
生成
一种
化合反应
一种
生成
两种
两种以上
分解反应
1、列实验操作图示正确的是( )
C
2、在利用一定质量的双氧水和二氧化锰制取氧气的实验过程中,相关量的变化与时间的对应关系如图所示,则纵坐标可能表示( )
A.水的质量 B.氧气的质量
C.双氧水的质量 D.二氧化锰的质量
D
3、二氧化钛”是一种能降解甲醛、一氧化氮等有害气体的光触媒。在降解过程中“二氧化钛”不挥发,不消耗,具有长效性。
(1)根据题意,在降解过程中“二氧化钛”的作用是____________________。
(2)一氧化氮在空气中易与氧气反应,反应方程式为2NO+O =2NO ,该反应属于_______(选填“化合”或“分解”)反应。
催化(催化剂)
化合
4、小明同学在探究“氧化铁是否可以作过氧化氢分解反应的催化剂”中进行了如下实验。
实验I:在装有10毫升5%的过氧化氢溶液的试管中,加入一生锈的铁钉(铁锈的成分是氧化铁),观察到试管中很快出现了大量气泡。
实验II:取10毫升5%的过氧化氢溶液于另一支试管中,加入铁,没有观察到明显现象。
(1)实验I中小明要检验试管中出现的气泡是氧气的操作是:____________________________________________________________________。
(2)小明通过设置实验II的目的是_________________________。
(3)小明得出氧化铁可以作过氧化氢分解反应的催化剂的结论。小红认为这样不恰当,还需要继续实验,需验证氧化铁的_________________________在反应前后保持不变。
用一根带火星的木条伸入试管,若带火星的木条复燃,则证明生成了氧气
设置对照组,排除铁能加快过氧化氢的分解
质量和化学性质
同课章节目录
- 第1章 电与磁
- 第1节 指南针为什么能指方向
- 第2节 电生磁
- 第3节 电磁铁的应用
- 第4节 电动机
- 第5节 磁生电
- 第6节 家庭用电
- 第7节 电的安全使用
- 第2章 微粒的模型与符号
- 第1节 模型、符号的建立与作用
- 第2节 物质的微观粒子模型
- 第3节 原子结构的模型
- 第4节 组成物质的元素
- 第5节 表示元素的符号
- 第6节 表示物质的符号
- 第7节 元素符号表示的量
- 第3章 空气与生命
- 第1节 空气与氧气
- 第2节 氧化和燃烧
- 第3节 化学方程式
- 第4节 二氧化碳
- 第5节 生物的呼吸和呼吸作用
- 第6节 光合作用
- 第7节 自然界中的氧循环和碳循环
- 第8节 空气污染与保护
- 第4章 植物与土壤
- 第1节 土壤的成分
- 第2节 各种各样的土壤
- 第3节 植物的根与物质吸收
- 第4节 植物的茎与物质运输
- 第5节 植物的叶与蒸腾作用
- 第6节 保护土壤
- 研究性学习课题
- 一 设计简单的电磁控制电路
- 二 化学反应中质量守恒的研究
- 三 研究植物的呼吸
- 四 当地水土状况调查
