第2节 物质的微观粒子模型(第1课时)
图片预览








文档简介
课件43张PPT。第 2 节物质的微观粒子模型(1课时)1、物理变化复习与回顾:没有别的物质生成的变化2、化学变化有别的物质生成的变化3、物理性质和化学性质不需要化学变化就能表现出来的性质,如
颜色、气味、软硬、晶体的熔点、液体的
沸点、物质的溶解性。物理性质:需要发生化学变化才能表现出来的性质,如
酸碱性、可燃性等。化学性质: 复习与导入新课 我们知道水是由分子构成的。
右边的两幅图描述了水的什么变化?
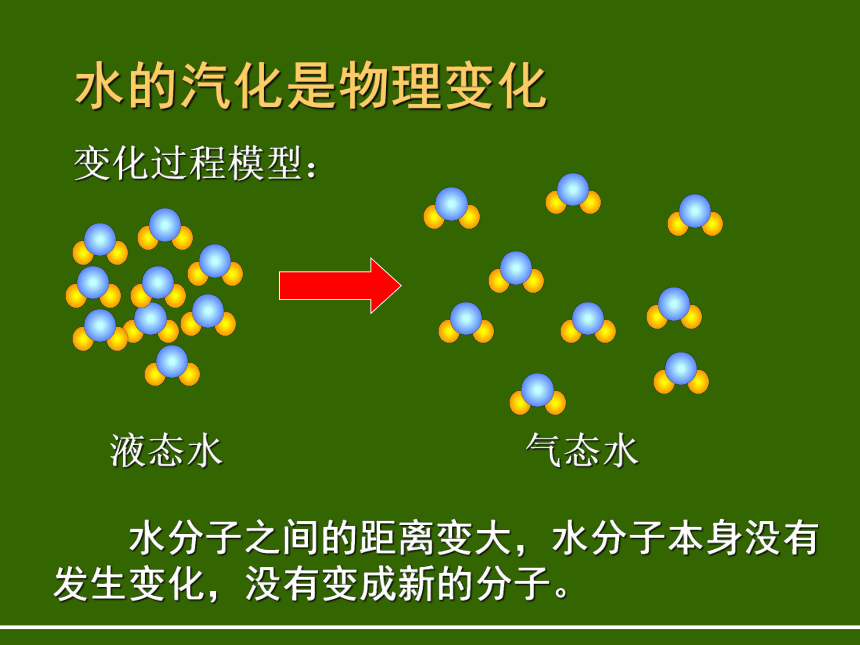
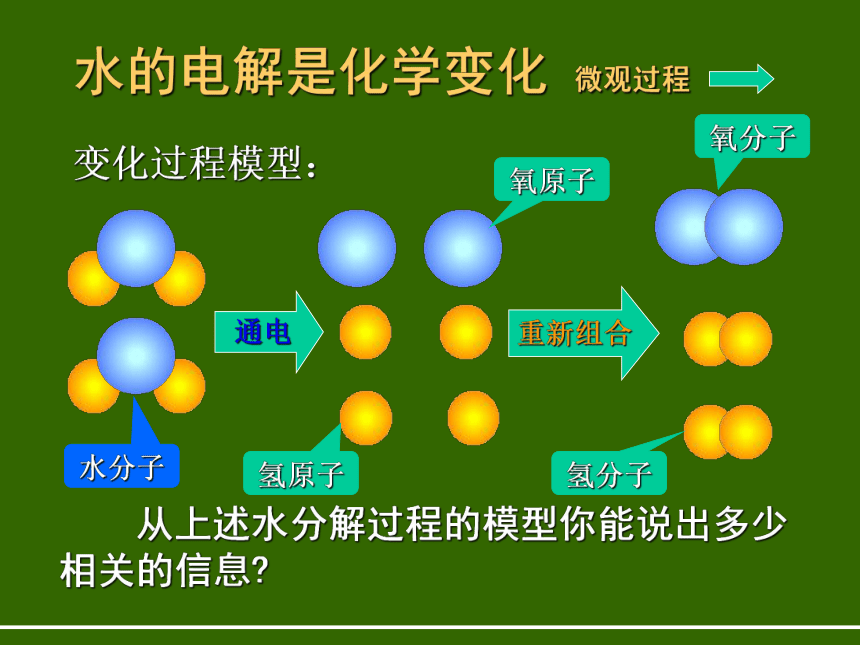
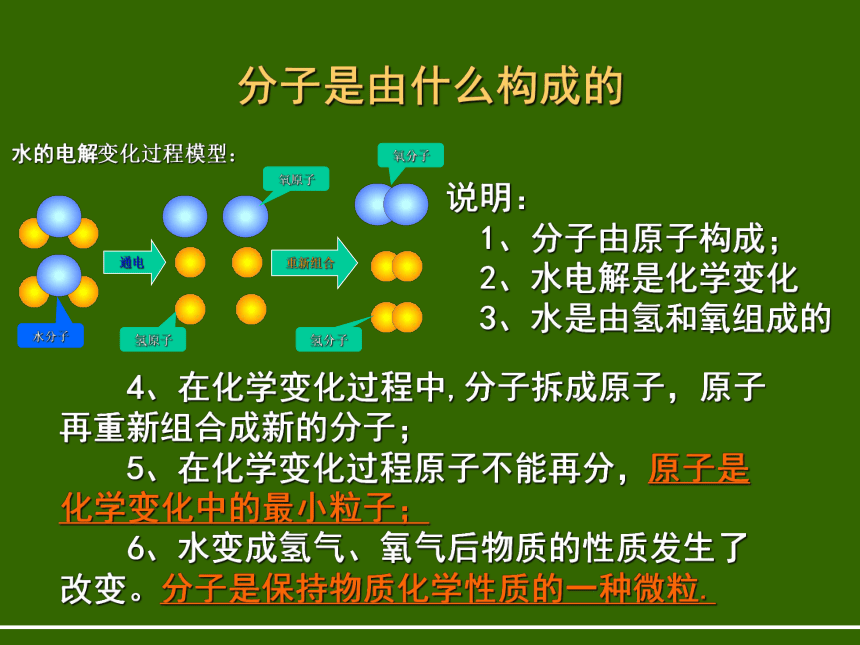
属于水的什么性质? 怎样用模型的方式来表示呢?水的汽化是物理变化变化过程模型:液态水气态水 水分子之间的距离变大,水分子本身没有发生变化,没有变成新的分子。水的电解是化学变化 微观过程变化过程模型:通电重新组合水分子 从上述水分解过程的模型你能说出多少相关的信息?分子是由什么构成的说明:
1、分子由原子构成;
2、水电解是化学变化
3、水是由氢和氧组成的 4、在化学变化过程中,分子拆成原子,原子再重新组合成新的分子;
5、在化学变化过程原子不能再分,原子是化学变化中的最小粒子;
6、水变成氢气、氧气后物质的性质发生了改变。分子是保持物质化学性质的一种微粒.硅原子图像分子、原子概念 分子是保持物质化学性质的最小粒子。
原子是化学变化中的最小粒子。 分子能保持物质的化学性质,但不能保持物质的物理性质。如液态水变成冰时,此时水分子不变,水的化学性质就不变,但水的状态已变(即物理性质已变)。原子存在的证明 图1-5思考:在电解水的反应中什么发生 了变化?什么没有变化? 水分子变成了氧分子、氢分子,氧原子、氢原子没有变化。
所以在化学变化中分子分成原子,原子再重新组合成新的分子。这就是化学变化的实质。物质是由什么构成的?先看一杯水的情况: 一杯水是由___________构成,________ 是由___________________ 构成。
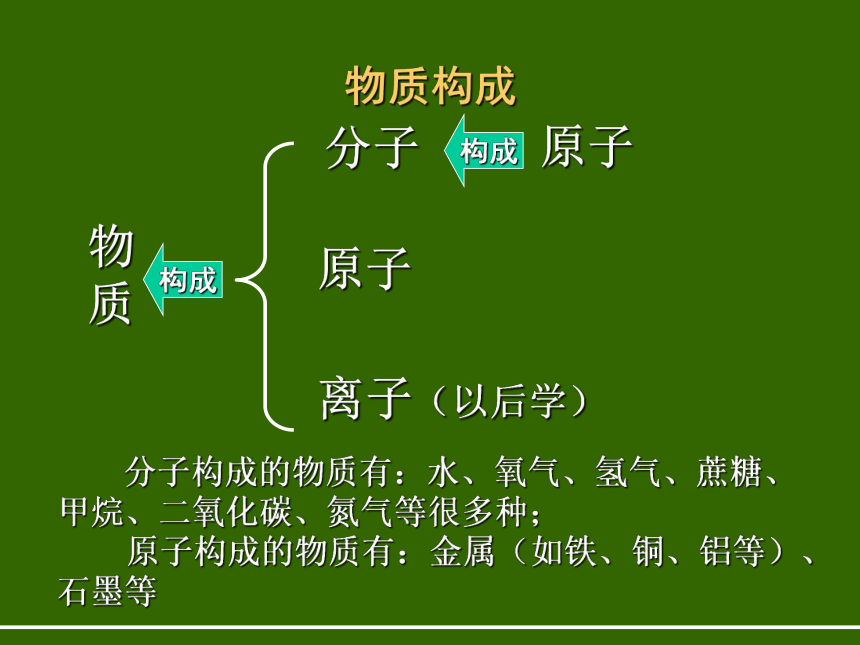
一个水分子是由_____________________构成。许多水分子水分子氧原子和氢原子一个氧原子和二个氢原子构成物质构成物质分子原子离子(以后学)构成 分子构成的物质有:水、氧气、氢气、蔗糖、甲烷、二氧化碳、氮气等很多种;
原子构成的物质有:金属(如铁、铜、铝等)、石墨等原子分子的性质有哪些?1、分子的体积和质量都很小;
2、分子在不断地做无规则运动;
3、分子之间有间隔;
4、同种分子性质相同,不同种物质分子性质各异。小结:分子与原子的比较 保持物质化学性质的最小粒子。在化学反应中分裂,重新组成新物质的分子。 化学变化中的最小粒子。在化学反应中不可再分,化学反应后没有变成其他原子。 质甚微,体甚小,有间隙,永恒运动,同种性相同,异种性各异。 分子分裂成原子,原子组成分子(分子由原子构成),都可以构成物质。 分子比构成分子本身的原子大,但不能说原子一定比分子小。一些物质的分子模型氨气分子 臭氧分子 三氧化硫分子 二氯化甲烷分子 二氧化碳分子 甲醛分子 苯分子 水分子 甲烷分子 C60分子下载http://orgchem.nease.net/index.htm原子构成不同的物质氢原子 碳原子 氧原子氢分子氧分子臭氧分子一氧化碳分子水分子过氧化氢分子
或双氧水分子二氧化碳分子甲烷分子 由此可见构成分子的原子可以是同种原子,也可以是不同种原子。
同种原子构成不同物质时结构是不一样的。
如氧气与臭氧,金刚石、石墨和足球烯(C60)氧分子臭氧分子金刚石 石墨 足球烯 1、一滴水的分子个数:1021个水分子构成,1ml水需要约20滴水组成。2、如果把水分子放大到乒乓球那么大,那么乒乓球就要放大到地球那么大。 数的启示?3、铅笔留下的黑色的笔迹是碳原子的堆积,一个句号竟有1018个碳原子。启示:分子、原子都很小粒子的大小与质量 分子、原子等微观粒子虽然都很小,但都有一定的体积和质量。如:小结:一、物质是由分子、原子等粒子构成的;
分子是由原子构成的;
二、分子、原子等粒子具有体小、质微、有隙、
永动等特点;
三、化学变化的实质是变化中分子分裂成原子,
原子重新组合成新的分子;
物理变化只是分子间的距离发生了改变,
没有生成新的分子
四、用模型表示分子、原子等微观粒子;
五、由不同种类和数目的原子构成种类繁多物质
世界。练习三:判断题1、分子一定比原子大 ( )
2、分子能直接构成物质,原子不能直接物质( )
3、分子一定比原子的质量大 ( )
4、分子能保持物质的化学性质,而原子不能( )×
×
×
×练习二:课本P8 3氨气分子随堂联想解题1、“墙角数枝梅,凌寒独自开。遥知不是雪,
为有暗香来。”(王安石《梅花》诗人在远处
就能闻到淡淡的梅花香味的原因是( )A、分子很小
B、分子是可分的
C、分子之间有间隔
D、分子在不断运动D2、氧化汞受热时的变化可用下图表示(大圆圈表示汞原子、小圆圈表示氧原子)据图得出的下列结论错误的是( )DA、氧化汞受热能分解成汞和氧气
B、原子是化学变化中的最小粒子
C、分子在化学变化中可以再分
D、所有的物质都是由分子构成的3、下列关于分子的叙述正确的是
( )BA、分子是构成物质的惟一微粒B、分子之间有空隙C、分子紧紧靠在一起D、分子之间有一定的空隙,这种空隙固定
不变的。4、用放大镜观察一块蔗糖,下
列说法正确的是( )BA、在放大镜下,我们看到了蔗糖分子
B、我们看到的是放大的蔗糖,不是它的分子
C、把蔗糖碾碎后,我们能看到蔗糖分子
D、蔗糖的水溶液中,没有蔗糖分子A、盛夏将自行车放在阳光下,车胎爆炸
B、通常把氧气加压到1.5X107Pa,贮存在蓝
色的钢瓶中
C、绿豆和黄豆混合后,总体积小于混合前它们的
体积之和
D、酒精和水混合后的总体积小于混合前它们的体
积之和C5、下列不能说明分子间有间隔的
事实是第 2 节物质与微观粒子模型(2课时)7、小珂在家做糖溶于水的实验时,观察到如
下图所示的现象请用分子的观点来解释。解释:1、分子在不断运动
2、分子之间有间隔构成物质的基本微粒有三种:原子、分子、离子2.有些物质是由分子构成的。如:水、氧气、二氧化碳、酒精、蔗糖等。1.有些物质是由原子直接构成的。如:铁、铝、铜等金属,以及金刚石、石墨等3.有些物质是由离子构成的。如:氯化钠、硝酸钾、碳酸钙等(关于离子稍后学)分子、原子的真实存在苯分子硅原子用超真空扫描隧道显微镜获得的苯分子的图像通过移走硅原子构成的图像一、原子、分子大量的研究证实:原子是构成物质的基本单元问题1:有些物质是由原子直接构成的。如:铁、铝、铜等金属,以及金刚石、石墨等一块铁的内部结构碳原子构成的石墨碳原子构成
的金刚石同种原子不同的排列方式,构成不同的物质。碳原子构成的石墨碳原子构成
的金刚石碳60分子是由原子构成的。可以由同种原子构成,也可以由不同原子构成。 由同种原子构成的分子,如:问题2: 有些物质是由分子构成的。如:氧气、氢气、臭氧、水、二氧化碳、酒精、蔗糖等。(用元素符号来表示分子组成的式子叫分子式)氧气是氧分子构成的;
氧分子是由两个氧原子构成的。C60分子一个碳-60分子特殊:氦——单原子分子 由不同种原子构成的分子。如:一个水分子(H2O ) 是由一个氧原子和两个氢原子组成一滴水大约有1.7×1021个水分子
分子乒乓球乒乓球地球一个酒精分子: C2H6O一个葡萄糖分子: C6H12O6有的分子非常复杂结论:当原子构成分子时,原子的种类、数量和结构是多种多样的,因而分子也是多种多样的。第一个建立原子学说的科学家——道尔顿“原子学说”的建立通常认为是近代化学的开始,因此,道尔顿通常被认为是近代化学的创始人。 英国物理学家、化学家约翰·道尔顿
(1766——1844)
原子论的建立者— 道尔顿.本 节 重 点:1.构成物质的基本微粒有三种:分子、原子、离子有的物质是由分子构成,有的物质是由原子直接构成,有的物质是由离子构成。2.原子是构成物质的基本单元分子是由原子构成的。分子可以由同种原子构成,也可以由不同原子构成3.“原子学说”的建立通常认为是近代化学的开始,因此,道尔顿通常被认为是近代化学的创始人。硅原子的电子隧道显微镜图像。
颜色、气味、软硬、晶体的熔点、液体的
沸点、物质的溶解性。物理性质:需要发生化学变化才能表现出来的性质,如
酸碱性、可燃性等。化学性质: 复习与导入新课 我们知道水是由分子构成的。
右边的两幅图描述了水的什么变化?
属于水的什么性质? 怎样用模型的方式来表示呢?水的汽化是物理变化变化过程模型:液态水气态水 水分子之间的距离变大,水分子本身没有发生变化,没有变成新的分子。水的电解是化学变化 微观过程变化过程模型:通电重新组合水分子 从上述水分解过程的模型你能说出多少相关的信息?分子是由什么构成的说明:
1、分子由原子构成;
2、水电解是化学变化
3、水是由氢和氧组成的 4、在化学变化过程中,分子拆成原子,原子再重新组合成新的分子;
5、在化学变化过程原子不能再分,原子是化学变化中的最小粒子;
6、水变成氢气、氧气后物质的性质发生了改变。分子是保持物质化学性质的一种微粒.硅原子图像分子、原子概念 分子是保持物质化学性质的最小粒子。
原子是化学变化中的最小粒子。 分子能保持物质的化学性质,但不能保持物质的物理性质。如液态水变成冰时,此时水分子不变,水的化学性质就不变,但水的状态已变(即物理性质已变)。原子存在的证明 图1-5思考:在电解水的反应中什么发生 了变化?什么没有变化? 水分子变成了氧分子、氢分子,氧原子、氢原子没有变化。
所以在化学变化中分子分成原子,原子再重新组合成新的分子。这就是化学变化的实质。物质是由什么构成的?先看一杯水的情况: 一杯水是由___________构成,________ 是由___________________ 构成。
一个水分子是由_____________________构成。许多水分子水分子氧原子和氢原子一个氧原子和二个氢原子构成物质构成物质分子原子离子(以后学)构成 分子构成的物质有:水、氧气、氢气、蔗糖、甲烷、二氧化碳、氮气等很多种;
原子构成的物质有:金属(如铁、铜、铝等)、石墨等原子分子的性质有哪些?1、分子的体积和质量都很小;
2、分子在不断地做无规则运动;
3、分子之间有间隔;
4、同种分子性质相同,不同种物质分子性质各异。小结:分子与原子的比较 保持物质化学性质的最小粒子。在化学反应中分裂,重新组成新物质的分子。 化学变化中的最小粒子。在化学反应中不可再分,化学反应后没有变成其他原子。 质甚微,体甚小,有间隙,永恒运动,同种性相同,异种性各异。 分子分裂成原子,原子组成分子(分子由原子构成),都可以构成物质。 分子比构成分子本身的原子大,但不能说原子一定比分子小。一些物质的分子模型氨气分子 臭氧分子 三氧化硫分子 二氯化甲烷分子 二氧化碳分子 甲醛分子 苯分子 水分子 甲烷分子 C60分子下载http://orgchem.nease.net/index.htm原子构成不同的物质氢原子 碳原子 氧原子氢分子氧分子臭氧分子一氧化碳分子水分子过氧化氢分子
或双氧水分子二氧化碳分子甲烷分子 由此可见构成分子的原子可以是同种原子,也可以是不同种原子。
同种原子构成不同物质时结构是不一样的。
如氧气与臭氧,金刚石、石墨和足球烯(C60)氧分子臭氧分子金刚石 石墨 足球烯 1、一滴水的分子个数:1021个水分子构成,1ml水需要约20滴水组成。2、如果把水分子放大到乒乓球那么大,那么乒乓球就要放大到地球那么大。 数的启示?3、铅笔留下的黑色的笔迹是碳原子的堆积,一个句号竟有1018个碳原子。启示:分子、原子都很小粒子的大小与质量 分子、原子等微观粒子虽然都很小,但都有一定的体积和质量。如:小结:一、物质是由分子、原子等粒子构成的;
分子是由原子构成的;
二、分子、原子等粒子具有体小、质微、有隙、
永动等特点;
三、化学变化的实质是变化中分子分裂成原子,
原子重新组合成新的分子;
物理变化只是分子间的距离发生了改变,
没有生成新的分子
四、用模型表示分子、原子等微观粒子;
五、由不同种类和数目的原子构成种类繁多物质
世界。练习三:判断题1、分子一定比原子大 ( )
2、分子能直接构成物质,原子不能直接物质( )
3、分子一定比原子的质量大 ( )
4、分子能保持物质的化学性质,而原子不能( )×
×
×
×练习二:课本P8 3氨气分子随堂联想解题1、“墙角数枝梅,凌寒独自开。遥知不是雪,
为有暗香来。”(王安石《梅花》诗人在远处
就能闻到淡淡的梅花香味的原因是( )A、分子很小
B、分子是可分的
C、分子之间有间隔
D、分子在不断运动D2、氧化汞受热时的变化可用下图表示(大圆圈表示汞原子、小圆圈表示氧原子)据图得出的下列结论错误的是( )DA、氧化汞受热能分解成汞和氧气
B、原子是化学变化中的最小粒子
C、分子在化学变化中可以再分
D、所有的物质都是由分子构成的3、下列关于分子的叙述正确的是
( )BA、分子是构成物质的惟一微粒B、分子之间有空隙C、分子紧紧靠在一起D、分子之间有一定的空隙,这种空隙固定
不变的。4、用放大镜观察一块蔗糖,下
列说法正确的是( )BA、在放大镜下,我们看到了蔗糖分子
B、我们看到的是放大的蔗糖,不是它的分子
C、把蔗糖碾碎后,我们能看到蔗糖分子
D、蔗糖的水溶液中,没有蔗糖分子A、盛夏将自行车放在阳光下,车胎爆炸
B、通常把氧气加压到1.5X107Pa,贮存在蓝
色的钢瓶中
C、绿豆和黄豆混合后,总体积小于混合前它们的
体积之和
D、酒精和水混合后的总体积小于混合前它们的体
积之和C5、下列不能说明分子间有间隔的
事实是第 2 节物质与微观粒子模型(2课时)7、小珂在家做糖溶于水的实验时,观察到如
下图所示的现象请用分子的观点来解释。解释:1、分子在不断运动
2、分子之间有间隔构成物质的基本微粒有三种:原子、分子、离子2.有些物质是由分子构成的。如:水、氧气、二氧化碳、酒精、蔗糖等。1.有些物质是由原子直接构成的。如:铁、铝、铜等金属,以及金刚石、石墨等3.有些物质是由离子构成的。如:氯化钠、硝酸钾、碳酸钙等(关于离子稍后学)分子、原子的真实存在苯分子硅原子用超真空扫描隧道显微镜获得的苯分子的图像通过移走硅原子构成的图像一、原子、分子大量的研究证实:原子是构成物质的基本单元问题1:有些物质是由原子直接构成的。如:铁、铝、铜等金属,以及金刚石、石墨等一块铁的内部结构碳原子构成的石墨碳原子构成
的金刚石同种原子不同的排列方式,构成不同的物质。碳原子构成的石墨碳原子构成
的金刚石碳60分子是由原子构成的。可以由同种原子构成,也可以由不同原子构成。 由同种原子构成的分子,如:问题2: 有些物质是由分子构成的。如:氧气、氢气、臭氧、水、二氧化碳、酒精、蔗糖等。(用元素符号来表示分子组成的式子叫分子式)氧气是氧分子构成的;
氧分子是由两个氧原子构成的。C60分子一个碳-60分子特殊:氦——单原子分子 由不同种原子构成的分子。如:一个水分子(H2O ) 是由一个氧原子和两个氢原子组成一滴水大约有1.7×1021个水分子
分子乒乓球乒乓球地球一个酒精分子: C2H6O一个葡萄糖分子: C6H12O6有的分子非常复杂结论:当原子构成分子时,原子的种类、数量和结构是多种多样的,因而分子也是多种多样的。第一个建立原子学说的科学家——道尔顿“原子学说”的建立通常认为是近代化学的开始,因此,道尔顿通常被认为是近代化学的创始人。 英国物理学家、化学家约翰·道尔顿
(1766——1844)
原子论的建立者— 道尔顿.本 节 重 点:1.构成物质的基本微粒有三种:分子、原子、离子有的物质是由分子构成,有的物质是由原子直接构成,有的物质是由离子构成。2.原子是构成物质的基本单元分子是由原子构成的。分子可以由同种原子构成,也可以由不同原子构成3.“原子学说”的建立通常认为是近代化学的开始,因此,道尔顿通常被认为是近代化学的创始人。硅原子的电子隧道显微镜图像。
同课章节目录
- 第1章 电与磁
- 第1节 指南针为什么能指方向
- 第2节 电生磁
- 第3节 电磁铁的应用
- 第4节 电动机
- 第5节 磁生电
- 第6节 家庭用电
- 第7节 电的安全使用
- 第2章 微粒的模型与符号
- 第1节 模型、符号的建立与作用
- 第2节 物质的微观粒子模型
- 第3节 原子结构的模型
- 第4节 组成物质的元素
- 第5节 表示元素的符号
- 第6节 表示物质的符号
- 第7节 元素符号表示的量
- 第3章 空气与生命
- 第1节 空气与氧气
- 第2节 氧化和燃烧
- 第3节 化学方程式
- 第4节 二氧化碳
- 第5节 生物的呼吸和呼吸作用
- 第6节 光合作用
- 第7节 自然界中的氧循环和碳循环
- 第8节 空气污染与保护
- 第4章 植物与土壤
- 第1节 土壤的成分
- 第2节 各种各样的土壤
- 第3节 植物的根与物质吸收
- 第4节 植物的茎与物质运输
- 第5节 植物的叶与蒸腾作用
- 第6节 保护土壤
- 研究性学习课题
- 一 设计简单的电磁控制电路
- 二 化学反应中质量守恒的研究
- 三 研究植物的呼吸
- 四 当地水土状况调查
