江苏省淮安市刘老庄初级中学沪教版九年级化学全册课件:7.1 酸的性质(共16张PPT)
文档属性
| 名称 | 江苏省淮安市刘老庄初级中学沪教版九年级化学全册课件:7.1 酸的性质(共16张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 390.4KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2016-02-29 00:00:00 | ||
图片预览




文档简介
课件16张PPT。 酸的性质淮安人不容易,
一周过四季:
周一穿卫衣,
周二穿衬衣,
周三穿短袖,
周四马上穿毛衣,
周五必须穿大衣,
周六日不知穿何衣?小明到校医室,校医开了一盒斯达舒!服用后感觉好多了!斯达舒主要成分:Al(OH)3请问: 为什么斯达舒可以治疗胃反 酸、吐酸水,反应原理又是什 么呢? 反应原理: 酸碱中和反应
畅所欲言: 关于酸碱中和反应,你还知道哪些? 1、酸碱中和反应是复分解反应类型
2、酸碱中和反应是放热反应
3、恰好完全反应时,PH=7思考:
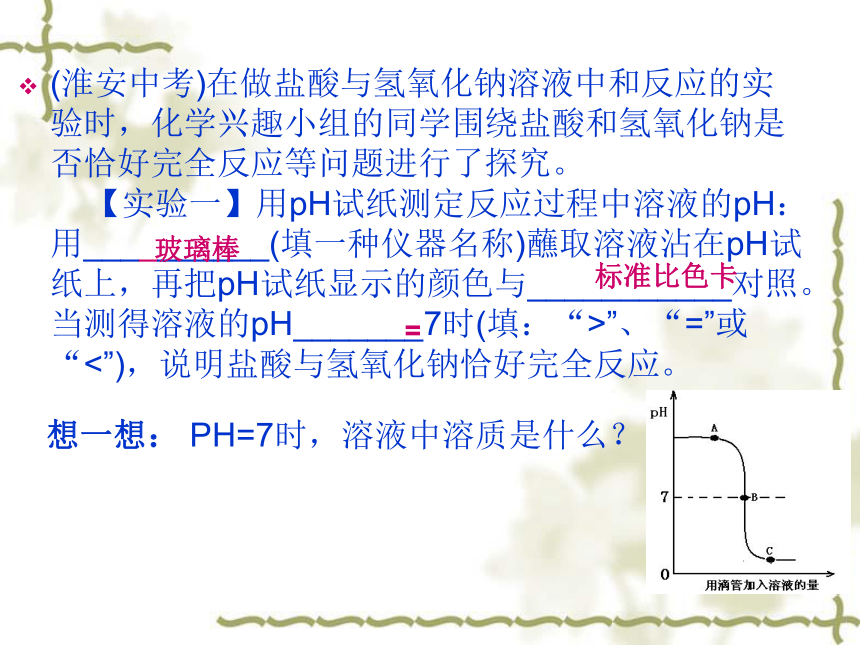
酸溶液和碱溶液发生中和反应时,一般没有明显现象,有哪些方法可以观察到反应发生了呢?(淮安中考)在做盐酸与氢氧化钠溶液中和反应的实验时,化学兴趣小组的同学围绕盐酸和氢氧化钠是否恰好完全反应等问题进行了探究。 【实验一】用pH试纸测定反应过程中溶液的pH:用__________(填一种仪器名称)蘸取溶液沾在pH试纸上,再把pH试纸显示的颜色与___________对照。当测得溶液的pH_______7时(填:“>”、“=”或“<”),说明盐酸与氢氧化钠恰好完全反应。想一想: PH=7时,溶液中溶质是什么?
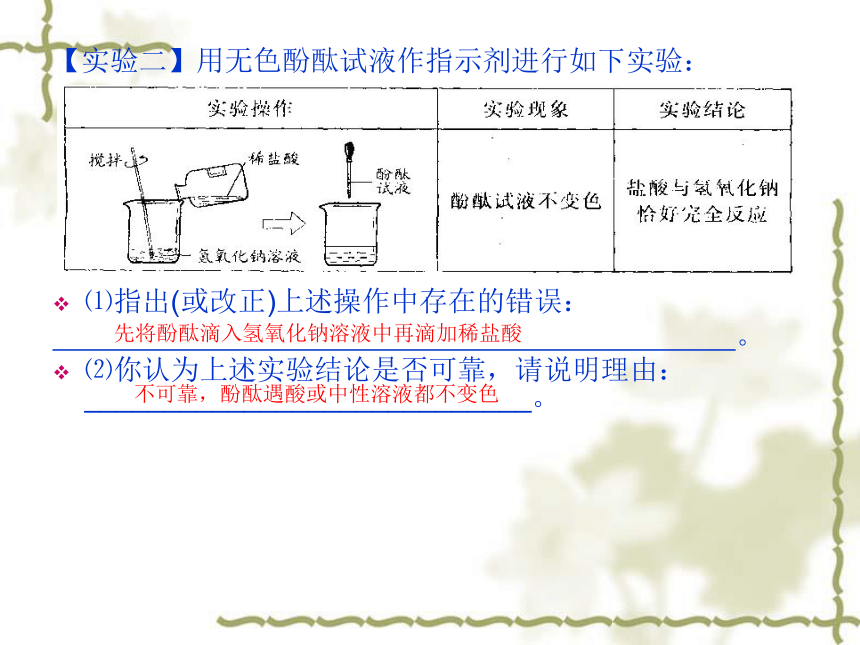
玻璃棒标准比色卡=【实验二】用无色酚酞试液作指示剂进行如下实验:
⑴指出(或改正)上述操作中存在的错误:
。
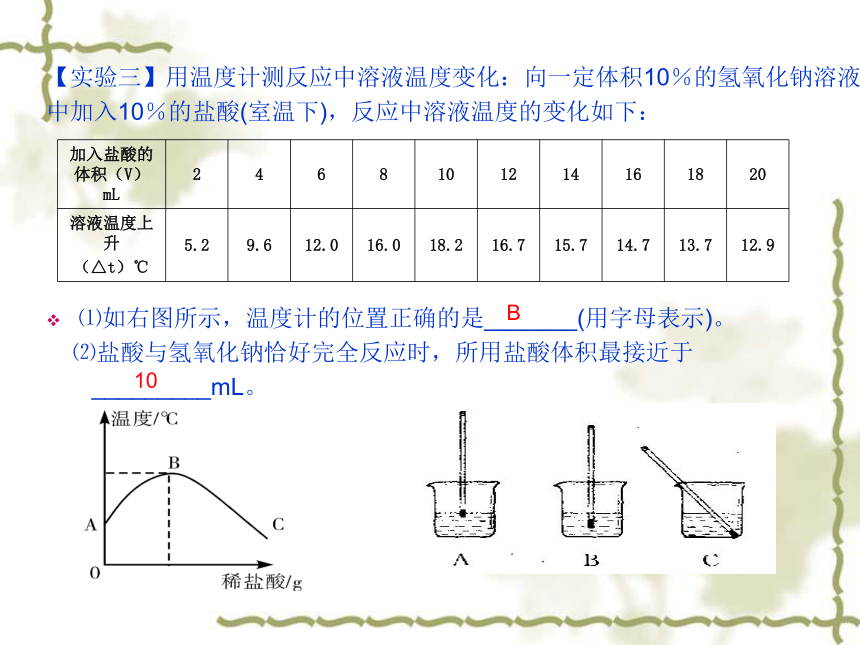
⑵你认为上述实验结论是否可靠,请说明理由:____________________________。先将酚酞滴入氢氧化钠溶液中再滴加稀盐酸不可靠,酚酞遇酸或中性溶液都不变色【实验三】用温度计测反应中溶液温度变化:向一定体积10%的氢氧化钠溶液
中加入10%的盐酸(室温下),反应中溶液温度的变化如下:
⑴如右图所示,温度计的位置正确的是_______(用字母表示)。
⑵盐酸与氢氧化钠恰好完全反应时,所用盐酸体积最接近于
_________mL。B10小明中午放学回家后,告诉了妈妈早上的事,妈妈听完从厨房拿出一袋饼干,并且笑眯眯地说:“这个也行”!苏打饼干成分中含有NaHCO3
反应原理:NaHCO3+HCl==NaCl+H2O+CO2↑
试一试:Na2CO3 + 2HCl==2NaCl+H2O+CO2↑
(淮安中考) 医院救治病人急需一批生理盐水,制药厂积极支援,用含有少量碳酸钠的氯化钠为原料生产纯净的氯化钠,再用其配制生理盐水。某化学学习小组运用所学知识,在实验室设计了如图5的氯化钠的生产流程。
请根据上述内容回答下列问题:
(1) 操作①中常用玻璃棒搅拌,其目的是 。
(2) 操作②中应加入的试剂B为 ,该小组同学认为过量的B无需再用试剂除去,最终对氯化钠的纯度不会造成影响,其原因是 。
使物质充分溶解稀盐酸稀盐酸的溶质为氯化氢气体,加热蒸发时易挥发 晚上小明回家看到“洁厕灵”。 洁厕灵成分中含有
盐酸注意:
安全放置勿让本品
与金属接触 他把生锈的铁钉放在小碗里,倒了些洁厕灵他看到什么现象?___________________。一段时间后,他又有新的发现: ____________________ 。请写出小明动手实验中涉及的两个化学方程式。
铁锈逐渐消失,溶液变成棕黄色铁钉表面有气泡Fe+2HCl==FeCl2+H2↑Fe2O3+6HCl==2FeCl3+3H2O考考你:哪些活泼金属可以与酸反应呢?如何比较它们的活泼性呢?
2、(2010年淮安)同学们为探究不同金属的活动性强弱,设计如下
实验方案,下列方案中实验设计、现象、结论均正确一组是
选项 实验设计 现 象 结论
( 金属的活动性)
A将铝丝放放硫酸铜溶液 无现象 Cu>Al
B将铝丝放入硫酸镁溶液中 铝丝表面有固体析出 Al>Mg
C分别将锌粉与铁丝放入
相同浓度的稀盐酸中 锌粉产生气泡的速率比铁丝快 Zn>Fe
D分别将铁丝与铜丝放入相同
浓度的稀盐酸中铁丝表面产生气泡 铜丝无现象 Fe>Cu
D小明感觉今天过了充实的一天,他把今天的收获都写在自己的日记本上!他还写下了他的疑问:盐酸有这些特性,硫酸也有吗?碳酸盐 盐酸复分解反应置换反应金属氧 化物金属练习:小苏打(主要成分为NaHCO3)中常含有少量氯化钠化学兴趣小组的同学为了测定某品牌小苏打中NaHCO3的质量分数。进行了以下实验:称量样品置于烧杯中,向其中慢慢滴加稀盐酸,至不再产生气泡为止,测得的有关数据如下表所示 试计算:(计算结果保留一位小数) (1)样品中的NaHCO3质量分数; (2)所得溶液中NaCl的质量分数。 .解:根据质量守恒定律得CO2的质量==9+75.4-80==4.4 g
设NaHCO3质量为X,生成的NaCl的质量为Y。则:
NaHCO3+HCl== NaCl+H2O+CO2↑
84 58.5 44
X Y 4.4g
84 44 58.5
x = 4.4g = y
x=8.4g
y=5.85g
样品中NaHCO3的质量分数: 8.4÷9×100%==93.3%
样品中NaCl的质量==9g -8.4 g ==0.6 g
NaCl的总质量==0.6g+5.85g g==6.45g
NaCl溶液中NaCl的质量分数==6.45g÷80×100%==8.1%
一周过四季:
周一穿卫衣,
周二穿衬衣,
周三穿短袖,
周四马上穿毛衣,
周五必须穿大衣,
周六日不知穿何衣?小明到校医室,校医开了一盒斯达舒!服用后感觉好多了!斯达舒主要成分:Al(OH)3请问: 为什么斯达舒可以治疗胃反 酸、吐酸水,反应原理又是什 么呢? 反应原理: 酸碱中和反应
畅所欲言: 关于酸碱中和反应,你还知道哪些? 1、酸碱中和反应是复分解反应类型
2、酸碱中和反应是放热反应
3、恰好完全反应时,PH=7思考:
酸溶液和碱溶液发生中和反应时,一般没有明显现象,有哪些方法可以观察到反应发生了呢?(淮安中考)在做盐酸与氢氧化钠溶液中和反应的实验时,化学兴趣小组的同学围绕盐酸和氢氧化钠是否恰好完全反应等问题进行了探究。 【实验一】用pH试纸测定反应过程中溶液的pH:用__________(填一种仪器名称)蘸取溶液沾在pH试纸上,再把pH试纸显示的颜色与___________对照。当测得溶液的pH_______7时(填:“>”、“=”或“<”),说明盐酸与氢氧化钠恰好完全反应。想一想: PH=7时,溶液中溶质是什么?
玻璃棒标准比色卡=【实验二】用无色酚酞试液作指示剂进行如下实验:
⑴指出(或改正)上述操作中存在的错误:
。
⑵你认为上述实验结论是否可靠,请说明理由:____________________________。先将酚酞滴入氢氧化钠溶液中再滴加稀盐酸不可靠,酚酞遇酸或中性溶液都不变色【实验三】用温度计测反应中溶液温度变化:向一定体积10%的氢氧化钠溶液
中加入10%的盐酸(室温下),反应中溶液温度的变化如下:
⑴如右图所示,温度计的位置正确的是_______(用字母表示)。
⑵盐酸与氢氧化钠恰好完全反应时,所用盐酸体积最接近于
_________mL。B10小明中午放学回家后,告诉了妈妈早上的事,妈妈听完从厨房拿出一袋饼干,并且笑眯眯地说:“这个也行”!苏打饼干成分中含有NaHCO3
反应原理:NaHCO3+HCl==NaCl+H2O+CO2↑
试一试:Na2CO3 + 2HCl==2NaCl+H2O+CO2↑
(淮安中考) 医院救治病人急需一批生理盐水,制药厂积极支援,用含有少量碳酸钠的氯化钠为原料生产纯净的氯化钠,再用其配制生理盐水。某化学学习小组运用所学知识,在实验室设计了如图5的氯化钠的生产流程。
请根据上述内容回答下列问题:
(1) 操作①中常用玻璃棒搅拌,其目的是 。
(2) 操作②中应加入的试剂B为 ,该小组同学认为过量的B无需再用试剂除去,最终对氯化钠的纯度不会造成影响,其原因是 。
使物质充分溶解稀盐酸稀盐酸的溶质为氯化氢气体,加热蒸发时易挥发 晚上小明回家看到“洁厕灵”。 洁厕灵成分中含有
盐酸注意:
安全放置勿让本品
与金属接触 他把生锈的铁钉放在小碗里,倒了些洁厕灵他看到什么现象?___________________。一段时间后,他又有新的发现: ____________________ 。请写出小明动手实验中涉及的两个化学方程式。
铁锈逐渐消失,溶液变成棕黄色铁钉表面有气泡Fe+2HCl==FeCl2+H2↑Fe2O3+6HCl==2FeCl3+3H2O考考你:哪些活泼金属可以与酸反应呢?如何比较它们的活泼性呢?
2、(2010年淮安)同学们为探究不同金属的活动性强弱,设计如下
实验方案,下列方案中实验设计、现象、结论均正确一组是
选项 实验设计 现 象 结论
( 金属的活动性)
A将铝丝放放硫酸铜溶液 无现象 Cu>Al
B将铝丝放入硫酸镁溶液中 铝丝表面有固体析出 Al>Mg
C分别将锌粉与铁丝放入
相同浓度的稀盐酸中 锌粉产生气泡的速率比铁丝快 Zn>Fe
D分别将铁丝与铜丝放入相同
浓度的稀盐酸中铁丝表面产生气泡 铜丝无现象 Fe>Cu
D小明感觉今天过了充实的一天,他把今天的收获都写在自己的日记本上!他还写下了他的疑问:盐酸有这些特性,硫酸也有吗?碳酸盐 盐酸复分解反应置换反应金属氧 化物金属练习:小苏打(主要成分为NaHCO3)中常含有少量氯化钠化学兴趣小组的同学为了测定某品牌小苏打中NaHCO3的质量分数。进行了以下实验:称量样品置于烧杯中,向其中慢慢滴加稀盐酸,至不再产生气泡为止,测得的有关数据如下表所示 试计算:(计算结果保留一位小数) (1)样品中的NaHCO3质量分数; (2)所得溶液中NaCl的质量分数。 .解:根据质量守恒定律得CO2的质量==9+75.4-80==4.4 g
设NaHCO3质量为X,生成的NaCl的质量为Y。则:
NaHCO3+HCl== NaCl+H2O+CO2↑
84 58.5 44
X Y 4.4g
84 44 58.5
x = 4.4g = y
x=8.4g
y=5.85g
样品中NaHCO3的质量分数: 8.4÷9×100%==93.3%
样品中NaCl的质量==9g -8.4 g ==0.6 g
NaCl的总质量==0.6g+5.85g g==6.45g
NaCl溶液中NaCl的质量分数==6.45g÷80×100%==8.1%
